
- DAZ.online
- News
- Spektrum
- COVID-19-Impfstoff von ...
Sicher und wirksam, aber kontrovers
COVID-19-Impfstoff von AstraZeneca – kommt bald die Zulassung in den USA?
Stuttgart - 26.03.2021, 07:00 Uhr
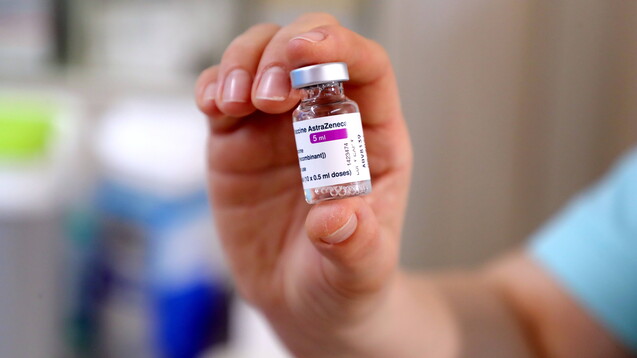
Ursprünglich zählte auch AstraZeneca zu den fünf aussichtsreichsten Corona-Impfstoff-Kandidaten in den USA („Operation Warp Speed“). Doch Berichte der „New York Times“ verraten, dass es schon früh Patzer vonseiten AstraZenecas gab, die zum Vertrauensverlust der US-Zulassungsbehörden führten. (Foto: IMAGO / Eastnews)
AstraZeneca und sein COVID-19-Impfstoff haben es nicht leicht – oder sollte man besser sagen, AstraZeneca macht es seinem Corona-Impfstoff nicht leicht? Während es in Europa vor allem Kontroversen über die Lieferfähigkeit gibt – von möglichen seltenen Nebenwirkungen einmal abgesehen – haben in den USA wohl kommunikative Probleme dazu geführt, dass der Impfstoff es dort noch immer nicht zur Zulassung geschafft hat. Doch auch in den USA spricht man von einem wahrscheinlich sehr guten Impfstoff.
Der Preis und die Lagerung machten den COVID-19-Impfstoff von AstraZeneca von Beginn an zu einem weltweiten Hoffnungsträger der Corona-Pandemie. Laut einem Bericht von Nature, wurde der Impfstoff bereits in 100 Ländern zugelassen – allerdings nicht in den USA. Dies führte zuletzt immer wieder zu verwirrender Berichterstattung in den Medien. Aber auch schon zuvor gab es auch außerhalb der USA viel mediales Chaos rund um die kommunizierten Wirksamkeitsdaten von AstraZeneca, was – genauso wie neue potenzielle Sicherheitsbedenken – den Impfstoff aber nie in echten Misskredit gebracht hat. Es folgte auf jeden Verdacht bislang immer eine Art „Freispruch“.
Mehr zum Thema
STIKO zu thromboembolischem Sicherheitssignal
AstraZeneca weiterhin entsprechend der dritten STIKO-Impfempfehlung einsetzen
Informiert entscheiden
EMA zu AstraZeneca: Nutzen bei weitem größer als die Risiken
Am Ende bleibt dennoch jedes Mal ein fader Beigeschmack, den der Impfstoff nicht mehr loszuwerden scheint. Gerade das zuletzt bekannt gewordene „Kommunikationsdesaster“ aus den USA könnte nun aber der Anfang vom Ende sein, und den Impfstoff schließlich vom faden Beigeschmack befreien. Nämlich dann, wenn auch die FDA den Impfstoff zulässt.

Corona-Impfstoff
EU-Kommission bleibt gegenüber AstraZeneca auf Konfrontationskurs

90 oder 62 Prozent Wirksamkeit?
Erste Wirksamkeitsdaten zum Corona-Impfstoff von AstraZeneca
„AstraZeneca bereitet COVID-19-Impfstoff für FDA-Antrag vor – mit 79 Prozent Wirksamkeitsrate“, titelte das Nachrichtenportal „Fierce Pharma“ am 22. März. Demnach erwartet AstraZeneca, seinen Antrag in der ersten April-Hälfte bei der FDA einzureichen – sobald die (Notfall-)-Zulassung erteilt werde, sollen 30 Millionen Dosen schnell ausgeliefert werden. Die US-Versorgung werde in den USA produziert und sei somit von den Versorgungsengpässen in anderen Ländern nicht betroffen.
Allerdings gab es bei dieser Nachricht einen Haken. Am 23. März veröffentlichte das „National Institute of Allergy an Infectious Disease“ (NIAID) ein Statement:
Am späten Montag meldete das Data and Safety Monitoring Board (DSMB) dem NIAID, BARDA und AstraZeneca, dass es über die von AstraZeneca veröffentlichten Informationen zu den ersten Daten aus der klinischen Studie mit dem Impfstoff COVID-19 besorgt sei. Das DSMB drückte seine Besorgnis darüber aus, dass AstraZeneca möglicherweise veraltete Informationen aus dieser Studie einbezogen hat, die ein unvollständiges Bild der Wirksamkeitsdaten vermittelt haben könnten. Wir fordern das Unternehmen auf, mit dem DSMB zusammenzuarbeiten, um die Wirksamkeitsdaten zu überprüfen und sicherzustellen, dass die genauesten und aktuellsten Wirksamkeitsdaten so schnell wie möglich veröffentlicht werden.“
NIAID, 23. März 2021
In den Medien wurde diese öffentliche Rüge gerne aufgegriffen und von verschiedenen Expert:innen als durchaus bemerkenswert wahrgenommen. Doch wurden damit in der Bevölkerung nur wieder „unnötige“ Zweifel gesät? Tatsächlich hatte auch das NIAID bereits am 22. März in einer Mitteilung verkündet: „Die Ergebnisse einer großen klinischen Studie in den USA und Südamerika zeigen, dass der COVID-19-Impfstoff von AstraZeneca, AZD1222, gut verträglich ist und vor symptomatischer COVID-19-Erkrankung schützt, einschließlich schwerer Erkrankungen oder Krankenhausaufenthalten. Das unabhängige Data and Safety Monitoring Board (DSMB), das die Studie überwacht, hat keine Sicherheitsbedenken in Bezug auf den Impfstoff festgestellt.“






















1 Kommentar
Astrazeneca
von Uwe Schalhorn am 05.04.2021 um 11:32 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.