
- DAZ.online
- News
- Spektrum
- COVID-19-Impfstoff von ...
Sicher und wirksam, aber kontrovers
COVID-19-Impfstoff von AstraZeneca – kommt bald die Zulassung in den USA?
Stuttgart - 26.03.2021, 07:00 Uhr
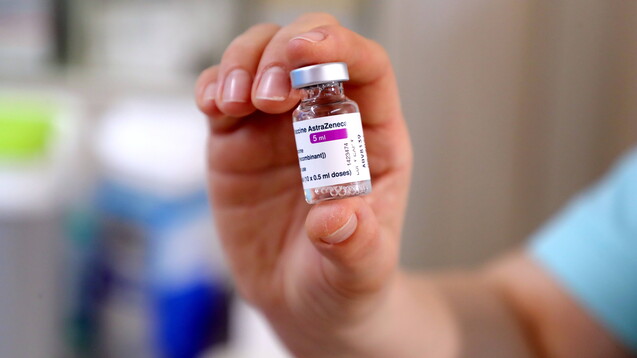
Ursprünglich zählte auch AstraZeneca zu den fünf aussichtsreichsten Corona-Impfstoff-Kandidaten in den USA („Operation Warp Speed“). Doch Berichte der „New York Times“ verraten, dass es schon früh Patzer vonseiten AstraZenecas gab, die zum Vertrauensverlust der US-Zulassungsbehörden führten. (Foto: IMAGO / Eastnews)
AstraZeneca und sein COVID-19-Impfstoff haben es nicht leicht – oder sollte man besser sagen, AstraZeneca macht es seinem Corona-Impfstoff nicht leicht? Während es in Europa vor allem Kontroversen über die Lieferfähigkeit gibt – von möglichen seltenen Nebenwirkungen einmal abgesehen – haben in den USA wohl kommunikative Probleme dazu geführt, dass der Impfstoff es dort noch immer nicht zur Zulassung geschafft hat. Doch auch in den USA spricht man von einem wahrscheinlich sehr guten Impfstoff.
Der Preis und die Lagerung machten den COVID-19-Impfstoff von AstraZeneca von Beginn an zu einem weltweiten Hoffnungsträger der Corona-Pandemie. Laut einem Bericht von Nature, wurde der Impfstoff bereits in 100 Ländern zugelassen – allerdings nicht in den USA. Dies führte zuletzt immer wieder zu verwirrender Berichterstattung in den Medien. Aber auch schon zuvor gab es auch außerhalb der USA viel mediales Chaos rund um die kommunizierten Wirksamkeitsdaten von AstraZeneca, was – genauso wie neue potenzielle Sicherheitsbedenken – den Impfstoff aber nie in echten Misskredit gebracht hat. Es folgte auf jeden Verdacht bislang immer eine Art „Freispruch“.
Mehr zum Thema
STIKO zu thromboembolischem Sicherheitssignal
AstraZeneca weiterhin entsprechend der dritten STIKO-Impfempfehlung einsetzen
Informiert entscheiden
EMA zu AstraZeneca: Nutzen bei weitem größer als die Risiken
Am Ende bleibt dennoch jedes Mal ein fader Beigeschmack, den der Impfstoff nicht mehr loszuwerden scheint. Gerade das zuletzt bekannt gewordene „Kommunikationsdesaster“ aus den USA könnte nun aber der Anfang vom Ende sein, und den Impfstoff schließlich vom faden Beigeschmack befreien. Nämlich dann, wenn auch die FDA den Impfstoff zulässt.

Corona-Impfstoff
EU-Kommission bleibt gegenüber AstraZeneca auf Konfrontationskurs

90 oder 62 Prozent Wirksamkeit?
Erste Wirksamkeitsdaten zum Corona-Impfstoff von AstraZeneca
„AstraZeneca bereitet COVID-19-Impfstoff für FDA-Antrag vor – mit 79 Prozent Wirksamkeitsrate“, titelte das Nachrichtenportal „Fierce Pharma“ am 22. März. Demnach erwartet AstraZeneca, seinen Antrag in der ersten April-Hälfte bei der FDA einzureichen – sobald die (Notfall-)-Zulassung erteilt werde, sollen 30 Millionen Dosen schnell ausgeliefert werden. Die US-Versorgung werde in den USA produziert und sei somit von den Versorgungsengpässen in anderen Ländern nicht betroffen.
Allerdings gab es bei dieser Nachricht einen Haken. Am 23. März veröffentlichte das „National Institute of Allergy an Infectious Disease“ (NIAID) ein Statement:
Am späten Montag meldete das Data and Safety Monitoring Board (DSMB) dem NIAID, BARDA und AstraZeneca, dass es über die von AstraZeneca veröffentlichten Informationen zu den ersten Daten aus der klinischen Studie mit dem Impfstoff COVID-19 besorgt sei. Das DSMB drückte seine Besorgnis darüber aus, dass AstraZeneca möglicherweise veraltete Informationen aus dieser Studie einbezogen hat, die ein unvollständiges Bild der Wirksamkeitsdaten vermittelt haben könnten. Wir fordern das Unternehmen auf, mit dem DSMB zusammenzuarbeiten, um die Wirksamkeitsdaten zu überprüfen und sicherzustellen, dass die genauesten und aktuellsten Wirksamkeitsdaten so schnell wie möglich veröffentlicht werden.“
NIAID, 23. März 2021
In den Medien wurde diese öffentliche Rüge gerne aufgegriffen und von verschiedenen Expert:innen als durchaus bemerkenswert wahrgenommen. Doch wurden damit in der Bevölkerung nur wieder „unnötige“ Zweifel gesät? Tatsächlich hatte auch das NIAID bereits am 22. März in einer Mitteilung verkündet: „Die Ergebnisse einer großen klinischen Studie in den USA und Südamerika zeigen, dass der COVID-19-Impfstoff von AstraZeneca, AZD1222, gut verträglich ist und vor symptomatischer COVID-19-Erkrankung schützt, einschließlich schwerer Erkrankungen oder Krankenhausaufenthalten. Das unabhängige Data and Safety Monitoring Board (DSMB), das die Studie überwacht, hat keine Sicherheitsbedenken in Bezug auf den Impfstoff festgestellt.“
Ein Fehler auf beiden Seiten?
Das National Institute of Allergy and Infectious Diseases (NIAID) gehört nach eigenen Angaben zu den National Institutes of Health. Das NIAID und die Biomedical Advanced Research and Development Authority (BARDA), die zum Office of the Assistant Secretary for Preparedness and Response des U.S. Department of Health and Human Services gehöre, unterstützten die AstraZeneca-Studie finanziell im Rahmen des Bundesprogramms COVID-19, heißt es. Und: „AZD1222 zeigte eine statistisch signifikante Wirksamkeit des Impfstoffs von 78,9 Prozent bei der Vorbeugung von symptomatischem COVID-19 und eine 100-prozentige Wirksamkeit bei der Vorbeugung von schwerer oder kritischer Erkrankung und Krankenhauseinweisung. Bei Teilnehmern ab 65 Jahren, die 20 Prozent der Studienpopulation ausmachten, betrug die Impfstoffwirksamkeit gegen symptomatische COVID-19 79,9 Prozent.“
Diese Zahlen entsprechen der Mitteilung von AstraZeneca vom 22. März, die der NIAID am 23. März aber kritisiert. Auch die Aussage, dass das DSMB (Data and Safety Monitoring Board) in der Studie die in Europa bekannt gewordenen thrombotischen Ereignisse und zerebralen Sinusthrombosen (CVST) überprüft hat und kein erhöhtes Risiko für diese Erkrankungen bei den geimpften Teilnehmer:innen fand, steht sowohl in der Mitteilung von AstraZeneca als auch in der vom NIAID.
Wirksamkeit von 69 bis 74 Prozent
Laut dem Nature-Bericht verfügt die „Washington Post“ über einen Brief, in dem das DSMB dem NIAID aber mitteilt, dass es AstraZeneca aufgefordert habe, stattdessen eine Wirksamkeit von 69 bis 74 Prozent zu kommunizieren, die auf aktuelleren Daten basiere. AstraZeneca reagierte prompt am 23. März auf die öffentliche Rüge und teilte mit, sich mit dem DSMB in Verbindung zu setzen. Innerhalb von 48 Stunden wollte man die neuen Ergebnisse verkünden.
Nun hat AstraZeneca am 25. März neue Ergebnisse in einer Pressemitteilung bekannt gegeben. Die Ergebnisse beziehen sich demnach auf 49 zusätzliche symptomatische COVID-19-Fälle. Das hat dazu geführt, dass die Wirksamkeit, eine symptomatische COVID-19-Infektion zu verhindern nun nur noch mit 76 Prozent angegeben wird (Konfidenzintervall 68 bis 82 Prozent). Die Ergebnisse seien über alle Altersgruppen hinweg vergleichbar gewesen, bei Erwachsenen ab 65 Jahren wird die Wirksamkeit mit 85 Prozent (Konfidenzintervall: 58 bis 95 Prozent) angegeben. Die 100-prozentige Wirksamkeit bei der Vorbeugung von schwerer oder kritischer Erkrankung und Krankenhauseinweisung wird erneut bestätigt. Es habe acht solcher schweren Fälle gegeben und alle seien in der Placebo-Gruppe aufgetreten. Die Zahlen könnten sich nun immer noch leicht ändern heißt es, weil es 14 weitere Fälle gebe, über die noch nicht entschieden wurde.
Laut Nature hofft Stephen Evans, ein Biostatistiker an der London School of Hygiene & Tropical Medicine, nun, dass die FDA den Ruf des Impfstoffs wiederherstellt. Im Gegensatz zu anderen Aufsichtsbehörden nutze die FDA die Rohdaten der Studien für ihre eigene Analyse. Evans erwartet, dass die FDA den Impfstoff schließlich zulassen wird.
Harsche Worte
Im US-amerikanischen Fernsehen hatte auch Anthony S. Fauci, der NIAID-Direktor, die Vorgänge eingeordnet. Er bezeichnete die Nachricht der DSMB an AstraZeneca als Reaktion auf deren Pressemitteilung, bei der er offenbar im Cc stand, als „rather harsh“ (barsch). Die Absicht des DSMB sei lediglich gewesen, dass AstraZeneca klarstellen sollte, dass die Daten der Pressemitteilung „ein wenig“ irreführend sein könnten. Daraufhin habe der NIAID seine Mitteilung am 23. März veröffentlicht. AstraZeneca habe sich mit seiner ersten Pressemitteilung unnötig selbst geschadet, denn Fauci meint, dass es sich sehr wahrscheinlich um einen sehr guten Impfstoff handelt. Letztlich zeige der ganze Vorfall aber, dass die Sicherungssysteme funktionierten. Schließlich verweist auch Fauci mit großem Nachdruck auf die FDA. Sie werde sich am Ende unabhängig jedes Detail der Daten selbst anschauen und sich nicht auf die Interpretation von anderen verlassen. Er meint, das solle vor allem die amerikanische Bevölkerung bedenken, und wohl auch der Rest der Welt.
Mehr zum Thema

Operation Warp Speed
USA: Die fünf aussichtsreichsten COVID-19-Impfstoffkandidaten
Ursprünglich zählte auch AstraZeneca zu den fünf aussichtsreichsten Corona-Impfstoff-Kandidaten in den USA („Operation Warp Speed“). Doch Berichte der „New York Times“ verraten, dass es schon früh ähnliche Patzer vonseiten AstraZenecas gab, die zum Vertrauensverlust der US-Zulassungsbehörden führten. Die aktuellen Geschehnisse könnten also nur eine Fortsetzung dessen sein.
Bis es zur Zulassung in den USA kommt, könnten die aktuellen Sicherheitsbedenken in Europa (Hirnvenenthrombosen und Thrombopenien) schon geklärt sein. Die EMA hat für den 29. März erneut eine Ad-hoc-Expertengruppe einberufen. Externe Expert:innen aus den Bereichen Hämatologie (Thrombose und Hämostase), kardiovaskuläre Medizin, Infektionskrankheiten, Virologie, Neurologie, Immunologie und Epidemiologie sollen zusammenkommen, um den Pharmakovigilanzausschuss der EMA zu beraten. Man ist laut einer aktuellen Mitteilung der EMA noch immer auf der Suche nach einem plausiblen Mechanismus, um die möglicherweise durch den Impfstoff ausgelösten Nebenwirkungen zu erklären.





















1 Kommentar
Astrazeneca
von Uwe Schalhorn am 05.04.2021 um 11:32 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.