
- DAZ.online
- News
- Pharmazie
- EMA schätzt: Ein zusä...
NDMA in Valsartan
EMA schätzt: Ein zusätzlicher Krebsfall pro 5000 Patienten
Stuttgart - 02.08.2018, 17:45 Uhr

Die EMA hat sich zum Valsartan-Fall am 2. August erneut geäußert und benennt das Patienten-Risiko mit geschätzten Zahlen. ( r/ Foto: Matt Crossick / imago)
Welches Risiko geht vom NDMA im Valsartan des chinesischen Wirkstoffherstellers Zhejiang Huahai Pharmaceuticals aus? Nach der FDA nennt seit heute auch die Europäische Arzneimittelagentur EMA Zahlen. Pro 5000 Patienten, die die betroffenen Präparate in der 320-mg-Dosierung über sieben Jahre täglich eingenommen haben, könnte einer vorläufigen Auswertung zufolge ein zusätzlicher Krebsfall auftreten. Die gute Nachricht: Außer Valsartan soll kein weiterer Wirkstoff dieses Herstellers von der Verunreinigung betroffen sein.
Dem NDMA-Risiko einen Namen gab vergangene Woche als erste Institution die Arzneimittelkommission der Apotheker (AMK). In einer vorläufigen Stellungnahme, auf Basis der vom ZL in Stichproben gemessenen Werte und der daraus resultierenden Abschätzung der maximalen täglichen Belastung, hat die AMK einen Risikoscore, den sogenannten Margin of Exposure, ermittelt, dessen Höhe als besorgniserregend einzustufen sei, wie es hieß.
Mehr zum Thema
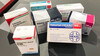
Erste Analyseergebnisse
Deutlich erhöhte Belastung durch NDMA in Valsartan-Präparaten

Zentrallaboratorium Deutscher Apotheker
NDMA bei Stichproben in Valsartan-Tabletten nachgewiesen
Eine Bewertung aus toxikologischer Sicht
Wie gefährlich ist NDMA in Valsartan?
Ebenfalls noch in der vergangenen Woche äußerte sich dann auch die FDA, die US-amerikanische Arzneimittelbehörde, zu dem Thema und nahm eine Risikoeinschätzung mit weniger abstrakten Zahlen vor als die AMK. Den Schätzungen der FDA-Wissenschaftler zufolge tritt bei 8000 Patienten, die über einen Zeitraum von vier Jahren täglich 320 mg des verunreinigten Valsartans eingenommen haben, ein zusätzlicher Krebsfall auf.
Neue Stellungnahme der EMA
In ihrer heutigen Stellungnahme schreibt nun auch die EMA, dass NDMA sowohl in manchen Lebensmitteln als auch in Wasser vorkommen kann, jedoch voraussichtlich keinen Schaden verursacht, wenn es in sehr geringen Mengen aufgenommen wird. Bezüglich des NDMA-Risikos in den zurückgerufenen Valsartan-Präparaten schätzt nun die EMA das Risiko auf Basis vorläufiger Auswertungen wie folgt ein: Es könnte zu einem zusätzlichen Krebsfall pro 5000 betroffenen Patienten kommen, die über sieben Jahre täglich das verunreinigte Valsartan in der (höchsten) 320-mg-Dosierung eingenommen haben.
Kein „unmittelbares“ Risiko und keine weiteren Wirkstoffe betroffen
Die EMA stützt diese Schätzung auf Durchschnittswerte der Verunreingung, die im Valsartan von Zhejiang Huahai Pharmaceuticals (60 parts per million) gefunden wurden. Das mögliche Krebsrisiko wurde wiederum von Tierstudien ausgehend extrapoliert und solle im Zusammenhang mit dem grundsätzlichen Risiko im Leben an Krebs zu erkranken betrachtet werden. Außerdem solle man auch die NDMA-Exposition durch andere Quellen bedenken. Die vorläufige Schätzung der EMA geht davon aus, dass die NDMA-Menge im Wirkstoff der Menge in den fertigen Präparaten entspricht. Konkrete Zahlen über die tatsächliche NDMA-Menge in den Endprodukten liegen somit immer noch nicht vor. Der Zeitplan des EMA-Verfahrens kann im Internet eingesehen werden.
Weiterhin weist die EMA darauf hin, dass kein unmittelbares Risiko für die Patienten bestehe. Patienten sollten zwar von Valsartan zu einem anderen Präparat wechseln, wer dies aber noch nicht getan hat, sollte Valsartan nicht einfach absetzen, ehe er nicht ein Ersatzpräparat erhalten hat. Laut EMA sollen in der EU mehrere Valsartan-Präparate, die nicht vom Rückruf betroffen sind, weiterhin erhältlich sein. Alle verunreinigten Valsartane von Zhejiang Huahai Pharmaceuticals wurden EU-weit zurückgerufen.
Mehr zum Thema

NDMA-Verunreinigung
Valsartan: FDA jongliert mit nicht nachvollziehbaren Zahlen zum Krebsrisiko

NDMA-Verunreinigung
Das Kontrollversagen in der Valsartan-Affäre

Eine etwas andere Herangehensweise zur Einordnung des gesundheitlichen Risikos
Valsartan, Nelfinavir und der Umgang mit genotoxischen Verunreinigungen
Die EMA beschreibt NDMA immer noch als „unerwartete“ (unexpected) Verunreinigung. Man „glaube“ (believed to), dass sie als Nebenprodukt entstanden ist, nachdem Zhejiang Huahai 2012 Änderungen im Produktionsprozess vorgenommen hat. Jedoch seien keine anderen Wirkstoffe aus der Produktion von Zhejiang Huahai von der Verunreinigung betroffen.




















9 Kommentare
nachweislich sichere Medikamente
von Kritiker am 05.08.2018 um 8:04 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Spitze des Eisbergs?
von Kritiker am 03.08.2018 um 11:28 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Spitze des Eisbergs
von Heiko Barz am 03.08.2018 um 12:58 Uhr
AW: Spitze des Eisbergs
von Kritiker am 03.08.2018 um 14:07 Uhr
Was bedeutet das?
von Ichhabeaberpanik am 03.08.2018 um 0:43 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
EMA + FDA
von Bernd Küsgens am 02.08.2018 um 19:43 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Keine Panik !!
von Bernd Küsgens am 02.08.2018 um 19:39 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Bezug des Wirkstoffs vom Hersteller -wie lange schon?
von Betroffene Patientin am 02.08.2018 um 18:29 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Bezug des Wirkstoffs vom Hersteller -wie
von Clodo am 02.09.2018 um 22:56 Uhr
Das Kommentieren ist aktuell nicht möglich.