
- DAZ.online
- News
- Pharmazie
- Widersprüchliches zu ...
Beschleunigte Zulassung bei der FDA?
Widersprüchliches zu Remdesivir – hilft es bei COVID-19?
Stuttgart - 30.04.2020, 16:30 Uhr
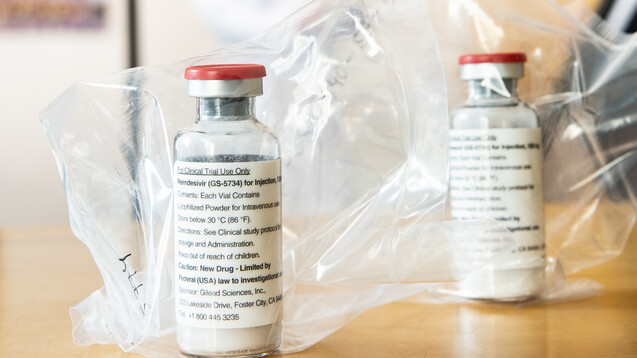
Die Studiendaten zu Remdesivir bei COVID-19 sind widersprüchlich. (m / Foto: picture alliance/Ulrich Perrey/dpa-POOL/dpa)
Hilft Remdesivir gegen COVID-19? Diese Frage beschäftigt die Welt als potenzielle Patienten, Gilead als Pharmaunternehmen hinter dem Virostatikum und Forscher auf der Suche nach einem ersten Wirkstoff gegen Corona. Studien laufen, erste Daten aus China, publiziert im Lancet, und Vorabauswertungen der NIH-Studie in den USA sind widersprüchlich. Dennoch soll das Arzneimittel Medienberichten zufolge in einem Eilverfahren bei der FDA zugelassen werden.
Remdesivir gilt als einer der Hoffnungsträger bei virostatischen Arzneimitteln gegen das neuartige Coronavirus SARS-CoV-2. Ursprünglich wurde der RNA-Polymeraseinhibitor zur Behandlung von Ebola erforscht, nun wird Remdesivir forciert bei COVID-19 untersucht. Derzeit laufen mehrere Studien, unter anderem in China und den USA. Zwei neue Berichte haben widersprüchliche Ergebnisse über die potenzielle Wirksamkeit von Remdesivir erbracht.
Eher entmutigende Resultate einer chinesischen Untersuchung wurden am 29. April 2020 im Lancet veröffentlicht: Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial.
Am selben Tag ging auch das Nationale Gesundheitsinstitut NIH (National Institut of Health) mit vorläufigen, doch eher zuversichtlichen Daten an die Öffentlichkeit: NIH Clinical Trial Shows Remdesivir Accelerates Recovery from Advanced COVID-19. Als Teil des NIH untersucht das National Institute of Allergy and Infectious Diseases (NIAID) Remdesivir in der ersten klinischen Studie (Adaptive COVID-19 Treatment Trial, ACTT ) in den Vereinigten Staaten und sponsert diese auch.
Zusätzlich gab Gilead, das pharmazeutische Unternehmen hinter Remdesivir, bekannt, dass es nun auch Daten zur Therapiedauer aus einer vom Unternehmen finanzierten Open-Label-Phase-3-Studie (SIMPLE) an Patienten mit schwerer COVID-19-Krankheit gibt.
RKI-Chef: Noch keine endgültige Aussage möglich
Zurückhaltung oder Zuversicht – was ist geboten bei Remdesivir? Die „Ergebnisse“ sind nicht kongruent. Der Präsident des Robert-Koch-Instituts, Lothar Wieler, erklärte in der am heutigen (30. April 2020) RKI-Pressekonferenz zu Remdesivir: „Die Daten machen einen positiven Eindruck, aber es sind noch nicht genügend Daten da, um eine endgültige Aussage zu treffen.“ US-Präsident Donald Trump ist „The Wall Street Journal“ zufolge interessiert, schnellstmöglich eine Zulassung für Remdesivir zu erreichen. Trump dränge die U.S. Food and Drug Administration, die Notfallgenehmigung für das Gilead-Medikament zu erteilen.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.