
- DAZ.online
- News
- Pharmazie
- Remdesivir auf Vorrat
COVID-19
Remdesivir auf Vorrat?
Stuttgart - 16.07.2020, 07:00 Uhr
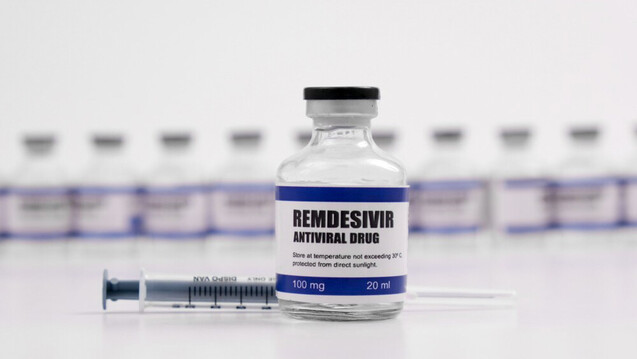
Bei Remdesivir geht nichts den normalen Weg, auch die Beschaffung des ersten COVID-19-Arzneimittels erfolgt nur über ausgewählte Krankenhausapotheken. (m / Foto: Kunal / stock.adobe.com)
Bedingt zugelassen ist Remdesivir seit kurzem auch in Deutschland verfügbar. Dennoch werden die meisten Apotheker mit dem ersten COVID-19-Arzneimittel nicht in Berührung kommen, die Verteilung steuert STAKOB zentral und zunächst nur für ausgewählte Kliniken. Wie läuft der Weg von Remdesivir? Und können sich Krankenhäuser jetzt schon für eine potenziell zweite Welle rüsten und bevorraten, wie bei Intensivarzneimitteln? DAZ.online hat mit Professor Hans-Peter Lipp von der Uniklinikapotheke Tübingen gesprochen sowie beim BMG und bei Gilead nachgefragt.
Die EU-Kommission hat das erste Arzneimittel gegen COVID-19 am 3. Juli auch in der EU zugelassen, zumindest „bedingt“. Der Überprüfungsprozess bei der Europäischen Arzneimittel-Agentur EMA lief schnell: Die CHMP-Empfehlung zur Zulassung erfolgte knapp drei Wochen nachdem Gilead die Zulassungsunterlagen eingereicht hatte, und nur wenige Tage darauf folgte sodann das „Go“ der Kommission.
Doch damit ist die „Extra Wurst“ von Remdesivir nicht gegessen – denn auch der Bezug des Virostatikums läuft alles andere als „normal“ – nicht jede Apotheke darf bestellen, und das Arzneimittel wird – außer bei Härtefallprogrammen oder Studienware – nicht beim Hersteller Gilead geordert.
Mehr zum Thema

Erstes COVID-19-Arzneimittel
Remdesivir erhält Zulassung in Europa
Arzneimittel bei COVID-19
Wo stehen wir bei Remdesivir?
DAZ.online hat bei Gilead, dem Bundesgesundheitsministerium (BMG) und bei Professor Hans-Peter Lipp, Chef der Universitätsklinikapotheke Tübingen, nachgefragt. Wie funktioniert die Versorgung mit Remdesivir – können Kliniken wirklich nur über das BMG an Remdesivir kommen? Und vor allem: Können sich Krankenhäuser jetzt bereits für eine mögliche zweite Coronawelle rüsten und Remdesivir bevorraten?
Studie, Härtefallprogramm und STAKOB
„Remdesivir ist in Deutschland aktuell auf drei Wegen verfügbar“, erklärt Professor Lipp. Für klinische Studien liefere der Hersteller Gilead das Arzneimittel, ebenso für den Einsatz bei Härtefallprogrammen. Ein weiterer Bezug erfolge über die STAKOB (Ständiger Arbeitskreis der Kompetenz- und Behandlungszentren für Krankheiten durch hochpathogene Erreger) im Rahmen der vorübergehenden Ausnahmeregelung nach der AMG-Zivilschutzausnahmeverordnung, so der Chefapotheker. Allerdings wurde nicht jede Krankenhausapotheke oder krankenhausversorgende Apotheke Deutschlands im STAKOB-Programm versorgt, sondern nur „ausgewählte“.
Der Weg des Remdesivir
Auf Nachfrage der Redaktion erläutert das BMG den Weg, den Remdesivir nimmt. So habe Gilead noch vor EMA-Zulassung eine limitierte Menge zusätzlicher Behandlungseinheiten an Remdesivir über die Bundesregierung auf der Grundlage einer vorübergehenden Ausnahmeregelung nach der AMG-Zivilschutzausnahmeverordnung verfügbar gemacht. Dieses Remdesivir stelle das BMG nun „über Krankenhausapotheken den Kliniken zur Anwendung bei erkrankten COVID-19 Patientinnen und Patienten, die von einer solchen Therapie profitieren könnten, zur Verfügung“, erklärt eine Sprecherin des Ministeriums.
Die Verteilung von Remdesivir erfolge kostenlos, von zentraler Stelle und auf Grundlage eines etablierten Verteilkonzeptes an „ausgewählte Apotheken von Universitätskliniken und STAKOB-Behandlungszentren auf deren konkrete Bestellung“. Von einer dieser Apotheken könnten dann wiederum weitere Krankenhausapotheken und krankenhausversorgenden Apotheken Remdesivir zur Therapie erhalten.
Kriterien für Remdesivir-Order
Welche Kriterien erfüllt sein müssen, um Remdesivir einsetzen zu können, hat die STAKOB zusammengefasst:
- Labordiagnostisch oder klinische//epidemiologisch bestätigte Infektion durch SARS-CoV-2
- Vorliegen eines schweren Erkrankungsgrades:
- Periphere Sauerstoffsättigung </= 94 Prozent unter Raumluft oder Notwendigkeit einer Sauerstoffgabe ODER
- Notwendigkeit einer nicht invasiven oder invasiven Beatmungstherapie, inklusive ECMO
- Dei Behandlung mit Remdesivir sollte möglichst früh im Erkrankungsverlauf begonnen werden, der Einsatz > 10 Tage nach Symptombeginn bringt vermutlich keinen Benefit.
Bei Professor Lipp fordern Krankenhäuser, die in seinen Zuständigkeitsbereich fallen, Remdesivir „patientenindividuell“ an, dann würden Patientendaten und Krankheitsstadium gecheckt und der Transport organisiert. „Klappt ohne Probleme“, so der erfahrene Klinikapotheker. Die Ordermenge richtet sich nach Schwere der Erkrankung: Remdesivir wird bei Patienten ohne invasive Beatmungstherapie oder ECMO über insgesamt fünf Tage (gegebenenfalls mit einer Verlängerung auf insgesamt zehn Tage) und bei Patienten mit invasiver Beatmungstherapie oder ECMO über insgesamt zehn Tage verabreicht. Für die Dosierung gilt jeweils eine Loading-Dose mit 200 mg Remdesivir intravenös am ersten Behandlungstag, gefolgt von einer Erhaltungsdosis von 100 mg i.v. Remdesivir einmal täglich über weitere vier beziehungsweise neun Tage. Diese Kriterien hatte das RKI (mit Unterstützung der STAKOB) jüngst nach Sichtung der aktuellen Datenlage zu Remdesivir veröffentlicht.
Hamstern unmöglich
DAZ.online wollte auch wissen: Können sich Kliniken jetzt schon bevorraten, zum Beispiel für eine etwaige zweite Welle gegen Ende des Jahres? Doch hier gibt es ein klares „nein“: „Eine Bevorratung ist momentan nicht möglich. Die Zuteilung von Remdesivir soll nur den unmittelbaren Bedarf decken und hängt vom weltweiten Zulassungsstatus von Remdesivir und der allgemeinen epidemiologischen Entwicklung der COVID-19-Pandemie ab“, sagt Gilead dazu.
Mehr zum Thema

Erstes Arzneimittel gegen COVID-19
USA horten Remdesivir – was sagt die Bundesregierung?
Nach Bevorratung der USA
EU will sich Remdesivir ebenfalls sichern

Gilead vergibt Lizenzen
Remdesivir wird generisch
Auch Professor Lipp erklärt: „Eine Hamsterbevorratung geht gar nicht!“, entwickle sich ein Zentrum zum neuen COVID-19-Hotspot, werde eine Nachlieferung von Remdesivir über die STAKOB in Aussicht gestellt.
Reicht Remdesivir?
Jüngst sorgte die Nachricht, die Vereinigten Staaten hätten sich mehr als 500.000 Remdesivir-Behandlungen (beziehungsweise die Option hierauf) gesichert, für Unmut und Bauchschmerzen. 500.000 Behandlungen entsprechen 100 Prozent der geplanten Produktionsmenge für Juli sowie jeweils 90 Prozent für August und September. Gibt es Bedenken, dass Remdesivir „ausgeht“? Das BMG gibt sich optimistisch und baut auf eine positive Entwicklung der Pandemie: „Aufgrund der derzeit günstigen epidemiologischen Entwicklung der COVID-19-Pandemie in Deutschland mit einem Rückgang der Erkrankungs- und Hospitalisierungszahlen steht Remdesivir zurzeit in ausreichender Menge für die zugelassene Indikation zur Verfügung“, erklärt die Ministeriumssprecherin.




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.