
- DAZ.online
- News
- Pharmazie
- Adalimumab wird ...
Zum Patentablauf von Humira
Adalimumab wird patentfrei: Das Wichtigste über den Blockbuster
Stuttgart - 16.10.2018, 13:45 Uhr
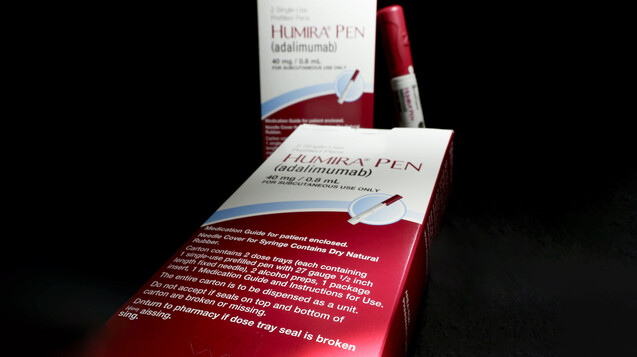
In der EU ist das Patent für Humira nun abgelaufen, in den USA kann Abbvie den Wirkstoff noch exklusiv vertreiben. ( r / Foto: picture alliance / AP Photo)
In der Europäischen Union läuft um Mitternacht das Patent des weltweit umsatzstärksten Arzneimittels, Humira®, ab. Pünktlich zu dem Termin hat die Novartis-Tochter Sandoz auch ihren Patentstreit mit Orginalhersteller AbbVie beigelegt, der Einführung der Adalimumab-Biosimilars steht also nichts mehr in Wege. Anlass genug, den Wirkstoff noch einmal vorzustellen.
Im September 2003 erhielt Humira® (Wirkstoff Adalimumab) die Zulassung in der Europäischen Union. Monoklonale Antikörper gab es zwar vorher schon. Aber anders als diese wurde Adalimumab mithilfe der Phagen-Display-Technology aus einer Bank humaner Immunglobulinsequenzen identifiziert und war somit der erste vollständig humane Antikörper auf dem Markt. Für die wissenschaftlichen Grundlagen dafür gab es 2018 den Chemie-Nobelpreis.
Entwickelt wurde der Wirkstoff ursprünglich von der BASF gemeinsam mit Cambridge Antibody Technology unter dem Namen D2E7 als Hoffnungsträger gegen Rheuma. Das Unternehmen entschloss sich aber im Jahr 2000 seine Pharmasparte inklusive D2E7, das sich damals in Phase-III-Studien befand, an den US-Konzern Abbot zu verkaufen. Das jährliche Umsatzpotenzial sah man bei einer Milliarde Dollar – also durchaus Blockbuster-tauglich. Allerdings hatte BASF Medienberichten zufolge Bedenken, das ohne Partner realisieren zu können. Für knapp 7 Milliarden Dollar war BASF seine Pharmasparte dann los. Abbott entwickelte die Substanz weiter und brachte sie schließlich als Humira® auf den Markt. Seit 2013 führt es die Liste der umsatzstärksten Arzneimittel an. 2016 machte Originalhersteller AbbVie, ein Unternehmen, das als Abspaltung von Abbott Laboratories gegründet wurde, mit Humira® weltweit 16 Milliarden US-Dollar Umsatz. Allein im deutschen GKV-Markt waren es laut dem Wissenschaftlichen Institut der AOK (WIdO) bis 2017 8,1 Milliarden Euro, die Abbvie mit dem Mittel umsetzte.
Mehr zum Thema

Ilse Zündorf und Theo Dingermann kommentieren den diesjährigen Chemie-Nobelpreis
Alles „nur“ eine Momentaufnahme
Das Beste aus 2017
Diese „mabs“ sollten Apotheker kennen
Erst nur bei rheumatoider Arthritis
Die ursprüngliche Zulassung beschränkte sich auf die Behandlung der rheumatoiden Arthritis bei Erwachsenen in Kombination mit Methotrexat oder als Monotherapeutikum. Mittlerweile ist Adalimumab bei zahlreichen Autoimmunerkrankungen zugelassen, darunter Morbus Crohn, Psoriasis oder Ankylosierende Spondylitis. In einigen Indikationen, zum Beispiel bei polyartikulärer juveniler idiopathischer Arthritis, kann der Wirkstoff bereits ab einem Alter von zwei Jahren eingesetzt werden.
So wirkt Adalimumab
Der humane monoklonale IgG1-Antikörper besteht aus 1330 Aminosäuren und hat ein Molekulargewicht von etwa 148 kDa. Hergestellt wird er in CHO-Zellen. Er bindet spezifisch an den Tumornekrosefaktor alpha (TNF-alpha) und neutralisiert dessen biologische Funktion, indem es die Interaktion mit den zellständigen p55- und p75-TNF-Rezeptoren blockiert. Adalimumab beeinflusst dadurch biologische Reaktionen, die durch TNF ausgelöst oder gesteuert werden. Dazu gehört auch die Reduzierung der Konzentration von für die Leukozytenmigration verantwortlichen Adhäsionsmolekülen (ELAM-1, VCAM-1 und ICAM-1). Bei Patienten mit rheumatoider Arthritis nahm nach einer Behandlung mit Adalimumab im Vergleich zu den Ausgangswerten die Konzentration der Akute-Phase-Entzündungsparameter (C-reaktives Protein und Blutkörperchen-Senkungsgeschwindigkeit) sowie der Serumzytokine (IL-6) ab. Die Serumspiegel von Matrixmetalloproteinasen (MMP-1 und MMP-3), welche die für die Knorpelzerstörung verantwortliche Gewebsumwandlung hervorrufen, waren ebenfalls vermindert. Bei mit Adalimumab behandelten Patienten besserte sich im Allgemeinen die mit einer chronischen Entzündung einhergehende Veränderung der Blutwerte.
Rechtsstreit beendet, Biosimilars können kommen
Verabreicht wird Adalimumab subkutan, in der Erhaltungstherapie in den meisten Indikationen alle zwei Wochen 40 mg. Je nach Krankheitsbild und Ansprechen kann er aber auch wöchentlich gegeben werden. Bei einigen Anwendungsgebieten wird zudem eine Induktionsdosis empfohlen, bei Colitis ulcerosa beispielweise 160 mg in Woche 0 (als vier Injektionen innerhalb eines Tages oder als zwei Injektionen pro Tag an zwei aufeinanderfolgenden Tagen) und 80 mg in Woche 2. Resorption und Verteilung von Adalimumab sind langsam. Die maximale Serumkonzentration wird ungefähr fünf Tage nach Verabreichung erreicht. Die Halbwertszeit beträgt etwa zwei Wochen. Der Einfluss von Geschlecht und Alter auf die Adalimumab-Clearance scheint gering zu sein. Zu den häufigsten möglichen unerwünschten Wirkungen gehören Infektionskrankheiten, Reaktionen an der Injektionsstelle, Kopfschmerzen und Hautausschläge. TNF-alpha-Inhibitoren können selten schwere Infektionen und maligne Erkrankungen verursachen.
Mehr zum Thema

Pharmakonzerne
AbbVie erfolgreich dank Humira
Das Patent ist ab dem morgigen Mittwoch in der EU abgelaufen. In den USA wird das erst 2023 der Fall sein. Zahlreiche Biosimilar-Hersteller wollen nun auch ein Stück vom Kuchen. Fünf Firmen haben nach Informationen der europäischen Arzneimittebehörde EMA bereits Zulassungen für Adalimumab-Präparate erhalten. Die Unternehmen Sandoz und Amgen planen sogar, mehrere untereinander identische Adalimumab-Biopharmazeutika auf den Markt zu bringen, die sich in ihren Anwendungsgebieten unterscheiden. Weitere Pharmaunternehmen, darunter Fresenius Kabi und Pfizer, wollen ebenfalls ihren Hut in den Ring werfen. Rechtzeitig zum Stichtag hat die Novartis-Tochter Sandoz nun auch alle diesbezüglichen Rechtsstreitigkeiten mit dem Originalhersteller Abbvie beigelegt.
Wie die Deutsche Presseagentur unter Berufung auf Novartis berichtet, gewährt AbbVie Sandoz eine nicht-exklusive Lizenz für das geistige Eigentum von AbbVie an Humira, die je nach Ländern zu unterschiedlichen Zeitpunkten startet. In den meisten Ländern der Europäischen Union am 16. Oktober. Weiter heißt es, dass Sandoz AbbVie Lizenzgebühren für die Lizenzierung seiner Humira-Patente zahlen werde. AbbVie hingegen werde keine Zahlungen an Sandoz leisten, wobei die genauen Bedingungen zwischen den Parteien vertraulich seien.
Werden die GKV-Ausgaben sinken?
Die Einigung ebnet laut Novartis den Weg für die Markteinführung 2018 in wichtigen europäischen Märkten und sichere den für 2023 geplanten Markteintritt in den USA, schreibt die dpa. Sie könnte allerdings auch zu höheren Preisen führen. Das befürchtet zumindest das beim AOK-Bundesverband angesiedelte WIdO. Der Markteintritt der Biosimilars zu Humira sei durch Lizenzvereinbarungen und entsprechende Lizenzzahlungen der Hersteller an AbbVie erkauft worden, heißt es in einer Mittelung aus der vergangenen Woche. Dieser höhere Kostendruck könnte geringere Preisabschläge zur Folge haben. Große Einsparungen erwartet das WIdO ohnehin nicht. Die Arzneimittelausgaben der Krankenkassen werden trotz des einsetzenden Wettbewerbs wahrscheinlich nicht sinken, schätzt das Institut. Die Preise der Biosimilars lägen üblicherweise nur geringfügig unter denen der Originalanbieter, so das WIdO.
Ab November könnten die ersten Adalimumab-Biosimilars in der Taxe zu finden sein. Die Situation, dass mehrere Wettbewerber vor dem Stichtag marktreif sind, ist einmalig in der Geschichte der Biosimilars. In der Vergangenheit ging zwischen Patentablauf und Biosimilar-Zulassung in manchen Fällen einige Zeit ins Land.



















1 Kommentar
Das Kommentieren ist aktuell nicht möglich.