
- DAZ.online
- News
- Recht
- Bundespatentgericht: ...
Schlappe für Gilead
Bundespatentgericht: Truvada-Schutzzertifikat ist nichtig
Berlin - 23.05.2018, 13:50 Uhr
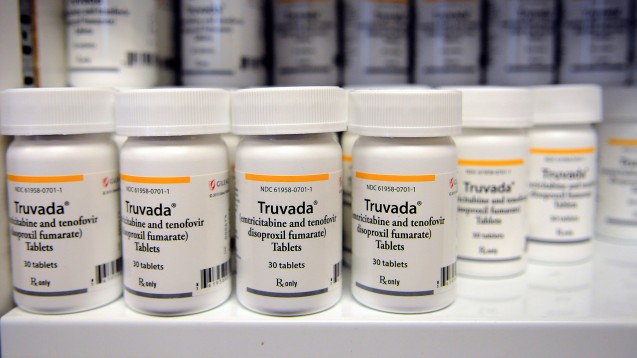
Gilead kämpft in vielen Ländern um seinen Patentschutz für Truvada. (Foto: imago)
Schon seit vergangenem Sommer sind in Deutschland Generika zum HIV-Präparat Truvada auf dem Markt. Hexal bietet sein Präparat in einem Modellprojekt zur HIV-Präexpositions-Prophylaxe sogar besonders günstig an. Dem Original-Hersteller Gilead missfällt die Konkurrenz mächtig. Er sieht sein Patent verletzt. Doch vor dem Bundespatentgericht musste das Unternehmen nun eine Schlappe hinnehmen: Denn dieses hält das ergänzende Schutzzertifikat für Truvada für nichtig. Rechtskräftig ist die Entscheidung noch nicht.
Die patentrechtliche Situation des Gilead-Präparats Truvada (Tenofovirdisoproxil + Emtricitabin), das sowohl zur HIV-Behandlung als auch zur HIV-Prä-Expositions-Prophylaxe (PrEP) zugelassen ist, ist umstritten. Während der ursprüngliche Patentschutz für den Wirkstoff Tenofovirdisoproxil im vergangenen Juli ausgelaufen ist, verweist Gilead für das Kombinationspräparat Truvada auf ein bis Februar 2020 erteiltes ergänzendes Schutzzertifikat. Dennoch sind seit Sommer 2017 diverse Generika auf den deutschen Markt gekommen, insgesamt elf sind derzeit in der Lauer-Taxe gelistet, sechs davon haben auch eine PrEP-Zulassung. Die Preise der Generika liegen deutlich unter dem des Originalpräparats. Die 30er-Packung Truvada kostet 819 Euro (Apothekenverkaufspreis), zwei Generika sind schon für rund 70 Euro zu haben. Ins Gespräch kamen die Truvada-Generika nicht zuletzt im Zusammenhang mit einem PrEP-Modellprojekt, an dem sich Apotheken deutschlandweit beteiligen. Hier ist die PrEP-Therapie für rund 50 Euro im Monat zu haben.
Mehr zum Thema
Kritik des WidO
AOK-Institut: „Wegen Gilead bleibt die HIV-Therapie teuer“

Lancet-Studie in Großbritannien
HIV-Präexpositionsprophylaxe könnte kosteneffektiv sein – irgendwann
Vier Unternehmen, die Truvada als Generikum anbieten, haben Nichtigkeitsklagen gegen das Verfügungszertifikat Gileads beim Bundespatentgericht erhoben – und waren damit nun in erster Instanz erfolgreich. Der 4. Nichtigkeits-Senat des Bundespatentgerichts hat vergangene Woche das für die Wirkstoffzusammensetzung Tenofovirdisoproxil und Emtricitabin erteilte und angegriffene Arzneimittel-Schutzzertifikat für nichtig erklärt. Damit hat er die Rechtsauffassung der klagenden Generika-Hersteller bestätigt, dass das Schutzzertifikat gar nicht hätte erteilt werden dürfen. Für Gilead heißt das: Das ausschließliche Vermarktungsrecht für Arzneimittel mit diesen Wirkstoffen ist Geschichte.
Allerdings: Ganz so schnell geht es nicht. Gegen das Urteil des Bundespatengerichts kann noch Berufung zum Bundesgerichtshof in Karlsruhe eingelegt werden.
Ein Streit in vielen Ländern – der EuGH ist bereits angerufen
Das Bundespatentgericht weist ist seiner Pressemitteilung darauf hin, dass sich derzeit europaweit Gerichte mit dem Schutzzertifikat für Truvada befassen – einschließlich des Gerichtshofs der Europäischen Union (EuGH). Letzterer wurde vom Londoner High Court of Justice angerufen. Nun müssen die Luxemburger Richter prüfen, wie die europäische Verordnung (EG) 469/2009 über das ergänzende Schutzzertifikat für Arzneimittel auszulegen ist.
Ergänzende Schutzzertifikate für Arzneimittel werden von den nationalen Ämtern erteilt, in der Bundesrepublik Deutschland ist dies das Deutsche Patent- und Markenamt.
Dem nun ergangenen Urteil ist im Juli 2017 bereits eine Eilentscheidung des Landgerichts München vorausgegangen. Damals war Gilead gegen sieben potenzielle Konkurrenten vorgegangen und wollte erreichen, dass diese keine Truvada-Generika auf den Markt bringen dürfen. Damit scheiterte das Unternehmen. Das Landgericht stützte seine Entscheidung auf einen damals abgegebenen „qualifizierten Hinweis“ des Bundespatentgerichts, dass das Schutzzertifikat nicht rechtsbeständig sei – nun hat es dieses also tatsächlich für nichtig erklärt.
Urteil des Bundespatentgerichts vom 15. Mai 2018, Az.: 4 Ni 12/17 verbunden mit 4 Ni 14/17, 4 Ni 19/17 und 4 Ni 21/17























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.