
- DAZ.online
- DAZ / AZ
- DAZ 28/2022
- Wundheilung mit ...
Phytotherapie
Wundheilung mit Birkenrinden-Extrakt
Erstmals ein Phytopharmakon bei Epidermolysis bullosa zugelassen
Birken gedeihen überwiegend in den kühlen und gemäßigten Zonen der Nordhalbkugel. Je nach Standort finden sich verschiedene Formen – von bis zu 30 Meter hohen, schlanken Bäumen bis hin zu kleinen Tundrabüschen. Die Gattung Betula aus der Familie der Betulaceae umfasst je nach Autor 40 bis 60 Arten, in Europa sind vorwiegend die weißrindige Hänge-Birke (Betula pendula) und die Moor-Birke (Betula pubescens) vertreten. Die Verwendung unterschiedlicher Pflanzenteile der Birke hat in der traditionellen Medizin verschiedener Völker eine lange Tradition, neben den Blättern spielte dabei auch schon immer die Rinde eine gewisse Rolle. Bereits Hildegard von Bingen erwähnte sie als probates Mittel zur Unterstützung der Wundheilung und auch von verschiedenen indigenen Völkern Nordamerikas wurden Zubereitungen aus Birkenrinde bei Hautverletzungen angewendet [1].
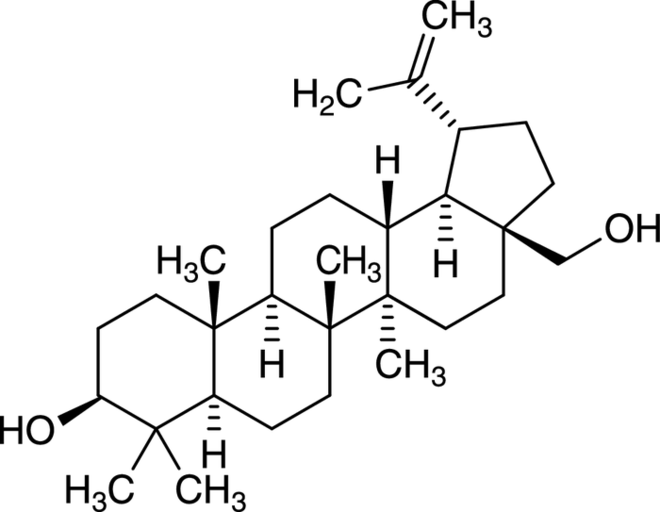
Die äußeren, weißen Korkschichten der Birkenrinde beinhalten 20 bis 30% Triterpenoide und damit die höchste Konzentration an derartigen Stoffen im gesamten Pflanzenreich. Allgemein wird angenommen, dass die enthaltenen Substanzen die Widerstandsfähigkeit der Birke gegenüber Pflanzenschädlingen erhöhen. Bereits 1788 wurde – als einer der ersten Naturstoffe überhaupt – das pentacyclische Triterpenderivat Betulin aus der Birkenrinde charakterisiert. Tatsächlich ist das Betulin (Abb. 1) die dominierende Verbindung in der Rinde, begleitet wird es von geringen Mengen weiterer Triterpene vom Oleanan- bzw. Lupantyp wie Betulinsäure, Lupeol, Erythrodiol und Oleanolsäure. Aufgrund ihrer hohen Lipophilie und damit einhergehenden schlechten Löslichkeit in polaren Lösungsmitteln gelten Triterpene allerdings trotz einiger interessanter pharmakologischer Effekte – wie z. B. der antiinflammatorischen und das Wachstum bestimmter Krebszellen hemmenden Eigenschaften der Betulinsäure – als eher ungeeignet für die Entwicklung von Arzneistoffen [2].
Anfang dieses Jahrtausends konnte jedoch gezeigt werden, dass ein mit heißem n-Heptan gewonnener, triterpenreicher Trockenextrakt aus den äußeren Korkschichten der Birkenrinde mit chemischen und pflanzlichen Ölen thixotrope Oleogele bildet, deren Festigkeit bei Körpertemperatur höher ist als bei Raumtemperatur. Der Trockenextrakt kann somit als Wirkstoff und gleichzeitig als Gelbildner fungieren, sodass eine Zubereitung ohne weitere Hilfsstoffe hergestellt werden kann [3]. Ein Oleogel aus 10% Birkenrinden-Extrakt und 90% Sonnenblumenöl wurde unter dem Namen Episalvan® patentiert (Birken GmbH, umbenannt in Birken AG 2011, Amryt AG seit 2017). Nun fehlte nur noch die geeignete Indikation, um dieses in der Tat recht innovative Oleogel vermarkten zu können. In den Folgejahren wurden zu diesem Zweck verschiedene klinische Studien durchgeführt und gleichzeitig potenzielle Wirkmechanismen, insbesondere im Hinblick auf eine mögliche Unterstützung der Wundheilung, beleuchtet.
Eine erste Pilotstudie ergab Hinweise auf eine Wirksamkeit bei Patienten mit aktinischer Keratose, allerdings ließen sich diese vielversprechenden Resultate in einer größeren Folgestudie nicht in dem Umfang bestätigen, der die Einleitung eines Zulassungsverfahrens gerechtfertigt hätte. Erfolgreicher verlief dagegen 2010 eine Untersuchung zum Einsatz bei Patienten mit chirurgischen Wunden, sogenannten Spalthautentnahmewunden. Spalthaut wird zum Zwecke der Transplantation z. B. in der plastischen Chirurgie oder zur Versorgung von Brandwunden entnommen. Durch die Entnahme entstehen leicht standardisierbare oberflächliche Wunden, die sich gut für vergleichende Untersuchungen in der Arzneistoffentwicklung eignen. Im Rahmen der Studie wurden 24 Wunden analysiert, die immer zur einen Hälfte mit Episalvan® sowie einer Wundauflage und zur anderen Hälfte mit der entsprechenden Wundauflage allein behandelt wurden. Der Vorteil dieses Designs, bei dem eine Wunde quasi geteilt und somit gleichzeitig mit verschiedenen Therapeutika versorgt werden kann, liegt darin, dass interindividuelle Unterschiede bei der Wundheilung keine Rolle spielen. Bei 20 der 24 Wunden wurde mit Episalvan® eine signifikant schnellere Heilung bei guter Verträglichkeit beobachtet. Von 2012 bis 2014 fanden dann drei größere multizentrische Studien mit einem vergleichbaren Design an insgesamt 280 Patienten statt. In zwei der Studien wurde das Präparat wiederum an Spalthautentnahmewunden untersucht, in der dritten Studie wurden Patienten mit Brandwunden des Grades IIa behandelt. Die ärztliche Begutachtung der Wunden ergab erneut eine signifikant schnellere Wundheilung von 1,8 bis 2,5 Tagen unter Verum. Zusätzlich fand eine weitere Untersuchung des Heilungsverlaufes nach drei Monaten und einem Jahr statt, die deutliche Vorteile für Episalvan® hinsichtlich der Faktoren Hautstruktur, Rötung und Pigmentierung ergab. Insgesamt ähnelte das Hautbild häufiger der gesunden Haut als in dem Bereich der Wunde, die lediglich mit einer Wundauflage versorgt worden war [4]. Diese positiven klinischen Ergebnisse bei einer Indikation mit bislang begrenzten therapeutischen Möglichkeiten führten 2016 zur Erteilung einer europäischen Zulassung für Episalvan® zur Behandlung von oberflächlichen Hautwunden (Epidermis und obere Dermis) und Verbrennungswunden der Haut des Grades IIa bei Erwachsenen, ein entsprechendes Präparat ist allerdings bisher in Deutschland nicht auf dem Markt verfügbar, nur in den Niederlanden.
Zusätzlich wurden stattdessen klinische Untersuchungen zu einer weiteren Indikation durchgeführt. In einer randomisierten Phase-III-Studie (EASE, NCT03068780) wurden 223 Patienten mit Epidermolysis bullosa entweder mit dem Birkenrinden-Extrakt-haltigen Gel (hier unter dem Namen Oleogel-S10) oder mit einem Placebo-Gel behandelt, wobei insbesondere solche Patienten von der Behandlung profitierten, die unter einer rezessiven Epidermolysis bullosa dystrophica litten (s. Müller C, Buchheit M. Mit Birkenrinden-Extrakt gegen Epidermolysis bullosa: CHMP empfiehlt Zulassung von Filsuvez®-Gel, DAZ 2022, Nr. 18, S. 26). Die Studienautoren schlussfolgerten, dass Oleogel-S10 Hinweise auf eine beschleunigte Wundheilung bei schweren Subtypen der Epidermolysis bullosa zeige und somit eine gut verträgliche Therapieoption für Patienten mit dieser schwer behandelbaren Krankheit darstelle. Dieser Einschätzung folgte nun auch die Europäische Kommission und ließ das Präparat unter der Bezeichnung Filsuvez® zur „Behandlung von partiellen Wunden im Zusammenhang mit dystrophischer und junktionaler Epidermolysis bullosa bei Patienten ab sechs Monaten“ zu. Im Unterschied dazu lehnte die FDA im Februar eine Zulassung ab und forderte das Unternehmen auf, weitere Nachweise für die Wirksamkeit von Oleogel-S10 vorzulegen.
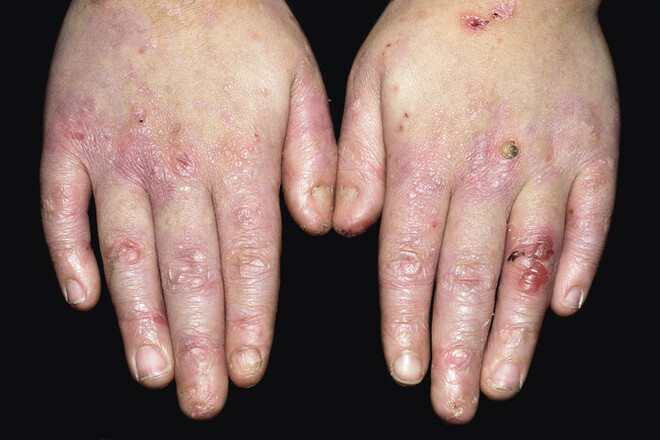
Die Epidermolysis bullosa ist eine seltene Hauterkrankung, bei der es zur Blasenbildung auf der Haut kommt, vor allem an Händen und Füßen. Möglich sind auch eine generalisierte Blasenbildung an Haut und Schleimhäuten und die Schädigung innerer Organe.
Parallel zu den klinischen Untersuchungen wurden in Kooperation mit verschiedenen universitären Forschungsgruppen mögliche Wirkmechanismen des Birkenrinden-Extraktes in unterschiedlichen Phasen der Wundheilung analysiert. Prinzipiell erfolgt die Wundheilung in drei Schritten. Nach dem Ende der Blutung setzt zunächst ein kontrollierter Entzündungsprozess ein, Cytokine und Wachstumsfaktoren werden freigesetzt, Granulozyten und Makrophagen wandern ein, verhindern im Idealfall eine bakterielle Infektion und sorgen für den Abbau abgestorbener Gewebe. Im zweiten Schritt kommt es zur Wanderung und Proliferation von Keratinozyten und Fibroblasten (Reepithelialisierung, Bildung von Granulationsgewebe) und zur Angiogenese (Bildung neuer Blutgefäße). Schließlich wird altes Kollagen erneuert und eine Narbe bildet sich aus. Für den Birkenrinden-Extrakt konnten in vitro und ex vivo Einflüsse auf verschiedene Stadien der Wundheilung nachgewiesen werden. So kommt es unter anderem zu einem zeit- und konzentrationsabhängigen Anstieg der COX-2 und IL-6 mRNA in primären humanen Keratinozyten, also zu einer Hochregulation von Mediatoren, die während der Phase der kontrollierten Entzündung eine Rolle spielen. Dieser Effekt ist allerdings temporär, sodass es nicht zu einer schädlichen Verlängerung der Entzündungsphase kommen kann. Die Hochregulation der mRNA scheint nicht durch einen Einfluss des Extraktes auf den Transkriptionsfaktor NF-κB bedingt zu sein, stattdessen wurde eine Verlängerung der Lebensdauer der mRNA beobachtet. In der zweiten Phase der Wundheilung fördert der Extrakt die Migration von humanen Keratinozyten, und zwar vermutlich durch einen Einfluss auf das Aktin-Zytoskelett. Die Effekte konnten sowohl für den Gesamtextrakt als auch für einzelne Verbindungen nachgewiesen werden, allerdings erwies sich die Hauptkomponente Betulin in einem Ex-vivo-Modell zur Wundheilung an Schweineohren als weniger wirksam als der Extrakt, sodass die Autoren schlussfolgern, dass das Zusammenspiel der einzelnen Extraktkomponenten für die Wirksamkeit wesentlich ist [5]. Insgesamt zeigt das Beispiel des Birkenrinden-Extraktes, dass der Einsatz von Naturstoffen nicht nur für die Kosmetik-Industrie interessant ist, wo Betulin (z. B. Imlan Creme, Psoriasum Betulin Creme) und ein Extrakt aus Birkenrinde (z. B. Birkenrinden Creme Resana) ebenfalls eingesetzt werden.
Im Fall von Filsuvez® konnte demonstriert werden, dass es auch heutzutage – trotz häufig kritisierter hoher Anforderungen – möglich ist, pflanzenbasierte Wirkstoffe zu entwickeln und auf der Basis solider Forschungsarbeit erfolgreich europäische Zulassungsverfahren zu durchlaufen. Ob das Phytopharmakon allerdings tatsächlich alle Hoffnungen, die insbesondere von Epidermolysis-bullosa-Patienten gehegt werden, erfüllen kann, muss die Zukunft und damit die Anwendung unter realen Alltagsbedingungen zeigen. Nach Angaben des Herstellers Amryt Pharma soll das Präparat Filsuvez® am 1. September 2022 in Deutschland eingeführt werden. |
Literatur
[1] Wick BM. Die Birke: Botanik, medizinische Nutzung und kulturelle Bedeutung. Schweizer Zeitschrift für Ganzheitsmedizin 2017;29:168-177
[2] Krasutsky PA. Birch bark research and development. Natural Product Reports 2006;23:919-942
[3] Laszczyk M, Jäger S, Simon-Haarhaus B et al. Physical, chemical and pharmacological characterization of a new oleogel-forming triterpene extract from the outer bark of birch (betulae cortex). Planta Medica 2006;72:1389-1395
[4] Scheffler A. The Wound Healing Properties of Betulin from Birch Bark from Bench to Bedside. Planta Medica 2019;85:524-527
[5] Ebeling S, Naumann K, Pollok S et al. From a Traditional Medicinal Plant to a Rational Drug: Understanding the Clinically Proven Wound Healing Efficacy of Birch Bark Extract. Plos one 2014;9:e86147, doi:10.1371/journal.pone.0086147






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.