
- DAZ.online
- DAZ / AZ
- DAZ 13/2021
- Das Potenzial der ...
Pandemie Spezial
Das Potenzial der Selbsttests
Was Sensitivität und Spezifität in der Praxis bedeuten
Stellen wir uns einen Test vor, der eine Sensitivität von 80,0% und eine Spezifität von 97,0% aufweist. Das entspricht den Mindestanforderungen (Sensitivität > 80,0%, Spezifität von > 97,0%), die das Paul-Ehrlich-Institut (PEI) und das Robert Koch-Institut (RKI) an die Selbsttests stellen (vgl. Mindestkriterien für SARS-CoV-2 Antigentests im Sinne von § 1 Abs. 1 Satz 1 TestVO: Antigenschnelltests vom 15.01.2021) [1]. Mit diesem Test wurden 100.000 Menschen untersucht. Von diesen sind 420 Menschen infiziert, bei ihnen wurde mittels PCR SARS-CoV-2 nachgewiesen. Diese Zahl darf nicht mit der Inzidenz verwechselt werden: Erstens werden wegen der Dunkelziffer nicht alle Infizierten erfasst und zweitens gibt die Inzidenz die Neuinfektionen an. Die Infizierten bleiben aber über einen längeren Zeitraum infiziert [2].
Die sich hieraus ergebenden Szenarien werden in Abbildung 1 dargestellt. Insgesamt zeigen in diesem Beispiel von den 100.000 durchgeführten Tests 96.677 Tests ein negatives Testergebnis (84 falsch negativ + 96.593 richtig negativ). Tatsächlich richtig angezeigt wurden also 96593 /96677 = 99,91%. Dementsprechend wäre ein negatives Testergebnis in diesem Szenario als ziemlich sicher zutreffend zu bewerten, sofern der Test korrekt durchgeführt wurde. Diese Wahrscheinlichkeit wird auch als negativer Vorhersagewert bezeichnet. Anders sieht dies bei den Schnelltests mit positivem Ergebnis aus. In dem fiktiven Szenario in Abb. 1 wurden 3323 positive Tests erhalten (336 richtig positive + 2987 falsch positive). Damit stammen jedoch nur 10,11% (336 / 3323) von Personen, die tatsächlich nachweislich mit dem Coronavirus infiziert sind. Dies ist der positive Vorhersagewert.
Abb. 1: Mögliche Konstellationen aus Infektionsstatus und Schnelltestergebnis bei der Durchführung von Schnelltests.
Wie verändern sich die Vorhersagewerte mit der Inzidenz?
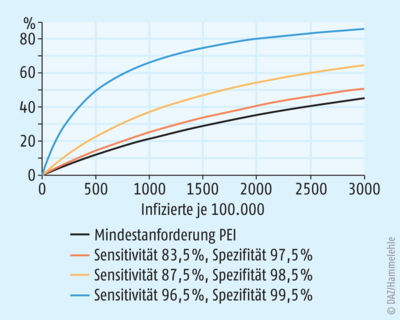
Wir haben in dieser Pandemie die Situation, dass statistisch gesehen nur ein geringer Prozentsatz der Bevölkerung tatsächlich infiziert ist. Eine breite zufällige Testung (also ohne vorliegende Symptome) wird daher aufgrund der Masse zu vergleichsweise vielen positiven Testergebnissen führen, die nicht auf eine Infektion mit SARS-CoV-2 zurückzuführen sind. Je mehr Infizierte sich tatsächlich in der Testgruppe befinden, umso höher wird die Wahrscheinlichkeit, dass ein positiver Test auch eine Infektion bedeutet. Dies wird für Tests unterschiedlicher Sensitivität und Spezifität in Abbildung 2 dargestellt:
Für eine statistische Wahrscheinlichkeit von 50%, dass ein positiver Test korrekt ist, müssten sich unter den 100.000 getesteten Personen für den orangefarbenen Test (Spezifität 97,5%) mehr als 2900 Infizierte
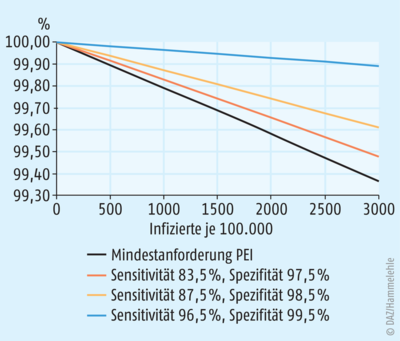
befinden. Mit dem gelben Test wird eine entsprechende Wahrscheinlichkeit bei knapp über 1700 Infizierten je 100.000 Tests erreicht. Der blaue Test (Spezifität 99,5%) hingegen hat diese Wahrscheinlichkeit schon bei nur etwas über 500 infizierten Personen je 100.000 Getesteten erreicht. Bevor wir uns die bereits zugelassenen Tests genauer ansehen, betrachten wir noch kurz den negativen Vorhersagewert, also die rechnerisch ermittelte Wahrscheinlichkeit, dass ein negatives Testergebnis auch von einer nicht infizierten Person stammt. Er ist in Abbildung 3 dargestellt. Sie zeigt deutlich, dass ein negativer Test in der von PEI/BfArM geforderten Sensitivität und Spezifität unter den herrschenden Anteilen infizierter Personen eine annähernd 100%ige Aussagekraft besitzt. Besonders hier ist es aber wichtig, sich zu vergegenwärtigen, dass diese Berechnung nur dann annähernd die Realität widerspiegelt, wenn die Probenahme und das Handling der Tests adäquat erfolgen.
Abb. 3. Der negative Vorhersagewert beschreibt die Wahrscheinlichkeit dafür, dass ein negatives Testergebnis auch tatsächlich von einer nicht infizierten Person stammt. Hierbei muss jedoch eine korrekte Handhabung der Tests vorausgesetzt werden. Zudem ist auch hier zu berücksichtigen, dass es sich bei einem solchen Test um eine Momentaufnahme handelt und ein Test, der wenige Stunden später erfolgt, unter Umständen schon ein anderes Ergebnis liefern kann.
Was gilt es bei der Übertragung der Vorhersagewerte in die Realität zu beachten?
Die meisten Angaben zur Sensitivität und Spezifität der einzelnen Tests stammen aus kleinen Herstellerstudien. Das PEI und das RKI haben gemeinsam festgelegt, dass eine ausreichende Sensitivität der Schnelltests dann gegeben ist, wenn mehr als 80% unselektierter PCR-positiver Proben auch im Antigenschnelltest positiv sind. Hierzu sollen mindestens 100 Patienten mit COVID-19-Symptomen innerhalb von sieben Tagen nach Symptombeginn parallel mit diagnostischem PCR-Test und dem Antigentest untersucht werden.
Für eine ausreichende Spezifität wird gefordert, dass bei einer Untersuchung von mindestens 100 asymptomatischen Personen ohne konkretes Expositionsrisiko mit dem Antigenschnelltest mehr als 97% negativ getestet werden, wobei reaktive Proben mit PCR abgeklärt werden müssen.
Es ist also ausreichend, 200 Proben mit einem Test zu untersuchen und daraus Sensitivität und Spezifität zu ermitteln. Tatsächlich sind einige der Herstellerstudien mit einer größeren Probenzahl durchgeführt worden, wie Tabelle 1 zu entnehmen ist, jedoch bleibt die Stichprobe im Vergleich zur Realität klein. Dieser Tatsache wird durch die Angabe der 95%igen Vertrauensbereiche Rechnung getragen. Schon diese erstrecken sich jedoch im besten Fall über einen Bereich von 1 Prozentpunkt auf bis zu 4 Prozentpunkte für die Spezifität und circa 4 bis 17 Prozentpunkte für die Sensitivität. Daher ist keine genügend sichere Aussage darüber möglich, welchen positiven Vorhersagewert ein konkreter Test hat. Zudem sind Studien, die vom Hersteller selbst durchgeführt werden, grundlegend kritischer zu betrachten als unabhängige Studien. Eine Informationsquelle hierzu bietet das Uniklinikum Heidelberg unter www.klinikum.uni-heidelberg.de/diagnostics-global-health [4]. Auch die hier gelisteten häufig deutlich umfangreicheren Studien erlauben jedoch keine bis auf die zweite Kommastelle genaue Einordnung der Testsensitivität und -spezifität.
Tab. 1: Studien zu Sensitivität und Spezifität verschiedener Selbsttests, die in den Gebrauchsinformationen aufgeführt sind (Stand der Information: 21. März 2020) [Informationen der Hersteller, Eigenrecherche]. X = Vorgaben des PEI erfüllt | ||||||||||||||||||||||
Testbezeichnung (Kurzbezeichnung) | Handelsname | Art der Probenahme | Probenkollektiv | Probenahme | Anzahl Proben | Sensitivität | Spezifität | Anmerkung | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
oropharyngeal | nasopharyngeal | (anterio-)nasal | Sputum | keine Angabe | symptomatisch | asymptomatisch | keine Angabe | medizinisches Personal | Selbstentnahme | keine Angabe | PCR-positiv | PCR-negativ | berechneter Wert | untere Grenze 95%iger Vertrauensbereich | obere Grenze 95%iger Vertrauensbereich | berechneter Wert | untere Grenze 95%iger Vertrauensbereich | obere Grenze 95%iger Vertrauensbereich | ||||
Clinitest Rapid COVID-19 Antigentest – Coronavirus Ag Rapid Test Cassette (Swab) (Clinitest) | Clinitest Rapid COVID-19 Antigentest – Coronavirus Ag Rapid Test Cassette (Swab) Siemens Healthcare GmbH | X | X | X | X | 119 | 746 | 98,32% | 94,06% | 99,80% | 99,60% | 98,83% | 99,92% | |||||||||
Clinitest Rapid COVID-19 Antigentest – Coronavirus Ag Rapid Test Cassette (Swab) Siemens Healthcare GmbH | X | X | X | X | 109 | 128 | 97,25% | 92,17% | 99,43% | 100,00% | 97,69% | 100,00% | ||||||||||
Clinitest Rapid Test Cassette (Swab) TriPart Logistic GmbH | X | X | X | 61 | 256 | 96,72% | 88,65% | 99,60% | 99,2% | 97,21% | 99,91% | |||||||||||
Boson SARS-CoV-2 Antigen Schnelltest (Boson) | Boson SARS-CoV-2 Antigen Schnelltest Technomed Service GmbH | X | X | X | 164 | 714 | 93,64% | 93,47% | 99,21% | 99,16% | 98,49% | 99,83% | 1 | |||||||||
Boson SARS-CoV-2 Antigen Schnelltest Löwe Medizintechnik | X | X | X | 164 | 714 | 93,64% | 93,47% | 99,21% | 99,16% | 98,49% | 99,83% | 1 | ||||||||||
QuickProfile COVID-19 Antigen Test CardMedipro medizinische diagnostische Produkte GmbH | X | X | X | 102 | 464 | 96,08% | 92,31% | 99,85% | 99,14% | 98,30% | 99,98% | 1 | ||||||||||
blnk Rapid SARS-CoV-2 Antigen Test Card Trekstor GmbH | X | X | X | 313 | 714 | 96,17% | 94,04% | 98,29% | 99,16% | 98,49% | 99,83% | 1 | ||||||||||
Novel Coronavirus (COVID-19)Antigen Test Kit (Colloidal Gold) (Lyher) | Novel Coronavirus (COVID-19) Antigen Test Kit (Colloidal Gold) Lissner Qi GmbH | X | X | X | 158 | 267 | 97,47% | 93,65% | 99,31% | 100,00% | 98,63% | 100,00% | ||||||||||
X | X | X | 133 | 147 | 95,49% | 90,44% | 98,33% | 93,32% | 96,27% | 99,98% | ||||||||||||
X | X | X | 152 | 250 | 95,39% | 90,74% | 98,13% | 99,60% | 97,79% | 99,99% | ||||||||||||
X | X | X | X | X | 443 | 664 | 96,16% | 93,93% | 97,75% | 99,70% | 98,92% | 99,96% | ||||||||||
SARS-CoV-2 Rapid Antigen Test Nasal (Roche) | SARS-CoV-2 Rapid Antigen Test Nasal Roche Diagnostics GmbH | X | X | X | X | X | 150 | 546 | 82,70% | 75,60% | 88,40% | 99,10% | 97,90% | 99,70% | 2 | |||||||
X | X | X | X | k. A. | k. A. | 89,60% | 79,70% | 95,70% | 99,10% | 96,90% | 99,90% | 3 | ||||||||||
X | X | X | X | k. A. | k. A. | 89,10% | 78,80% | 95,50% | 99,00% | 97,20% | 99,80% | 3 | ||||||||||
AMP Rapid Test SARS-CoV-2 Ag (AMP) | AMP Rapid Test SARS-CoV-2 Ag Dr. Lonsdorfer GmbH & Co. KG | X | X | X | 111 | 139 | 97,30% | 90,00% | 99,80% | 100,00% | 96,60% | 100,00% | 4 | |||||||||
AMP Rapid Test SARS-CoV-2 Ag Sputum (AMP) | X | X | X | 141 | 189 | 92,20% | 86,10% | 96,60% | 100,00% | 98,50% | 100,00% | 5 | ||||||||||
Aesku.Rapid SARS-CoV-2 (Aesku) | Aesku.Rapid SARS-CoV-2 Cerascreen GmbH | X | X | X | k. A. | k. A. | 85,00% | 78,00% | 90,00% | 98,00% | 95,00% | 99,00% | 6 | |||||||||
Biosynex COVID-19 Ag BSS (Biosynex) | Biosynex COVID-19 Ag BSS Aidian Germany GmbH | X | X | X | 99 | 149 | 96,00% | 93,60% | 98,40% | 100,00% | 100,00% | 100,00% | 7 | |||||||||
Biosynex COVID-19 Ag BSS Hirsch Apotheke OHG | X | X | X | 99 | 149 | 96,00% | 93,60% | 98,40% | 100,00% | 100,00% | 100,00% | 7 | ||||||||||
Anmerkungen: 1: Testung innerhalb von 7 Tagen nach Symptombeginn bei Verdachtsfällen (laut Gebrauchsinformation), 2: Proben für PCR oropharyngeal und nasopharyngeal kombiniert (laut Gebrauchsinformation), 3: nur für ct-Werte bis 30 (laut Gebrauchsinformation), 4: Test-Sensitivität kann für Oropharyngeal- und Anertior-nasal-Abstrich aus physiologischen Gründen um rund 10% geringer sein (laut Gebrauchsinformation), 5: keine in der Liste des BfArM verlinkte Gebrauchsanweisung (Anm. d. Autorin), 6: Verlinkte Gebrauchsinformation enthält keine weiteren Detailangaben. In anderen Unterlagen können mehr Details zur Abhängigkeit von der Viruslast und zur Anzahl der Proben gefunden werden. Testergebnisse wurden stärker gerundet, als es bei anderen Tests, 7: hier wurde sehr stark gerundet, Vertrauensbereich der Spezifität erscheint nicht plausibel, nachgerechnete Sensitivität: 96,11% (Anm. d. Autorin) | ||||||||||||||||||||||
Aussagekraft variiert je nach Grund der Testung
Die Herstellerangaben zur Testspezifität beruhen, wie oben dargestellt, auf einem asymptomatischen Probandenkollektiv ohne konkretes Expositionsrisiko. Eine Übertragbarkeit des berechneten positiven Vorhersagewertes auf eine anlasslose Testung erscheint damit plausibel.
Erfolgt jedoch ein Schnelltest aufgrund konkreter Symptome, eventuell sogar noch aufgrund eines Risikokontaktes, liegt eine grundsätzlich andere Situation vor, die durch die Studienlage zur herstellerseitigen Spezifitätsbestimmung nicht mehr abgedeckt ist. Hier ist eine höhere Wahrscheinlichkeit zu erwarten, dass einem positiven Testergebnis auch tatsächlich eine Infektion mit SARS-CoV-2 zugrunde liegt.
Unbewusste Fehler in der Anwendung können zu Falschaussagen der Tests führen
Die richtige Lagerung und Anwendung der Schnell- und Selbsttests bieten genügend Stoff für einen eigenen Artikel. An dieser Stelle kann daher nur dafür sensibilisiert werden, welche Fehlerquellen allgemein vorliegen:
- ungeeignete Temperatur während Lagerung bzw. Anwendung [3]
- Besiedlung der Nase mit anderen Viren oder Bakterien, auf die der Test positiv reagiert
- Verwechslung von Proben oder Tests bei Testung mehrerer Personen
- Entnahme von zu wenig oder ungeeignetem Probenmaterial
- Ablesen des Ergebnisses zum falschen Zeitpunkt
- Fehlinterpretation der Anzeige
Welche Sensitivität und Spezifität haben die bisher zugelassenen Selbsttests?
Um die Frage zumindest teilweise zu beantworten, wurden die in den Gebrauchsinformationen der Hersteller aufgeführten Studien in Tabelle 1 zusammengefasst. Enthielten die Gebrauchsinformationen mehrere Studien, sind auch alle in der Tabelle gelistet. Einbezogen wurden die Gebrauchsinformationen derjenigen deutschen Vertreiber, die in der „Liste der Antigen-Tests zum direkten Erregernachweis des Coronavirus SARS-CoV-2“ des BfArM für die Profitests geführt sind und die anhand der AT-Nummer aus der unter www.bfarm.de/DE/Medizinprodukte/Antigentests/_node.html zu findenden „Liste mit Sonderzulassungen des BfArM für Tests zur Eigenanwendung durch Laien zum Nachweis von SARS-CoV-2“ (Stand 21. März 2021) ausgewählt wurden [5].
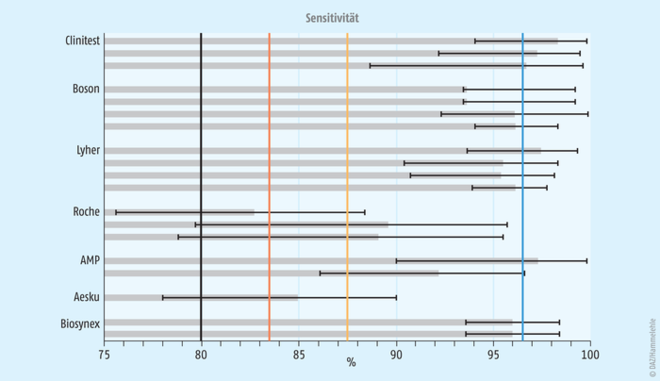
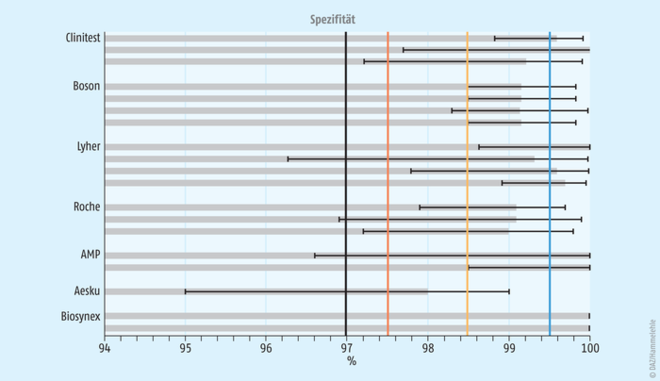
Die Bandbreite der Sensitivität und Spezifität der Tests nach den Ergebnissen der Herstellerstudien sind zudem in den Abbildungen 4 und 5 dargestellt. Zusätzlich finden sich dort Markierungen, die die fiktiven Tests aus den Diagrammen zum Vorhersagewert sowie die Mindestanforderungen von PEI/RKI kennzeichnen. Viele der Tests sind im Bereich des fiktiven blau dargestellten Tests zu finden und ein geringerer Anteil im Bereich des gelben oder orangenen Tests.
In den Diagrammen sind die jeweiligen 95%igen Vertrauensbereiche deutlicher dargestellt als die tatsächlich ermittelten Werte, um für die Ungenauigkeit der Angaben aufgrund der geringen Stichprobengröße zu sensibilisieren. Kleinere Vertrauensbereiche resultieren aus einer größeren Stichprobe. Der jeweilige Stichprobenumfang ist in Tabelle 1 nachzulesen. Die verschiedenen Studien zu einem Test lassen Anhaltspunkte zu weiteren Fragen zu, die nun zum Abschluss beantwortet werden sollen.
Abb. 4: Sensitivität verschiedener Schnelltests laut Angaben der Hersteller in den Gebrauchsanweisungen. Details zu den einzelnen Daten sind Tabelle 1 zu entnehmen. Dargestellt sind das Studienergebnis sowie der 95%ige Vertrauensbereich. Die senkrechten farbigen Striche kennzeichnen die fiktiven Tests, die für Abbildung 2 und Abbildung 3 genutzt wurden.
Abb. 5: Spezifität verschiedener Schnelltests laut Angaben der Hersteller in den Gebrauchsanweisungen. Details zu den einzelnen Daten sind Tabelle 1 zu entnehmen. Dargestellt sind das Studienergebnis sowie der 95%ige Vertrauensbereich. Die senkrechten farbigen Striche kennzeichnen die fiktiven Tests, die für Abbildung 2 und Abbildung 3 genutzt wurden.
Weitere Fragen zur Bewertung von Testcharakteristika und Testergebnissen
Wie groß sind die Schwankungen in Bezug auf die Testcharakteristika, wenn unterschiedliche Studien durchgeführt werden?
Hier liefert ein Blick auf die Studien zum Boson-Test erste Hinweise. Die jeweils vier in den Abbildungen dargestellten Balken zu diesem Test stammen aus vier verschiedenen Gebrauchsanleitungen. Zwei davon (Vertrieb durch Technomed bzw. Löwe Medizintechnik) enthalten exakt die gleichen Daten. Die anderen beiden beziehen sich jedoch offenkundig auf andere Studien. Hier gibt es zwar Unterschiede in den tatsächlich ermittelten Werten, die Vertrauensbereiche ähneln einander jedoch so sehr, dass zumindest hier eine Ungenauigkeit aufgrund einer kleinen Stichprobe kein auffälliges Problem zu sein scheint.
Auch der Clinitest wurde in verschiedenen Studien getestet. Erneut sind hier ähnliche Ergebnisse zu erkennen, die unterschiedlich breiten Vertrauensbereiche sind auf zum Teil stark unterschiedliche Stichprobengrößen zurückzuführen.
Zu diesem Thema sei weitergehend erneut auf die Übersicht der Uniklinik Heidelberg verwiesen.
Ist eine professionelle Probenahme vorteilhaft gegenüber der Selbsttestung?
Einen Hinweis dazu liefern die verschiedenen Studien zum Schnelltest der Firma Roche. Die Gebrauchsanleitung enthält hier eine differenzierte Auswertung. Es zeigte sich, dass die ermittelte Spezifität (99,1% vs. 99,0%) und die ermittelte Sensitivität (89,6% vs. 89,1%) statistisch nicht signifikant unterschiedlich waren, egal, ob die Proben durch Fachpersonal oder selbstständig entnommen wurden. Auch eine (bisher nur als Preprint verfügbare) Studie von Nikolai et al. [6] konnte für diesen Test keinen Unterschied zwischen den Ergebnissen aus professioneller Probenahme und eigenständiger Probenahme nach Anleitung feststellen. Diese Studie bewertet allerdings nur 228 Tests, die sich auf vier Gruppen aufteilen, bietet also vor allem den Vorteil der Unabhängigkeit, jedoch keine größere Stichprobe als die Herstellerstudien. In einem „research letter“ von Lindner et al. [7] wird ebenfalls ein Vergleich zwischen selbst entnommenen Nasenabstrichen und von Fachpersonal entnommenen Nasopharyngeal-Abstrichen mit diesem Test vorgenommen. Auch hier ist das Fazit, dass keine statistisch signifikanten Unterschiede zu finden sind.
Sind nasale Tests so gut wie nasopharyngeale Tests?
Zur Beantwortung dieser Frage ist zunächst ein Blick auf die verschiedenen Studien zum Lyher-Test geeignet, bei denen drei verschiedene Probenahmestellen verglichen wurden (oropharyngeal, nasopharyngeal und anteriornasal). Die vierte Auswertung fasst alle Arten zusammen. Auch hier zeigt sich, dass die Vertrauensbereiche für die Spezifität fast komplett überlappen. In Bezug auf die Sensitivität weist die oropharyngeale Probenahme einen größeren Vertrauensbereich auf, der sich durch die kleinere Stichprobe erklären lässt. Auch im bereits oben erwähnten Preprint von Nikolai et al. [6] (wobei wie erwähnt ein anderer Schnelltest genutzt wurde) wurden die nasopharyngeale und die anterior-nasale Probennahme verglichen, ohne signifikante Unterschiede zu finden.
Fazit
Richtig eingesetzt sind die Selbsttests ein mächtiges Instrument zur Eindämmung und Kontrolle der Pandemie. Wesentlich ist es dafür aber, dass ein positives Schnelltestergebnis immer zu einer sofortigen Selbstisolation und einer Abklärung mittels PCR führt. Andersherum darf auch ein negatives Schnelltestergebnis nicht dazu verführen, sich unbesorgt zu verhalten, da es immer nur eine Momentaufnahme darstellt und (sofern irgendein Kontakt zu potenziell infizierten Mitmenschen vergleichsweise kurz vor dem Test stattgefunden hat) keinen langen Zeitraum abdecken kann. Die vom BfArM für die Selbsttestung zugelassenen Tests unterscheiden sich teilweise etwas in ihrer Aussagekraft. Die Unterschiede werden jedoch bei der Bewertung der Ergebnisse einbezogen. So erscheint es sinnvoll, in erster Linie auf die Verfügbarkeit und eventuell den Preis zu achten und erst, wenn hier eine entsprechende Auswahl besteht, auch die Leistungsfähigkeit der Tests als Auswahlkriterium heranzuziehen. |
Literatur
[1] Palm T. Corona-Selbsttests: Nur noch kurz den COVID-Status checken. Zeit.online vom 7. März 2021, www.zeit.de/wissen/gesundheit/2021-03/corona-selbsttests-antigen-schnelltest-ergebnis-erklaerung?utm_referrer=https%3A%2F%2Fwww.google.com%2F lt
[2] Seifried J, Böttcher S, Oh DY, Michel J et al. Was ist bei Antigentests zur Eigenanwendung (Selbsttests) zum Nachweis von SARS-CoV-2 zu beachten? Epid Bull 2021;8:3-9, DOI 10.25646/8040
[3] weitere Informationen zum Einfluss der Lagertemperatur in Haage V et al. Impaired performance of SARS-CoV-2 antigen-detecting rapid diagnostic tests at elevated and low temperatures. Journal of Clinical Virology 2021, https://doi.org/10.1016/j.jcv.2021.104796
[4] Informationen des Uniklinikums Heidelberg, www.klinikum.uni-heidelberg.de/diagnostics-global-health
[5] Tests zur Eigenanwendung durch Laien. Liste mit Sonderzulassungen des BfArM für Tests zur Eigenanwendung durch Laien zum Nachweis von SARS-CoV-2 (Stand 21. März 2021), Informationen des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), www.bfarm.de/DE/Medizinprodukte/Antigentests/_node.html
[6] Nikolai O, Rohardt C, Tobian F et al. Anterior nasal versus nasal mid-turbinate sampling for a SARS-CoV-2 antigen-detecting rapid test: does localisation or professional collection matter? Preprint, doi: https://doi.org/10.1101/2021.02.09.21251274
[7] Lindner A, Nikolai O, Kausch F, Wintel M et al. Head-to-head comparison of SARS-CoV-2 antigen-detecting rapid test with self-collected nasal swab versus professional-collected nasopharyngeal swab. European Respiratory Journal 2020; DOI: 10.1183/13993003.03961-2020, https://doi.org/10.1183/13993003.03961-2020 (in press)
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.