
- DAZ.online
- DAZ / AZ
- DAZ 12/2021
- HIT mimicry durch AZD1222
Pandemie Spezial
HIT mimicry durch AZD1222
Ursachenforschung zu Sinus-/Venenthrombosen nach Impfungen mit AstraZeneca-Vakzine
In einer digitalen Pressekonferenz verkündete Professor Andreas Greinacher, Experte für medikamenteninduzierte Thrombozytopenien, stolz und sichtlich erleichtert die vorläufigen wissenschaftlichen Erkenntnisse rund um die mutmaßliche Aufklärung des Auftretens sehr seltener zerebraler Sinus-/Venenthrombosen im Zusammenhang mit AstraZeneca-Impfungen [1]. Er hob lobend hervor, dass hierfür Mitarbeitende der Abteilung für Transfusionsmedizin am Institut für Immunologie und Transfusionsmedizin der Universitätsmedizin Greifswald, deren Leiter er ist, und weitere deutsche und österreichische Forschungsgruppen sowie Mitarbeitende des Paul-Ehrlich-Instituts in den vergangenen 72 Stunden nahezu durchgearbeitet und dabei fantastisch kooperiert hätten.
Wissenschaftliche Erfolge in Rekordzeit
In der Kürze der Zeit konnten nicht nur die immunologische Aktivierung von Thrombozyten als ein wichtiger Pathomechanismus für das beobachtete Phänomen identifiziert, sondern auch bereits etablierte Testverfahren auf ihre Eignung zum Screening von Betroffenen überprüft werden. Die bedeutendste Errungenschaft sei aber die Erkenntnis gewesen, mit welcher Therapieoption man die sehr, sehr seltene Impfkomplikation gezielt adressieren könne. Dabei kam den Forschenden zugute, dass man über 30 Jahre an Erfahrung mit einem sehr ähnlich gelagerten Krankheitsbild verfüge, der Heparin-induzierten Thrombozytopenie (HIT), zu dem eine frappierende Parallelität bestünde, so Greinacher. Menschen müssten angesichts des nun verstandenen Mechanismus und der Screening- und Behandlungsmöglichkeiten im Falle des Auftretens von klinischen Symptomen keine Angst mehr vor der COVID-19-Impfung haben. Zudem darf in Erinnerung gerufen werden, dass es sich um ein absolut seltenes Phänomen handelt. Dem Paul-Ehrlich-Institut wurden bis zum 18. März 2021 13 Fälle von Sinus-/Hirnvenenthrombosen bei mehr als 1,6 Millionen Geimpften mit dem AstraZeneca-Vakzin AZD1222 gemeldet [2]. Nach Ansicht des Greifswalder Experten sei das kurzzeitige Aussetzen der Impfungen dennoch sehr sinnvoll gewesen, um die Hintergründe der schwerwiegenden Komplikationen zu ergründen und zu untersuchen, ob ein kausaler Zusammenhang besteht. Nun, da man dies aufgeklärt habe, könne man den Menschen wieder eine entsprechende Sicherheit geben.
Medikamenteninduzierte Thrombozytopenie
Die Heparin-induzierte Thrombozytopenie (HIT) ist mit Abstand die häufigste medikamenteninduzierte Thrombozytopenie. Es liegen ferner Fallberichte zu Tirofiban, Abciximab, Goldsalzen, Chinin, Chinidin, Clopidogrel, L-Dopa, Antikonvulsiva, Piperacillin/Tazobactam, Trimethoprim/Sulfamethoxazol, Ceftriaxon, Enalapril und weiteren vor [10].
Eindeutige Ergebnisse
Der Mediziner schilderte, dass man Blutproben von vier Betroffenen sehr intensiv untersucht habe und weitere drei Blutproben zur Bestätigung der wichtigsten Befunde hätte heranziehen können. Zudem lagen bei zwei weiteren Fällen klinische Informationen, aber keine Blutproben vor, die „ins Bild gepasst hätten“. Die Forschenden konnten in allen untersuchten Blutproben bestimmte Antikörper nachweisen, die den Abwehrstoffen ähneln, welche bei einer HIT II gebildet werden. Sie sind in der Lage, an ein Protein der Thrombozyten zu binden und diese, ohne dass eine Gefäßschädigung vorliegt, zu aktivieren. Die Vorbereitungen einer wissenschaftlichen Publikation zu den brisanten Erkenntnissen und der genauen Details laufe auf Hochtouren. Auch norwegische Forschende hatten den immunologischen Zusammenhang mit plättchenaktivierenden Antikörpern bereits als Hypothese formuliert.
Man vermutet, dass neben der immunologischen Aktivierung von Thrombozyten auch eine Aktivierung von weißen Blutkörperchen und Gefäßwänden stattfindet. Aber auch weitere Pathomechanismen wären noch denkbar. Die in der Folge der Thrombozytenaktivierung in Gang gesetzte Blutgerinnung führt bei den betroffenen Patienten zu Thrombosen, unter anderem zu den sehr seltenen zerebralen Sinus-/Venenthrombosen und einer Immunthrombozytopenie. Professor Greinacher hält es für möglich, dass in den Sinus und Hirnvenen ein bis dato unerkannter Faktor vorliegt, der diese Gefäße besonders für die impfstoffassoziierten Thrombosen prädestiniert.
Risikofaktor weibliches Geschlecht?
Überwiegend habe es sich um weibliche Betroffene jüngeren bis mittleren Alters gehandelt, was mehreren Umständen geschuldet sein mag. So wären Frauen von Autoimmunerkrankungen generell häufiger betroffen als Männer. Zudem könnten hormonelle Einflussfaktoren eine Rolle bei der Entstehung von zerebralen Sinus-/Venenthrombosen gespielt haben. Aber es sollte auch die epidemiologische Perspektive bedacht werden, schließlich wurden in der Anfangsphase der Impfkampagne mit AZD1222 vorrangig Frauen geimpft. Grund hierfür ist, dass in den für eine COVID-19-Impfung priorisierten Berufsgruppen mehr Frauen als Männer arbeiten (Gesundheitspersonal, Erzieherinnen oder Lehrerinnen). Ältere Patienten unter den Geimpften haben hingegen ein etwas weniger aktives Immunsystem und reagieren womöglich etwas moderater, so Greinachers Vermutung. Die Detailabklärung würde aber in den kommenden Wochen und Monaten erfolgen.
Sind alle COVID-19-Vakzine betroffen?
Die in Greifswald untersuchten Fälle von vermutlich impfstoffassoziierten Thrombosen gingen alle auf Impfungen mit der AstraZeneca-Vakzine zurück. Nach Angaben des Transfusionsmediziners muss noch weiter untersucht werden, ob die Komplikation durch den Impfstoff selbst oder den verwendeten Vektor ausgelöst wurde, oder ob unspezifische Inflammationsreaktionen auf die Impfung als Kofaktor eine Rolle gespielt haben könnten. Noch sei unklar, ob das Phänomen auch bei mRNA-basierten COVID-19-Impfstoffen auftreten könnte.
Worauf sollten Geimpfte achten?
Kein Grund zur Sorge besteht bei Auftreten von typischen Impfreaktionen, die sich meist in den ersten zwei bis drei Tagen in Form von grippeähnlichen Symptomen äußern. Die eine schwere Komplikation auslösenden Antikörper werden erst nach vier oder fünf Tagen gebildet (in Analogie zur HIT), also dann, wenn es den Geimpften nach Abklingen der möglichen Impfreaktion wieder besser geht. In dieser Zeit sollte man auf Anzeichen einer Thrombose achten, zum Beispiel schmerzhafte, geschwollene Beine oder Arme, Kurzatmigkeit oder Brustschmerzen. Kleine punktförmige Hautblutungen (Petechien) können, neben anderen Ursachen, auf eine Thrombozytopenie hindeuten. Für das Auftreten einer zerebralen Sinus-/Venenthrombose könnten sehr starke, anhaltende Kopfschmerzen oder andere neurologische Symptome (halbseitige Lähmungen und/oder Gefühlsstörungen, Schwindel, Seh- oder Sprachstörungen, epileptische Anfälle) sprechen.
Kurzer Zeitraum
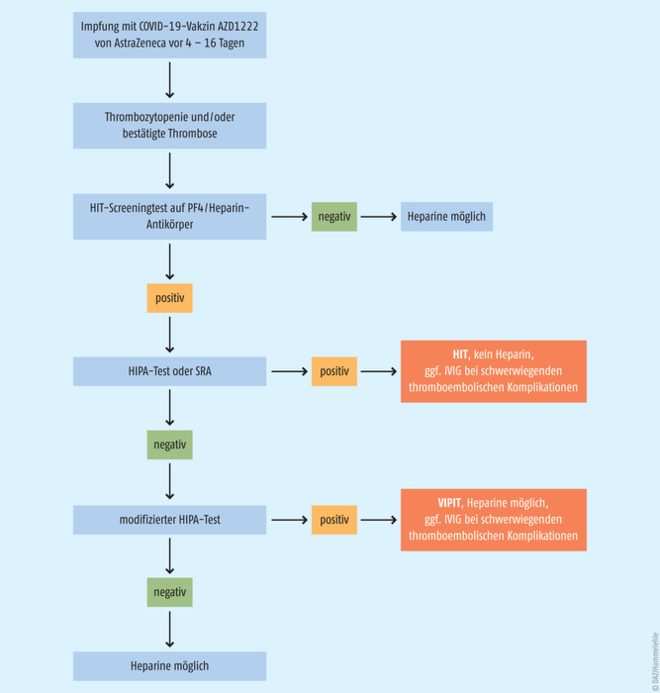
Aus der HIT-Forschung und den aktuell untersuchten Fällen besteht berechtigter Grund zur Annahme, dass mögliche Reaktionen nur in einem überschaubaren Zeitraum von fünf bis 16 Tagen nach der Impfung auftreten und sonst nicht mehr. Greinacher betonte, dass diese Vermutung aufgrund der bisher untersuchten kleinen Fallzahlen jedoch noch nicht vollständig wissenschaftlich belastbar sei. Es würde aber eine immense Beruhigung für alle bedeuten, die bereits seit mehr als zwei Wochen geimpft sind. Geimpften wird geraten, sich im Falle der geschilderten Symptome unverzüglich in ärztliche Behandlung zu begeben, um die Plausibilität des Verdachts zu überprüfen und eine Differenzialdiagnose, beispielsweise hinsichtlich eines Migräneanfalls, durchführen zu lassen. In der Diagnostik lasse sich zuverlässig entscheiden, ob eine Thrombozytopenie und HIT mimicry sowie eine CVST vorliegen würde (Abb. 1). Ärzte könnten dann eine parenteral verabreichte antithrombotische Therapie einleiten, die sich nach der Ursache der Thrombozytopenie richtet, sowie in bestimmten Fällen der neu definierten Vakzin-induzierten prothrombotischen Immunthrombozytopenie (VIPIT) auf eine spezielle Behandlungsoption zurückgreifen.
Abb. 1: Diagnostischer und therapeutischer Algorithmus bei Patienten mit Thrombozytopenie/Thrombose nach Impfung mit der COVID-19-Vakzine AZD1222 von AstraZeneca. Bei Nebenwirkungen, die mehr als drei Tage nach erfolgter Impfung anhalten oder neu auftreten und für eine Thrombozytopenie/Thrombose sprechen, sollte eine ärztliche Diagnostik zur Abklärung einer Thrombose erfolgen. HIT = Heparin-induzierte Thrombozytopenie, PF4 = Plättchenfaktor 4, HIPA = heparininduzierte Plättchenaktivierung, SRA = serotonin-release assay, Serotoninfreisetzungstest, IVIG = hochdosiertes intravenöses Immunglobulin, VIPIT = Vakzin-induzierte prothrombotische Immunthrombozytopenie [3].
Therapie mit IVIG
Diese besteht in Form von intravenös verabreichtem Immunglobulin G (IVIG) und dient effektiv der Durchbrechung der fehlgeleiteten Thrombozytenaktivierung und Thrombinbildung. Sie ist zugelassen für die Behandlung zahlreicher Autoimmunerkrankungen, so auch der HIT und bei Immundefizienz. In allen in Greifswald untersuchten Proben hemmte IVIGG in einer Konzentration von 10 mg/10 ml den der Erkrankung zugrunde liegenden Mechanismus. Intravenös verabreichtes Immunglobulin G blockiert dabei den thrombozytenständigen Fcγ-Rezeptor IIa und verhindert dadurch, dass die gebildeten Antikörper an Thrombozyten binden können, sodass deren massive Aktivierung unterbleibt. Es wird empfohlen, IVIG in einer Dosierung von 1 g/kg Körpergewicht pro Tag an zwei aufeinanderfolgenden Tagen zu verabreichen [3].
Wer muss aufpassen?
Laut Aussage von Professor Greinacher kann niemand vor der Impfung wissen, ob er zu der sehr seltenen Risikogruppe gehört, die eine VIPIT entwickelt. Er warnte davor, dass keine Möglichkeit bestünde und es auch nicht sinnvoll wäre, das individuelle Risiko vorab zu testen. Patienten mit positiver Thromboseanamnese und/oder bei denen eine Thrombophilie bekannt ist, haben laut Gesellschaft für Thrombose- und Hämostaseforschung e. V. (GTH) aufgrund der immunologischen Genese des beobachteten Phänomens kein erhöhtes Risiko, diese spezifische und sehr seltene Komplikation zu erleiden [3].
Was ist überhaupt eine Sinusvenenthrombose?
Das sehr seltene Krankheitsbild rückte erst durch ihr gehäuftes Auftreten in zeitlichem Zusammenhang mit COVID-19-Vakzinen der Firma AstraZeneca in den Fokus der Öffentlichkeit. Vorweg muss erläutert werden, dass die Begrifflichkeit „Sinusvenenthrombose“ unpräzise ist, da es die „Sinusvenen“ anatomisch betrachtet nicht gibt [4]. Vielmehr handelt es sich bei den Sinus durae matris um Blutleiter venösen Blutes, die im Gegensatz zu Venen keine Klappen und Muskelfasern besitzen. Zudem müsste je nach Lokalisation differenziert werden in Thrombosen der Sinus und Thrombosen zerebraler Venen, die isoliert, aber auch in Kombination auftreten können. Die korrekte Bezeichnung lautet daher zerebrale Sinus-/Venenthrombosen (CVST).
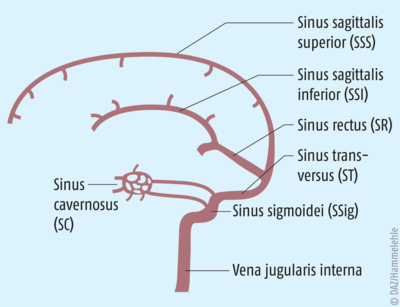
Die Sinus durae matris verlaufen in der harten Hirnhaut (Dura mater), sind durch zahlreiche Anastomosen miteinander verbunden und transportieren sauerstoffarmes (venöses) Blut vom Gehirn zum Herzen (siehe Abb. 2). Bei einer Thrombose dieser Gefäße kommt es konsekutiv zu einer gestörten Liquorresorption, wodurch der intrakranielle Druck steigt, was sich bei 90% der Betroffenen in Form von starken Kopfschmerzen äußert. Ebenfalls können Stauungsblutungen, zytotoxische Ödeme und hämorrhagische Schlaganfälle durch den Gefäßverschluss resultieren und weitere neurologische Komplikationen bedingen [4]. Auch epileptische Anfälle sind möglich.
Abb. 2: Sinus durae matris: CVST betreffen in erster Linie die duralen Sinus (SSS, ST, SSig, SR, SC) sowie die größeren inneren und kortikalen Hirnvenen [4]. Bei circa drei Viertel der Patienten sind mehrere Sinus- bzw. Venensysteme gleichzeitig von Thrombosen betroffen (adaptiert nach [5]).
Niedrige Inzidenz
Man nimmt an, dass pro Jahr nur drei bis vier Fälle pro eine Millionen Erwachsene zu verzeichnen sind [5], die tatsächliche Inzidenz ist aber aufgrund der extrem heterogenen Symptomatik und asymptomatischer Fälle unbekannt [4]. Es zeigt sich eine Häufung bei Personen unter 40 Jahren, bei Patienten mit Thrombophilie und bei Frauen, die dreimal häufiger als Männer betroffen sind. Dass es sich bei der CVST um eine relativ seltene Erkrankung handelt, wurde in einer Online-Umfrage, an der sich zwischen 2015 und 2016 42,8 % aller 250 zertifizierten Stroke-Units (SU) in Deutschland beteiligten, bestätigt [7]. Hier gaben über die Hälfte der SUs an, nur fünf bis zehn Patienten mit einer zerebralen Sinus/Venenthrombose pro Jahr zu behandeln (in regionalen SUs 54,4 %, in überregionalen SUs 55,3 %), 7 % der regionalen Stroke-Units und 29,8 % der überregionalen Stroke-Units versorgten mehr als zehn CVST-Patienten pro Jahr.
Die Ätiologie der zerebralen Sinus-/Venenthrombosen ist entzündlicher oder nichtentzündlicher (blander) Natur und es bestehen verschiedene Risikofaktoren, die an der Entstehung beteiligt sind (siehe Tabelle 1). In der aktuellen S2k-Leitlinie Zerebrale Venen- und Sinusthrombose werden als Hauptursachen idiopathische Auslöser (20 bis 35% der Fälle), orale Kontrazeptiva (in 10% der Fälle alleiniger Auslöser) und heterozygote oder homozygote Faktor-V-Leiden-Mutation (10 bis 25% der Fälle) genannt [6].
Thrombophilie | Antithrombin III-, Protein-C- oder Protein-S-Mangel |
Resistenz gegen aktiviertes Protein C (APC-Resistenz), in der Regel hervorgerufen durch eine Faktor-V-Leiden-Mutation | |
Faktor-II-Mutation (Prothrombin-G20210A-Mutation) | |
Antiphospholipid-Antikörper (APL-AK) | |
Hyperhomozysteinämie (z. B. durch Mutationen innerhalb des Methylentetrahydrofolatreduktase(MTHFR)-Gens) | |
Frauenspezifische Faktoren | hormonelle Kontrazeptiva |
Postpartalphase | |
Gravidität (letztes Trimenon) | |
Hormonersatztherapie | |
Infektion und Inflammation | lokalisierte Infektionen (Otitis media, Mastoidits, Sinusitis, Tonsillitis, Meningitis) |
systemische Infektionen (bakteriell: Septikämie, Endokarditis, Typhus, Tuberkulose, viral: Masern, Hepatitis, Enzephalitis (HSV, HIV), Zytomegalievirus, parasitär: Malaria, Trichinose, Pilzinfektionen: Aspergillose) | |
Vaskulitiden (Morbus Behçet, Wegener-Granulomatose, Sarkoidose) | |
chronisch entzündliche Darmerkrankungen (M. Crohn, Colitis ulcerosa) | |
Kollagenosen (Lupus erythematodes, Sjögren-Syndrom) | |
Hämatologisch-onkologische Erkrankungen | Malignome (Karzinom, Lymphom, Karzinoid, Leukämie) |
Polyzythämie, Sichelzellanämie, essenzielle Thrombozythämie | |
Paroxysmale nächtliche Hämoglobinurie (PNH) | |
Trauma | Schädel-Hirn-Trauma |
neurochirurgische Eingriffe | |
lokale Verletzung der Halsvenen oder Sinus | |
lumbale Liquorpunktion | |
Sonstige | nephrotisches Syndrom |
Medikamentös-toxische Ursachen |
CVST bei HIT
Bei der immunologisch vermittelten Heparin-induzierten Thrombozytopenie (HIT Typ II) zeigen etwa die Hälfte der Patienten venöse oder arterielle thrombotische Komplikationen [8]. Als neurologische Komplikationen, die in einer retrospektiven Studie bei elf der untersuchten 120 konsekutiven HIT-II-Patienten auftraten, wurden zerebrale Ischämien (bei 5,8% der Patienten) und seltener Sinus-/Hirnvenenthrombosen (bei 2,5% der Patienten) beobachtet [9]. Bei diesen Patienten war eine deutlich erhöhte Mortalität im Vergleich zu HIT-II-Patienten ohne neurologische Komplikationen zu verzeichnen (55% versus 11%) [9]. Gerade die Zusammenhänge zwischen CSVT und HIT/HIT mimicry sind aus aktuellem Anlass von besonderem Interesse und müssen weiter ergründet werden. |
Literatur
[1] Pressekonferenz Universitätsmedizin Greifswald. 19.03.2021. https://www.medizin.uni-greifswald.de/de/ueber-die-umg/aktuelles/astrazeneca-impfung/
[2] Paul-Ehrlich-Institut.
[3] Aktualisierte Stellungnahme der GTH nach dem Beschluss der EMA, die Impfungen mit dem AstraZeneca COVID-19 Vakzin fortzusetzen. Gesellschaft für Thrombose- und Hämostaseforschung e.V. 22.03.2021
[4] Koennecke HC. Zerebrale Sinus- und Venenthrombosen. In: Berlit P. (eds) Klinische Neurologie. Springer Reference Medizin. Springer, Berlin, Heidelberg 2020. https://doi.org/10.1007/978-3-662-60676-6_150
[5] Piazza G. Cerebral Venous Thrombosis. Circulation 2012;125:1704-1709
[6] Weimar C et al. Zerebrale Venen- und Sinusthrombose. S2k-Leitlinie. AWMF-Registernummer 030/098. Nervenarzt 2019;90:379–387. https://doi.org/10.1007/s00115-018-0654-6
[7] Geisbüsch C et al. Diagnose- und Behandlungsstandards der zerebralen Sinus /Venenthrombose. Nervenarzt 2017;88:1159–1167. https://doi.org/10.1007/s00115-017-0377-0
[8] Macha K et al. Zerebrovaskuläre Komplikationen der Heparininduzierten Thrombozytopenie Typ II (HIT-II). Fortschr Neurol Psychiatr 2014;82(3):149-154. DOI: 10.1055/s-0034-1365923
[9] Pohl C et al. Neurologic complications in immune-mediated heparin-induced thrombocytopenia. Neurology 2000;54(6):1240-5. doi: 10.1212/wnl.54.6.1240.
[10] Selleng K und Greinacher A. Medikamentinduzierte Thrombozytopenien. intern. praxis 2006;46:753-765
Weitere Beiträge des Pandemie Spezials in DAZ 2021, Nr. 12
- Mehr Corona-Infektionen durch Pollenflug? Risiko für virale Atemwegsinfekte auch bei Allergikern nicht erhöht
- Startschuss nach Ostern: Hausärzte sollen in wenigen Wochen gegen COVID-19 impfen können
- Nach überstandener Infektion kann die Impfung warten: Aktuelle Empfehlungen der STIKO
- Corona-Ticker: Neues zu SARS-CoV-2 in Kürze






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.