
- DAZ.online
- DAZ / AZ
- DAZ 52/2020
- „Ordentliche“ ...
Pandemie Spezial
„Ordentliche“ Impfstoff-Zulassung für die EU
Warum eine Notfallzulassung nur eine Genehmigung ist und die EU mehr wollte
Seit Ende November lag der Antrag auf Zulassung für den Biontech/Pfizer-Impfstoff bei der Europäischen Arzneimittelagentur, wo die Unterlagen einer eingehenden wissenschaftlichen Prüfung unterzogen wurden. Großbritannien hat schon am 2. Dezember 2020 als erstes Land bereits eine Genehmigung für die mRNA-Vakzine erteilt. Wie die britische Arzneimittelbehörde MHRA (Medicines and Healthcare products Regulatory Agency) betont, handelt es sich hierbei jedoch keineswegs um eine Zulassung, sondern um die vorübergehende (temporary) Genehmigung der Anwendung bestimmter Chargen des COVID-19-Impfstoffs, basierend auf den Daten zur Qualität, Sicherheit und Wirksamkeit, die Pfizer/Biontech der MHRA in dem Zeitraum zwischen dem 1. Oktober und dem 2. Dezember übermittelt habe. Kanada hat am 9. Dezember eine bedingte Zulassung (with conditions) gewährt und die USA zwei Tage später eine Notfallzulassung (Emergency Use Authorization, EUA). Damit war der Druck auf die Europäische Arzneimittel-Agentur (EMA) immens gewachsen. Inzwischen hat die USA am 18. Dezember auch für den mRNA-Impfstoff von Moderna eine EUA erteilt, die EMA möchte am 6. Januar 2020 über den ihr vorliegenden Antrag entscheiden.
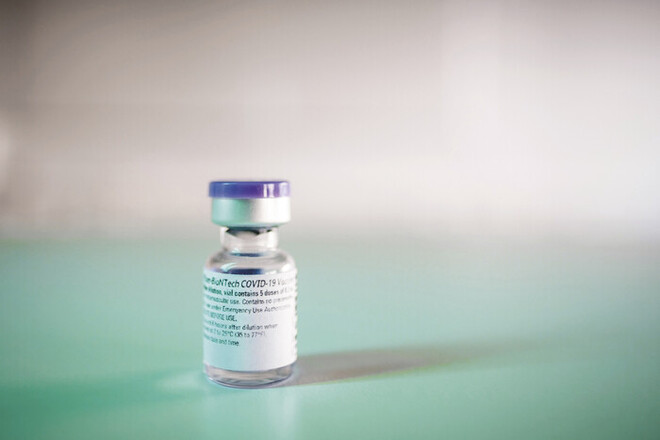
Der Biontech-Impfstoff Comirnaty® ist der erste EU-weit verfügbare Impfstoff gegen COVID-19.
Mit einer Pressemitteilung hat die Europäische Kommission Mitte Dezember versucht, Licht in das ganze Wirrwarr um Notfall-, bedingte und normale Zulassungen zu bringen. Darin hebt sie eingangs hervor, dass die EMA politisch unabhängig arbeite, angesichts der aufgeheizten Situation eine wichtige Feststellung. Außerdem hätten alle EU-Staaten entschieden, anstelle nationaler Genehmigungen den Weg zu einer europaweit gültigen Marktzulassung des Impfstoffes zu beschreiten. Damit sind die Optionen im Falle einer unzureichenden Datenlage, so wie sie für die COVID-19-Impfstoffe aktuell noch besteht, klar vorgezeichnet.
Die bedingte Zulassung
Für den Biontech/Pfizer-Impfstoff wurde eine bedingte Marktzulassung (conditional marketing authorization, CMA) beantragt. Bei einer solchen Zulassung, die zunächst auf ein Jahr befristet ist, werden die fehlenden Unterlagen mit einer Auflage nachgefordert (Art. 14-a der Verordnung [EG] Nr. 726/2004). Ist diese erfüllt, geht die CMA in eine reguläre Zulassung über. Ungeachtet dessen stellt auch eine bedingte Zulassung sicher, dass das Sicherheitssystem für Arzneimittel der EU vollumfänglich greift. Dieses beinhaltet Herstellerkontrollen einschließlich Chargenkontrollen für Impfstoffe sowie die Überwachung nach der Zulassung inklusive der Berichtspflichten über unerwünschte Arzneimittelwirkungen und eines Risikomanagementplans (RMP). Conditional marketing authorizations sind ein erprobtes Instrument. Seit ihrer Einführung wurden im zentralen Zulassungsverfahren bereits 33 bedingte Zulassungen erteilt, unter anderem für das erste COVID-19-Therapeutikum Remdesivir (Veklury®) Anfang Juli dieses Jahres. Bislang wurde für keine erteilte bedingte Zulassung das Ruhen oder der Widerruf angeordnet. Das Verfahren hat sich also bewährt.
Europäische Notfallzulassung?
Daneben besteht im zentralen Zulassungsverfahren auch noch die Möglichkeit, eine Zulassung „unter außergewöhnlichen Umständen“ (under exceptional circumstances) zu erwirken (Art. 14[8] der Verordnung [EG] Nr. 726/2004). Das Instrument ist jedoch nur für sehr eingeschränkte Fallkonstellationen gedacht, und zwar im Wesentlichen dann, wenn der Antragsteller nachweisen kann, dass er voraussichtlich auch in Zukunft keine vollständigen Daten über die Wirksamkeit und Sicherheit des Arzneimittels zur Verfügung stellen kann, etwa weil die Indikationen für das betreffende Arzneimittel so selten vorkommen. Bislang wurden auf zentralem Wege immerhin schon 40 Zulassungen „unter außergewöhnlichen Umständen“ erteilt. Trotzdem dürfte dieser Weg für einen COVID-19-Impfstoff angesichts der Kriterien kaum infrage kommen. Damit sind die Möglichkeiten für solche Sonderzulassungen im zentralen Verfahren ausgeschöpft.
Der nationale Weg
Bleibt der nationale Weg, und hier kommt die „Notfallzulassung“ ins Spiel. Nach dem EU-Kodex für Humanarzneimittel können die Mitgliedstaaten als Reaktion auf die vermutete oder bestätigte Verbreitung von krankheitserregenden Substanzen … vorübergehend das Inverkehrbringen eines nicht genehmigten Arzneimittels erlauben (Art. 5[2] der Richtlinie 2001/83/EG). Die Europäische Kommission betont in ihren Erläuterungen, dass eine solche Notfallgenehmigung keine Zulassung bedeutet, sondern die Genehmigung der vorübergehenden Anwendung eines nicht zugelassenen Arzneimittels, hier „Impfstoffs“ in einer Notsituation.
In Deutschland können die zuständigen Behörden in Krisenzeiten bei einer Pandemie im Einzelfall gestatten, dass Arzneimittel, die hierzulande nicht zugelassen sind, befristet in den Verkehr gebracht werden (§ 79 Abs. 5 AMG). Dies gilt im Falle eines Versorgungsmangels mit den Arzneimitteln, die für die Vorbeugung oder Behandlung einer bedrohlichen übertragbaren Krankheit benötigt werden. Das Bundesministerium für Gesundheit (BMG) hatte einen solchen Versorgungsmangel mit Blick auf das neuartige Coronavirus (COVID-19) vorsorglich schon am 27. Februar 2020 bekannt gemacht, hat sich aber indessen für den einheitlichen europäischen Weg entschieden.
Eingehendere Prüfung
Zwischen einer bedingten EU-Marktzulassung und nationalen Notfallzulassungen gibt es wesentliche Unterschiede. So muss bei einer bedingten Marktzulassung der ganze Katalog an Daten und Unterlagen, den das strenge EU-Zulassungsrecht vorsieht, vorgelegt und im Detail geprüft werden. Bei einer nationalen Notfallzulassung entscheidet ein Mitgliedstaat dagegen selbst darüber, welche Daten für eine solche Zulassung erforderlich sind und welche Anforderungen er an die Verwendung und Überwachung des Impfstoffs stellt. Hier können unter Umständen Abstriche gemacht werden, beispielsweise in Bezug auf den Umfang der klinischen Daten und Wirksamkeitsanalysen. Die EU-Kommission betont in ihren Erläuterungen, dass die behördliche Beurteilung der Daten deswegen mehr Zeit benötigen kann als ein Notfallzulassungsverfahren. Außerdem sind an der Überprüfung zentraler Zulassungsanträge regelmäßig viele Experten aus allen Mitgliedstaaten beteiligt, so dass ein weitreichender Konsens hergestellt werden muss. Auch vor der eigentlichen Erteilung der zentralen Zulassung durch die Kommission werden die Experten in den Mitgliedstaaten über den „Ständigen Ausschuss für Humanarzneimittel“ (nicht zu verwechseln mit dem CHMP) regelmäßig noch einmal zu dem Entwurf des Bescheides und den informierenden Texten angehört. So können sich die Anwender und Empfänger des neuen Impfstoffs am Ende auch in dieser unsicheren Lage darauf verlassen, dass vor Erteilung einer so weitreichenden Genehmigung alle „Netze und doppelten Boden“ genutzt wurden, die das Arzneimittelrecht der EU zum Schutz der Bürger vorhält.
Jetzt haftet der Hersteller
Ein weiterer gravierender Unterschied ist die Haftungsfrage. Bei einer bedingten EU-Marktzulassung haftet wie bei einer „normalen“ Zulassung deren Inhaber, also das herstellende Pharmaunternehmen. Im Falle einer Notfallzulassung für den vorübergehenden Vertrieb als nicht zugelassenes Produkt müssen die Mitgliedstaaten den Hersteller wie auch den Verantwortlichen für das Inverkehrbringen nach EU-Recht von der administrativen und zivilrechtlichen Haftung ausnehmen, wenn sie eine solche Notfallverwendung empfehlen oder vorschreiben. Dies dürfte für die Länder, die sich bei der Zulassung von COVID-19-Impfstoffen für die europäische Lösung ausgesprochen haben, ebenfalls eine maßgebliche Rolle gespielt haben. |
Literatur
Fragen und Antworten zum Zulassungsverfahren. Pressemitteilung der Europäischen Kommission vom 15. Dezember 2020. https://ec.europa.eu/germany/news/20201215-biontech-impfstoff_de
Weitere Beiträge des Pandemie Spezials in DAZ 2020, Nr. 52
- Kostenlos, aber nicht beratungslos: Was Apotheken ihren Kunden zu FFP2-Masken mit auf den Weg geben sollten
- Grünes Licht für Corona-Impfung: mRNA-Impfstoff Tozinameran von Biontech/Pfizer erhält bedingte Zulassung in der EU
- Wer wann geimpft werden darf: STIKO-Empfehlungen sind nicht vollständig in die Coronavirus-Impfverordnung eingegangen
- Genesen – aber nicht gesund: Symptome von „Long COVID“ belasten viele Patienten lange nach der akuten Infektion
- Corona-Ticker: Neues zu SARS-CoV-2 in Kürze





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.