
- DAZ.online
- DAZ / AZ
- DAZ 50/2020
- Ungewollt kinderlos
Schwerpunkt: Künstliche Befruchtung
Ungewollt kinderlos
Beratung zu Arzneimitteln vor und während einer Kinderwunschbehandlung
Die Weltgesundheitsorganisation definiert Sterilität (Synonym: Infertilität) als das Ausbleiben einer Schwangerschaft nach mindestens zwölf Monaten regelmäßigen ungeschützten Geschlechtsverkehrs zu optimalen Zeitpunkten. In Deutschland betrifft das etwa 7 bis 9% aller Paare im reproduktiven Alter. Die Ursachen für ungewollte Kinderlosigkeit sind vielfältig. Genetische Faktoren, Hormonstörungen, Infektionen (z. B. mit Chlamydien), organische Ursachen wie Samenleiterverschluss, schwerwiegende Erkrankungen wie Endometriose und psychische Faktoren sind die wichtigsten [1]. Zunehmend häufiger wird eine reproduktionsmedizinische Behandlung in Anspruch genommen, um sich den Wunsch nach einer eigenen Familie mithilfe Dritter zu erfüllen, zum Beispiel von homosexuellen Paaren. Weitere Informationen dazu finden sich im Beitrag „Künstliche Befruchtung im 21. Jahrhundert – Wissenswertes rund um die Reproduktionsmedizin“ in dieser Ausgabe der DAZ.
Lebensstilfaktoren nicht unterschätzen
Auch eine Reihe von Lebensstilfaktoren können sich negativ auf die Fruchtbarkeit auswirken. So konnte in Studien gezeigt werden, dass bei Frauen sowohl ein BMI < 17 kg/m² als auch ein BMI > 27 kg/m² häufiger zu Ovulationsstörungen und Infertilität führt. Nicht nur Frauen, sondern auch Männern mit Adipositas wird deshalb bei unerfülltem Kinderwunsch zu einer Gewichtsabnahme geraten. Weitere fertilitätsrelevante Risikofaktoren sind Rauchen, Alkohol- und Drogenkonsum und bei Frauen intensive sportliche Betätigung, insbesondere Leistungssport mit einer Dauer von mehr als fünf Stunden pro Woche.
Wenn die andrologische Untersuchung eine zu geringe Spermienqualität oder -quantität ergibt, konzentriert sich die Suche auf körperliche Ursachen wie Samenleiterverschluss, eine unfallbedingte Hodenverletzung, eine Infektion mit Mumps-Viren, einen zu spät korrigierten Hodenhochstand in der Kindheit oder sowie genetische Ursachen. Unterschätzt wird möglicherweise der Einfluss von Wärme auf die Fertilität, auch wenn die Datenlage für klare Empfehlungen noch nicht ausreicht. Einzelne Studien haben jedoch gezeigt, dass sich enge Kleidung, längeres Sitzen (z. B. in Kraftfahrzeugen), heiße Bäder oder regelmäßige Saunabesuche negativ auf die Spermienqualität und -menge auswirken können. So führten beispielsweise zweimal wöchentliche Saunabesuche über 15 Minuten bei Temperaturen zwischen 80 und 90 °C nachweislich zur Abnahme der Anzahl und Qualität der Spermien [1].
Beratung in der Apotheke
Eine häufige Ursache für Fertilitätsprobleme sind Rhythmusstörungen der Regelblutung (Regeltempo-Anomalien). Man unterscheidet dabei Oligomenorrhö (Zyklus länger als 21 Tage) und Polymenorrhö (Zyklus kürzer als 24 Tage). Für die Selbstmedikation dieser Beschwerden stehen verschiedene Präparate mit Extrakten aus Mönchspfefferfrüchten zur Verfügung (z. B. Agnolyt® Madaus Tinktur, Agnucaston® Filmtabletten, Femicur® N Hartkapseln). Empfohlen wird eine kurmäßige Anwendung ohne Unterbrechung. Bezüglich der Dauer (z. B. drei Monate) unterscheiden sich die Angaben in den Fachinformationen. Vor der Anwendung dieser Präparate sollte die Kundin vom Arzt abklären lassen, ob den Beschwerden eine schwerwiegende Ursache zugrunde liegt [2]. Bei unregelmäßigen Menstruationszyklen kann auch die Anschaffung eines Zykluscomputers (z. B. Clearblue advanced Fertilitätsmonitor) hilfreich sein. Er unterstützt die Frau dabei, ihre fruchtbaren Tage zu erkennen.
Viele Frauen sind darüber informiert, dass in der Schwangerschaft ein erhöhter Bedarf an Folsäure, Jodid, Vitamin D und gegebenenfalls weiteren Vitaminen und Mineralstoffen besteht. Dennoch werden die empfohlenen Zufuhrmengen offenbar nicht immer erreicht. In einer aktuellen Studie, die Daten zum Stillen und zur Säuglingsernährung in Deutschland erhoben hat, nahmen weniger als die Hälfte der 966 befragten Frauen wie empfohlen bereits vor Beginn der Schwangerschaft ein Folsäurepräparat ein. Ähnlich waren die Ergebnisse bei Jodid. Hier wird Frauen mit Kinderwunsch die Einnahme von 100 bis 150 µg täglich empfohlen [3]. Bei Folsäure sollten mindestens vier Wochen vor der Schwangerschaft und während der ersten drei Schwangerschaftsmonate zusätzlich zur Ernährung 400 µg eingenommen werden. Beginnt die Frau erst kurz vor oder bei Schwangerschaftsbeginn mit der Supplementation, wird eine Tagesdosis von 800 µg empfohlen. Zahlreiche Kombinationspräparate (z. B. Femibion®) sind verfügbar, um diese Zufuhrmengen zu erreichen [2].
Arzneimittel, die die Fruchtbarkeit beeinträchtigen können
Auch Arzneimittel können sich negativ auf die Zeugungs- oder Empfängnisfähigkeit auswirken. Die Bedeutung dieser Infertilitätsursache nimmt zu, wenn sich Paare erst in einem Alter für Kinder entscheiden, in dem das Risiko für Krankheiten wie Hypertonie, Fettstoffwechselstörungen oder Diabetes, aber auch Depressionen oder Tumorerkrankungen, bereits deutlich erhöht ist. In den Fachinformationen zahlreicher Arzneistoffe gegen diese und weitere Erkrankungen wird auf Nebenwirkungen wie sexuelle Dysfunktion, reduzierte Spermienqualität und -motilität oder verringerte Libido hingewiesen. Betroffen sind Wirkstoffe aus vielen verschiedenen Indikationsgebieten wie beispielsweise Antihypertonika, Urologika, Antiinfektiva und Psychopharmaka. Wird im Kundengespräch ein Wirkstoff mit einem derartigen Potenzial identifiziert, sollte von eigenmächtigem Absetzen dringend abgeraten werden. Der behandelnde Arzt kann in vielen Fällen einen alternativen Wirkstoff finden oder eine Behandlungspause vereinbaren, in der die fruchtbaren Tage für die Konzeption genutzt werden können [2, 4].
Fertilitätserhalt bei Krebspatienten
Die Behandlung einer Tumorerkrankung durch Operation, Strahlentherapie oder systemische Medikamente führt sehr häufig zu einer teilweisen oder kompletten Schädigung der Keimdrüsen, sowohl bei Männern als auch bei Frauen. Durch Kryokonservierung ist es möglich, vor einer Tumorbehandlung oder einer anderen keimzellschädigenden Therapie befruchtete oder unbefruchtete Eizellen, Ovarialgewebe, Spermienzellen oder Hodengewebe einzufrieren. Für gesetzlich Versicherte wurde 2019 ein Leistungsanspruch auf fertilitätserhaltende Maßnahmen gesetzlich festgeschrieben, wenn eine Behandlung, die die Fruchtbarkeit schädigt, vorgenommen werden muss.
Der Gemeinsame Bundesausschuss hat im Juli 2020 die Richtlinie zur Kostenübernahme für fertilitätsprotektive Maßnahmen beschlossen [5]. Darüber hinaus gibt es noch weitere fertilitätserhaltende Maßnahmen, die vor einer Krebstherapie eingesetzt werden. Dazu zählen vor einer Radiotherapie die operative Verlagerung der Eierstöcke aus dem Bestrahlungsfeld sowie die temporäre Suppression der Ovarien durch Applikation von Agonisten des Gonadotropin-Releasing-Hormons (GnRH-Agonisten) während der Chemotherapie [6].
Zuerst: Basisdiagnostik
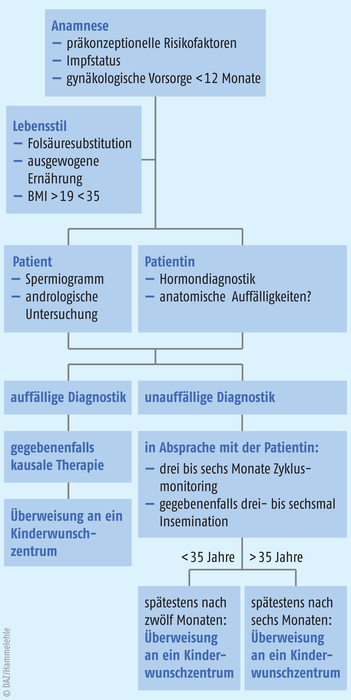
Die Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG) und ihre Schwestergesellschaften in der Schweiz (SGGG) und in Österreich (OEGGG) empfehlen das Vorgehen nach einem Flussdiagramm, wenn sich ein Paar mit unerfülltem Kinderwunsch in der gynäkologischen Praxis vorstellt. An die gründliche Anamnese und die Evaluation von Lebensstilfaktoren schließt sich eine endokrine Basisdiagnostik an, zu der bei der Frau die Bestimmung von Hormonen wie zum Beispiel FSH, LH, Prolaktin, Testosteron, Progesteron und Anti-Müller-Hormon (als Marker für die Eizellreserve) zählt. Beim Mann steht an erster Stelle die Aufnahme eines Spermiogramms sowie mindestens die Bestimmung von FSH und Testosteron. (s. Abb. 1). Auch die Bestimmung der Schilddrüsenfunktion gehört zur Basisdiagnostik bei vermuteter Infertilität der Frau, denn Schilddrüsen-Dysfunktionen sind eine häufige Ursache für unerfüllten Kinderwunsch und müssen deshalb vor einer reproduktionsmedizinischen Behandlung abgeklärt werden. Frauen mit einem TSH-Wert von > 2,5 U/l sollten so lange mit L-Thyroxin substituiert werden, bis er unter 2,5 mU/l liegt. Im Falle einer Hyperthyreose soll den ärztlichen Leitlinien zufolge eine Schilddrüsentherapie (Operation, Radiojod-Therapie) vor Therapiebeginn und Schwangerschaftseintritt abgeschlossen sein [1].
Abb. 1: Diagnostischer und zeitlicher Ablauf einer Abklärung bei unerfülltem Kinderwunsch (nach [1])
Negativ für Männer und Frauen: Hyperprolaktinämie
Bei einer pathologisch erhöhten Blutkonzentration des Hypophysenhormons Prolaktin – verantwortlich für Brustwachstum und Milchbildung – können bei Frauen Zyklusstörungen und bei Männern Libidoverlust und Potenzstörungen die Folge sein. Eine seltene Ursache für Hyperprolaktinämie ist ein hormonaktives Adenom des Hypophysenvorderlappens (Prolaktinom). Außerdem kann die Hormonstörung stressbedingt auftreten (latente Hyperprolaktinämie). Bei Gesunden erfolgt bei erhöhtem Prolaktin-Spiegel eine Rückkopplung zum Hypothalamus, worauf vermehrt Dopamin ausgeschüttet wird. Bei Prolaktin-bedingter Sterilität können die Dopamin(D2)-Rezeptor-Agonisten Bromocriptin (z. B. Pravidel®), Cabergolin (z. B. Dostinex®), Metergolin (Liserdol®) oder Quinagolid (Norprolac®) eingesetzt werden. Sie binden an D2-Rezeptoren an den laktotrophen Zellen der Hypophyse. Darüber hinaus gibt es Hinweise aus In-vitro-Studien, dass wässrig-alkoholische Mönchspfeffer-Extrakte, die bereits als Option für die Selbstmedikation erwähnt wurden, die Prolaktin-Freisetzung aus der Hypophyse hemmen können. Im Agnus-castus-Extrakt BNO 1095 wurden bizyklische Diterpene als diejenigen Substanzen identifiziert, die wahrscheinlich zur Prolaktin-senkenden Wirkung beitragen. In kultivierten Rattenhypophysenzellen kam es zur Bindung an den humanen Dopamin-Rezeptor Subtyp 2 und zu einer konzentrationsabhängigen Erniedrigung der Prolaktin-Freisetzung [2].
Eine weitere mögliche Ursache für Infertilität, die im Rahmen der Basisdiagnostik festgestellt werden kann, ist die hypergonadotrope Ovarialinsuffizienz. Diese Hormonstörung betrifft etwa 1 bis 2% der Frauen im fortpflanzungsfähigen Alter. Bei ihnen ist die Eizellreserve sehr gering und bereits vor Erreichen des 40. Lebensjahres erschöpft, sodass sie verfrüht in die Menopause kommen. Typisch sind hohe Konzentrationen der Gonadotropine FSH und LH, da die Hypophyse dadurch dem Mangel an reifen Follikeln gegenzusteuern versucht. Die einzige Möglichkeit für diese Frauen, einen Kinderwunsch zu realisieren, besteht in einer Eizellspende, was in Deutschland gesetzlich verboten ist.
Belastend: Endometriose und polyzystisches Ovarialsyndrom
Studien zufolge ist die Endometriose eine häufige Ursache für Infertilität. Die Behandlung erfolgt durch operative Eingriffe mit Entfernung der Endometriose-Herde oder durch verschiedene medikamentöse Optionen wie Gestagene (z. B. Dienogest), GnRH-Agonisten (Buserelin, Goserelin, Leuprorelin, Nafarelin, Triptorelin) oder kombinierte orale Kontrazeptiva (außer bei Kinderwunsch). Endometriose-Patientinnen mit Kinderwunsch müssen auch darüber aufgeklärt werden, dass bei ihnen im Falle einer Schwangerschaft das Risiko für Spontanaborte, vorzeitigen Blasensprung, vorzeitige Plazentalösung, Frühgeburtlichkeit, Gestationsdiabetes und weitere Schwangerschafts- und Geburtskomplikationen erhöht sein kann [7].
Auch das polyzystische Ovarialsyndrom (PCOS) betrifft viele Frauen im gebärfähigen Alter und wird daher bei ungewollter Kinderlosigkeit in Betracht gezogen. Die genauen Ursachen sind nicht bekannt. Die stark erhöhten Androgenkonzentrationen (Testosteron, Androstendion) im Blut führen zu typischen Vermännlichungs-Erscheinungen wie männlicher Behaarung und tiefer Stimmlage. Problematisch bei Kinderwunsch sind Zyklusstörungen wie Oligomenorrhö, Amenorrhö und Anovulation. Im Rahmen der hormonellen Basisdiagnostik werden normale bis erniedrigte FSH-Werte sowie stark erhöhte LH-Werte gemessen. Wenn Clomifen bei Frauen mit PCOS zur Ovulationsinduktion eingesetzt wird, ist besondere Vorsicht geboten, da sie verstärkt auf normale Dosierungen reagieren [2]. Auch der Aromatase-Hemmer Letrozol ist geeignet, jedoch in Deutschland für diese Indikation nicht zugelassen. Ebenfalls off label ist der Einsatz von Metformin oder Myo-Inositol bei polyzystischem Ovarialsyndrom und Infertilität [1, 8]. Corifollitropin alfa ist beim polyzystischen Ovarialsyndrom kontraindiziert.
Eingriff in die Hypothalamus-Hypophysen-Achse
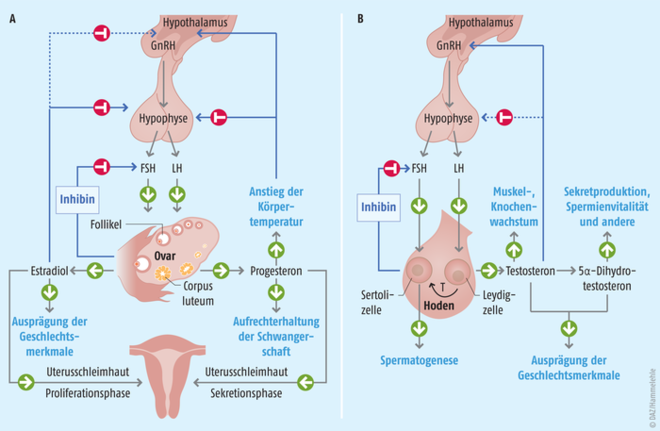
Die meisten Arzneimittel, die vor oder während einer assistierten Reproduktionsbehandlung eingesetzt werden, greifen in die Hypothalamus-Hypophysen-Gonaden-Achse ein (s. Abb. 2). Je nachdem, auf welcher Ebene die Störung vorliegt, kommen verschiedene Wirkstoffe zum Einsatz. Beim Mangel an Gonadotropin-Releasing-Hormon (GnRH, Gonadorelin) sendet der Hypothalamus nicht wie normalerweise etwa alle 90 Minuten einen GnRH-Puls an die Hypophyse zwecks Freisetzung von FSH und LH. Dies hat weitreichende negative Konsequenzen für die Sexualentwicklung, die Follikelreifung, die Ovulation und die Spermatogenese. Zu den Ursachen zählen Tumoren, Verletzungen wie Schädel-Hirn-Trauma, Stress und Leistungssport. Bei Frauen wird diese Störung als hypogonadotrope oder hypothalamische Ovarialinsuffizienz bezeichnet und geht unter anderem einher mit Amenorrhö bzw. Oligomenorrhö. Die Behandlung des Mangels ist bei Frauen und Männern durch eine Substitution mit Gonadorelin möglich, das durch ein Pumpsystem verabreicht wird (Lutrelef®, Lutrepulse®). Das Lutrepulse®-System besteht aus einem Handcomputer (Manager), den der Arzt programmiert, und einer kleinen Pumpe (Pod), die auf die Haut geklebt wird. Die Hormonabgabe erfolgt subkutan pulsatil in 90-minütigen (bei Frauen) bzw. 120-minütigen (bei Männern) Intervallen über einen Dauerkatheter. Der Pod muss alle drei Tage ausgewechselt werden. Die Behandlung wird ununterbrochen bis zum gewünschten Therapieerfolg (Spermatogenese bzw. Follikelreifung und Ovulation) fortgeführt [2, 9].
Abb. 2: An den hier dargestellten Abschnitten der hypothalamisch-hypophysären-gonadalen Achse können bei unerfülltem Kinderwunsch Störungen auftreten. Bei gesunden Frauen (A) führt die pulsatile Freisetzung von Gonadotropin-Releasing Hormon (GnRH) in der Hypophyse zur Ausschüttung des follikelstimulierenden Hormons (FSH) und des luteinisierenden Hormons (LH). Unter dem Einfluss von FSH kommt es im Ovar zur Follikelreifung sowie zur Bildung von Estradiol und von Inhibin. Inhibin und Estradiol inhibieren spezifisch die hypophysäre FSH-Freisetzung, nicht jedoch die LH-Freisetzung. Beim Mann (B) bewirken die GnRH-Pulse ebenfalls die Freisetzung von LH und FSH aus dem Hypophysenvorderlappen. LH stimuliert die Leydig-Zellen im Hoden zur Testosteron-Synthese. Testosteron hemmt sowohl die GnRH- als auch die LH-Freisetzung und stimuliert das Muskel- und Knochenwachstum. Zusammen mit FSH reguliert Testosteron (T) die Spermatogenese in den Sertolizellen, die ebenfalls Inhibin bilden, das selektiv die FSH-Freisetzung hemmt [nach Dingermann T, Winckler T, Zündorf I: Gentechnik Biotechnik. 3. Auflage 2019, Wissenschaftliche Verlagsgesellschaft mbH].
Auch das Stilben-Derivat Clomifen (z. B. Clomifen-ratiopharm®) greift an der Hypothalamus-Hypophysen-Achse an, wobei der Wirkmechanismus noch nicht vollständig geklärt ist. Wahrscheinlich bindet Clomifen an hypothalamische Estrogenrezeptoren und schwächt dadurch negative Feedback-Wirkungen der Estrogene ab. Es kommt zu einer verstärkten Freisetzung von Gonadorelin und infolgedessen zu einer vermehrten Sekretion von FSH und LH. Bei Frauen mit hypothalamisch-hypophysärer Dysfunktion mit Luteal-Insuffizienz, anovulatorischen Zyklen und Amenorrhö kann durch Clomifen ein Eisprung ausgelöst werden. Pro Zyklus sollte fünf Tage lang behandelt werden. Tritt bei einer Patientin nach drei Zyklen keine Ovulation auf, wird eine Fortsetzung der Behandlung nicht empfohlen. Die Höchstdauer liegt bei sechs Behandlungszyklen, danach ist erfahrungsgemäß nicht mehr mit einer Schwangerschaftsauslösung zu rechnen [2, 10].
Wirkstoffe | Präparate (Beispiele) | assistierte Reproduktionsbehandlung und weitere Indikationen | Anwendungshinweise | Nebenwirkungen (Auswahl), die in der Beratung angesprochen werden sollten |
|---|---|---|---|---|
Gonadotropin-Releasing-Hormon(GnRH)-Rezeptor-Agonisten | ||||
Buserelin | Metrelef® Nasenspray | Endometriose Ovulationshemmung bei einer assistierten Reproduktionsbehandlung | bei Schnupfen vor der Anwendung kräftig schnäuzen | Geruchs- und Geschmacksstörungen; durch Schwindel Beeinträchtigung des Reaktionsvermögens, z. B. beim Autofahren, möglich |
Nafarelin | Synarela® Nasenspray | Endometriose In-vitro-Fertilisation | mindestens 30 Minuten vor abschwellenden Nasensprays einsprühen | durch Schwindel Beeinträchtigung des Reaktionsvermögens, z. B. beim Autofahren, möglich |
Triptorelin | Decapeptyl® IVF Injektionslösung, s. c. | In-vitro-Fertilisation | Einstichstelle wechseln | erhöhtes Risiko von Stimmungsschwankungen und Depressionen |
Gonadotropin-Releasing-Hormon(GnRH)-Rezeptor-Antagonisten | ||||
Cetrorelix | Cetrotide® s. c. | Verhinderung eines vorzeitigen Eisprungs bei einer assistierten Reproduktionsbehandlung | im Kühlschrank lagern (2 °C bis 8 °C), 30 Minuten vor Anwendung herausnehmen; nicht einfrieren, Lichtschutz beachten, Einstichstelle wechseln | Überempfindlichkeitsreaktionen; bei Frauen mit starker Allergieneigung ist von der Behandlung abzuraten |
Ganirelix | Fyremadel® s. c., Orgalutran® s. c. | Verhinderung eines vorzeitigen Eisprungs bei einer assistierten Reproduktionsbehandlung | nicht einfrieren, Lichtschutz beachten, Einstichstelle wechseln | Überempfindlichkeitsreaktionen; bei Frauen mit starker Allergieneigung wird von der Behandlung abgeraten |
Gonadotropine | ||||
Corifollitropin alfa | Elonva® s. c. | kontrollierte ovarielle Stimulation (COS) bei einer assistierten Reproduktionsbehandlung | nur eine Injektion nötig anstelle täglich über sieben Tage bei rekombinantem FSH | falsch positiver hCG-Schwangerschaftstest möglich |
Follitropin beta | Puregon® s. c. | Anovulation, Follikelstimulation bei einer assistierten Reproduktionsbehandlung, Stimulation der Spermatogenese bei Männern | Einstichstelle wechseln | häufige Nebenwirkung bei Männern: Gynäkomastie |
Follitropin delta | Rekovelle® s. c. | kontrollierte ovarielle Stimulation bei einer assistierten Reproduktionsbehandlung | Schulung zur Anwendung des Fertigpens | Symptome eines ovariellen Hyperstimulationssyndroms beobachten (z. B. Abdominalschmerzen, aufgeblähtes Abdomen, Übelkeit, Erbrechen) |
humanes Choriongonadotropin (hCG) | Brevactid® 5000 IE i. m. | Ovulationsauslösung, abschließende Follikelreifung, Luteinisierung | zubereitete Lösung sofort nach Herstellung injizieren | falsch-positiver Schwangerschaftstest möglich |
Brevactid® 1500 IE i. m. | Herstellung der Fertilität bei Männern bei hypogonadotropem Hypogonadismus | |||
Choriongonadotropin alfa | Ovitrelle® s. c. | Anovulation; Superovulation bei einer assistierten Reproduktionsbehandlung | Geschlechtsverkehr am Tag der Injektion und am Folgetag empfohlen | falsch-positiver Schwangerschaftstest möglich |
Lutropin alfa | Luveris® s. c. | Stimulation der Follikelreifung bei schwerem FSH- und LH-Mangel | nach dem Öffnen der Zubereitung sofort verwenden | Symptome eines ovariellen Hyperstimulationssyndroms beobachten (z. B. Abdominalschmerzen, aufgeblähtes Abdomen, Übelkeit, Erbrechen) |
Menotropin (Lutropin + Follitropin) | Pergoveris® s. c. | Stimulation der Follikelreifung bei schwerem FSH- und LH-Mangel | nach dem Öffnen der Zubereitung sofort verwenden | Symptome eines ovariellen Hyperstimulationssyndroms beobachten (z. B. Abdominalschmerzen, aufgeblähtes Abdomen, Übelkeit, Erbrechen) |
Gestagene | ||||
Progesteron | Utrogest® luteal Vaginalkapseln | Unterstützung der Lutealphase bei einer assistierten Reproduktionsbehandlung | Weichkapsel tief in die Vagina einführen; nicht länger als bis zur zwölften Schwangerschaftswoche anwenden | wegen Schwindel und Schläfrigkeit Vorsicht bei Teilnahme am Straßenverkehr |
Lutinus®Vaginaltabletten | Anwendung beginnend am Tag der Oozyten-Entnahme, nach Feststellung der Schwangerschaft für maximal 30 Tage | |||
Crinone®Vaginalgel | wegen Gelverklumpung Austritt von kleinen, weißen Kügelchen aus der Scheide möglich | |||
IVF und ICSI: Arzneimittelgabe nach Protokollen
Spätestens wenn die Behandlungen mit den genannten Optionen nicht erfolgreich waren und die Entscheidung zugunsten einer assistierten Reproduktionsbehandlung gefallen ist, erfolgt in der Regel die Überweisung an ein Kinderwunschzentrum (s. Abb. 1).
In dieser Behandlungsphase werden die Ovulation und die Eizellreifung mithilfe verschiedener Wirkstoffe gezielt gesteuert (s. Tab.) und sonografisch überwacht. Dafür wurden verschiedene Protokolle entwickelt (z. B. „Agonisten-Protokoll“, „Antagonisten-Protokoll“).
GnRH-Agonisten sind länger und stärker wirkende Analoga des Peptidhormons GnRH. Ihre Anwendung führt zur Down-Regulation der GnRH-Rezeptoren an der Hypophyse und damit zur Unterbrechung der Sekretion der Gonadotropine FSH und LH. Dadurch wird die Bildung der Sexualhormone Estradiol und Testosteron herunterreguliert. GnRH-Agonisten werden wegen dieses Wirkprinzips nicht nur bei der ART, sondern auch bei der Behandlung hormonabhängiger Tumoren eingesetzt (Goserelin, Triptorelin und Leuprorelin z. B. beim Mamma- und Prostatakarzinom).
In der assistierten Reproduktionsbehandlung wird mit GnRH-Agonisten die Ovulationsinduktion vorbereitet. An dem Tag, an dem mittels humanem Choriongonadotropin (hCG) die Ovulationsauslösung beginnt, ist der GnRH-Agonist abzusetzen. Bei Buserelin und Nafarelin, die nasal appliziert werden, kann die Beratung in der Apotheke die Patientinnen bei der korrekten Anwendung unterstützen. Buserelin kann zur Reizung der Schleimhaut des Nasen-Rachen-Raumes führen. Neben Nasenbluten und Heiserkeit wurde auch über Geruchs- und Geschmacksstörungen als gelegentliche unerwünschte Wirkungen berichtet. Auf diese Nebenwirkung sollte die Kundin im Beratungsgespräch hingewiesen werden, da Geruchs- und Geschmacksstörungen auch als typische Symptome einer Infektion mit SARS-CoV-2 bekannt sind.
GnRH-Antagonisten
(s. Tab.) beeinflussen die Hypothalamus-Hypophysen-Gonaden-Achse durch kompetitive Bindung an die GnRH-Rezeptoren der Hypophyse. Es kommt zur schnellen, vollständigen und reversiblen Suppression endogener Gonadotropine, ohne dass initial eine Stimulation wie bei den GnRH-Agonisten erfolgt. Sie werden mit humanem FSH kombiniert, was zu einem schnelleren Follikelwachstum und damit zu einer Verkürzung der Zeit bis zur Entnahme reifer Eizellen führt [2, 10]. Studien haben gezeigt, dass die Anwendung von GnRH-Antagonisten versus GnRH-Agonisten-Protokollen das Risiko für ein schweres ovarielles Hyperstimulationssyndrom (OHSS, siehe Kasten „Risiko ovarielles Überstimulationssyndrom“) deutlich senken kann [11].
Risiko ovarielles Überstimulationssyndrom
Die Beratung in der Apotheke sollte Hinweise auf das Risiko des ovariellen Überstimulationssyndroms (OHSS) beinhalten, einer Nebenwirkung vieler Arzneimittel, die im Rahmen einer assistierten Reproduktionsbehandlung eingesetzt werden. Ein schweres OHSS ist potenziell lebensbedrohlich und kann sich durch Symptome wie akuter Abdominalschmerz, Dyspnoe und Oligurie ankündigen. Bei leicht bis mittelschwer ausgeprägtem ovariellen Überstimulationssyndrom treten Bauchschmerzen, Übelkeit und Durchfall auf. Die Patientin muss unverzüglich ihren Arzt aufsuchen, wenn sie diese Symptome bemerkt.
Gonadotropine kommen sowohl bei männlicher als auch bei weiblicher Infertilität in Kombination mit weiteren Arzneimitteln zum Einsatz. Die meisten Präparate werden heute gentechnisch durch Expression in Säugerzellen produziert.
Nach erfolgreichem Schwangerschaftsbeginn besitzt das Gestagen Progesteron eine große Bedeutung für den Erhalt der Schwangerschaft und wird deshalb auch bei der assistierten Reproduktionsbehandlung zur Unterstützung der Luteal-Funktion eingesetzt. Gleichwertig in der Wirkung ist humanes Choriongonadotropin. Progesteron besitzt jedoch ein niedrigeres Risiko für die Entwicklung eines ovariellen Überstimulationssyndroms. Progesteron-Zubereitungen werden in der Regel zwei- oder dreimal täglich lokal appliziert (s. Tab.). |
Literatur
[1] Diagnostik und Therapie vor einer assistierten reproduktionsmedizinischen Behandlung (ART). S2k-Leitlinie der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG), AWMF-Registernummer 015–085, Stand 1. Februar 2019, gültig bis 31. Januar 2022, www. awmf.org
[2] Fachinformationen der genannten Präparate, www.rote-liste.de
[3] Nur die Hälfte der Schwangeren nimmt Folsäure und Jod gemäß den Empfehlungen. Meldung des Berufsverbandes der Frauenärzte e.V. vom 16. Oktober 2020, www.frauenaerzte-im-netz.de/aktuelles/meldung/nur-die-haelfte-der-schwangeren-nimmt-folsaeure-und-jod-gemaess-den-empfehlungen/, Abruf am 6. November 2020
[4] Stahl V. Spermien in Gefahr. DAZ 2019;39:42
[5] Beschluss des Gemeinsamen Bundesausschusses über eine Richtlinie zur Kryokonservierung von Ei- oder Samenzellen oder Keimzellgewebe sowie entsprechende medizinische Maßnahmen wegen keimzellschädigender Therapie (Kryo-RL) vom 16. Juli 2020, www.g-ba.de/downloads/39-261-4393/2020-07-16_Kryo-RL_Erstfassung.pdf
[6] S2k-Leitlinie „Fertilitätserhalt bei onkologischen Erkrankungen“, AWMF-Registernummer 015/082, Stand September 2017, gültig bis September 2022, www. awmf.org
[7] Diagnostik und Therapie der Endometriose. S2k-Leitlinie der DGGG, SGGG and OEGGG, AWMF-Registernummer 015 – 045, Stand: 1. September 2020 , gültig bis 31. August 2023, www.awmf.org/leitlinien/detail/ll/015-045.html015/045, Abruf am 4. November 2020
[8] Blohmer JU, David M, Henrich M, Sehouli J (Hrsg.). Charité-Kompendium Gynäkologie 2020, 2. Auflage, De Gruyter
[9] Bartnitzky S et al. Behandlung der hypothalamischen Ovarialinsuffizienz mit der pulsatilen GnRH-Substitution., Hrsg. Schmedemann R, 1. Auflage 2014, ISBN-Nr. 978-3-00-045178-2
[10] Geisslinger G, Menzel S, Gudermann T, Hinz B, Ruth P. Mutschler Arzneimittelwirkungen. Pharmakologie – Klinische Pharmakologie –Toxikologie. 11., völlig neu bearbeitete Auflage 2020, Wissenschaftliche Verlagsgesellschaft Stuttgart
[11] Diedrich K, Ludwig M, Griesinger G (Hrsg.) Reproduktionsmedizin. 2. Auflage, Springer-Verlag GmbH, 2020






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.