
- DAZ.online
- DAZ / AZ
- DAZ 41/2020
- Gecheckt: ASS und NSAR
Arzneimittel und Therapie
Gecheckt: ASS und NSAR
Wann die thrombozytenaggregationshemmende Wirkung aufgehoben wird
Neben der ursprünglichen Nutzung als Analgetikum, Antipyretikum und Antiphlogistikum wird niedrig dosierte Acetylsalicylsäure (100 mg in Deutschland) seit den Achtzigerjahren des letzten Jahrhunderts auch intensiv als Thrombozytenaggregationshemmer unter anderem zur Sekundärprophylaxe des Myokardinfarkts, von transitorischen ischämischen Attacken und Schlaganfällen bei kardiovaskulären Risikopatienten genutzt und seit wenigen Jahren zudem zur Prävention des Kolonkarzinoms angewendet. Somit ist es nicht überraschend, dass ASS auf der Liste der unentbehrlichen Arzneimittel der WHO geführt wird.
Aufgrund des im Vergleich zu anderen nichtsteroidalen Antirheumatika (NSAR) höheren Potenzials für Magenreizungen wird Acetylsalicylsäure heute primär in geringerer Dosierung (100 mg in Deutschland, 300 mg in den USA) als Thrombozytenaggregationshemmer eingesetzt. In den letzten Jahren mehrten sich jedoch die Hinweise, dass die Wirksamkeit von ASS in Kombination mit anderen nichtsteroidalen Antirheumatika nachteilig beeinflusst wird.
Bereits 2001 wurde im renommierten „New England Journal of Medicine“ die erste derartige Interaktionsstudie publiziert [1]. Konkret erhielten in dieser Studie je sechs gesunde Probanden die folgenden Behandlungsschemata für jeweils sechs aufeinanderfolgende Tage:
- 81 mg ASS und zwei Stunden später 400 mg Ibuprofen,
- 81 mg ASS und zwei Stunden später 1000 mg Paracetamol und
- 81 mg ASS und zwei Stunden später 25 mg Rofecoxib.
Nach einer 14-tägigen Auswaschphase erhielten die Probanden im Cross-over-Design die identische Medikation, nur in umgekehrter Reihenfolge. Als Surrogate der Wirkung wurde im Plasma der Freiwilligen Thromboxan B2 – ein Marker für die Cyclooxygenase-Aktivität – und die Plättchenaggregation bestimmt. Es zeigte sich, dass Ibuprofen sowohl die Hemmung der Thromboxan-B2-Bildung reduzierte, wenn es vor der Acetylsalicylsäure eingenommen wurde, als auch drastisch die Thrombozytenaggregationshemmung, wohingegen die umgekehrte Einnahme und auch die Einnahme von Paracetamol und Rofecoxib in jeder Form keinen Einfluss hatten [1]. In einem weiteren Studienarm der Untersuchung wurde im Parallelgruppendesign der Einfluss von mehrmals täglicher Einnahme von Ibuprofen (400 mg um 10, 15 und 20 Uhr) oder Diclofenac (75 mg um 10 und 18 Uhr) auf die Wirksamkeit einer jeweils am Morgen eingenommenen magensaftresistenten Formulierung von ASS (81 mg um 8 Uhr) geprüft. Auch hier konnte im Plasma von sechs gesunden Freiwilligen eine drastisch reduzierte Hemmung der Thrombozytenaggregation bei Ibuprofen nachgewiesen werden, nicht aber bei Diclofenac. Der Grund für die dargestellte Interaktion liegt offensichtlich in einer Kompetition um den Wirkort von ASS und Ibuprofen bzw. anderer NSAR: der Cyclooxygenase 1 (COX-1). Allein eingenommen hemmt ASS durch Acetylierung eines Serin-Rests in Position 530 im katalytischen Zentrum die COX-1 irreversibel. Dadurch wird die Bindung des Substrates (Arachidonsäure) durch das Enzym unterbunden: Unter anderem kann die Cyclooxygenase 1 dann nicht mehr den starken Plättchenaktivator Thromboxan A2 bilden, und infolgedessen wird die Thrombozytenaggregation in gewünschter Art gehemmt. Die Dauer der Wirkung entspricht dabei der Lebensdauer der Blutplättchen (fünf bis zwölf Tage). Wird allerdings ein NSAR wie Ibuprofen mit einer hohen Bindungsaffinität zur COX-1 zeitlich vor der ASS eingenommen, so blockiert das zuvor eingenommene NSAR die Bindungsstelle und somit die Wirkung von Acetylsalicylsäure, die aufgrund des schnellen ASS-Abbaus (Plasmaeliminationshalbwertszeit t1/2 = ~0,5 bis 1 Stunde) auch später nicht wieder einsetzen kann. Bei Diclofenac scheint diese Interaktion nicht aufzutreten, da es einerseits an einer anderen Bindungsstelle der COX-1 anzugreifen scheint und andererseits aufgrund seiner geringeren Bindungsaffinität und kürzeren Verweildauer in der Zirkulation (t1/2 = 1 bis 2 Stunden) als Ibuprofen (t1/2 = 2 bis 4 Stunden). Rofecoxib hat als selektiver COX-2-Hemmstoff keinen direkten Einfluss auf die Thrombozytenaggregation, wohingegen Paracetamol nur ein schwacher COX-1-Hemmstoff ist und seine Wirkung über eine zentrale Cyclooxygenase 3 (Splicevariante der COX-1) zu entfalten scheint [2].
Gecheckt – Interaktionen erkennen und vermeiden
In unserer Serie „Gecheckt“ widmen wir uns klinisch relevanten Wechselwirkungen häufig eingesetzter Wirkstoffkombinationen. Kernelement jeder Folge ist eine grafische Zusammenfassung der wesentlichen Punkte, die einen schnellen Überblick über Interaktionspartner, die Art der Interaktion, Risiken und mögliche Maßnahmen bietet. Bisher sind erschienen:
- Simvastatin und Amiodaron: DAZ 2019, Nr. 28, S. 24
- Polyvalente Kationen: DAZ 2019, Nr. 32, S. 25
- Triple Whammy: DAZ 2019, Nr. 36, S. 37
- Orale Kontrazeptiva: DAZ 2019, Nr. 45, S. 31
- Tabakrauch: DAZ 2020, Nr. 1 - 2, S. 33
- Rivaroxaban: DAZ 2020, Nr. 12, S. 43
- Alkohol und Antibiotika: DAZ 2020, Nr. 18, S. 61
Ibuprofen zwei Stunden nach oder acht Stunden vor ASS
Die Befunde aus der dargestellten experimentellen Studie mit gesunden Freiwilligen konnte nachfolgend in einer retrospektiven Kohortenstudie aus Großbritannien mit über 7000 Patienten bestätigt werden [3]. Konkret war hierbei die Gesamtsterblichkeit bei der kombinierten Anwendung von ASS und Ibuprofen im Vergleich zur alleinigen Gabe von ASS nahezu verdoppelt (relatives Risiko [RR]: 1,93; 95%-Konfidenzintervall [KI]: 1,30 bis 2,87; p = 0,001), wohingegen die Einnahme von Diclofenac und anderen NSAR keinen Einfluss hatte. In einer amerikanischen Fall-Kontroll-Studie wurde eine ähnliche Tendenz gezeigt, die Unterschiede waren jedoch statistisch nicht signifikant (RR: 2,03) [4]. Eine Subgruppenanalyse der Physicians Health Study, einer placebokontrollierten randomisierten Doppelblindstudie mit über 22.000 männlichen Teilnehmern, zeigte, dass die Schutzwirkung von ASS (325 mg, jeden zweiten Tag eingenommen) durch gleichzeitige Anwendung von NSAR an mehr als 60 Tagen pro Jahr komplett aufgehoben wurde. Dabei wurde hier allerdings nicht zwischen den zusätzlich eingenommenen NSAR unterschieden und die Einnahmezeit nicht berücksichtigt [5].
Auch in der TARGET(Therapeutic Arthritis Research and Gastrointestinal Event Trial)-Studie, eine ebenfalls randomisierte, kontrollierte Studie, waren kardiovaskuläre Ereignisse häufiger bei Patienten, die neben ASS noch Ibuprofen einnahmen (1,48 pro 100 Patientenjahre) im Vergleich zu Patienten mit zusätzlicher Einnahme des COX-2-Hemmers Lumiracoxib (0,85 pro 100 Patientenjahre), auch wenn die Unterschiede nicht signifikant waren [6]. Nachfolgende Kohorten- oder Fall-Kontroll-Studien konnten dieses Risiko jedoch nicht eindeutig verifizieren, sodass seinerzeit keine klare Evidenz für eine klinisch relevante Interaktion zwischen Ibuprofen und ASS vorlag [7 – 9]. Nichtsdestotrotz wurde in der Folge bereits im Jahr 2009 vom Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) die Aktualisierung von Produktinformationen für Ibuprofen und niedrig dosierter Acetylsalicylsäure angeordnet und der Hinweis aufgenommen, dass Ibuprofen bei gleichzeitiger Anwendung mit Acetylsalicylsäure die Wirkung von niedrig dosierter Acetylsalicylsäure auf die Blutplättchenaggregation hemmen kann [10].
In der Folgezeit wurden zahlreiche weitere experimentelle Studien mit Ex-vivo-Beurteilung der Thrombozytenfunktion durchgeführt, die nicht nur für Ibuprofen, sondern auch für Indometacin und Naproxen eine signifikante Reduktion der Thrombozytenaggregationshemmung nachweisen konnten, nicht aber für selektive COX-2-Hemmer [11 – 16]. Diese Interaktion trat wie für Ibuprofen beschrieben bei vorheriger Einnahme des zusätzlichen NSAR (zwei Stunden) oder aber mehrtägiger Einnahme auf. Etwas überraschend waren in diesem Zusammenhang ähnliche In-vitro-Befunde für Metamizol [17], welches ähnlich wie Paracetamol nicht primär über Hemmung der COX-1 wirken soll [18].
Für Metamizol konnte in einer kleinen Beobachtungsstudie mit Patienten mit koronarer Herzkrankheit (KHK) gezeigt werden, dass die Hemmung der Thrombozytenaggregation durch ASS bei gleichzeitiger Einnahme von Metamizol aufgehoben war [19], wobei die Effekte reversibel und dosisabhängig waren und nicht auftraten, wenn Acetylsalicylsäure 30 Minuten vor Metamizol eingenommen wurde [20]. In einer weiteren Beobachtungsstudie mit 72 KHK-Patienten war die gleichzeitige Gabe von ASS und Metamizol nach einer im Mittel etwa dreijährigen Behandlung mit einem signifikant höheren Risiko für Herzinfarkt, Schlaganfall oder kardiovaskulär bedingtem Tod assoziiert (Odds Ratio [OR]: 4,5; 95%-KI: 1,7 bis 12,3; p = 0,0028) [21]. Eine andere Beobachtungsstudie mit 41 Schlaganfallpatienten bestätigte die bestehende Thrombozytenaggregation (fehlende ASS-Wirkung) bei 62% der Patienten, die ASS und Metamizol gleichzeitig einnahmen bei zudem schlechterer Erholung von neurologischen Defiziten [22]. Allerdings liegen auch Studien vor, die kein Risiko für das Auftreten der genannten Interaktion nachweisen konnten [23 – 24].
ASS 30 Minuten vor Metamizol
In diesem Zusammenhang wurde die Fachinformation von Metamizol-Präparaten bereits im Jahr 2014 um den Hinweis ergänzt, dass die gemeinsame Anwendung von ASS mit Vorsicht zu erfolgen hat, auch wenn diese Aussage nicht sehr praxistauglich ist. Trotz oder wohl gerade wegen der zum Teil kontroversen Datenlage und den unklaren Ableitungen für die Praxis empfahl die Arzneimittelkommission der Deutschen Ärzteschaft in einer Stellungnahme vom Mai 2018, dass bei gegebener Komedikation ASS etwa 30 Minuten vor Metamizol eingenommen werden sollte [25]. Metamizol sollte zudem in möglichst geringer Dosis zugeführt werden. Allerdings schränkt die Stellungnahme auch ein, dass bisher nicht klar ist, ob der genannte zeitliche Abstand einen Vorteil mit sich bringt, wenn beide Arzneistoffe in Dauermedikation eingenommen werden. Einige der zuvor genannten experimentellen Studien suggerieren dies [1, 13, 15]. Eine aktuelle Observationsstudie mit 80 KHK-Patienten bestätigte, dass Metamizol zur Minimierung der Interaktion in möglichst geringer Dosis, oral statt i. v. und 30 Minuten nach ASS eingenommen werden sollte [26].
Folgerichtig hat die Pharmakovigilanz-Arbeitsgruppe (PhVWP) des Ausschusses für Humanarzneimittel (CHMP) bei der Europäischen Arzneimittelbehörde (EMA) im Frühjahr dieses Jahres ähnlich wie bei Ibuprofen auch die Kombination von Metamizol und ASS als eine klinisch bedeutsame Interaktion eingestuft und die Änderung der jeweiligen Produktinformationen angeordnet [27]. Inwiefern dies Neuerungen im Vergleich zu den bereits im Jahr 2014 beschlossenen und umgesetzten Änderungen der Fachinformationen mit sich bringt, bleibt abzuwarten.
Zusammenfassend kann festgehalten werden, dass trotz häufiger Anwendung der genannten Arzneistoffe überzeugende Daten aus großen, randomisierten Doppelblindstudien mit der primären Zielstellung der Prüfung der kardiovaskulären Sicherheit bisher nicht bzw. nur unzureichend vorliegen. Vorliegende experimentelle Studien sowie Daten aus Beobachtungsstudien lassen aber folgende Ableitungen für die Praxis bei bestehender Therapie mit niedrig dosierter ASS zu [28]:
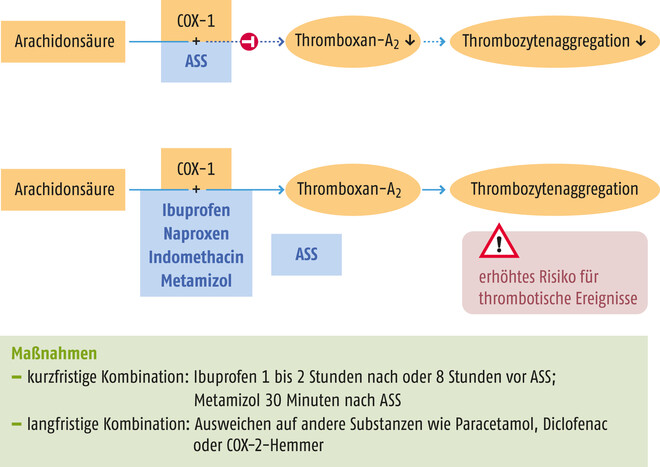
- Bei kurzfristiger Kombination mit Metamizol sollte Metamizol 30 Minuten nach ASS eingenommen werden (möglichst geringe Dosis). [Dieser Text wurde korrigiert. Korrekt ist sowohl in der Abbildung als auch in der Zusammenfassung, dass Metamizol 30 Minuten nach ASS genommen werden sollte. Wir bitten diesen Fehler zu entschuldigen.]
- Bei kurzfristiger Kombination mit Ibuprofen sollte Ibuprofen ein bis zwei Stunden nach oder acht Stunden vor ASS eingenommen werden (möglichst geringe Dosis). [Dieser Text wurde korrigiert. Korrekt ist sowohl in der Abbildung als auch in der Zusammenfassung, dass Ibuprofen ein bis zwei Stunden nach oder acht Stunden vor ASS eingenommen werden sollte.]
- Retardierte ASS scheint in Kombination mit Ibuprofen oder Metamizol keinen Vorteil gegenüber schnell freisetzenden Arzneiformen zu haben.
- Bei nötiger Dauertherapie mit ASS sollten Ibuprofen und Metamizol aus Sicherheitsgründen gemieden werden und auf andere Substanzen wie Diclofenac, Paracetamol oder COX-2-Hemmer ausgewichen werden.
Dieser konservativen Bewertung folgt unter anderem auch die Fachinformation Aspirin® protect 100, in der empfohlen wird: „Aspirin® protect 100 mg sollte daher nicht zusammen mit einem der o. g. Stoffe angewendet werden, ohne dass der Arzt ausdrücklich die Anweisung gegeben hat“ [31]. Ähnliche Aussagen finden sich wie bereits erwähnt auch in den Fachinformationen der Metamizol-Präparate.
Auf klinisch möglicherweise nicht unerhebliche Aspekte hebt die aktuelle Diskussion der Interaktion zwischen ASS und NSAR jedoch nicht ab:
- die überzeugend beschriebenen Unterschiede des kardiovaskulären Risikos von NSAR in der Langzeittherapie (Diclofenac > Ibuprofen > Naproxen) [29] und
- die in Deutschland insbesondere bei übergewichtigen Patienten (~50 bis 65% der Bundesbürger sind übergewichtig) möglicherweise zu geringe Dosierung von 100 mg ASS zur Thrombozytenaggregation [30].
Weitere klinische Studien zur Klärung dieser sehr praxisrelevanten Interaktion sind nötig, um in Abwägung des kardiovaskulären Risikopotenzials von alternativen NSAR eindeutige Evidenz für die Relevanz dieser Interaktion zu schaffen und fundierte Ableitungen für die Praxis liefern zu können. |
Literatur
[1] Catella-Lawson F et al. Cyclooxygenase inhibitors and the antiplatelet effects of aspirin. Engl J Med 2001;345(25):1809-1817
[2] Graham GG et al. Mechanism of action of paracetamol. Am J Ther 2005; 12(1):46-55
[3] MacDonald TM et al. Effect of ibuprofen on cardioprotective effect of aspirin. Lancet 2003;361(9357):573-574
[4] Kimmel SE et al. The effects of nonselective non-aspirin non-steroidal anti-inflammatory medications on the risk of nonfatal myocardial infarction and their interaction with aspirin. J Am Coll Cardiol 2004;43(6):985-990
[5] Kurth T et al. Inhibition of clinical benefits of aspirin on first myocardial infarction by nonsteroidal antiinflammatory drugs. Circulation 2003;108(10):1191-1195
[6] Farkouh ME et al. Comparison of lumiracoxib with naproxen and ibuprofen in the Therapeutic Arthritis Research and Gastrointestinal Event Trial (TARGET), cardiovascular outcomes: randomised controlled trial. Lancet 2004;364:675-684
[7] Curtis JP et al. Aspirin, ibuprofen, and mortality after myocardial infarction: retrospective cohort study. BMJ 2003;327(7427):1322-1323
[8] Patel TN et al. Use of aspirin and ibuprofen compared with aspirin alone and the risk of myocardial infarction. Arch Intern Med 2004;164(8):852-856
[9] García Rodríguez LA et al. Nonsteroidal antiinflammatory drugs and the risk of myocardial infarction in the general population. Circulation 2004;109(24):3000-3006
[10] Ibuprofen und niedrig dosierte Acetylsalicylsäure: aktualisierte Texte für die Produktinformationen. Informationen des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) vom 22. Juni 2009, www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RV_STP/g-l/ibuprofen-ass.html
[11] Gladding PA et al. The antiplatelet effect of six non-steroidal anti-inflammatory drugs and their pharmacodynamic interaction with aspirin in healthy volunteers. Am J Cardiol 2008;101(7):1060-1063
[12] Li X et al. Differential impairment of aspirin-dependent platelet cyclooxygenase acetylation by nonsteroidal antiinflammatory drugs. Proc Natl Acad Sci USA 2014; 11(47):16830-16835
[13] Anzellotti P et al. Low-dose naproxen interferes with the antiplatelet effects of aspirin in healthy subjects: recommendations to minimize the functional consequences. Arthritis Rheum 2011;63(3):850-859
[14] Yokoyama H et al. Influence of non-steroidal anti-inflammatory drugs on antiplatelet effect of aspirin. J Clin Pharm Ther 2013;38(1):12-15
[15] Gurbel PA et al. Thromboxane inhibition during concurrent therapy with low-dose aspirin and over-the-counter naproxen sodium. Thromb Thrombolysis 2018;45(1):18-26
[16] Schuijt MP et al. The interaction of ibuprofen and diclofenac with aspirin in healthy volunteers. British Journal of Pharmacology 2009;157:931-934
[17] Hohlfeld T et al. Pyrazolinone analgesics prevent the antiplatelet effect of aspirin and preserve human platelet thromboxane synthesis. Thromb Haemost 2008;6(1):166-173
[18] Pierre SC et al. Inhibition of cyclooxygenases by dipyrone. Br J Pharmacol 2007;151(4):494-503
[19] Polzin A et al. Dipyrone (metamizole) can nullify the antiplatelet effect of aspirin in patients with coronary artery disease. J Am Coll Cardiol 2013;62(18):1725-1726
[20] Polzin A et al. Prevention of dipyrone (metamizole) induced inhibition of aspirin antiplatelet effects. Thromb Haemost 2015;114(1):87-95
[21] Achilles A et al. Analgesic medication with dipyrone in patients with coronary artery disease: Relation to MACCE. Int J Cardiol 2017;236:76-81
[22] Dannenberg L et al. Dipyrone comedication in aspirin treated stroke patients impairs outcome. Vascul Pharmacol 2016;87:66-69
[23] Wilczyński M et al. Metamizole and Platelet Inhibition by Aspirin Following On-Pump Coronary Artery Bypass Grafting. J Cardiothorac Vasc Anesth 2018;32(1):178-186
[24] Börgermann J et al. Individual variability of response and non-response to acetyl salicylic acid after cardiac surgery. Platelets 2010;21(8):610-615
[25] Arzneimittelkommission der Deutschen Ärzteschaft. Kann Metamizol die Wirkung von ASS auf die Thrombozytenaggregation behindern? Dtsch Arztebl 2018;115(18):897-898
[26] Dannenberg L et al., Dose reduction, oral application, and order of intake to preserve aspirin antiplatelet effects in dipyrone co-medicated chronic artery disease patients. Eur J Clin Pharmacol 2019;75:13-20
[27] Moll D. PRAC/CMDH: Wechselwirkung ASS/Metamizol: klinisch relevant. DAZ.online vom 26. März 2020, www.deutsche-apotheker-zeitung.de/news/artikel/2020/03/26/wechselwirkung-ass-metamizol-klinisch-relevant
[28] Schnabel A et al. Interaktion von Metamizol und ASS: Reicht die Evidenz für klinische Konsequenzen? Arzneiverordnung in der Praxis 2019;46(1-2):45-51
[29] Arzneimittelkommission der deutschen Ärzteschaft. Nichtsteroidale Antirheumatika (NSAR) im Vergleich: Risiko von Komplikationen im oberen Gastrointestinaltrakt, Herzinfarkt und Schlaganfall. Dtsch Arztebl 2013;110(29-30):1447-1448
[30] Rothwell PM et al. Effects of aspirin on risks of vascular events and cancer according to bodyweight and dose: analysis of individual patient data from randomised trials. Lancet 2018;392(10145):387-399
[31] Fachinformation Aspirin® protect 100 mg, Stand: Dezember 2019





















1 Kommentar
vorher oder nachher
von Dr.Martin Schüßler am 11.10.2020 um 15:13 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.