
- DAZ.online
- DAZ / AZ
- DAZ 34/2020
- Älter werden mit HIV
Infektiologie
Älter werden mit HIV
Konsequente antiretrovirale Therapie verlängert die Lebenserwartung von Menschen mit HIV
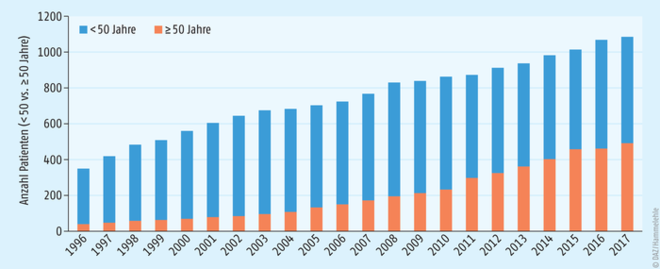
In Deutschland lebten Ende 2018 laut Robert Koch-Institut 87.900 Menschen mit HIV/AIDS, darunter 17.300 Frauen [1]. Mit 1600 von 2400 Neuinfektionen in 2018 waren die häufigsten Neuinfektionen in Deutschland bei Männern, die Sex mit Männern haben (MSM), zu beobachten. Seit Mitte der 1990er-Jahre steigt die Zahl von Menschen mit HIV kontinuierlich an. So hat sich bei den über 40-Jährigen die Gesamtzahl der mit HIV lebenden Menschen seit Anfang der 1990er- Jahre etwa verfünffacht [1]. Dies ist zum einen auf den Alterungsprozess der Population mit HIV bei deutlich verminderter Sterblichkeit durch Einführung der antiretroviralen Kombinationstherapie seit Mitte der 1990er-Jahre, zum anderen aber auch auf eine gestiegene Zahl von Neuinfektionen in höheren Altersgruppen zurückzuführen. Im eigenen Patientenkollektiv der Bonner HIV-Ambulanz liegt der Anteil der Personen, die über 50 Jahre alt sind, mittlerweile fast schon bei 50% (s. Abb. 1).
Dabei waren 2017 etwa 50% der HIV-infizierten Männer über 50 Jahre alt, gegenüber nur 30% der HIV-infizierten Frauen. In den USA waren 2015 bereits 47% der Menschen, die mit HIV leben über 50 Jahre alt und 16% über 65 Jahre [2]. Der zunehmende Anteil an älteren Patienten muss entsprechend in der HIV-Sprechstunde mit berücksichtigt werden, da hier andere Vorsorgeuntersuchungen und Anforderungen an die antiretrovirale Therapie zu beachten sind.
Änderung der Todesursachen bei HIV-Infizierten
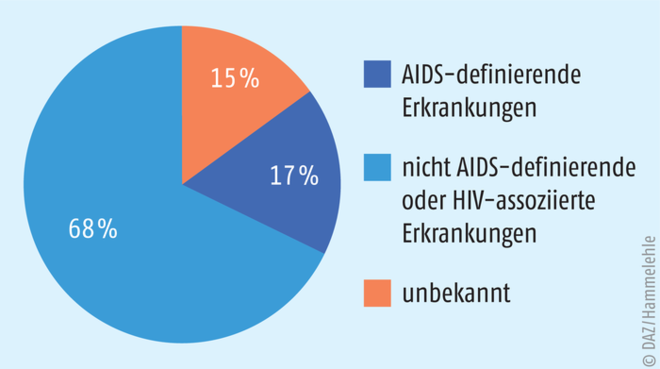
Mit den Verbesserungen in der antiretroviralen Therapie und der mittlerweile fast normalen Lebenserwartung, vorausgesetzt, dass die antivirale Therapie vor Ausbruch der AIDS-Erkrankung begonnen wurde, ist es zu einer deutlichen Änderung der Todesursachen bei HIV-Infizierten gekommen. Während im Jahre 2000 AIDS-definierende Ereignisse noch fast 50% der Todesursachen bei HIV-Infizierten ausmachten, sind es mittlerweile international (wo es komplikationslos Zugang zur antiretroviralen Therapie gibt) wie auch im eigenen Patientenkollektiv nur noch zwischen 17% bis 25% (s. Abb. 2) [3, 4]. Als Todesursache zugenommen haben dagegen onkologische, hepatische und kardiovaskuläre Erkrankungen. Die Tabelle 1 zeigt die im Bonner Patientenkollektiv ermittelten Todesursachen.
Abb. 2: Todesursachen bei HIV-Infizierten, wenn der Zugang zu einer antiretroviralen Therapie besteht (nach [3, 4]).
Todesursachen | Anzahl der Patienten (n) |
|---|---|
AIDS-definierende Erkrankungen | |
AIDS-assoziierte Infektionen | 9 |
Non-Hodgkin-Lymphome | 4 |
sonstige | 1 |
Nicht-AIDS Malignome | 16 |
kardiovaskuläre Erkrankungen | 11 |
Infektionen (Nicht HIV-assoziiert) | 10 |
Lebererkrankungen | 6 |
Suizid | 5 |
sonstige | 7 |
unbekannt | 12 |
Tumorerkrankungen sind inzwischen die häufigste Todesursache und treten in der HIV-Population dreimal häufiger auf als in der Gesamtbevölkerung. Das trifft nicht nur auf HIV-assoziierte Tumoren wie Kaposi-Sarkom und Non-Hodgkin-Lymphom zu, sondern auch auf Anal-, Genital-, Leber- und Lungentumoren. Der Grund hierfür ist, dass die genannten Krebserkrankungen oft mit anderen viralen Erkrankungen wie humanen Papillomviren und Hepatitis-Viren, die bei HIV-Patienten gehäuft vorkommen, assoziiert sind, oder mit Tabakkonsum in Zusammenhang stehen. Auch Schäden an der Leber, vor allem die Entwicklung einer nicht alkoholischen Fettleber (NAFL), können auftreten. Hinzu kommen Lebererkrankungen im Rahmen der bei HIV häufiger anzutreffenden Virushepatitis-Koinfektion. Häufig treten bei HIV-Infizierten auch Diabetes, Insulinresistenz, Fettstoffwechselstörungen und metabolisches Syndrom auf. Entsprechend hoch ist das Risiko für kardiovaskuläre Erkrankungen, auf die etwa 10% der Todesfälle zurückgehen. Dies ist zum Teil ebenfalls durch den erhöhten Tabakkonsum in dieser Population bedingt. Doch neben der hochaktiven antiretroviralen Therapie (ART) ist auch die chronische HIV-Infektion selbst ein Risikofaktor für die Herzgesundheit, da dauerhaft das Immunsystem aktiviert wird und somit eine chronische Entzündung vorliegt. Die entzündlichen Veränderungen an den Gefäßen führen so zur Arteriosklerose und entsprechenden Folgeerkrankungen. Zusätzlich werden aber auch unerwünschte Arzneimittelwirkungen, die die hochaktive antiretrovirale Therapie langfristig mit sich bringt, als ursächlich für das erhöhte kardiovaskuläre Risiko diskutiert, da unter einigen antiretroviralen Medikamenten vermehrt kardiovaskuläre Ereignisse beschrieben worden sind [5, 6]. Insgesamt sind allerdings die neueren antiretroviralen Substanzen besser verträglich als ältere, dennoch haben sie patientenindividuell und substanzspezifisch unterschiedliche Nebenwirkungen. Zu den langfristigen unerwünschten Arzneimittelwirkungen zählt eine Gewichtszunahme bis hin zu schwerem Übergewicht, die mit erhöhtem Risiko für Diabetes und Herz-Kreislauf-Erkrankungen einhergeht. Die ART-assoziierten Fettumverteilungsstörungen (Lipodystrophie), die unter den Erstgeneration Proteasehemmer oder D-Nukleosid-Analoga beobachtet wurden, sind seltener geworden [7].
Vergleich der Komorbiditäten bei HIV-seropositiven und HIV-seronegativen Männern
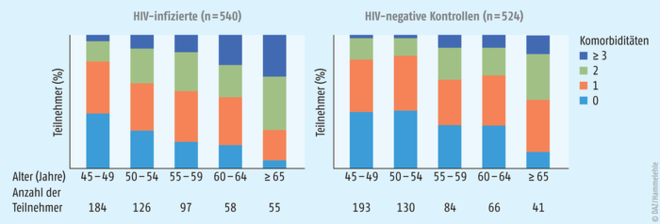
In verschiedenen Forschungskooperationen hat man sich bemüht, in altersgematchten Kontrollkollektiven der Frage nachzugehen, inwieweit Häufigkeit und Spektrum an Begleiterkrankungen sich bei HIV-positiven versus HIV-negativen Personen unterscheiden. So liegen Ergebnisse aus einer prospektiven niederländischen Querschnittsanalyse vor, die Alters-assoziierte, nicht übertragbare Komorbiditäten bei 540 Personen mit HIV-Infektion und 524 HIV-negativen Kontrollen verglichen hat [8]. Eingeschlossen wurden Personen die älter als 45 Jahre waren und die hinsichtlich Lebensstil, Eigenschaften und demografischen Merkmalen gematcht wurden. In der Abbildung 3 ist die Verteilung und Anzahl der Alters-assoziierten, nicht übertragbaren Erkrankungen stratifiziert nach Alter dargestellt.
Abb. 3: Häufigkeit von Komorbiditäten stratifiziert nach Altersgruppen bei HIV-infizierten versus HIV-negativen Männern modifiziert nach [8].
Die HIV-infizierten Studienteilnehmer (n = 540) wiesen insgesamt eine signifikant höhere Anzahl an Komorbiditäten als die HIV-negativen Kontrollpersonen auf (n = 524) (1,3 [SD, 1,14] vs. 1,0 [SD, 0,95]; p < 0,001) [8]. Dabei waren arterielle Hypertonie, Herzinfarkt, periphere arterielle Verschlusskrankheit (pAVK) und eingeschränkte Nierenfunktion deutlich häufiger bei den HIV-infizierten Individuen nachweisbar. Das Risiko für entsprechende Komorbiditäten war in der logistischen Regressionsanalyse unabhängig assoziiert mit Alter, Rauchen, positiver Familienanamnese für eine kardiovaskuläre Erkrankung oder metabolisches Syndrom und einem höheren Taille-Hüft-Quotienten, aber auch mit einer HIV-Infektion (Odds Ratio 1,58 [95%-Konfidenzintervall, 1,23 – 2,03]; p < 0,001). Bei den HIV-Infizierten war dabei das Risiko für Komorbiditäten höher als bei denjenigen, die länger eine CD4-Zellzahl < 200/µl aufwiesen, ein erhöhtes hoch sensitives C-reaktives Protein hatten sowie eine längere Behandlung mit höher dosiertem Ritonavir aufwiesen (≥ 400 mg/24 Stunden).
Disproportional größere Anstiege in Komorbiditäten bei HIV-Patienten mit zunehmendem Alter wurden auch innerhalb der HIV-Outpatient-Study(HOPS)-Kohorte aus den USA beschrieben [9]. Hierbei waren die häufigsten ermittelten Komorbiditäten bei 1540 supprimierten HIV-Patienten psychiatrische Erkrankungen (54,2%), Dyslipidämien (46,0%), arterielle Hypertonie (40,4%) und chronische Nierenerkrankungen (26,0%) [9]. In den meisten Studien überwiegen männliche Studienteilnehmer, sodass natürlich die Frage der Übertragbarkeit der Ergebnisse bei HIV-positiven Frauen auftaucht. Vor Kurzem wurde nun eine amerikanische Studie bei 3232 Frauen (2309 Frauen mit HIV-Infektion und 923 HIV-seronegativen Kontrollen) vorgestellt, die die Häufigkeit von Komorbiditäten gezielt bei Frauen untersucht hat [10]. In dieser Untersuchung mit einer medianen Nachbeobachtungszeit von 15 Jahren zeigte sich erneut eine erhöhte mittlere Anzahl an nicht übertragbaren Komorbiditäten bei den HIV-infizierten Frauen (3,6 vs. 3,0, p < 0,0001). Dabei fand sich bei den HIV-infizierten Frauen eine signifikant erhöhte Prävalenz an psychiatrischen Erkrankungen, Fettstoffwechselstörungen, nicht AIDS-definierenden Tumoren, Nieren-, Leber- und Knochenerkrankungen gegenüber den HIV-negativen Kontrollpersonen (alle p < 0,01) [10].
Auf einen Blick
- Der Anteil an älteren HIV-Patienten nimmt stetig zu und dürfte in Kürze bei mehr als der Hälfte aller betreuten Patienten liegen.
- Damit ergeben sich in der HIV-Sprechstunde ganz neue Herausforderungen.
- Früherkennung von Komorbiditäten und die entsprechende medikamentöse Behandlung von insbesondere Dyslipidämien, Altersdiabetes, Bluthochdruck und KHK nehmen dabei einen besonderen Stellenwert ein.
- Auch die Apotheker sind immer mehr gefragt, um bei zunehmender Polypharmazie etwaige Arzneimittelnebenwirkungen und Unter- oder Überdosierungen zu verhindern.
- Arzneimittelinteraktionen zwischen HIV-Therapeutika und Komedikationen für Begleiterkrankungen sind häufig und sollten mittels Interaktions-Webseiten bzw. Datenbanken überprüft werden.
- Wichtig ist auch die etwaige notwendige Dosisanpassung von Medikamenten bei zunehmender Niereninsuffizienz.
Kardiovaskuläres Risiko und HIV: Was bedeutet dies für die Praxis?
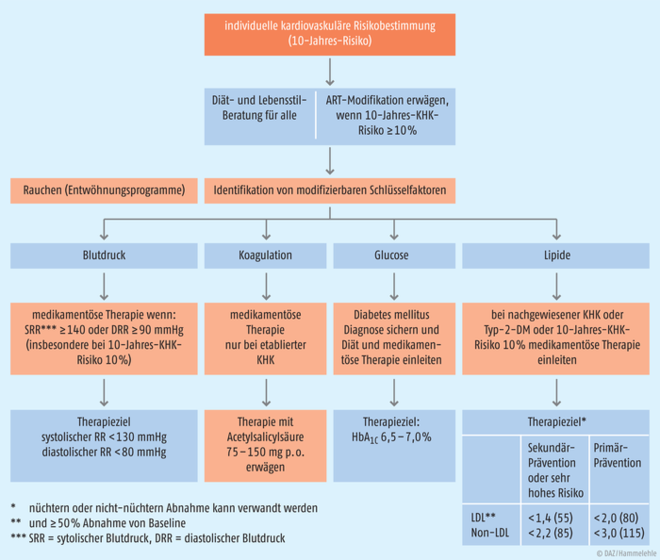
Es wird angenommen, dass bis 2030 73% aller HIV-infizierten Individuen ≥ 50 Jahre alt sein werden und 78% der HIV-Infizierten eine kardiovaskuläre Erkrankung aufweisen werden [11]. Damit spielen kardiovaskuläre Erkrankungen bei HIV eine ganz besondere Rolle zumal HIV selber bereits als eigenständiger Risikofaktor für das Auftreten einer entsprechenden Erkrankung angesehen werden muss [12]. Innerhalb der Leitlinien der Europäischen AIDS-Gesellschaft (EACS) spielen daher Komorbiditäten eine zentrale Rolle und es werden viele einfache Algorithmen für Screening und Früherkennung angeboten, die im klinischen Alltag gut nutzbar sind. Dabei orientieren sich Maßnahmen zur Lipid- oder Blutdrucksenkung am kardiovaskulären Risiko. Dasselbe gilt für die Thrombozytenaggregations-Hemmung. Als erster Schritt wird daher eine individuelle kardiovaskuläre Risikobestimmung empfohlen, welcher aus den einzelnen Risikofaktoren des jeweiligen Patienten eine Prognose für kardiovaskuläre Ereignisse in den nächsten zehn Jahren ermittelt. Dabei kann z. B. der Framingham Score verwendet werden oder ein alternativer Score, der von den nationalen Leitlinien empfohlen wird; eine Risikoberechnung, die in HIV-Kohorten evaluiert wurde, findet sich unter www.chip.dk/Tools-Standards/Clinical-risk-scores. Das von den EACS entwickelte Stufenschema zur Prävention von Herzerkrankungen ist in der Abbildung 4 zusammengefasst.
Arzneimittelinteraktionen beim älteren HIV-Patienten
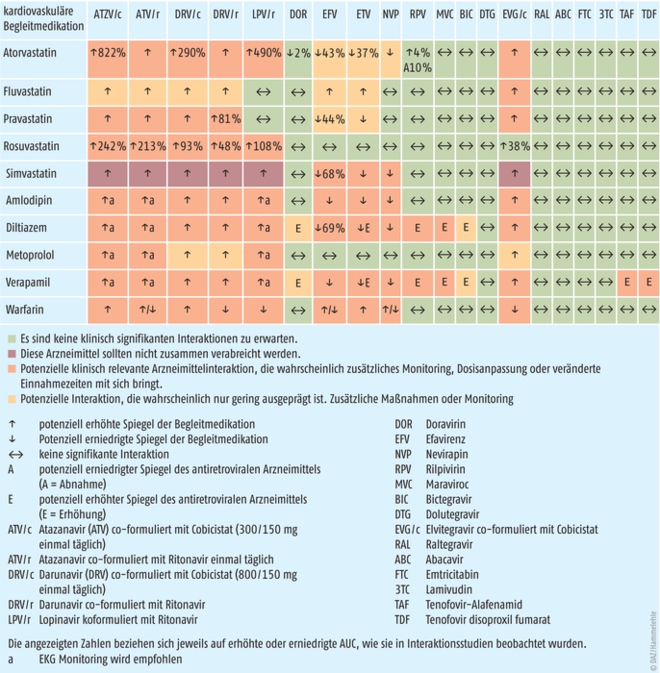
Bei der Auswahl an Komedikationen ist auf die vielfach bestehenden Medikamenteninteraktionen zwischen HIV-Therapie und Komedikationen hinzuweisen. Es empfiehlt sich entsprechend vor jeder neuen medikamentösen Therapie eine Arzneimittelinteraktionenwebsite zu konsultieren. Empfehlenswert ist zum Beispiel www.drug-interactions.org. Dabei spielen insbesondere Interaktionen zwischen HIV-Medikamenten, die über das Cytochrom-P450-System abgebaut werden wie HIV-Proteasehemmer und Komedikamente wie Statine, die ebenfalls über das Cytochrom-System abgebaut werden, eine große Rolle. Es gibt aber auch eine Fülle von Interaktionen über P-Glykoprotein und renale Transporter, daher ist die Nutzung einer Interaktionsdatenbank unumgänglich. In der Abbildung 5 sind die wichtigsten Interaktionen zwischen häufig eingesetzten kardiovaskulären Wirkstoffen und gängigen HIV-Therapien zusammengefasst. Insbesondere bei Lipidsenkern, Antihypertensiva und Antikoagulanzien sollte genau auf bestehende Interaktionen geachtet werden. Häufig kommt es auch zu schweren Nebenwirkungen bei Gabe von Steroiden (auch als intramuskuläre Injektion, Aerosol oder Augentropfen) die bei gleichzeitiger Therapie mit einem HIV-Proteasehemmer und konsekutiver Cortison-Spiegel Erhöhung zu einem ausgeprägten Cushing-Syndrom führen können [13]. Auch im Bereich von psychiatrischen Medikationen sollte genau auf Wechselwirkungen geachtet werden. Die mit zunehmendem Alter häufiger auftretende Niereninsuffizienz macht zudem nicht selten eine Dosisanpassung bei erniedrigter glomerulärer Filtrationsrate (GFR) notwendig. Insbesondere das häufig in der HIV-Therapie eingesetzte Tenofovir disoproxil fumarat sollte ab einer GFR < 50 ml/Minute entweder gar nicht mehr eingesetzt werden oder die Dosis adaptiert werden. Als Alternative steht inzwischen das deutlich nierenverträglichere Tenofovir-Alafenamid zur Verfügung. |
Abb. 5: Interaktionen zwischen antiretroviralen Arzneimitteln und häufig bei kardiovaskulären Erkrankungen eingesetzten Arzneimitteln (nach [14]).
Literatur
[1] an der Heiden M, Marcus U, Kollan C, Schmidt D, Gunsenheimer-Bartmeyer B, Bremer V. Schätzung der Zahl der HIV-Neuinfektionen und der Gesamtzahl von Menschen, die mit HIV in Deutschland leben. Stand Ende 2018, Epidemiologisches Bulletin des Robert Koch-Instituts 2019;46:483-492, DOI 10.25646/6410
[2] Aberg J. Aging and HIV infection: focus on cardiovascular disease risk. Top Antivir Med 2020;27:102-105
[3] Knieps L et al. Retrospective investigation into the causes of death in HIV-infected patients from Bonn in the era of combined Anti-Retroviral Therapy EACS 2019; PE20/8
[4] Morlat P et al. ANRS EN20 Mortalité 2010 Study Group. Causes of death among HIV-infected patients in France in 2010 (national survey): trends since 2000. AIDS 2014;28:1181-91
[5] Eyawo O et al. Risk of myocardial infarction among people living with HIV: an updated systematic review and meta-analysis. BMJ Open 2019;24;9(9):e025874
[6] Dorjee K et al. Risk of cardiovascular events from current, recent, and cumulative exposure to abacavir among persons living with HIV who were receiving antiretroviral therapy in the United States: a cohort study. BMC Infect Dis. 2017;17:708
[7] Eckard AR, McComsey GA. Weight gain and integrase inhibitors. Curr Opin Infect Dis 2020;33(1):10-19
[8] Schouten J et al. AGEhIV Cohort Study Group. Cross-sectional comparison of the prevalence of age-associated comorbidities and their risk factors between HIV-infected and uninfected individuals: the AGEhIV cohort study. Clin Infect Dis 2014;59:1787-1797
[9] Palella FJ Jr et al. HIV Outpatient Study (HOPS). Non-AIDS comorbidity burden differs by sex, race, and insurance type in aging adults in HIV care. AIDS 2019, doi: 10.1097/QAD.0000000000002349, [Epub ahead of print]
[10] Collins LF et al. The Prevalence and Burden of Non-AIDS Comorbidities among Women living with or at-risk for HIV Infection in the United States. Clin Infect Dis 2020, pii: ciaa204, doi: 10.1093/cid/ciaa204, [Epub ahead of print]
[11] Smit M et al. ATHENA Observational Cohort. Future challenges for clinical care of an ageing population infected with HIV: a modelling study. Lancet Infect Dis 2015;15:810-818
[12] Hsue PY and Waters DD. Time to Recognize HIV Infection as a Major Cardiovascular Risk Factor. Circulation 2018;138:1113-1115
[13] Schwarze-Zander C, et al. Triamcinolone and ritonavir leading to drug-induced Cushing syndrome and adrenal suppression: description of a new case and review of the literature. Infection. 2013;41(6):1183-1187
[14] Leitlinie der European AIDS Clinical Society (EACS). Version 10.0, November 2019, www.eacsociety.org/files/guidelines-10.0_final_german.pdf
Weitere Artikel zum Thema "Älter werden mit HIV" in dieser DAZ:
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.