
- DAZ.online
- DAZ / AZ
- DAZ 29/2019
- Stimmt das Timing
Chronopharmakologie
Stimmt das Timing?
Krebstherapie nach der inneren Uhr
Neben Begleiterkrankungen und Begleitmedikationen sorgen patientenindividuelle Unterschiede in der Elimination sowie genetisch bedingte Unterschiede in den Tumorzellen als pharmakologisches Target dafür, dass Krebstherapien bei dem einen Patienten besser und bei dem anderen schlechter wirken. Dieser interindividuellen Variabilität wird in der Regel durch eine Dosisanpassung während der Therapie anhand der eintretenden (Neben-)Wirkungen Rechnung getragen. Die Relation zwischen Dosis und therapeutischer Wirkung ist für die meisten Wirkstoffe – Antikörper und möglicherweise auch zielgerichtete Therapien können eine Ausnahme darstellen – dieselbe wie zwischen Dosis und Toxizität: Je höher die Dosis, desto stärker sowohl die Wirkung als auch die Toxizität. Die Idee der Chronotherapie ist es, genau den Zeitpunkt zu finden und zu nutzen, an dem die Tumorzellen empfindlich und die normalen Körperzellen resistent gegenüber dem Krebstherapeutikum sind. Im Idealfall führt dann eine intensivere Therapie nur zu mehr therapeutischer Wirkung, aber nicht zu erhöhter Toxizität. Ob das in klinisch relevantem Ausmaß funktioniert?
Angaben, zu welcher Tageszeit Arzneimittel eingenommen werden sollen, sind nur sehr selten durch vergleichende Studien begründet, sondern beruhen häufig auf allgemeinen Überlegungen zur Resorption und Pharmakokinetik. Und das, obwohl inzwischen die molekularen Grundlagen von Biorhythmen gut erforscht sind und eine daran angepasste Pharmakotherapie für eine Reihe von Arzneimitteln nachweislich sinnvoll ist. So hat sich für einige Wirkstoffgruppen eine dem Biorhythmus angepasste Chrono-Pharmakotherapie durchgesetzt: z. B. Steroide (zwei Drittel morgens einnehmen, ein Drittel abends), Antazida (abends) oder Theophyllin in der Asthmatherapie (zwei Drittel abends einnehmen, ein Drittel morgens). In der Onkologie ist das bisher nur ansatzweise gelungen.
Worin besteht der Zusammenhang zwischen der inneren Uhr und der Onkologie?
Das Prinzip eines „Dirigenten“, der als übergeordneter Taktgeber im Hypothalamus die zirkadiane Koordination des Orchesters der Organe, Gewebe und Zellen steuert, wurde in der DAZ 2019, Nr. 24 in den Beiträgen von Prof. Dr. Björn Lemmer „Warum der Hahn weiß, wann er krähen soll – Wissenschaftliche Grundlagen rund um die innere Uhr“ und „Arzneimitteltherapie im Takt – Wie sich Erkenntnisse der Chronopharmakologie nutzen lassen“ beschrieben. Der Hypothalamus gibt den zirkadianen Rhythmus vor und sorgt für die Anpassung an externe Stimuli [1]. Hierdurch werden nicht nur physiologische und pathophysiologische Vorgänge wie Schlaf-Wach-Rhythmus, Hunger-Satt-Gefühle, anabole und katabole Stoffwechselvorgänge und Wundheilungsprozesse reguliert, sondern auch Absorption, Verteilung, Elimination und molekulare Wirkung der Arzneistoffe (Pharmakokinetik und -dynamik) beeinflusst. Dies ist physiologisch möglich, weil jede Zelle molekulare Zeitgeber („Uhren“) aus etwa 15 verschiedenen Genen hat, die unter dem Einfluss des „Dirigenten“ über unterschiedliche Rückkopplungsschleifen mit den Zielgenen interagieren, die die Aktivität der Orchestermitglieder bestimmen. Darunter sind sowohl solche, die den Zellzyklus, DNA-Reparaturvorgänge oder die Apoptose regulieren, als auch solche, die onkologisch relevant sind [2, 3, 4].
Tagesrhythmus, Erkrankungen und Therapien beeinflussen sich wechselseitig: Der zirkadiane Rhythmus verändert die Wirkung und Nebenwirkung des Pharmakons, eventuell auch die Sensitivität bzw. Resistenz gegenüber der Krebstherapie [4, 5], und manche Pharmaka verschieben umgekehrt die physiologisch regulierte Taktgebung. Auch zwischen der Krebserkrankung und der zirkadianen Rhythmik besteht eine solche wechselseitige Beziehung: Dysregulation des zirkadianen Takts begünstigt die Krebsentstehung und/oder das Tumorwachstum in manchen Geweben [6, 7], und ein Tumor stört den tageszeitlichen Rhythmus [8]. Von 366 Varianten von Uhrengenen waren sieben in Form von Polymorphismen mit der Entstehung verschiedener Tumore (Brust, Prostata, Non-Hodgkin-Lymphom, Gliom, chronisch-lymphozytäre Leukämie, kolorektale Tumoren, nichtkleinzelliges Lungen- sowie Ovarialkarzinom) assoziiert [9]. Andere Uhrengene haben möglicherweise einen Einfluss auf die Schwere des Verlaufs, wie das Gen CRY1, das bei der chronisch lymphatischen Leukämie (CLL) im Allgemeinen hochreguliert, bei indolentem Verlauf, also wenn Lymphome durch einen langsamen Beginn und häufig chronischen Verlauf gekennzeichnet sind, aber abgeschaltet ist [10, 11]. In Gewebeproben verschiedener Tumoren zeigte sich, dass mehrere Tausend Zielgene den „Anschluss“ an die Uhrengene und manche Uhrengene den Kontakt untereinander verloren hatten. Unter diesen entkoppelten Zielgenen waren auch etliche, von denen bekannt ist, dass sie die Targets von zielgerichteten Krebs- und Immuntherapeutika kodieren [4]. Insofern ist auch denkbar, dass die molekulare Zelluhr ein pharmakologisches Target darstellt, das im Konzert mit der eigentlichen onkologischen Therapie zur erfolgreichen Behandlung oder sogar Heilung einer Krebserkrankung beitragen kann [12]. Studien hierzu sind noch im Anfangsstadium [13].
Auf einen Blick
- Der Hypothalamus steuert die zirkadiane Koordination der Organe, Gewebe und Zellen und auch Absorption, Verteilung, Elimination von Arzneistoffen.
- Wirkung und Nebenwirkung eines Wirkstoffs können sich nach dem zirkadianen Rhythmus ändern.
- Die meisten Untersuchungen sind bisher mit Ratten und Mäusen gemacht worden, eine Übertragung der Ergebnisse auf Menschen ist nicht direkt möglich.
- Durch die Einführung oraler Tumortherapien wäre eine tageszeitlich angepasste Applikation organisatorisch möglich, hierzu sind weitere klinische Studien notwendig.
- Irinotecan und Oxaliplatin können optimal wirken, wenn sie früh morgens appliziert werden.
- Melatonin kann als Zusatz zur Krebstherapie bei einigen Tumorentitäten die Therapie verbessern.
Krebstherapie nach der Uhr
Die meisten Studien mit Patienten wurden im Bereich Mamma-, Lungen- und Prostatakarzinom sowie malignen hämatologischen Erkrankungen durchgeführt. Kürzlich erschien auch eine Übersichtsarbeit für diverse endokrine Tumoren (darunter Ovarial- und Hodentumoren, maligne Erkrankungen der Schilddrüse und Nebenschilddrüse sowie der Nebennierenrinde) [13].Eine Reihe onkologischer Untersuchungen, vor allem mit klassischen Chemotherapeutika wie Irinotecan, 5-Fluorouracil (5-FU) und Oxaliplatin, hat einen verbesserten Therapieerfolg gezeigt, wenn man zirkadiane Unterschiede in der Pharmakokinetik und -dynamik berücksichtigt [14, 15, 16]. Studien mit dem Topoisomerase-II-Inhibitor Irinotecan wurden sowohl an (synchronisierten) Zellkulturen als auch an Mäusen durchgeführt. Die Ergebnisse zeigten signifikante Unterschiede in der Bioaktivierung und Inaktivierung, dem Transport und der molekularen Wirkung von Irinotecan, je nachdem, zu welcher Tageszeit es appliziert wurde. Ein optimaler Effekt wurde bei Applikationszeiten zwischen 03:00 Uhr und 07:00 Uhr morgens beobachtet [15]. Die Abhängigkeit von der molekularen inneren Uhr wurde dadurch belegt, dass der Effekt nach Hemmung des Uhrengens Bmal1 nicht mehr nachweisbar war [17].
Ähnlich signifikante Ergebnisse konnten bei der Untersuchung der tageszeitlichen Abhängigkeit von Wirkung und Nebenwirkung von Oxaliplatin an Mäusen und Patienten gezeigt werden. Hier wurde ein Optimum bei Applikation um 04:00 Uhr morgens gefunden [16]. Eine hohe Expressionsrate des Uhrengens Bmal1 war mit einer erhöhten Effizienz einer Oxaliplatin-basierten Chemotherapie bei Patienten mit kolorektalen Karzinomen assoziiert [5].
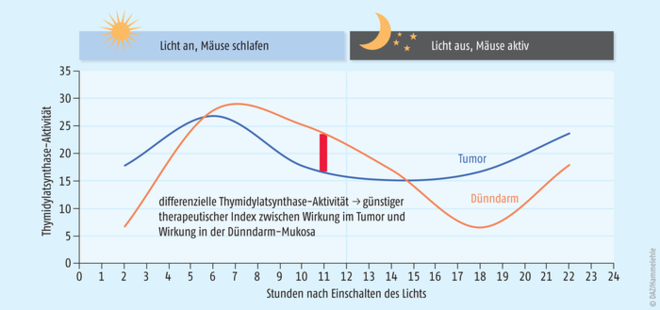
Der therapeutische Index von 5-Fluorouracil hängt von der Aktivität seines Targets, der Thymidylat-Synthase in den Tumor- und den normalen Körperzellen ab. Da die Toxizität von 5-Fluorouracil bei niedriger Aktivität der Thymidylat-Synthase am höchsten ist, ist der Index am günstigsten, wenn der Tumor die geringste und Zellen der gastrointestinalen Mukosa sowie des Knochenmarks die höchste Aktivität aufweisen (s. Abb. 1). In Mäusen bewirkte eine Gabe von 5-Fluorouracil kurz vor dem Zeitpunkt des Erwachens die geringste gastrointestinale und Myelotoxizität, die größte Antitumorwirkung und das längste Überleben. Zu dem Zeitpunkt war zugleich die Bmal1-Konzentration in den Zellkernen des Tumorgewebes am höchsten [14]. Beim Menschen zeigt die Aktivität der Thymidylat-Synthase in kernhaltigen Blutzellen ebenfalls zirkadiane Schwankungen [18], die eine tageszeitliche Abhängigkeit der Wirksamkeit erwarten lassen, sofern Tumorzellen diese Fluktuationen ebenfalls zeigen – und eine zeitabhängige Veränderung des therapeutischen Index, falls diese Fluktuationen gegenüber denen der gesunden Körperzellen zeitlich versetzt sein sollten. Über das oral anwendbare 5-FU-Prodrug Capecitabin ist aus Tierversuchen bekannt, dass mit der Tageszeit, zu der Capecitabin verabreicht wurde, die Halbwertszeit und Fläche unter der Kurve (AUC) von 5-FU und anderen Capecitabin-Metaboliten in Ratten variierten [19]. Ob die differenzielle Expression der Thymidylat-Synthase auch hier eine Optimierung des therapeutischen Index ermöglichen kann, wurde nach unserer Kenntnis noch nicht untersucht.
Die Pharmakokinetik (Cmax und die AUC) des oralen Krebstherapeutikums Sunitinib in Kaninchen ist davon abhängig, zu welcher Tageszeit der Rezeptor-Tyrosinkinase-Inhibitor verabreicht wurde: Bei der Gabe eine Stunde nach Beginn der zwölfstündigen Dunkelphase wurden höhere Werte erreicht als mit der Gabe eine Stunde nach Beginn der ebenfalls zwölfstündigen Hellphase [20].
Einige Studien haben gezeigt, dass Melatonin als Zusatz zur Krebstherapie bei bestimmten Tumorentitäten die Therapie verbessern kann. Hierfür werden verschiedene Mechanismen postuliert: antioxidative und antiinflammatorische Eigenschaften, Beeinflussung der Angiogenese, eine Modulation von Apoptose-Signalwegen, z. B. Mitochondrien, Bax, Bcl-2 und endogene Apoptoserezeptoren und andere [21, 22]. Ob Melatonin ein empfehlenswertes Adjuvans zu einer Krebstherapie ist, lässt sich derzeit noch ebenso wenig beantworten wie die oben gestellte Frage, ob ein chronotherapeutischer Ansatz in der Onkologie einen klinisch relevanten Nutzen hat. Aber erste Ansätze lassen hoffen, dass das der Fall ist.
Nutzung zirkadianer Fluktuationen in der Krebstherapie
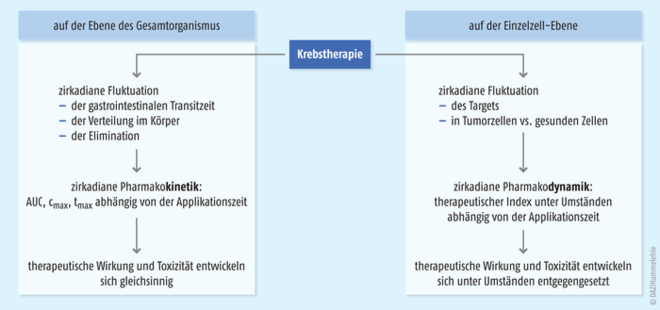
Zirkadiane Rhythmen der Prozesse, die die Pharmakokinetik der Krebstherapeutika beeinflussen, führen dazu, dass dieselbe Dosis einmal zu höheren und einmal zu niedrigeren Wirkstoffkonzentrationen (AUC, Cmax, tmax) führt. Dies lässt sich eventuell nutzen, um eine stärkere therapeutische Wirkung zu erzielen, allerdings werden die toxischen Wirkungen gleichermaßen zunehmen. Zirkadiane Rhythmen der Prozesse, die die Pharmakodynamik beeinflussen (oder auch die Pharmakokinetik auf Einzelzell-Ebene wie die Expression von inaktivierenden Enzymen oder Transportern in der jeweiligen Zelle), bergen das Potenzial, dass therapeutische und toxische Wirkung entkoppelt werden können – wenn die zeitliche Fluktuation in Tumor- und in gesunden Zellen unterschiedlich verläuft. Damit wäre der therapeutische Index davon abhängig, zu welcher Tageszeit die Therapie gegeben wird (s. Abb. 2). In der oralen Krebstherapie müsste dieses Prinzip nicht an einer mangelnden Praktikabilität scheitern. Hier hat der Patient die Einnahmezeiten selbst in der Hand und bräuchte nur einen Wecker und Durchhaltevermögen. |
Literatur
[1] Lemmer B. Warum der Hahn weiß, wann er krähen soll. Deutsche Apotheker Zeitung 2019;159(24):43-49
[2] Sancar A et al. Circadian clock control of the cellular response to DNA damage. FEBS Letters 2010;584:2618-2625
[3] El Athman R et al. The Ink4a/Arf locus operates as a regulator of the circadian clock modulating RAS activity. PLoS Biol 2017;15(12):e2002940
[4] Ye Y et al. The genomic landscape and pharmacogenomic interactions of clock genes in cancer chronotherapy. Cell Syst 2018;6(3):314-328.e2
[5] Zeng Z et al. Overexpression of the circadian clock gene Bmal1 increases sensitivity to oxaliplatin in colorectal cancer. Clin Cancer Res 2014; 20:1042-1052
[6] Cadenas C et al. Loss of circadian clock gene expression is associated with tumor progression in breastcancer, Cell Cycle 2014;13(20):3282-3291,
[7] Savvidis C et al. Circadian Rhythm Disruption in Cancer Biology. Mol Med 2012;18:1249-60
[8] Altman et al. MYC Disrupts the Circadian Clock and Metabolism in Cancer Cells. Cell Metabolism 2015;22:1009-1019
[9] Benna C et al. Genetic variation of clock genes and cancer risk: a field synopsis and meta-analysis. Oncotarget 2017;14 23978-23995
[10] Habashy DM et al. Cryptochrome-1 gene expression is a reliable prognostic indicator in Egyptian patients with chronic lymphocytic leukemia: a prospective cohort study. Turkish Journal of Haematology 2018;35:168-174
[11] Peng H et al. ARNTL hypermethylation promotes tumourigenesis and inhibits cisplatin sensitivity by activating CDK5 transcription in nasopharyngeal carcinoma. J Exp Clin Cancer Res 2019: 38:11
[12] Chang WH et al. Timing gone awry: distinct tumour suppressive and oncogenic roles of the circadian clock and crosstalk with hypoxia signalling in diverse malignancies. Transl Med 2019;17:132
[13] Angelousi, A et al. Clock genes and cancer development in particular in endocrine tissues. Endocr Relat Cancer 2019;pii: ERC-19-0094.R1
[14] Wood PA et al. Circadian clock coordinates cancer cell cycle progression, thymidylate synthase, and 5-fluorouracil therapeutic index. Mol Cancer Ther 2006;5(8):2023-2033
[15] Ballesta A et al. A systems biomedicine approach for chronotherapeutics optimization: focus on the anticancer drug irinotecan. In: New Challenges for Cancer Systems Biomedicine (d’Onofrio A et al., Eds.), Springer-Verlag 2012: 301-328
[16] Lévi F et al. Circadian timing in cancer treatments. Annu Rev Pharmacol Toxicol 2010;50:377-421
[17] Dulong S et al. Identification of circadian determinants of cancer chronotherapy through in vitro chronopharmacology and mathematical modeling. Mol Cancer Ther 2015;14:2154-2164
[18] Jacobs BAW et al. Pronounced between-subject and circadian variability in thymidylate synthase and dihydropyrimidine dehydrogenase enzyme activity in human volunteers. Br J Clin Pharmacol 2016;82(3):706-16
[19] Kobuchi S et al. Circadian variations in the pharmacokinetics of capecitabine and its metabolites in rats. Eur J Pharm Sci 2018;112:152-158
[20] Szałek E et al. The influence of the time-of-day administration of the drug on the pharmacokinetics of sunitinib in rabbits. Eur Rev Med Pharmacol Sci 2014;18(16):2393-2399
[21] Mortezaee K et al. Modulation of apoptosis by melatonin for improving cancer treatment efficiency: An updated review. Life Sci 2019;228:228-241
[22] Bojková B et al. Melatonin May Increase Anticancer Potential of Pleiotropic Drugs. Int J Mol Sci 2018;19(12), pii: E3910
Zum Weiterlesen
- Lemmer B. „Warum der Hahn weiß, wann er krähen soll – Wissenschaftliche Grundlagen rund um die innere Uhr“. DAZ 2019, Nr. 24, S. 42
- Lemmer B. „Arzneimitteltherapie im Takt – Wie sich Erkenntnisse der Chronopharmakologie nutzen lassen“. DAZ 2019, Nr. 24, S. 50


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.