
- DAZ.online
- DAZ / AZ
- DAZ 6/2018
- Die komplexe Therapie des...
Onkologie
Die komplexe Therapie des kolorektalen Karzinoms
Ein pharmazeutischer Blick auf die neue S3-Leitlinie
In Bezug auf die Mortalität liegt Darmkrebs mit ca. 25.500 Todesfällen pro Jahr in Deutschland an dritter Stelle hinter Lungenkrebs und Prostata- bzw. Brustkrebs. Die altersstandardisierten Sterberaten sind in den letzten zehn Jahren bei Frau und Mann um mehr als 20% gesunken. Die Inzidenz liegt bei 30 bis 40 Fällen pro 100.000 Einwohnern im Jahr in Europa – allerdings mit geografischen Unterschieden. In Deutschland entspricht das 13% aller Krebsneuerkrankungen. Das mittlere Erkrankungsalter liegt zwischen dem 70. und 75. Lebensjahr, 10% der Patienten erkranken vor dem 50. Lebensjahr [2, 3]. Die Mehrheit der älteren Patienten braucht je nach bestehender Erkrankung bereits vor einer Krebserkrankung Arzneimittel, sind also oft Stammkunden. Sie vertrauen „ihrer“ Apotheke und wollen weiter pharmazeutisch betreut werden. Die aktualisierten Leitlinien sind eine Quelle für praktische Informationen und bieten gute Hilfestellungen für die Beratungspraxis [4].
S3-Leitlinie mit pharmazeutischer Beteiligung
Die Leitlinie zum kolorektalen Karzinom wurde erstmals 1999 veröffentlicht und 2013 das letzte Mal überarbeitet. Die aktuelle S3-Leitlinie „Kolorektales Karzinom (KRK)“ entstand im Rahmen des Leitlinienprogramms Onkologie unter der Federführung der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS). Zum ersten Mal war bei der Überarbeitung auch ein pharmazeutischer Mandatsträger dabei. Das Leitlinienprogramm wird getragen von der Arbeitsgemeinschaft der Wissenschaftlich Medizinischen Fachgesellschaften (AWMF), der Deutschen Krebsgesellschaft (DKG) als wissenschaftlich-onkologische Fachgesellschaft und der Deutschen Krebshilfe. Die Fachdisziplin Pharmazie wird durch die Arbeitsgemeinschaft Onkologische Pharmazie (OPH) in der Sektion B der DKG organisiert und kooperiert zu diesem Zweck mit der Deutschen Gesellschaft für Onkologische Pharmazie (DGOP). Die Arbeitsgemeinschaft Onkologische Pharmazie und die Deutsche Gesellschaft für Onkologische Pharmazie stellen Mandatsträger für Leitlinien. Geben Sie auf DAZ.online in das Suchfeld den Webcode Y8CW5 ein und Sie gelangen direkt zur „S3-Leitlinie Kolorektales Karzinom“.
Patienten mit Metastasen und in der palliativen Situation im Fokus
Das therapeutische Vorgehen bei Metastasierung und in der palliativen Versorgung zählt auch aus pharmazeutischer Sicht zu den Kernthemen der Überarbeitung der S3-Leitlinie. Bei Patienten mit Metastasen steht die zielgerichtete, patientenbezogene Therapie unter Berücksichtigung von molekularen Grundlagen im Mittelpunkt. Um eine Unter- und Übertherapie zu vermeiden, beinhaltet die Leitlinie eine strukturierte Einteilung der Patienten unter Zuhilfenahme von Anzahl, Größe und Histologie der entfernten Gewebeveränderungen, verbunden mit konkreten Vorgaben zur Vorgehensweise (siehe Kasten „Auswahl der Patienten“).
Auswahl der Patienten
Um die optimale Erstlinien-Therapie auszuwählen, werden die Patienten definierten Behandlungsgruppen zugeordnet. Wichtig sind dabei drei Entscheidungsebenen
- Allgemeinzustand (Tolerabilität einer intensiven Therapie)
- Krankheitsausdehnung inklusive Lokalisation (therapeutische Optionen beinhalten Fragen nach Resektabilität oder lokoregionärer Intervention)
- Molekularbiologie des Tumors (Definition der optimalen gezielten Therapie)
Der Allgemeinzustand entscheidet als erstes darüber, ob ein Patient für intensive Therapie geeignet ist oder nicht.
Die Ausdehnung der metastasierten Erkrankung entscheidet über lokale, lokoregionäre oder primär systemische Behandlungsansätze. Gibt es kurative Behandlungsoptionen (resektable Erkrankung, potenziell resektable Erkrankung) oder ist die Therapieausrichtung eher palliativ (Oligometastasierung, wahrscheinlich nicht/nie resektable, disseminierte Erkrankung).
Die Kenntnis der Molekularbiologie des Tumors bildet die Grundlage für eine adäquate Therapieentscheidung, um eine optimale zielgerichtete Behandlung zu finden. Dazu werden molekularpathologische Subgruppen (erweiterte RAS-Analytik [KRAS, NRAS, Exone 2-4], RAS-Wildtyp [RAS-wt]) und die Tumorlokalisation ermittelt.
Quelle: [1]
Die Empfehlungen zur Nachkontrolle nach einer Koloskopie wurden im Detail optimiert. Zum Beispiel soll die endoskopische lokale Nachsorge nach kompletter Entfernung von Low-risk-Karzinomen weiterhin nach einem halben Jahr erfolgen, die komplette Koloskopie erfolgt allerdings erst nach drei Jahren statt bisher nach zwei Jahren.
Die Empfehlungen zum zeitlichen Abstand einer adjuvanten Chemotherapie zur Operation eines Kolonkarzinoms sowie zur neoadjuvanten Therapie und adjuvanten Chemotherapie beim Rektumkarzinom sind weiterhin gültig. Dagegen sind für die abschließende Beurteilung der Frage der Therapiesequenz in Bezug auf die Überlegenheit der neoadjuvanten Chemotherapie vor oder nach Radiochemotherapie beim Rektumkarzinom weitere Studien bzw. deren Auswertung nötig.
Die Leitlinie befasst sich neben allgemeinen Kapiteln zu Prävention, Vorsorge/Früherkennung der asymptomatischen Bevölkerung, Risikogruppen, präoperative Diagnostik, Chirurgie und Nachsorge hauptsächlich mit der adjuvanten und neoadjuvanten Therapie sowie dem therapeutischen Vorgehen bei Metastasierung und in der palliativen Situation. Zur Prävention und Vorsorge steht für patientenbezogen arbeitende Apotheken primär die Information zur Vermeidung von Risikofaktoren, wie Übergewicht, Nicotin-Abusus, mangelnde körperliche Aktivität, hoher Alkoholkonsum, ballaststoffarme fleisch- und fettreiche Kost, im Vordergrund (siehe Beitrag „Wir haben die Wahl – Ernährung kann das Risiko für ein kolorektales Karzinom reduzieren“, auf S. 37 in dieser DAZ). Die sekundäre Prävention hingegen beinhaltet Screeningmaßnahmen wie digitale rektale Untersuchung, totale Koloskopie als medizinische Themen und Test auf Blut im Stuhl (seit 1. April 2017 als immunologisch fäkaler Okkultbluttest, iFOBT).
Operation
Die UICC-Stadieneinteilung (Stadien 0 bis IV) wurde von der Union Internationale Contre le Cancer (UICC) eingeführt. Sie basiert auf statistischen Untersuchungen und gibt Auskunft über die Ausbreitung der Tumorerkrankung. Diese Einteilung nach
- T: Ausdehnung und Verhalten des Primärtumors,
- N: Fehlen bzw. Vorhandensein von regionären Lymphknotenmetastasen und
- M: Fehlen bzw. Vorhandensein von Fernmetastasen
ist die Grundlage bei Prognose- und Therapieplanerstellung [1]. Interessant ist, dass in ca. 80% der Fälle die Therapie des Kolonkarzinoms durch operative Entfernung des Tumors erfolgt. Die Operation in kurativer Absicht beinhaltet die laparoskopische Resektion des tumorbefallenen Abschnitts plus Mesenterium mit mindestens zwölf Lymphknoten. Das Rektumkarzinom im UICC-Stadium I wird primär operiert, im UICC-Stadium II/III soll bei Tumoren im unteren und mittleren Drittel eine neoadjuvante Radiochemotherapie oder Kurzzeit-Radiotherapie vor Operation erfolgen.
Eine palliative Operation erfolgt rein zur Vermeidung von Komplikationen. Das Vorgehen nach Operation richtet sich nach dem jeweiligen Stadium der Erkrankung angelehnt an den operativen Befund. Eine Empfehlung für oder gegen eine adjuvante Chemotherapie nach erfolgter neoadjuvanter Radiochemotherapie kann nach S3-Leitlinie noch nicht gegeben werden [1, 5].
Adjuvante und neoadjuvante Therapie
Die adjuvante, also die Wahrscheinlichkeit für ein Rezidiv (Wiederkehren) der Erkrankung senkende Therapie sollte allein aus Altersgründen nicht unterlassen werden. Bei Patienten über 75 Jahren gibt es jedoch keine ausreichende Evidenz für eine Chemotherapie. Bei Patienten über 70 Jahren sollte eine Therapie mit Oxaliplatin nicht erfolgen. Als Kontraindikationen für eine Chemotherapie sind ein schlechter Allgemeinzustand, unkontrollierte Infektionen, Leberzirrhose, schwere koronare Herzkrankheit und Herzinsuffizienz, präterminale und terminale Niereninsuffizienz, eingeschränkte Knochenmarksfunktion, andere die Lebenserwartung bestimmende Komorbidität und Unvermögen, an regelmäßigen Kontrolluntersuchungen teilzunehmen, zu nennen [1].
Im Stadium II sollte eine adjuvante 5-FU-haltige Chemotherapie als Monotherapie beim Kolonkarzinom nur in ausgewählten Risikosituationen (u. a. Tumorperforation, geringe Anzahl untersuchter Lymphknoten) erwogen werden. Als adjuvante Chemotherapie des Kolonkarzinoms Stadium III soll eine oxaliplatinhaltige Therapie erfolgen, und diese sollte baldmöglichst innerhalb von acht Wochen postoperativ starten. Das Schema Folfox 4 führt z. B. zu einer signifikanten Verbesserung des krankheitsfreien Überlebens und Gesamtüberlebens [1]. Die ausführlichen Therapieschemata finden Sie in den Tabellen. Monoklonale Antikörper oder Irinotecan sollen adjuvant nicht eingesetzt werden. Es liegt aktuell keine Empfehlung für oder gegen eine adjuvante Chemotherapie nach erfolgter Radiochemotherapie beim Rektumkarzinom vor. Bei Gefahr für ein lokoregionäres Rezidiv ohne Vorbehandlung sollte jedoch eine adjuvante Radiochemotherapie durchgeführt werden [1].
Wirkstoff |
Dosis |
Applikation |
Zyklustag/Infusionsdauer |
|---|---|---|---|
Folfox 4, Wiederholung Tag 15, zwölf Zyklen
| |||
Oxaliplatin |
85 mg/m2/Tag
|
i. v. |
1/über zwei Stunden |
Folinsäure |
200 mg/m2/Tag
|
i. v. |
1, 2/zwei Stunden,
an Tag 1 zeitgleich mit Oxaliplatin
|
5-Fluorouracil |
400 mg/m2/Tag
|
i. v. |
1, 2/Bolus |
5-Fluorouracil |
600 mg/m2/Tag
|
kontinuierlich i. v. |
1, 2/über 22 Stunden |
modifiziertes Folfox 6, Wiederholung Tag 15, zwölf Zyklen, international am meisten eingesetzt
| |||
Oxaliplatin |
85 mg/m2/Tag
|
i. v. |
1/über zwei Stunden |
Folinsäure |
400 mg/m2/Tag
|
i. v. |
1/über zwei Stunden,
zeitgleich mit Oxaliplatin
|
5-Fluorouracil |
400 mg/m2/Tag
|
i. v. |
1/Bolus |
5-Fluorouracil |
2400 mg/m2/Tag
|
kontinuierlich i. v. |
1, über 46 Stunden |
Capecitabin-Monotherapie, Wiederholung Tag 22, acht Zyklen | |||
Capecitabin |
2 × 1250 mg/m2/Tag
|
p. o. |
1 bis 14 |
Capecitabin/Oxaliplatin, Wiederholung Tag 22, acht Zyklen | |||
Oxaliplatin |
130 mg/m2/Tag
|
i. v. |
1/über zwei Stunde |
Capecitabin |
2 × 1000 mg/m2/Tag
|
p. o. |
1 bis 14 |
Wirkstoff |
Dosis |
Applikation |
Zyklustag/Infusionsdauer |
|---|---|---|---|
Folfiri, Wiederholung Tag 15, bis zum Progress oder inakzeptablen Nebenwirkungen | |||
Folinsäure |
400 mg/m2
|
i. v. |
1/zwei Stunden |
Irinotecan |
180 mg/m2
|
i. v. |
1/1,5 Stunden
zeitgleich mit Folinsäure
|
5-Fluorouracil |
2600 mg/m2
|
Kontinuierlich i. v. |
1/über 46 Stunden
im Anschluss an Folinsäure
|
Folfoxiri, Wiederholung Tag 15, bis zum Progress oder unakzeptabler Toxizität | |||
Irinotecan |
165 mg/m2
|
i. v. |
1/eine Stunde |
Oxaliplatin |
85 mg/m2
|
i. v. |
1/über zwei Stunden |
Folinsäure |
200 mg/m2
|
i. v. |
1/über zwei Stunden |
5-Fluorouracil |
3200 mg/m2
|
Kontinuierlich i. v. |
1/über 48 Stunden |
Folfiri/Bevacizumab, Wiederholung Tag 15, bis zum Progress oder unakzeptablen Nebenwirkungen | |||
Bevacizumab |
5 mg/kg Körpergewicht |
i. v. |
1/1,5 Stunden
ab 2. Zyklus 60 Minuten, bei guter Verträglichkeit ab dritten Zyklus 30 Minuten
|
Irinotecan |
180 mg/m2/Tag
|
i. v. |
1/1,5 Stunden |
Folinsäure |
400 mg/m2/Tag
|
i. v. |
1/120 Minuten |
5-Fluorouracil |
400 mg/m2/Tag
|
i. v. |
1/Bolus |
5-Fluorouracil |
2400 mg/m2
|
Kontinuierlich i. v. |
1/über 46 Stunden |
Folfiri/Cetuximab, Wiederholung Tag 15, bis zum Progress unakzeptablen Nebenwirkungen | |||
Cetuximab |
400 mg/kg Körpergewicht |
i. v. |
erster Zyklus 1/zwei Stunden |
Cetuximab |
250 mg/kg Körpergewicht |
i. v. |
erster Zyklus 8/eine Stunden |
Cetuximab |
250 mg/kg Körpergewicht |
i. v. |
ab zweiten Zyklus 1, 8/eine Stunde |
Irinotecan |
180 mg/m2/Tag
|
i. v. |
1/bis 1,5 Stunden |
Folinsäure |
400 mg/m2/Tag
|
i. v. |
1/über zwei Stunden |
5-Fluorouracil |
400 mg/m2/Tag
|
i. v. |
1/Bolus |
5-Fluorouracil |
2400 mg/m2
|
kontinuierlich i. v. |
1/über 46 Stunden |
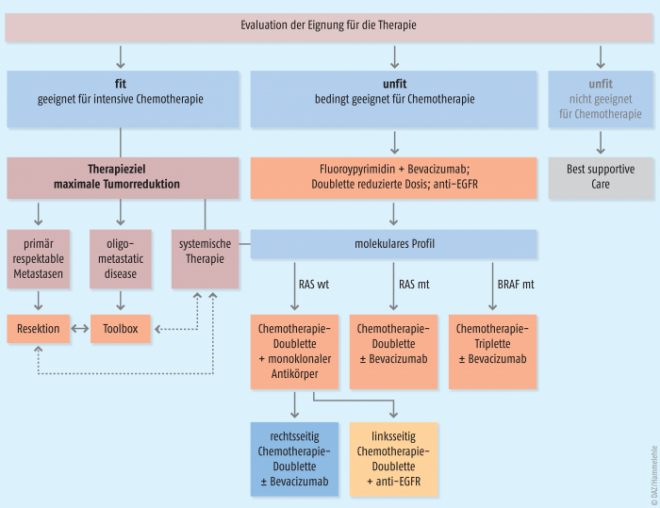
Der Allgemeinzustand des Patienten ist wichtig für die Entscheidung über das therapeutische Vorgehen beim Nachweis von Metastasen (Stadium IV, davon sind 25% in der Regel nicht palliativ) und in der palliativen Situation. Patienten mit gutem Allgemeinzustand können einer intensiven Behandlung mit Operation oder Chemotherapie unterzogen werden (siehe Kasten „Auswahl des Patienten“). Die therapeutische Strategie sollte im Rahmen einer Tumorkonferenz interdisziplinär festgelegt werden. Die optimale Wahl der Erstlinien-Therapie beinhaltet auch Fragen der Lokalisation und Molekularbiologie des Tumors mit Bestimmung von RAS- und BRAF-Mutationen (siehe Abb.). Die BRAF-Mutation bedeutet eine schlechte Prognose, daher kann frühzeitig eine intensivierte Chemotherapie, z. B. mit Folfoxiri und Bevacizumab, eingeleitet werden. Die Bestimmung eines Dihydropyrimidin-Dehydrogenase(DPD)-Mangels vor einer Fluoropyrimidin-Therapie (5-FU/Folinsäure, Capecitabin) kann durchgeführt werden, um eine Dosisreduktion vorzunehmen oder sehr selten eine Kontraindikation festzustellen. Bei reduziertem Allgemeinzustand kann eine initiale Behandlung mit einem Fluoropyrimidin und Bevacizumab oder eine dosisreduzierte Chemotherapie-Doublette als Kombination von Fluoropyrimidin mit Oxaliplatin oder Irinotecan +/- Bevacizumab durchgeführt werden.
Bei RAS-Wildtyp und Tumoren im linken Kolon oder im Rektum kann auch eine anti-EGFR-Monotherapie mit Cetuximab oder Panitumumab erfolgen. Patienten mit nicht reduziertem Allgemeinzustand mit RAS-Wildtyp und linksseitiger Lokalisation des Primärtumors sollen mit einer Chemotherapie-Doublette plus anti-EGFR behandelt werden. Bei RAS-Mutation sollte primär eine Chemotherapie-Doublette gewählt werden, ob eventuell auch eine Chemotherapie-Triplette (Fluoropyrimidin plus Oxaliplatin und Irinotecan) und ob mit Bevacizumab, ist nicht belegt. Die Kombination mit einem monoklonalen Antikörper steigert nachweislich die Remissionsraten, das progressionsfreie Überleben (median ca. zehn Monate) und teilweise auch das Gesamtüberleben (median ca. 30 Monate) [6]. Im direkten Vergleich sind die Therapieschemata Folfox und Folfiri (siehe Kasten „Therapieschema“ sowie in den Tabellen) hinsichtlich ihrer Wirksamkeit als gleichwertig zu betrachten. Sie unterscheiden sich durch ihre Toxizitäten. Bei Irinotecan stehen als starke Nebenwirkungen Diarrhö und Neutropenie im Vordergrund und bei Oxaliplatin Thrombozytopenie und die häufig nach drei bis Monaten einsetzende Polyneuropathie. Die Kombination mit einem Triplett führt im Vergleich zur Doublette zu höheren Remissionsraten. Insgesamt werden im Rahmen multimodaler Therapiekonzepte Therapiesequenzen mit individualisierter Anpassung bis zur dritten Linie angestrebt. Anti-VEGFR-Antikörper wie Bevacizumab, Ramucirumab und das Fusionsprotein Aflibercept werden bei allen Genotypen eingesetzt. Bevacizumab zusätzlich bei RAS-Wildtyp und rechtsseitigem Tumor.
Therapieschema
In der Therapie des kolorektalen Karzinoms werden eine Vielzahl an Wirkstoffkombinationen eingesetzt. Gängige Schemata sind zum Beispiel:
- Folfiri: Kombination aus Folinsäure (Fol), 5-Fluorouracil (F) und Irinotecan (Iri)
- Folfox: Kombination aus Folinsäure (Fol), 5-Fluorouracil (F) und Oxaliplatin (Ox)
- Folfoxiri: Kombination aus Folinsäure (Fol), 5-Fluorouracil (F), Oxaliplatin (Ox), Irinotecan (Iri)
Die Zweit- und Drittlinien-Therapie ist in Bezug auf die Auswahl der Schemata vom Zulassungsstatus, von vorangehenden Therapien, der therapiefreien Zeit und dem individuellen Patienten abhängig und zwar jeweils mit Berücksichtigung des Behandlungsziels und der vorliegenden histo- und molekularpathologischen Diagnostik. Eine weitere vom RAS-Status unabhängige Therapie steht mit der Wirkstoffkombination Trifluridin/Tipiracil zur Verfügung und sollte bei Patienten, welche alle verfügbaren Chemotherapien/ Antikörper durchlaufen haben oder für diese nicht geeignet sind, eingesetzt werden [1, 5, 6, 7, 8].
Ab wann zur Vorsorge?
In der aktuellen Leitlinie wird dargelegt, wann eine Vorsorgeuntersuchung sinnvoll ist:
- Liegen keine Risiken für das Auftreten eines kolorektalen Karzinoms vor, sollten asymptomatische Personen mit der Darmkrebs-Vorsorge/-Früherkennung ab dem Alter von 50 Jahren beginnen.
- Eine obere Altersbegrenzung für die Darmkrebs-Vorsorge/-Früherkennung kann bei steigender Lebenserwartung nicht gegeben werden. Hier sollte eine individuelle Entscheidung unter Berücksichtigung der Begleiterkrankungen getroffen werden.
- Personen, die ein familiär gesteigertes Risiko für ein kolorektales Karzinom haben, dessen genetische Grundlagen zur Zeit noch nicht umfassend bekannt sind, die nachgewiesene oder mögliche Anlageträger für ein hereditäres kolorektales Karzinom sind und die eine chronisch entzündliche Darmerkrankung haben, zählen als Risikogruppe.
Im Mittelpunkt der Patient
In der medikamentösen Behandlung von Krebspatienten werden Wirkstoffe mit meist geringer therapeutischer Breite und einer Vielzahl an möglichen Nebenwirkungen eingesetzt. Die auftretenden Nebenwirkungen wie Übelkeit und Erbrechen, Haarausfall, Fatigue-Syndrom mit Erschöpfung und Müdigkeit, Leukopenie und Infektionsneigung sind die Folge der Wirkung auf alle schnellteilenden Körperzellen. Eine supportive, das heißt unterstützende Therapie sollte immer Bestandteil der onkologischen Therapie sein. So sollen Komplikationen wie die zwangsweise Pausenverlängerung bei der Durchführung der Therapiezyklen vermieden werden. Die beratenden und betreuenden Ärzte und Apotheker sind hier gefordert, um durch verständliche Beratung die richtige Anwendung gerade der Supportivtherapie wie z. B. die Antiemese sicherzustellen und die Adhärenz zu fördern. Das Fatigue-Syndrom nimmt im Lauf der Behandlung zu, dauert in der Regel noch Monate danach an und ist ein Ansatz für weitere pharmazeutische Betreuung [10].
Die anti-EGFR-Therapie mit Cetuximab oder Panitumumab bei RAS-Wildtyp-Tumoren geht mit charakteristischen Nebenwirkungen an der Haut einher (akneiformes Exanthem).
Eine Chemotherapie darf nur durchgeführt werden, wenn sie mit einer adäquaten Supportivtherapie einhergeht, z. B. auch gegen Übelkeit und Erbrechen, die an das emetogene Potenzial der eingesetzten Wirkstoffe angepasst ist.
Als wichtige Neuerung wurde in die S3-Leitlinie aufgenommen, dass die Patienten regelmäßig zu einem effektiven Selbst-Management der Symptome angeleitet und geschult werden sollen. Es gilt als belegt, dass durch ein effektives Selbst-Assessment und die Fähigkeit einer angemessenen Kommunikation krankheits- und therapiebedingte Belastungen (Toxizitäten wie Diarrhoe, Übelkeit und Erbrechen, Mucositis/Stomatitis, Obstipation und Neuropathien) reduziert werden können. Ziel ist es, Therapieabbrüche zu vermeiden und eine Verschlechterung therapie- und krankheitsbedingter Symptome zu verhindern.
Unter Chemotherapie bei Metastasierung und in der palliativen Situation sollen regelmäßig krankheits- und therapiebedingte Nebenwirkungen hinterfragt und mit den Zielen der Verlängerung des progressionsfreien- und Gesamtüberlebens bei geringerer Toxizität abgeglichen werden [11]. |
Literatur
[1] AWMF. S3-Leitlinie Kolorektales Karzinom. Langversion 2.0 – November 2017, Studienregisternummer: 021/007 OL
[2] Zentrum für Krebsregisterdaten/Robert Koch-Institut: Krebs in Deutschland 2013 – 2014, Häufigkeiten und Trends: Darm, 11. Auflage 2017:36–39
[3] Fritsch R, Zirlik K. Kolorektales Karzinom. In: Berger DP, Mertelsmann R. Das Rote Buch. ecomed Medizin 2017:918
[4] Höckel M. Kolorektales Karzinom. In: Rose F. Angewandte Arzneimitteltherapie. Wiss. Verlagsgesellschaft mbH 2015
[5] Fritsch R, Zirlik K. Kolorektales Karzinom. In: Berger DP, Mertelsmann R. Das Rote Buch. ecomed Medizin 2017:921–923
[6] Deutsche Gesellschaft für Hämatologie und Onkologie (DGHO). Onkopedia Leitlinien: Kolonkarzinom und Rektumkarzinom mit medikamentöser Tumortherapie, Stand: August 2017
[7] Ettrich TJ, Seufferlein T. Metastastasiertes kolorektales Karzinom - Moderne Therapiekonzepte zwischen Heute und Morgen. Onkologe 2016;22:109-114
[8] Lorenzen S. Metastasiertes Kolorektalkarzinom: Therapiesequenz abhängig von Molekularpathologie und Tumorlokalisation. Onkologe 2017;23(11): Beilage zertifizierte Fortbildung
[9] Gnadt M. Keine Scheu vor Leitlinien. DAZ 2014;43:46 ff
[10] Höckel M, Heckl U, Nagel G. Der Krebspatient in der Apotheke. Deutscher Apotheker Verlag, Stuttgart 2003:238–240
[11] Labianca R, Nordlinger B, Beretta GD et al. Early colon cancer: ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol 2013;24:vi64–vi72






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.