
- DAZ.online
- DAZ / AZ
- DAZ 40/2018
- Der Fall Duogynon
Arzneimittelsicherheit
Der Fall Duogynon
Ein zweiter Contergan-Skandal?
Eine wissenschaftliche und gesellschaftliche Auseinandersetzung mit Duogynon ist wichtig und lohnend. Sie zeigt prinzipielle Probleme des Arzneimittelwesens, gerade im Hinblick auf Regulierung und Überwachung sowie dem damaligen Verantwortungsbewusstsein der Industrie. Zugleich besteht aber auch ein großes Aufklärungsinteresse jener Personen, die der Überzeugung sind, durch eine Duogynon-Einnahme ihrer Mütter während der Schwangerschaft geschädigt worden zu sein.
Was genau war Duogynon?
Bei Duogynon handelt es sich um ein hormonelles Kombinationspräparat, das vom Berliner Pharmaunternehmen Schering ab 1950 auf den westdeutschen Markt gebracht wurde. Zunächst gab es nur eine Injektionslösung, die 20 mg des Gestagens Progesteron und 2 mg des Östrogens Estradiolbenzoat pro ml enthielt. Indiziert war das Mittel bei einer sekundären Amenorrhö (Ausbleiben der Menstruationsblutung) und zur Erkennung einer Schwangerschaft. Im Oktober 1958 brachte Schering Duogynon zudem in Dragée-Form auf den Markt, welches zugleich in England unter dem Namen Primodos eingeführt wurde. Die Dragées enthielten die synthetischen Wirkkomponenten Norethisteronacetat (10 mg) und Ethinylestradiol (0,02 mg), also ebenfalls eine Gestagen-Östrogen-Kombination. Das Indikationsgebiet der Dragées entsprach dem der Injektionslösung. Ergänzt wurden die beiden Präparate seit September 1962 durch Duogynon simplex, bei dem es sich um eine vereinfachte Injektionslösung handelte, die 50 mg Progesteron und 3 mg Estradiolbenzoat pro ml enthielt und ebenso für die sekundäre Amenorrhö und die Erkennung einer Schwangerschaft indiziert war [1].
Die Einführung Duogynons 1950/57 erfolgte noch in der vorgesetzlichen Zeit des Arzneimittelrechts. Voraussetzung für die Herstellung neuer Arzneifertigwaren war allein eine behördliche Ausnahmegenehmigung, da die sog. Stopp-Verordnung von 1943 als weiterhin gültig betrachtet wurde. Zwar verlangten die zuständigen Landesbehörden dabei Unterlagen über die pharmakologische und klinische Wirkung. Hierfür reichten aber kurze ärztliche Erfahrungsberichte aus, die meist nur wenige Blatt umfassten. Die Sicherheit der Präparate konnte dieses Verfahren kaum gewährleisten.
Das relativ laxe Regulierungssystem entsprach einem gesamtgesellschaftlich nur schwach ausgeprägten Bewusstsein für Arzneimittelrisiken. Medikamente hatten in der Nachkriegszeit ein positives Image, zumal sich die altbekannten „Geißeln der Menschheit“ mit den neuesten Mitteln, etwa Penicillin, nun einfach therapieren ließen. So blieb der pharmazeutische Fortschrittsglaube einstweilen ungebrochen, was einem zuversichtlichen Zeitgeist des „Wirtschaftswunders“ entsprach.
Obwohl die Duogynon-Präparate auch für therapeutische Zwecke zugelassen waren, wurden sie oftmals nur als Schwangerschaftstest verwendet. Praktische und ungefährliche Tests, wie sie heute in Apotheken, Drogerien und Supermärkten erhältlich sind, gab es bis in die 1960er-Jahre noch nicht (siehe DAZ 2018, Nr. 21). Stattdessen konnte eine Frau, die wissen wollte, ob sie schwanger ist oder nicht, sich von ihrem Hausarzt oder Gynäkologen zwei Dragées oder eine Injektion des Hormonpräparats verordnen bzw. verabreichen lassen. Blieb in den Folgetagen eine Blutung aus, so war die Frau schwanger.
Contergan und teratogene Risiken
In den 1960er-Jahren begann sich die Risikowahrnehmung von Arzneimitteln sowohl in den Fachkreisen als auch in der Gesellschaft tiefgreifend zu wandeln. Hintergrund war der Contergan-Skandal, der auch über die Fachwelt hinaus für das Problem unerwünschter Arzneimittelwirkungen sensibilisierte – gerade während der Schwangerschaft. Der Skandal hatte auch deshalb eine besondere Breitenwirkung, weil er eine Grundsatzkritik am wachsenden Arzneikonsum mit einem seit geraumer Zeit schwelenden Diskurs um eine Zunahme von Fehlbildungen verband.
Als eine Expertenkommission Ende 1961 den Zusammenhang zwischen Contergan und den Fehlbildungsfällen aufklären sollte, rückten auch andere Mittel in den Fokus der Mediziner, darunter Duogynon [2].
Schien Duogynon zunächst entlastet, so richtete sich der Verdacht bald wieder auf das Präparat. Die erste Warnung kam 1967 aus England. Dort hatte die Ärztin Isabel Gal in der Fachzeitschrift „Nature“ eine kurze Arbeit veröffentlicht, in der sie über eine nachträgliche Erfassung von 100 Fehlbildungsfällen berichtete. Wie die Befragung der Mütter ergab, hatten 19 einen hormonellen Schwangerschaftstest verwendet, in der Kontrollgruppe waren es dagegen nur vier. Auch wenn Gal eine rein zufällige Abweichung nicht ausschloss, sah sie die Möglichkeit einer teratogenen Wirkung als gegeben, wobei sie Primodos explizit erwähnte [3].
Erste Reaktionen Scherings
Bei Schering erhielt man bald Kenntnis von Gals Verdacht, sah ihn aber als unbegründet an, obwohl bald weitere Arbeiten einen ähnlichen Verdacht äußerten. Wie die Verantwortlichen Scherings später erklärten, hielten sie diese Arbeiten für nicht aussagekräftig, weil sie nicht nach Indikation, Präparat, Anwendungsdauer, Dosierung oder Schwangerschaftsphase differenzierten. Zugleich verwiesen sie auf die Lehrmeinung, die eine Hormontherapie in der Schwangerschaft empfahl. Die Firmenleitung blieb bei dieser Haltung, obwohl die Warnungen auch aus der eigenen Tochterfirma kamen. Der englische Schering-Direktor zeigte sich bestürzt und forderte 1969 von der Berliner Zentrale weitere Maßnahmen, da auch in „ethischer Hinsicht […] nicht genügend geschehen“ sei. Der Plan einer eigenen Prospektivstudie an 5.000 Frauen verlief allerdings im Sande, was zu abermaliger Kritik des Mitarbeiters führte.
Wie in der Pharmabranche üblich, wurden nach der Markteinführung weitere Tierversuche unternommen, nun aber intensiviert. Laut den vorliegenden Protokollen wurden die Wirkkomponenten teils in massivster Überdosierung (bis 750-fach und mehr) appliziert. Dabei kam es in mehreren Fällen zu einer Erhöhung der Resorptionsrate.
Teratogene Anomalien wurden nur vereinzelt bei größeren Überdosierungen beobachtet, weshalb laut den Prüfern teratogene Wirkungen bei extremen Dosen „nicht ausgeschlossen werden“ konnten [4]. Bei Versuchen mit Affen, also den Menschen besonders nahestehenden Tieren, wurden trotz großer Überdosierungen keine teratogenen Effekte erzielt.
Da die Verantwortlichen die Verdachtsmomente gegen Duogynon als nicht stichhaltig werteten, betonte Schering die Ungefährlichkeit des Präparats für Schwangere. Gleichwohl strich Schering 1970 die Indikation Schwangerschaftstest in England. Anlass war kein behördliches Verbot, sondern die erforderliche Streichung dieser nichttherapeutischen Indikationen, damit das Mittel weiterhin zulasten des englischen NHS verordnet werden konnte. Dessen ungeachtet zeigte die Kritik Wirkung. Noch im Jahr 1970 warnte die britische Arzneimittelkommission vor Primodos. Zum Rückgang der Fehlbildungen führte die Indikationsänderung nicht. Im Gegenteil: Die Fallzahlen nahmen anschließend kontinuierlich zu.
Die Situation in der Bundesrepublik
In der Bundesrepublik wurde erstmals 1971 im industriekritischen „Arznei-Telegramm“ vor Duogynon gewarnt. Zum Handeln veranlasste dies Schering nicht, zumal es auch Kritik an den Studien von Gal und anderen gab. Im November 1973 strich Schering dann die Indikation Schwangerschaftstest für die Dragées. Begründet wurde dies als reine Vorsichtsmaßnahme, da die Gestagen-Komponente eine geringe androgene Restwirkung besitze und daher Virilisierungserscheinungen weiblicher Föten theoretisch nicht auszuschließen seien. Die Ärzte wurden entsprechend unterrichtet.
Schering sah sich durch zwei umfassende Studien in der Bundesrepublik bestätigt, die nach dem Fall Contergan teratologische Fragen klären sollten. Dabei handelte es sich um prospektive Studien, in denen Frauen bereits während der Schwangerschaft ärztlich begleitet und beobachtet wurden (und die methodisch hochwertiger waren als retrospektive Befragungen).
Eine Studie der Deutschen Forschungsgemeinschaft (DFG) wertete seit 1964 rund 14.800 Schwangerschaften an 21 Unikliniken akribisch aus. Eine zweite Studie lief seit 1969 in Göttingen und hatte bis April 1972 über 3.500 Schwangerschaften dokumentiert. Angesichts der Warnungen aus England bat die deutsche Arzneimittelkommission 1973 beide Stellen um Auskunft. Laut dem im Deutschen Ärzteblatt publizierten Ergebnis gab es „keinen signifikanten Anhalt“ für einen Zusammenhang zwischen Fehlbildungen und Geschlechtshormonen. Dies wurde durch beide Studien später weiter bestätigt [5].
Doch die Verdachtsfälle aus dem Ausland, auch aus der englischen Schering-Tochter, ebbten nicht ab. Im Mai 1975 bat das Bundesgesundheitsamt (BGA) Schering daher um Stellungnahme. Schering verwies auf gravierende Mängel dieser Berichte und die deutschen Prospektivstudien. Das BGA erkundigte sich im Juni 1975 daher selbst in Göttingen. Dort waren bei 3.879 Schwangerschaften ohne hormonelle Tests 96 Fehlbildungen (2,47 Prozent), bei 789 Schwangerschaften mit solchen Tests 22 Fehlbildungen aufgetreten (2,66 Prozent). Auch wenn eine Kausalität demnach unwahrscheinlich war, sprach sich der Studienleiter gegen orale Tests aus. Auch die Arzneimittelkommission empfahl allen Herstellern oraler Östrogen-Gestagen-Präparate Mitte 1975 vorsorglich, die Indikation Schwangerschaftstest zu streichen. Die Injektionsform galt dagegen als unbedenklich, da sie den Ester des natürlich vorkommenden weiblichen Sexualhormons enthielt.
1977 erfasste die Debatte auch die Tagespresse. Angesichts neuer Warnungen aus England berichteten nun auch Massenmedien wie der Spiegel (43/1977) über den Verdacht, wobei nicht selten der Eindruck erweckt wurde, als stehe ein Zusammenhang mit Fehlbildungen bereits fest.
Die Debatte um Duogynon sollte in den folgenden Jahren nicht mehr verstummen, stand aber in gewissem Kontrast zum Fachdiskurs. So wurden noch 1977 in dem neu aufgelegten Standardlehrbuch zur Gynäkologie hormonelle Schwangerschaftstests empfohlen. Auch ein 1977 veröffentlichter Zwischenbericht der DFG-Studie konnte keinen signifikanten Zusammenhang erkennen.
Alarmiert durch die Presseartikel bat nun auch das Bundesministerium für Jugend, Familie und Gesundheit (BMJFG) das BGA im Oktober 1977 um Informationen. In der Folge entwickelte sich ein intensiver Austausch zwischen beiden Behörden. Die Haltung des BGA war eindeutig: Trotz umfassender Beobachtungsstudien sei ein Zusammenhang zwischen Duogynon und Fehlbildungen in Deutschland „nicht beobachtet“ worden. Die Studien aus England kritisierte das BGA als „ungenügend“, zumal sie auf nachträglichen Befragungen beruhten. Weitere Maßnahmen seien weder möglich noch erforderlich, da die Duogynon-Dragées ohnehin seit 1973 für die Schwangerschaft kontraindiziert seien. Das BMJFG beschloss daher, auf eine eigene Stellungnahme zu verzichten [6].
Angesichts der anrollenden Diskussion ging Schering nun dazu über, den Fall vermehrt durch die Rechtsabteilung bearbeiten zu lassen, die nach außen einen resoluten Abwiegelungskurs durchsetzte – wohl auch aus dem Bewusstsein, dass die Firma Ende der 1960er-Jahre selbst nur wenig zur Aufklärung getan und sich vor allem auf Studien anderer verlassen hatte. So wurde etwa bei einer Prüfung der Rechtslage in England festgestellt, dass die firmeninternen Warnungen – egal, ob berechtigt oder nicht – sich als „Dynamit“ in den Händen von Klägern erweisen könnten [7].
Umbenennung in Cumorit
Im Januar 1978 teilte Schering dem BGA mit, die Indikation Schwangerschaftstest auch für die Injektionsform zu streichen. Das Unternehmen begründete diesen Schritt mit der vermehrten Verfügbarkeit einfacher immunologischer Tests, bemühte sich aber zugleich, das Fehlen eines teratogenen Risikos herauszustellen. Dazu verwies Schering auf eine Stellungnahme einer Kommission der Deutschen Gesellschaft für Endokrinologie vom Februar 1978, in der es hieß: „Auch wenn das teratogene Risiko – falls ein solches überhaupt existieren sollte – minimal sein dürfte, ist Zurückhaltung bei der Anwendung von Sexualhormonen zur Schwangerschaftserhaltung geboten.“ [8]
Ende März 1978 informierte Schering Behörden und Ärzte über die geänderte Gebrauchsanweisung, nach der vor der Anwendung auch der Injektionsform „eine Schwangerschaft auszuschließen“ sei. Am 27. Juni 1978 kündigte Schering dann an, die Duogynon-Präparate in Cumorit umzubenennen. Was manchen als fragwürdiges PR-Manöver erschien, begründete Schering als Schritt, um dem eingefahrenen, nicht bestimmungsgemäßen Gebrauch entgegenzuwirken. Zugleich sollten maßgebende Stellen von der Hinlänglichkeit der eigenen Maßnahmen überzeugt werden.
Mediale Aufmerksamkeit und öffentliche Debatte
Vor allem beim BGA war man damit erfolgreich. Angesichts der öffentlichen Kritik bezeichnete ein Mitarbeiter sich und das BGA als „Advokaten der Firma Schering“ [9]. Die mediale Berichterstattung in der Bundesrepublik erlebte ab Sommer 1978 ihren Höhepunkt, wobei die Artikel zwischen Abwiegelung und Anklage changierten. Im Juli 1978 forderte die Arzneimittelkommission daher erneut, orale Östrogen-Gestagen-Kombinationen in der Schwangerschaft zu meiden. Die Bundesregierung reagierte mit einer Mischung aus Besorgnis und Beschwichtigung. In mehreren Presseerklärungen erklärte sie, dass es in der Bundesrepublik „keinen Hinweis“ auf einen Zusammenhang gebe, ein Restrisiko aber niemals auszuschließen sei. Duogynon sei daher nicht in der Schwangerschaft anzuwenden.
Da ein Verbot des Mittels nicht möglich war, forderten die Behörden, Verpackung und Beipackzettel für Cumorit mit deutlichen Warntexten zu versehen. Dies geschah, und ein Arztbrief Scherings vom August forderte erneut dazu auf, das Präparat nur bei Ausschluss einer Schwangerschaft anzuwenden. Am 1. September wurde der Name Duogynon durch Cumorit ersetzt. Die öffentliche Debatte führte zur Bildung von Interessengemeinschaften in Deutschland und England, wo sich Schering Ende 1978 mit Klagen konfrontiert sah. Dort war Primodos zu Jahresbeginn vom Markt genommen worden, nachdem der Umsatz stark gesunken war (die Fehlbildungen nahmen indes zu). In der Bundesrepublik schalteten sich nun vermehrt Fachverbände ein und kritisierten eine unsachliche Berichterstattung in der Tagespresse.
Als Reaktion auf die Debatte erfolgte Mitte Oktober 1978 eine Anhörung im BGA, bei der sich internationale Experten zu dem Problemkreis äußerten. Nach eingehender Diskussion aller bekannten Studien hieß das Ergebnis: „Die Annahme eines Zusammenhanges zwischen Hormon-Einnahme und allgemeiner Zunahme von Missbildungshäufigkeit ließ sich nicht belegen.“ [10]
Beginnende Ermittlungsverfahren
Angesichts der Presseberichte erstattete der Vater eines fehlgebildeten Kindes im August 1978 Strafanzeige wegen Körperverletzung (auch mit Todesfolge). Die Staatsanwaltschaft Berlin leitete daraufhin ein Ermittlungsverfahren gegen drei leitende Mitarbeiter Scherings ein. Bis 1980 gingen weitere Anzeigen ein, darunter eine der Interessengemeinschaft Duogynon-geschädigter Kinder, die der Staatsanwaltschaft die Namen von über 400 Betroffenen nannte. Die Ermittlungen konzentrierten sich auf die Kausalitätsfrage, die Vernehmung der Beschuldigten und Auswertung der Firmenunterlagen. Schering stellte ab Ende 1978 umfangreiches Material zur Verfügung (heute im Landesarchiv Berlin). Durchsuchungen oder Beschlagnahmungen erfolgten nicht.
Am 19. Dezember 1980 wurde das Verfahren eingestellt. Laut Staatsanwaltschaft war eine Kausalität nicht nachweisbar. Zwar werde die teratogene Wirkung in der Wissenschaft insgesamt widersprüchlich bewertet, doch mehrheitlich verneint, hieß es. Besonders die methodisch valideren Prospektivstudien ließen insgesamt keinen statistisch signifikanten Zusammenhang erkennen.
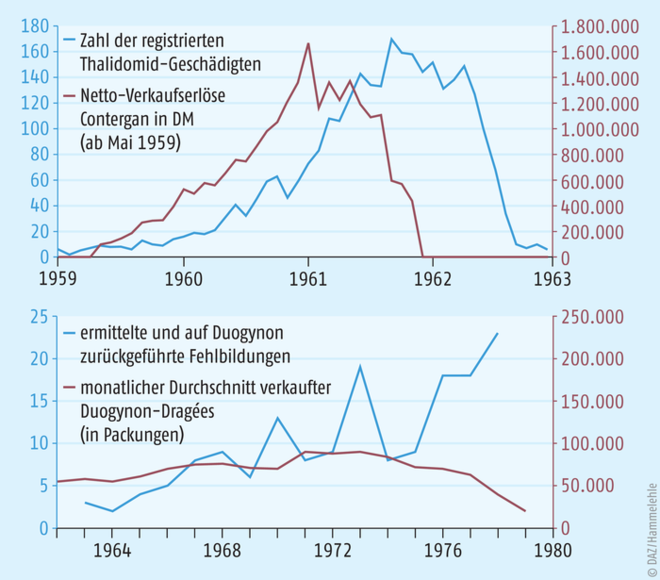
Auch war – anders als bei Contergan – keine Korrelation zwischen Absatz und Fehlbildungsfällen festzustellen, die auf Duogynon zurückgeführt wurden (siehe Diagramme auf der rechten Seite). Ein zeitliches und örtliches Zusammentreffen bestand ebenso wenig wie ein spezifischer Fehlbildungstyp, wie es ihn bei Contergan gab („Phokomelie“). Aufgrund zweier Gutachten von Prof. Widukind Lenz, der die teratogene Wirkung Contergans entdeckt hatte, zogen die Staatsanwälte das Fazit, eine Duogynon-Schädigung werde sich in vielen Fällen ausschließen lassen. In den übrigen sei eine solche jedenfalls nicht zu beweisen. Auch mit Blick auf die Tierversuche sei unklar, ob die wenigen aufgetretenen Anomalien in Zusammenhang mit Hormongaben stünden.
Auch in rechtlicher Hinsicht war der Sachverhalt schwer greifbar. Körperverletzungs- und Tötungsdelikte kamen nicht infrage, weil nach dem deutschen Strafrecht solche Delikte nur an einer Person begangen werden konnten, ein Embryo oder Fötus aber keine Person im Sinne des Strafgesetzbuches ist. Das keimende Leben war und ist nach dem deutschen Strafrecht nur durch die Bestimmungen zum Schwangerschaftsabbruch und, mit Blick auf Arzneimittel, durch die Strafvorschriften der Arzneimittelgesetze von 1961 und 1976 geschützt. Hierzu war aber ein Nachweis der Schädlichkeit bzw. Gefährlichkeit bei bestimmungsgemäßem Gebrauch erforderlich [11].
Marktrücknahme in Deutschland
Das Thema Duogynon blieb auch nach der Umbenennung in Cumorit in der Öffentlichkeit präsent, zumal das Ermittlungsverfahren und die Aktionen der Interessengemeinschaft wiederholt Schlagzeilen lieferten. Angesichts der intensiven wissenschaftlichen Debatte fand im BGA im Februar 1980 ein Expertengespräch zum Thema Hormonbehandlung der sekundären Amenorrhö statt, deren Ergebnisse im Deutschen Ärzteblatt veröffentlicht wurden. Demnach war die Gabe von Östrogen-Gestagen-Präparaten nur in wenigen Einzelfällen indiziert. Schering teilte daraufhin im September 1980 mit, die Behandlung sekundärer Amenorrhö durch Cumorit sei medizinisch überholt; die Produktion werde eingestellt. Mit dem schriftlichen Verzicht erlosch am 11. September auch die Zulassung. Der Vertrieb des Präparates wurde Ende Februar 1981 eingestellt.
Aktivitäten der Betroffenen
Mit der Marktrücknahme schwand auch das öffentliche Interesse am Thema Duogynon, zumal auch weiteren rechtlichen Schritten gegen Schering im In- und Ausland kein Erfolg beschieden war. Erst im neuen Jahrtausend erfuhr das Thema wieder vermehrt Aufmerksamkeit. Auch pharmakritische Verbände griffen den Fall Duogynon auf. Da Schering 2006 von Bayer aufgekauft worden war, forderten Geschädigte aus England, die ihre Schädigung auf Primodos zurückführten, auf der Bayer-Hauptversammlung im Mai 2009 eine Entschädigung und eine Entschuldigung des Konzerns.
Im Sommer 2010 berichteten diverse Medien über die Kampagne „Duogynon-Opfer“. Eine Haftungsklage gegen Bayer blieb 2011 erfolglos, weil das Unternehmen die Einrede der Verjährung genutzt hatte. Nachdem das Thema zeitweilig abgeflaut war, kam es 2016 zu einem vorläufigen Höhepunkt der Berichterstattung, als Kampagnenvertreter Einsicht in die staatsanwaltlichen Akten im Landesarchiv Berlin erhalten hatten und neue Hoffnung schöpften. Diverse Medien wie „Spiegel“ oder die TV-Reihe „Die Story“ berichteten empört über die Einflussnahme Scherings auf das BGA und den Weiterverkauf des Präparats, obwohl Tierversuche eine teratogene Wirkung nicht mit Sicherheit ausschließen konnten (siehe oben). Dabei folgten nicht wenige der Berichte eher einer investigativen Sensationslogik als einer sachlich-ausgewogenen Darstellungsweise. Dass die Wissenschaft für eine teratogene Wirkung mehrheitlich keinen Anhaltspunkt sah, ging in der medialen Berichterstattung oft ebenso unter wie die fehlende Korrelation zwischen Duogynon-Absatz und Fehlbildungen.
Angesichts des öffentlichen Aufsehens hatte das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) das Berliner Pharmakovigilanzzentrum für Embryonaltoxikologie bereits 2010 beauftragt, den Verdacht gegen Duogynon anhand des vorhandenen Datenmaterials zu prüfen. Die Mediziner der Charité führten einen statistisch deutlichen Zusammenhang mit Blasenekstrophien auf ein Bias zurück, ausgelöst durch die mediale Berichterstattung (in der ein solcher Fall im Fokus stand), zumal selbst Duogynon-kritische Publikationen eine solche Koinzidenz nicht beschrieben hatten. Zudem gebe es für die Duogynon-Wirkstoffe keine Informationen über eine Häufung von Fehlbildungen, obschon sie auch heute noch hunderttausendfach eingesetzt werden, etwa in der „Pille danach“. Auch wenn die Autoren eine fruchtschädigende Wirkung nicht mit absoluter Sicherheit widerlegen konnten, kamen sie zu dem Schluss: „Ein teratogener oder embryotoxischer Effekt von Duogynon, zu welchem Zwecke auch immer angewendet, ist unwahrscheinlich.“ [12]
Die Ergebnisse dieser Studie wurden im Oktober 2017 noch einmal bestätigt. Aufgrund einer Kampagne in England hatte das britische Parlament im Herbst 2015 einen Ausschuss eingesetzt, der den Zusammenhang zwischen Primodos und den Fehlbildungen untersuchen sollte. Nach Auswertung des gesamten verfügbaren Datenmaterials kam der Ausschuss in einer 144-seitigen Studie zu dem Ergebnis, dass keine Anhaltspunkte für einen kausalen Zusammenhang zwischen dem Präparat und Fehlbildungen vorliegen. Dagegen wies ein schottischer Biologe in einer Studie von 2018 darauf hin, dass sich bei hohen Dosierungen Entwicklungsschäden am Zebrafisch-Embryo erzeugen lassen. Auch wenn der Autor davor warnt, solche Ergebnisse ohne Weiteres auf andere Spezies zu übertragen, ist klar: Ein Ende der Debatte ist noch lange nicht in Sicht. |
Literatur
[1] Gutachten BGA, 14.11.1978, Landesarchiv Berlin, B Rep. 58, Nr. 1807, Bl. 18–22.
[2] Protokoll Expertenkommission, 30.11.1961, Landesarchiv NRW R, Gerichte Rep. 139, Nr. 55, Bl. 192.
[3] Nature 216/5110 (1967), S. 83.
[4] Bericht Nr. 983, 12.06.1973, Landesarchiv Berlin, B Rep. 58, Nr. 13226. Bei der verwendeten Dosis handelte es sich um 0,3 mg/kg Ethinylestradiol. Umgerechnet auf einen 70 kg schweren Menschen entsprach dies einer Dosis von 21 mg, also einer Menge von 1.050 Dragées! Ein britischer Untersuchungsausschuss (s. u.) hat die Versuchsprotokolle aus dem Landesarchiv Berlin zum Download zur Verfügung gestellt: https://mhra.filecamp.com/public/files/2rbs-ceca8bra [20.08.2018].
[5] Dt. Ärzteblatt 1973, S. 1901; Dt. Ärzteblatt 1974, S. 1013–1015.
[6] Siehe die Unterlagen des BMJFG in: Bundesarchiv, B 353/1465.
[7] Notiz Rechtsabteilung Schering, 22.12.1972, Landesarchiv Berlin, B Rep. 58, Nr. 13201, Bl. 379.
[8] Dt. Ärzteblatt 1978, S. 1752.
[9] Notiz Pharma Deutschland Leitung, 03.08.1978, Landesarchiv Berlin, B Rep. 58, Nr. 13199, Bl. 117.
[10] Siehe die Unterlagen in: Bundesarchiv, B 353/1465.
[11] Vgl. Einstellungsverfügung, 19.12.1980, Landesarchiv Berlin, Rep. 58, Nr. 1819.
[12] Bulletin zur Arzneimittelsicherheit Nr. 4 (2012), S. 20–23, Zitat S. 23.



























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.