
- DAZ.online
- DAZ / AZ
- DAZ 12/2011
- Immunbiologische Effekte ...
Mikronährstoffe
Immunbiologische Effekte von Mikronährstoffen
Gemeinsames Merkmal aller Vitamin-D-aktiven Verbindungen (sog. Calciferole) ist ihr Steroid-ähnliches Grundgerüst, das bei den einzelnen Vertretern unterschiedlich substituiert ist. Zu den wichtigsten Verbindungen der Vitamin-D-Gruppe zählen Ergocalciferol (Vitamin D2), Cholecalciferol (D3) und 25-Hydroxycholecalciferol (25-D3; Calcidiol), die Pro-Vitamine Ergosterol und 7-Dehydrocholesterol sowie die eigentlich biologisch aktive Vitamin-D-Form, das 1,25-Dihydroxycholecalciferol (Calcitriol).
Aufgrund seines Steroidcharakters nimmt Vitamin D unter den Mikronährstoffen nicht nur in chemischer Hinsicht eine Sonderstellung ein. Auch der Umstand, dass der menschliche Organismus bei ausreichender Sonnenlichtexposition in der Lage ist, den lebensnotwendigen Stoff vollständig und in ausreichendem Maße zu bilden, macht ihn zu einem Ausnahmefall (siehe Kasten "Vitamin-D-Bildung"). Denn während Vitamine definitionsgemäß Substanzen sind, die über die Nahrung zugeführt werden müssen, trifft dies für Vitamin D nur dann zu, wenn die für die endogene Synthese erforderliche UV-B-Strahlung nicht in ausreichendem Maße zur Verfügung steht. Daher wird Vitamin D von Ernährungsforschern auch als konditionell-essenzieller Nährstoff bezeichnet und aufgrund seiner physiologischen Eigenschaften eher den Steroidhormonen als den Vitaminen zugeordnet [1].
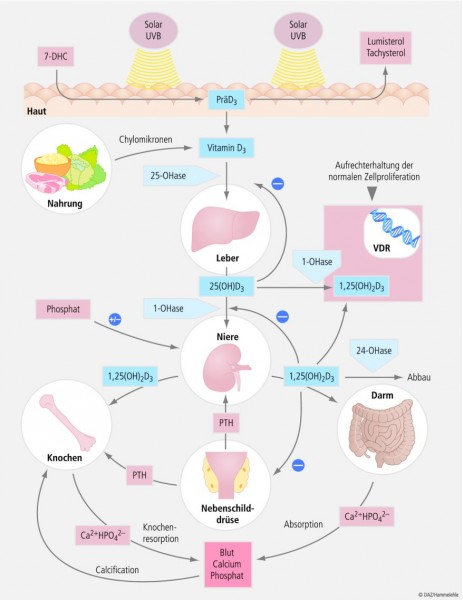
Vitamin-D-Bildung – "Photosynthese" der besonderen ArtDie Bildung von Calcitriol erfolgt beim Menschen in mehreren Reaktionsschritten (siehe Abb. 1): 1. Bildung von Cholecalciferol in der Haut. Als Ausgangssubstrat dient das bereits erwähnte 7-Dehydrocholesterol, dessen B-Ring in der Haut unter Einfluss von UV-B-Licht (Wellenlänge 290 – 315 nm) gespalten wird. Dabei entstehen unter Einfluss von Wärme Cholecalciferol sowie – bei starker UV-B-Exposition – Sekundärmetabolite wie Lumisterol und Tachysterol, die allerdings keine Vitamin-D-Wirksamkeit besitzen; eine UV-B-induzierte Vitamin-D-Intoxikation ist deshalb nicht möglich. Das in der Haut gebildete Cholecalciferol gelangt in die Blutbahn, wo es an ein spezifisches Eiweißmolekül, das Vitamin-D-bindende Protein (DBP), gekoppelt wird und über den Blutkreislauf zur Leber gelangt. 2. Bildung von Calcidiol in der Leber. Das von der Leber aufgenommene Cholecalciferol unterliegt in den Parenchymzellen einer einfachen Hydroxylierung an Position 25 des C-Skeletts. Katalysiert wird die Reaktion von einer Cytochrom-P450-abhängigen Hydroxylase; als Produkt entsteht Calcidiol. Die Vitamin-D-Synthese ist auf dieser Stufe nur unzureichend reguliert (einfache Produkthemmung), so dass sich der Serum-Wert an Calcidiol proportional zur Vitamin-D-Aufnahme über die Nahrung bzw. zur UV-Exposition verhält. Aus diesem Grund gilt die Menge an Calcidiol im Serum als zuverlässigster Indikator der Vitamin-D-Versorgung. 3. Bildung von Calcitriol in der Niere. Der letzte Schritt der Bioaktivierung von Vitamin D erfolgt in den Epithelzellen des proximalen Nierentubulus. Dort gelangt der über den Blutstrom herantransportierte Komplex aus Calcidiol und DBP über Megalinrezeptoren, die der Familie der Lipoproteinrezeptoren zuzuordnen sind, in die jeweiligen Körperzellen. Das intrazellulär freigesetzte Calcidiol unterliegt hier einer weiteren Hydroxylierung an Position 1 seines C-Skeletts, wobei das eigentlich biologisch aktive Calcitriol entsteht. Das hierfür verantwortliche Enzym (1α-Hydroxylase) unterliegt einer genauen Kontrolle: Calcium und Phosphat stellen die wichtigsten Repressoren, Parathormon den wichtigsten Induktor dar. Entsprechend ist die Calcitriolsynthese bei unzureichendem Angebot an Calcium und Phosphat gesteigert, bei ausreichender Versorgung dagegen gehemmt. Quelle: [1] |
Vitamin D – "Klassische" Funktionen
Auf der Ebene des Gesamtorganismus ist Calcitriol primär an der Regulation des Calcium- und Phosphathaushalts beteiligt. Auf molekularer Ebene ist dieser Effekt darauf zurückzuführen, dass Calcitriol als Bindungspartner (Ligand) des bereits erwähnten Vitamin-D-Rezeptors (VDR) dient (siehe Kasten "Vitamin-D-Bildung"). Analog zu den Schilddrüsenhormonen bindet der aus Calcitriol und VDR bestehende Komplex zusammen mit anderen Zellkernrezeptoren (Retinoidrezeptoren) an entsprechende Genabschnitte (sog. Vitamin-D-Response-Elemente; VDRE). Auf diese Weise wird die Synthese unterschiedlicher Proteine entweder induziert oder reprimiert – und zwar in Abhängigkeit des jeweiligen Zielgens. Damit ist Calcitriol ein zentraler Regulator der Genexpression. Betroffen sind primär Gene, die für Proteine des Calcium- und Phosphat-Haushalts kodieren. Auf Organebene bilden Darm, Niere, Knochen und Nebenschilddrüse die Angriffspunkte von Calcitriol [1, 3]:
Darm. Im Dünndarm – genauer im Jejunum und Ileum – steigert Calcitriol die Aufnahme von Calcium aus der Nahrung ins Blut. Vermittelt wird dieser Effekt durch im Dünndarmepithel lokalisierte Transportproteine, die unter Einfluss von Calcitriol vermehrt exprimiert werden. Dazu zählen Calciumkanäle (ECaC1 und ECaC2), das Transportprotein Calbindin und Calcium-ATPasen (PMCA1). Davon unabhängig steht auch die Phosphatabsorption im Darm unter der Kontrolle von Calcitriol: Hohe Konzentrationen steigern die Synthese eines Proteins, das den Natrium-gekoppelten Transport von Phosphat in die Blutbahn vermittelt. Fällt die Konzentration des Calcitriols dagegen ab, wird dieser Prozess gehemmt.
Niere. In den Nierentubuli stimuliert Calcitriol die Rückresorption von Calcium aus dem Primärharn. Der zugrunde liegende molekulare Mechanismus weist erstaunliche Parallelen zu den Vorgängen auf, wie sie für den Darm beschrieben wurden. So induziert Calcitriol auch im Nierenepithel die Synthese mehrerer Calcium-Transportproteine, die denen der Dünndarmzellen ähneln. Ebenfalls in den Nieren steigert Calcitriol die Rückresorption von Phosphat aus dem Primärharn und unterdrückt seine eigene enzymatische Synthese (siehe Kasten "Vitamin-D-Bildung"). Diese negative Rückkopplung gewährleistet, dass die Konzentration von Calcitriol in engen Grenzen gehalten wird.
Nebenschilddrüse. Calcitriol übt auf die Nebenschilddrüse einen zweifachen Effekt aus. Zum einen reprimiert es direkt die Expression von Parathormon (PTH); zum anderen vermindert es das Wachstum der Nebenschilddrüsenzellen über eine Hemmung verschiedener mitogener Signale (u. a. TGF-α und EGFR).
Knochen. Am Skelettsystem entfaltet Calcitriol sowohl anabole als auch katabole Effekte. Seine anabole Wirkung beruht darauf, dass es Osteoblasten zur Synthese von Proteinen anregt, die an der Knochenmineralisation (Osteocalcin, Matrix-Gla-Protein) und am Aufbau der Knochenmatrix (u. a. Osteopontin) beteiligt sind. Verstärkt wird dieser direkte Effekt durch die oben erwähnte Hemmung der PTH-Sekretion.Bei einem Abfall des Blut-Calciumspiegels bewirkt Calcitriol hingegen den gegenteiligen Effekt und steigert zusammen mit PTH die Aktivität und die Anzahl der Osteoklasten – ein Vorgang, der die Auslagerung von Calcium aus den Knochen zur Folge hat. Da Osteoklasten im Gegensatz zu Osteoblasten keine Vitamin-D-Rezeptoren besitzen, stimuliert Calcitriol die Osteoklastenbildung nur auf indirektem Wege.
Vitamin D – "Neue" immunobiologische Funktionen
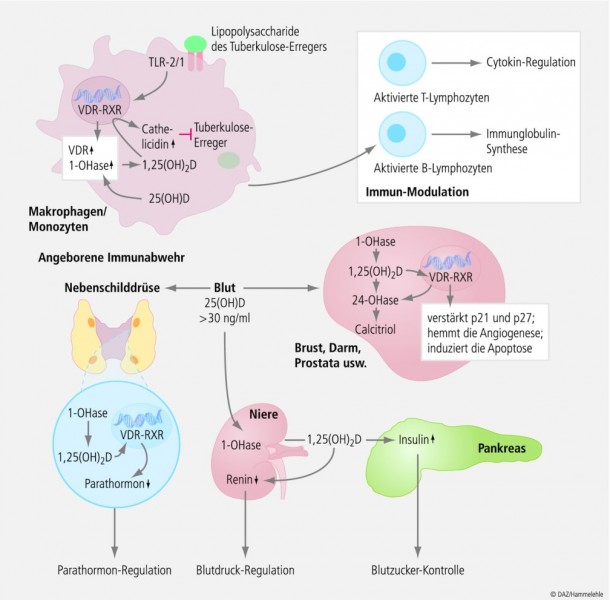
Eine interessante Entdeckung der letzten Jahre besteht darin, dass Calcitriol nicht nur die oben beschriebenen endokrinen Effekte vermittelt; vielmehr übt Vitamin D auch auto- und parakrine Wirkungen aus [1, 3]. Diese Einsicht basiert auf dem Befund, dass zahlreiche Körperzellen (u. a. Darm-, Brust-, Prostata- und Endothelzellen) über die enzymatische Voraussetzung zur Synthese von Calcitriol aus seinem Präkursor Calcidiol verfügen. Da Schätzungen zufolge mehr als 500 der etwa 20.488 Gene des Menschen unter Kontrolle von Calcitriol stehen und auch die meisten Körperzellen Vitamin-D-Rezeptoren besitzen, entfaltet Vitamin D vielfältige extraskelettale Wirkungen [4] (Abb. 2).
Zur großen Überraschung hat sich dabei gezeigt, dass auch immunkompetente Zellen wie Makrophagen, dendritische Zellen sowie B- und T-Lymphozyten Vitamin-D-Rezeptoren besitzen bzw. zur Calcitriolsynthese befähigt sind. Während Makrophagen und dendritische Zellen den Vitamin-D-Rezeptor konstitutiv exprimieren, wird dieser in T-Zellen erst nach Aktivierung gebildet [5].
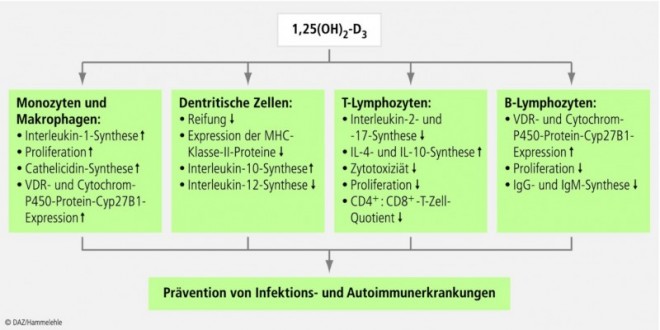
Vor diesem Hintergrund verwundert es nicht, dass sich Vitamin D als ein potenter Immunmodulator erwiesen hat. So fördert systemisch oder lokal synthetisiertes Calcitriol u. a. die Differenzierung von Monozyten zu Makrophagen und deren Phagozytoserate sowie die Aktivität lysosomaler Enzyme in Makrophagen (Abb. 3).
Vitamin D und Infektabwehr
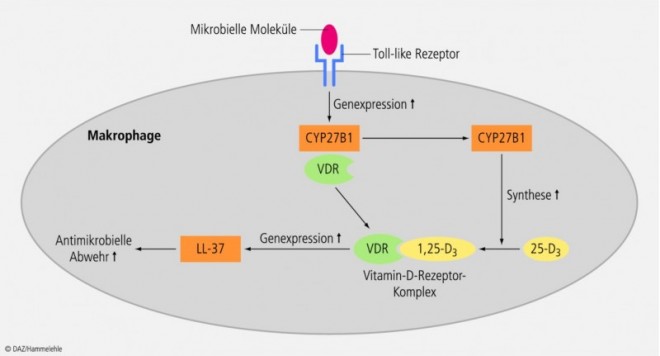
Eine für die unspezifische Infektabwehr wesentliche Funktion von Calcitriol besteht darin, dass es die Synthese antimikrobiell wirksamer Peptide, die sog. Cathelicidine, induziert. Im Gegensatz zu anderen Säugern exprimieren humane Zellen wie Keratinozyten und Makrophagen nur ein bestimmtes Cathelicidin (LL-37), das nach erfolgter Infektion vermehrt gebildet wird. Dabei induziert die Antigenbindung an Toll-like-Rezeptoren die Calcitriol-vermittelte Bildung von LL-37. Letzteres ist in der Lage, bakterielle Membranen zu penetrieren, worauf die bakterizide Wirkung dieses Cathelicidins zurückzuführen ist. Aber auch über die Transaktivierung des epidermalen Wachstumsfaktors (EGF) und über die intrazelluläre Calcium-Mobilisation beeinflusst LL-37 die primäre Immunabwehr u. a. an der Hautoberfläche [5].
Besonders gut untersucht ist die Interaktion von Calcitriol mit dem LL-37-System im Rahmen der Immunabwehr von Mycobacterium tuberculosis (MTB) durch Monozyten/Makrophagen. So führt die Infektion mit MTB nicht nur zur Hochregulation des Vitamin-D-Rezeptors sondern auch zu einer vermehrten Expression des Enzyms 1-α-Hydroxylase. Letzteres katalysiert die Synthese von Calcitriol aus seiner Vorstufe Calcidiol. Der Calcitriol-VDR-Komplex induziert dann als Transkriptionsfaktor die Cathelicidin-Expression (siehe Abbildung 4), so dass die MTB-Resistenz entscheidend von der Vitamin-D-Versorgung mitbestimmt wird. Dieser überraschende biochemische Befund wirft auch neues Licht auf die seit Ende der 1890er Jahre in Mitteleuropa verbreitete physikalische Therapie der systemischen Tuberkulose, die auf das Engste mit den Forschungsarbeiten des späteren Medizin-Nobelpreisträgers Niels Ryberg Finsen (1860 – 1904) in Verbindung steht. In umfangreichen Untersuchungen hatte Ryberg entdeckt, dass sich Sonnenlicht nicht nur zur Heilung von verschiedenen Hauterkankungen (u. a. Lupus vulgaris) einsetzen lässt, sondern auch den Verlauf der Tuberkulose – insbesondere den der pulmonalen – günstig beeinflusst. Die wissenschaftlich begründete Heliotherapie der TBC und die damit verbundene Kultur der Sonnensanatorien in den hochalpinen Regionen nahmen damit ihren Ausgang.
Wenngleich der therapeutische Stellenwert der Heliotherapie immer auch kritisch beurteilt worden war und ihr spätestens mit dem Einzug der modernen pharmakologischen Kombinationstherapie in Form von Isoniazid, Rifampicin, Ethambutol und Pyrazinamid nur noch eine medizinhistorische Bedeutung zukommen dürfte, so lassen sich die bei TBC-Patienten unter Heliotherapie erzielten Erfolge heute sehr gut auf dem Boden der oben erwähnten immunbiologischen Befunde zum Vitamin-D-Stoffwechsel erklären: Unter Sonnenexposition bildet der Organismus vermehrt Calcidiol, dieses gelangt in die Makrophagen, wird dort zu Calcitriol hydroxyliert und induziert die Bildung der mikrobiziden Cathelicidine. Damit schließt sich auf elegante Weise ein medizinhistorisch-biochemischer Kreis [6].
In diesem Zusammenhang sind auch neuere Befunde aus der Epidemiologie von Interesse. Hier ergab eine Metaanalyse aller relevanten Beobachtungsstudien, dass Personen mit adäquater Vitamin-D-Versorgung ein um 32% vermindertes TBC-Risiko aufwiesen, verglichen mit Personen, die mangelhaft mit Vitamin D versorgt waren (RR: 0,68; 95% CI 0,43 – 0,93) [7]. Zudem ist auch das Risiko, dass es nach einer Infektion mit Myobacterium tuberculosis zum Ausbruch der Erkrankung kommt, abhängig von der Versorgung mit Vitamin D. Dabei gilt die Assoziation: Je besser die Vitamin-D-Versorgung, desto geringer das Risiko [8].
Auch bei weniger dramatischen Infektionserkrankungen existiert eine solche inverse Beziehung zwischen dem Vitamin-D-Status und der Infektionsresistenz. So war in einer populationsbezogenen Querschnittsstudie mit 18.883 Teilnehmern (Third National Health and Nutrition Examination Survey; NHANES III 1988 – 1994) das Risiko für Atemwegsinfekte bei Personen (> 12 Jahre) mit unzureichender Vitamin-D-Versorgung (< 25 nmol/l Calcidiol) 36% höher, verglichen mit ausreichend versorgten Personen (> 75 nmol/l Calcidiol) (OR: 1,36; 95% -KI: 1,01 - 1,84) [9]. Auch ältere Beobachtungsstudien bei Kindern belegen, dass eine mangelhafte Versorgung mit Vitamin D das Risiko für Atemwegsinfektionen erhöht [10, 11].
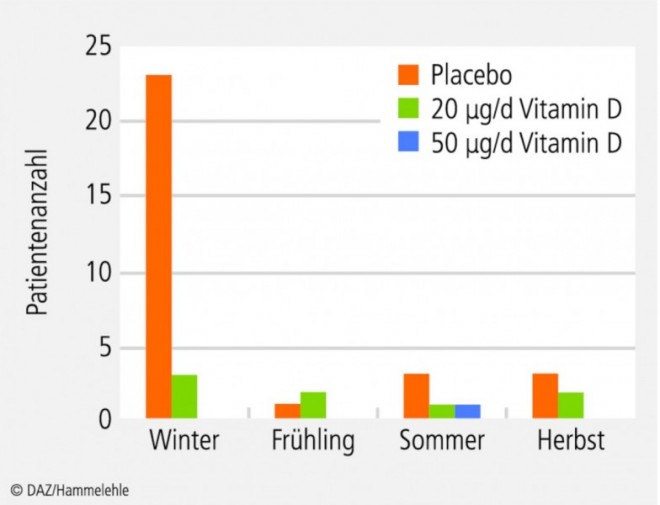
Unterstrichen wird der Schutzeffekt von Vitamin D bei Infektionserkrankungen durch die Ergebnisse zweier placebokontrollierter Doppelblindstudien. Die erste Untersuchung wurde an postmenopausalen Afro-Amerikanerinnen (n = 208) im Staat New York durchgeführt. Die Studienteilnehmerinnen erhielten für die Dauer von 36 Monaten entweder ein Vitamin-D-haltiges Supplement (20 µg/Tag Vitamin D während der ersten zwei Jahre, dann 50 µg/Tag bis Studienende) oder ein Placebo. Primärer Untersuchungsparameter war der Einfluss der Supplementierung auf die Knochendichte.
Wie die Sekundäranalyse der Daten ergab, kam es unter der Vitamin-D-Supplementierung zu wesentlich weniger jahreszeitlich bedingten Atemwegsinfekten bzw. grippalen Infekten (Abb. 5). Verglichen mit den Teilnehmerinnen der Placebogruppe wiesen Personen, die täglich 20 µg Vitamin D zuführten, ein um 60% vermindertes Erkrankungsrisiko auf; bei jenen, die 50 µg/Tag supplementierten, verringerte sich das Erkältungsrisiko sogar um 90% [12].
Eine ähnliche Dosis-Wirkungsbeziehung wurde auch in einer zweiten randomisierten, doppelverblindeten Untersuchung an japanischen Kindern beobachtet. 334 Schulkinder erhielten während des Interventionszeitraums (Dezember 2008 bis März 2009) täglich 30 µg Vitamin D oder ein Placebo. Unter der Vitamin-D-Substitution verminderte sich das Risiko, an Influenza A zu erkranken, um 62% (RR, 0,58; 95% CI: 0,34, 0,99; P = 0,04). Besonders ausgeprägt war der protektive Effekt bei jenen Kindern, die keine anderen Vitamin-D-haltigen Präparate einnahmen (RR: 0,36; 95% CI: 0,17, 0,79; P = 0,006) [13].
Vitamin D – Ätiopathogenetische Relevanz bei Autoimmunerkrankungen
Ausgehend von der Beobachtung, dass Vitamin D einen potenten Modulator der erworbenen Immunität darstellt, die Immunbalance zwischen Th1- und Th2-Zellen zugunsten letzterer verschiebt und damit die Autoimmuntoleranz zu regulieren vermag, wird Vitamin D als relevanter Faktor bei der Ätiopathogenese von verschiedenen Autoimmunerkrankungen diskutiert (siehe Tab. 1).
Beispielhaft sei hier das Krankheitsbild der multiplen Sklerose (MS) näher ausgeführt. Hier belegt eine wachsende Zahl an epidemiologischen und mechanistisch-experimentellen Befunden, dass eine inadäquate Vitamin-D-Versorgung das Erkrankungsrisiko erhöht [5]. So steigt die Prävalenz der multiplen Sklerose global betrachtet mit steigender Entfernung vom Äquator bzw. sinkender UV-B-Exposition. Andererseits findet sich ein ausgeprägter inverser Zusammenhang zwischen der Vitamin-D-Versorgung und dem Auftreten von MS.
Dass die UV-B-Exposition bzw. die exogene Vitamin-D-Versorgung einen relevanten modifizierbaren Risikofaktor bei MS darstellt, wird auch durch den Umstand unterstrichen, dass Personen seltener erkranken, wenn sie
in Bergregionen leben oder
eine hohe Vitamin-D-Zufuhr über die Nahrung aufweisen [5] oder
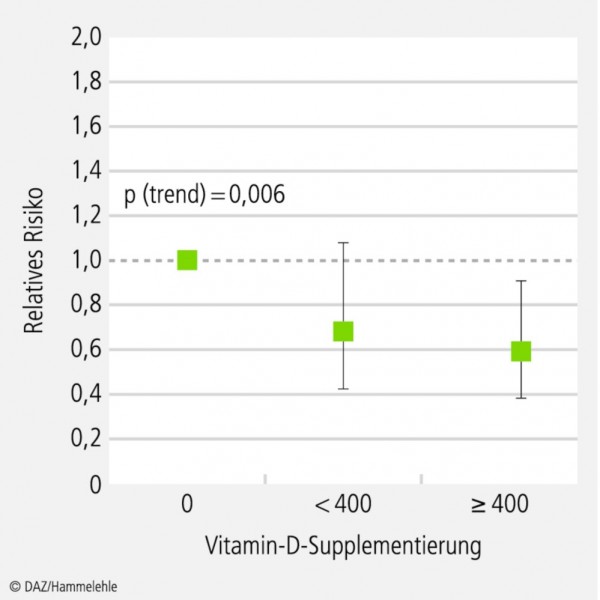
höher dosierte Vitamin-D-Supplemente einnehmen (Abb. 6).
Die Vitamin-D-Hypothese der MS wird auch durch die Ergebnisse einer prospektiven Beobachtungsstudie untermauert. Hier war das MS-Risiko umso geringer, je besser die Vitamin-D-Versorgung war (odds ratio [OR] pro Zunahme um 50 nmol/l Serum-Calcidiol: 0,59; 95% CI 0,36 – 0,97). Auch eine kürzlich publizierte Fall-Kontroll-Studie konnte bei Frauen eine inverse Korrelation zwischen der mittleren Serum-Calcidiol-Konzentration und dem Erkrankungsrisiko nachweisen; für einen Anstieg des Calcidiol-Werts um 10 nmol/l verminderte sich das MS-Risiko um 19% (odds ratio 0,81; 95% CI 0,69 - 0,95) [5]. Im Verein mit den in Tabelle 1 aufgeführten biologisch-mechanistischen Befunden legen die umfangreichen epidemiologischen Daten die Vermutung nahe, dass Vitamin D tatsächlich in kausaler Weise das MS-Risiko zu modifizieren vermag. [19]. Biostatischen Berechnungen zufolge ließen sich etwa 75% aller MS-Fälle durch eine adäquate Vitamin-D-Versorgung (Zielwert: > 100 nmol/l Serum-Calcidiol) vermeiden [18].
Vitamin D zur Prävention von (Autoimmun)-Erkrankungen
Aufgrund der Tatsache, dass Vitamin D auch bei verschiedenen anderen Autoimmunerkrankungen als potenzieller Schutzfaktor gilt (siehe Tab. 1), wird die Frage nach der wünschenswerten Versorgung und Zufuhr gegenwärtig intensiv diskutiert. Während Konsens darüber herrscht, dass die Serumkonzentration von Calcidiol als aussagekräftigster Parameter der Vitamin-D-Versorgung anzusehen ist, wird die Frage nach dem wünschenswerten Serumwert unterschiedlich beantwortet. Basierend auf der Studienlage plädieren die meisten Vitamin-D-Forscher für eine präventive Calcidiol-Serumkonzentration von ≥ 75 nmol/l (≥ 30 ng/ml). Bei dieser Konzentration scheint das Risiko für die o. g. Autoimmunerkrankungen wie Diabetes mellitus Typ 1 und multiple Sklerose deutlich reduziert zu sein [20]. Auch mit Blick auf die anderen skelettalen und extraskelettalen Effekte von Vitamin D wie Knochengesundheit, Darmkrebsrisiko und Muskelfunktion, ist bei diesem Grenzwert mit den günstigsten Wirkungen zu rechnen [21]. Im Unterschied dazu wurde vom US-amerikanischen Institute of Medicine (IOM) kürzlich ein deutlich niedrigerer wünschenswerter Blutspiegel von ≥ 50 nmol/l Calcidiol (20 ng/ml) als Richtwert postuliert [22]. Anzumerken ist jedoch, dass dieser Wert lediglich auf die skelettalen Wirkungen von Vitamin D abzielt; sonstige Effekte auf die Gesundheit, wie z. B. mögliche protektive immunologische Wirkungen, blieben bei der Ableitung des Grenzwertes unberücksichtigt. Entsprechend wurden bereits kritische Stimmen laut, welche den IOM-Zielwert als zu niedrig erachten [23, 24].
Unabhängig von der Frage, ob der eher konservative IOM-Richtwert von ≥ 50 nmol/l (20 ng/ml) oder der von der Mehrheit der Vitamin-D-Forscher favorisierte Serumspiegel von ≥ 75 nmol/l (≥ 30 ng/ml) als wünschenswert erachtet wird, stellt sich die Frage, wie solche Werte in der Praxis zu erreichen sind. Da die Zufuhr von 1 µg Vitamin D/Tag aus der Nahrung die Ausgangsspiegel nur durchschnittlich um 1 nmol/l erhöhen [25 – 27], ist es ohne entsprechende Sonnenexposition nahezu unmöglich, eine ausreichende Vitamin-D-Versorgung über die normale Ernährung sicherzustellen. So zeigen neuere Studien, dass während der Winterzeit eine tägliche Vitamin-D-Zufuhr von 20 – 40 µg notwendig ist, um bei der Mehrzahl der Erwachsenen einen präventiven Blutspiegel (≥ 75 nmol/l) zu erreichen [26, 28]. Auch für ältere Personen (> 64 Jahre) ohne Sonnenbestrahlung ist eine ähnlich hohe Zufuhr (43 µg/Tag) erforderlich [25]. In Übereinstimmung mit diesen Befunden wurde bereits in der Vergangenheit empfohlen, ohne entsprechende UV-B-Exposition täglich mindestens 17, besser aber 25 µg Vitamin D zuzuführen [4, 21, 29] – ein Wert, der weit über den Zufuhrempfehlungen der meisten nationalen und internationalen Ernährungsfachgesellschaften liegt. Allerdings hat das IOM seine Empfehlungen jüngst überarbeitet und die wünschenswerte tägliche Zufuhr auf 15 µg für Personen bis zum 70. Lebensjahr und auf 20 µg für Personen über 70 Jahre deutlich erhöht [22].
Optimierte Mikronährstoffversorgung zur Verbesserung der Immunkompetenz
Vor dem Hintergrund der bisherigen Ausführungen ist auch von Interesse, inwieweit die Supplementierung von Mikronährstoffen im Allgemeinen dazu beitragen kann, die Immunkompetenz zu verbessern. Die Beantwortung dieser Frage wird jedoch dadurch erschwert, dass eine Vielzahl von Kodeterminanten existieren, die die Wirkung von Vitamin- und Mineralstoffpräparaten beim Menschen beeinflussen (Tab. 2).
Tab. 2: Einflussfaktoren auf die immunbiologische Wirkung von Mikronährstoffsupplementen [5] | |
Personenbezogene Kodeterminanten |
Mikronährstoffbezogene Kodeterminanten |
|
|
Entsprechend der Vielzahl der Einflussfaktoren sind auch viele Interventionsstudien im Bereich der Ernährungsimmunologie heterogener Natur, so dass eine zusammenfassende und abwägende Betrachtung notwendig ist. Bei der Bewertung der Interventionsstudien sind u. a. folgende Faktoren zu berücksichtigen [5]:
Einflussfaktor "Dosis". Dass die Dosis nicht nur das Gift sondern auch die erwünschte Wirkung macht, ist nicht erst seit den Tagen von Paracelsus bekannt. Tatsächlich dürften beispielsweise die uneinheitlichen Ergebnisse zur Wirksamkeit einer Vitamin-D-Supplementierung bei Infektionserkrankungen [12, 30, 31] auf die unterschiedliche Dosis der eingesetzten Vitamin-D-Präparate zurückzuführen sein, wie die post-hoc-Analyse einer kontrollierten Interventionsstudie gezeigt hat [12]. Eine ähnliche Dosis-Wirkungsbeziehung wurde auch für die Einnahme von Vitamin-C-Supplementen und die Dauer von Erkältungskrankheiten bei Kindern beschrieben. So ergab die gepoolte Auswertung von vier Interventionsstudien mit einer Vitamin-C-Dosis von 200 – 750 mg/Tag eine Reduktion der Krankheitsdauer um 7% (95% CI - 19 bis - 5) und bei einer Dosis von 1000 mg/Tag (sechs Studien) eine Reduktion der Krankheitsdauer um 18% (95% CI - 32 bis - 3) im Vergleich zu Placebo [32].
Einflussfaktor "Belastung". Sowohl das Ausmaß der körperlichen Aktivität als auch die klimatischen Bedingungen beeinflussen den Nährstoffbedarf und die Immunkompetenz. Diese Abhängigkeit wird abermals deutlich am Beispiel "Vitamin C und Erkältungskrankheiten". Während die prophylaktische Supplementierung von Vitamin C in der Durchschnittsbevölkerung keinen klinischen Nutzen im Hinblick auf die Dauer von Erkältungskrankheiten erkennen lässt (RR, an einer Erkältung zu erkranken, schwankt in den Verumgruppen der Einzelstudien zwischen 0,39 und 1,36; gepoolter RR-Wert von 30 Studien: 0,96 (95% CI 0,92 – 1,00), zeigt die Subgruppenanalyse ein differenziertes Bild. Danach profitieren Personen, die besonderen Stresssituationen und damit einer erhöhten Infektanfälligkeit ausgesetzt sind (z. B. Marathonläufer), von einer prophylaktischen Vitamin-C-Einnahme (RR 0,50; 95% CI 0,38 – 0,66) [32].
Einflussfaktor "Synergismus". Im Hinblick auf ihre physiologische Funktion weisen viele Mikronährstoffe ausgesprochene Synergieeffekte auf. Die Vitamine E und C sind z. B. in ein antioxidatives Netzwerk eingebunden, wobei Vitamin C das wichtigste Antioxidans in der hydrophilen Phase darstellt, während Vitamin E in den lipophilen Zellkompartimenten wirksam ist [33]. Ein ähnlicher Synergismus existiert auch bei den Vitaminen Folsäure und Vitamin B12 im Rahmen des Homocysteinstoffwechsels [34]. Mit Blick auf die Immunkompetenz ist die Supplementierung mit einzelnen, hochdosierten Mikronährstoffen nicht zuletzt deshalb als wenig zielführend anzusehen. Vielmehr lassen sich klinische Wirkungen primär durch Mikronährstoffkombinationen erreichen [35].
Einflussfaktor "Versorgungsstatus". Der Nutzen einer Mikronährstoffsupplementierung im Hinblick auf die Immunkompetenz wird entscheidend durch den basalen Nährstoffstatus mitbestimmt. Dabei gilt: Je schlechter die Versorgung der untersuchten Personen, desto größer der Nutzen einer Intervention mit Mikronährstoffen [36]. Entsprechend können Patienten mit einem nutritiv bedingten Immundefizit von der Supplementierung mit einem physiologisch dosierten Multivitamin-Multimineralpräparat profitieren. Während z. B. die Supplementierung eines Multivitamin-Multimineralpräparats bei gesunden, gut versorgten Senioren keine Verbesserung der Immunkompetenz bewirkt, zeigt die Subgruppenanalyse der vorliegenden Studien wiederum ein anderes Bild. Danach reduziert sich das Infektionsrisiko bei Senioren (≥ 65 Jahre) mit unzureichendem Nährstoffstatus durch eine solche Maßnahme (gewichtete mittlere Differenz - 0,67; CI - 1,24; - 0,10, Verum versus Placebo) [36].
Therapeutische Effekte einer Supplementierung
Wie aus den bisherigen Ausführungen hervorgeht, stellt die Mikronährstoffzufuhr einen Expositionsfaktor dar, der die Immunkompetenz des Menschen maßgeblich beeinflusst. Der Immunstatus stellt daher einen sensitiven Indikator für die Versorgung mit Mikronährstoffen dar. Umgekehrt übt die Aktivität des Immunsystems einen Einfluss auf den Nährstoffstatus und den Nährstoffbedarf aus. Es kann daher nicht verwundern, dass sowohl akute als auch chronische Erkrankungen, die eine immunologische Komponente aufweisen, mit einem Mikronährstoffdefizit bzw. einem erhöhten Mikronährstoffbedarf assoziiert sind. Besonders eindrücklich beschrieben ist dieser Zusammenhang bei konsumierenden Erkrankungen wie dem aquired immunodeficiency syndrome (AIDS) oder bei Tumorerkrankungen, wo häufig ein multiples Mikronährstoffdefizit beschrieben wird [5, 37].
Aber auch bei inflammatorischen Prozessen, wie sie bei der rheumatoiden Arthritis zu beobachten sind, bei der Einnahme bestimmter Medikamente und infolge der altersassoziierten Abnahme der Immunkompetenz ist der Verbrauch bzw. der Bedarf an Mikronährstoffen oftmals erhöht. Mit einer üblichen Ernährung gelingt es in diesen Situationen häufig nicht, den Nährstoffbedarf zu decken oder gar entleerte Nährstoffspeicher wieder aufzufüllen. Dies wird vielfach dadurch verstärkt, dass ohnehin eine eingeschränkte Nahrungsauswahl besteht, die zu einer einseitigen Kostzusammenstellung führen kann. Es ist evident, dass bei manifesten Krankheiten, die den Nährstoffbedarf erhöhen, diesem Umstand diätetisch Rechnung zu tragen ist.
Vor dem Hintergrund der oben dargestellten Ausführungen lassen sich mit Blick auf die Immunkompetenz drei Indikationsbereiche für Mikronährstoffsupplemente definieren [5]:
Gezielte Supplementierung bei krankheitsbedingtem Mehrbedarf und/oder zur Kompensation eines Nährstoffdefizits.
Gezielte Supplementierung im Sinne einer günstigen Beeinflussung der Krankheitssymptomatik.
Gezielte Supplementierung zur Verzögerung bzw. Verhinderung des Voranschreitens oder Wiederauftretens der Erkrankung und zur Vermeidung von Folgeerscheinungen.
Generell gilt für den Nutzen von Mikronährstoffen bei nutritiv bedingten Immundefiziten: Je ausgeprägter die Nährstoffunterversorgung ist und je stärker die Synergieeffekte der Vitamine und der Mineralstoffe Beachtung finden, desto größer wird der Benefit sein. Umgekehrt gilt: Verbessert sich die Immunkompetenz infolge der Gabe von Mikronährstoffen, dann deutet dies auf eine unzureichende Ausgangsversorgung bei den Personen hin. Dies wird u. a. deutlich bei älteren Personen, die aufgrund ihrer besonderen Lebenssituation häufig ein multiples Defizit an Vitaminen (Folsäure, B1, B6, B12, Niacin und Vitamin C) und Mineralstoffen (Magnesium, Eisen, Zink und Selen) aufweisen. Hieraus resultieren u. a. Einschränkungen der Immunkompetenz. Entsprechend lässt sich bei unzureichender Versorgung mit Vitaminen und Mineralstoffen die Immunfunktion durch eine entsprechende Supplementierung verbessern, wie verschiedene Interventionsstudien zeigen [36]. Stellvertretend sei hier die Untersuchung von Langkamp-Henken et al. [38] genannt. In dieser placebokontrollierten Studie, in die Personen von 50 bis 65 Jahre eingeschlossen wurden, wiesen knapp die Hälfte der Probanden zu Studienbeginn eine Unterversorgung mit einem oder mehreren Mikronährstoffen auf. Im Rahmen einer zwölfmonatigen Intervention erhielten die Versuchsteilnehmer täglich eine Multivitamin-Multimineral-Kombination bzw. ein entsprechendes Placebo. Durch die Intervention kam es in der Verum-, nicht aber in der Placebogruppe, zu einer Verbesserung der Mikronährstoffversorgung, wie exemplarisch am Biomarker der Tocopherol-Versorgung gezeigt wurde. Gleichzeitig konnte auch die Immunfunktion positiv beeinflusst werden. So waren signifikant höhere Antikörperreaktionen nach einer Grippeimpfung nachweisbar sowie ein signifikant stärkerer Anstieg der T-Lymphozyten und der CD4+-Helferzellen. Besonders beachtenswert ist der Befund, dass hierdurch auch das Infektionsrisiko reduziert wurde. So betrug die durchschnittliche Anzahl von Krankheitstagen infolge von Infektionen der oberen Atemwege in der Supplement-Gruppe 11,1 ± 0,8, während sie in der Placebo-Gruppe mit 23,7 ± 2,1 Tage doppelt so hoch war.
Fazit
Mikronährstoffe beeinflussen verschiedene Stoffwechselbereiche, die unmittelbar mit den Immunfunktionen in Beziehung stehen. Entsprechend führen nutritive Defizite, wie sie als Folge von besonderen Belastungen oder auch Erkrankungen auftreten können, zu einer eingeschränkten Immunkompetenz. Umgekehrt kommt es bei Infektionen und anderen immunologisch assoziierten Erkrankungen zu einem gesteigerten Umsatz von Mikronährstoffen und damit zu einem erhöhten Bedarf. In diesem Kontext sind insbesondere die Vitamine C und D in den Fokus des wissenschaftlichen Interesses gerückt. So zeigt sich eine enge Abhängigkeit zwischen der Versorgung mit den genannten Vitaminen und der Immunfunktion. Dies betrifft vor allem die mikrobiozide Aktivität von Makrophagen wie auch – im Falle von Vitamin D – die T-Zell-Funktion. Ein Vitamin-C-Defizit zeigt sich entsprechend auch in einer verminderten Resistenz gegenüber verschiedenen Erregern, während eine defizitäre Vitamin-D-Versorgung mit der Entstehung verschiedener Autoimmunerkrankungen in Zusammenhang gebracht wird, wie zahlreiche Beobachtungsstudien nahelegen.
Literatur
[1] Ströhle A. Vitamin D – ein "archaischer" Steroidabkömmling im Blickfeld der aktuellen Ernährungsforschung. Naturw Rdsch 117 (2011) (in Druck)
[2] Wolters M, Ströhle A, Hahn A: Neue Erkenntnisse zu Vitamin D und Vitamin B12. Dtsch Apothek Z 145, 221 – 228 (2005)
[3] Dusso AS , Brown AJ, Slatopolsky E: Vitamin D. Am J Physiol Renal Physiol 289, F8-28 (2005)
[4] Holick MF: Vitamin D deficiency. N Engl J Med 357, 266 – 281 (2007)
[5] Ströhle A, Wolters M, Hahn A. Micronutrients at the interface between inflammation and infection ascorbic Acid and calciferol. Part 2: calciferol and the significance of nutrient supplements. Inflamm Allergy Drug Targets 10, 64 – 74 (2011)
[6] Müller NJ. Infektionen und Autoimmunerkrankungen: eine neue Rolle für Vitamin D? Schweiz Z Ernährungsmed 2, 18 – 20 (2009)
[7] Nnoaham KE, Clarke A. Low serum vitamin D levels and tuberculosis: a systematic review and meta-analysis. Int J Epidemiol 37, 113 – 9 (2008)
[8] Gibney KB, MacGregor L, Leder K, Torresi J, Marshall C, Ebeling PR, Biggs BA. Vitamin D deficiency is associated with tuberculosis and latent tuberculosis infection in immigrants from sub-Saharan Africa. Clin Infect Dis 46, 443 – 6 (2008)
[9] Ginde AA, Mansbach JM, Camargo CA Jr. Association between serum 25-hydroxyvitamin D level and upper respiratory tract infection in the Third National Health and Nutrition Examination Survey. Arch Intern Med 169, 384 – 90 (2009)
[10] Wayse V, Yousafzai A, Mogale K, Filteau S. Association of subclinical vitamin D deficiency with severe acute lower respiratory infection in Indian children under 5 y. Eur J Clin Nutr 58, 563 – 7 (2004)
[11] Muhe L, Lulseged S, Mason KE, Simoes EA. Case-control study of the role of nutritional rickets in the risk of developing pneumonia in Ethiopian children. Lancet 349, 1801 – 4 (1997)
[12] Aloia JF, Li-Ng M. Re: epidemic influenza and vitamin D. Epidemiol Infect 135:1095– 6; author reply 1097 – 8 (2007)
[13] Urashima M, Segawa T, Okazaki M, Kurihara M, Wada Y, Ida H. Randomized trial of vitamin D supplementation to prevent seasonal influenza A in schoolchildren. Am J Clin Nutr 91: 1255 – 60 (2010)
[14] Baeke F, Takiishi T, Korf H, Gysemans C, Mathieu C. Vitamin D: modulator of the immune system. Curr Opin Pharmacol 10, 482 – 96 (2010)
[15] Kampman MT, Wilsgaard T, Mellgren SI: Outdoor activities and diet in childhood and adolescence relate to MS risk above the Arctic Circle. J Neurol, 254: 471 – 477 (2007)
[16] Orton SM, Wald L, Confavreux C, Vukusic S, Krohn JP, Ramagopalan SV, Herrera BM, Sadovnick AD, Ebers GC. Association of UV radiation with multiple sclerosis prevalence and sex ratio in France. Neurology 76, 425 – 31 (2011)
[17] Pierrot-Deseilligny C. Clinical implications of a possible role of vitamin D in multiple sclerosis. J Neurol 256, 1468-79 (2009)
[18] Ascherio A, Munger KL. Environmental risk factors for multiple sclerosis. Part II: Noninfectious factors. Ann Neurol 61, 504 – 13 (2007)
[19] Hanwell HE, Banwell B. Assessment of evidence for a protective role of vitamin D in multiple sclerosis. Biochim Biophys Acta 1812, 202 – 12 (2011)
[20] Souberbielle JC, Body JJ, Lappe JM et al.: Vitamin D and musculoskeletal health, cardiovascular disease, autoimmunity and cancer: Recommendations for clinical practice. Autoimmun Rev 9, 709 – 715 (2010)
[21] Bischoff-Ferrari HA, Giovannucci E, Willett WC et al.: Estimation of optimal serum concentrations of 25-hydroxyvitamin D for multiple health outcomes. Am J Clin Nutr. 2006 Jul;84(1):18 – 28. Review. Erratum in: Am J Clin Nutr 84, 18 – 28 (2006)
[22] Ross AC, Manson JE, Abrams SA et al.: The 2011 report on dietary reference intakes for calcium and vitamin d from the institute of medicine: what clinicians need to know. J Clin Endocrinol Metab 96, 53 – 58 (2011)
[23] Grant WB: Is the Institute of Medicine Report on Calcium and Vitamin D Good Science? Biol Res Nurs. 2011 Jan 17 [Epub ahead of print]
[24] Heaney R, Holick MF: Why the IOM recommendations for vitamin D are deficient. J Bone Miner Res 2011 Jan 4. [Epub ahead of print]
[25] Cashman KD, Wallace JM, Horigan G et al.: Estimation of the dietary requirement for vitamin D in free-living adults ≥ 64 y of age. Am J Clin Nutr 89, 1366 – 1374 (2009)
[26] Cashman KD, Hill TR, Lucey AJ et al.: Estimation of the dietary requirement for vitamin D in healthy adults. Am J Clin Nutr 88, 1535 – 1542 (2008)
[27] Aloia JF, Patel M, Dimaano R et al.: Vitamin D intake to attain a desired serum 25-hydroxyvitamin D concentration. Am J Clin Nutr 87, 1952 – 1958 (2008)
[28] Nelson ML, Blum JM, Hollis BW et al.: Supplements of 20 microg/d cholecalciferol optimized serum 25-hydroxyvitamin D concentrations in 80% of premenopausal women in winter. J Nutr 139, 540 – 546 (2009)
[29] Bischoff-Ferrari HA: The 25-hydroxyvitamin D threshold for better health. J Steroid Biochem Mol Biol 103, 614 – 619 (2007)
[30] Wejse C, Gomes VF, Rabna P, Gustafson P, Aaby P, Lisse IM, Andersen PL, Glerup H, Sodemann M. Vitamin D as supplementary treatment for tuberculosis: a double-blind, randomized, placebo-controlled trial. Am J Respir Crit Care Med 179, 843 – 50 (2009)
[31] Li-Ng M, Aloia JF, Pollack S, Cunha BA, Mikhail M, Yeh J, Berbari N. A randomized controlled trial of vitamin D3 supplementation for the prevention of symptomatic upper respiratory tract infections. Epidemiol Infect 137, 1396 – 404 (2009)
[32] Douglas RM, Hemilä H, Chalker E, Treacy B. Vitamin C for preventing and treating the common cold. Cochrane Database Syst Rev. 2007 Jul 18;(3):CD000980
[33] Packer L, Kraemer K, Rimbach G. Molecular aspects of lipoic acid in the prevention of diabetes complications. Nutrition 17, 888 – 95 (2001)
[34] Ströhle A, Wolters M, Hahn A. Folic acid and colorectal cancer prevention: molecular mechanisms and epidemiological evidence (Review). Int J Oncol 26, 1449 – 64 (2005)
[35] Shenkin A. Micronutrients in health and disease. Postgrad Med J 82, 559 – 67 (2006)
[36] Stephen AI, Avenell A. A systematic review of multivitamin and multimineral supplementation for infection. J Hum Nutr Diet 19, 179 – 90 (2006)
[37] Ströhle A, Zänker K, Hahn A. Nutrition in oncology: the case of micronutrients (review). Oncol Rep 24, 815 – 28 (2010)
[38] Langkamp-Henken B, Bender BS, Gardner EM, Herrlinger-Garcia KA, Kelley MJ, Murasko DM, Schaller JP, Stechmiller JK, Thomas DJ, Wood SM. Nutritional formula enhanced immune function and reduced days of symptoms of upper respiratory tract infection in seniors. J Am Geriatr Soc 52, 3 – 12 (2004)
Autoren
Dr. Alexander Ströhle*, Dr. Maike Wolters, Prof. Dr. Andreas Hahn
* Anschrift des Korrespodenzautors:
Dr. Alexander Ströhle, Institut für Lebensmittelwissenschaft und Humanernährung, Leibniz Universität Hannover, Am Kleinen Felde 30, 30167 Hannover, Fax: +49-511-762-5729, E-Mail: stroehle@nutrition.uni-hannover.de





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.