
- DAZ.online
- News
- Pharmazie
- FDA genehmigt COVID-19-...
USA (Update)
FDA genehmigt COVID-19-Impfstoffe für Kinder ab 6 Monaten
Stuttgart - 17.06.2022, 16:45 Uhr
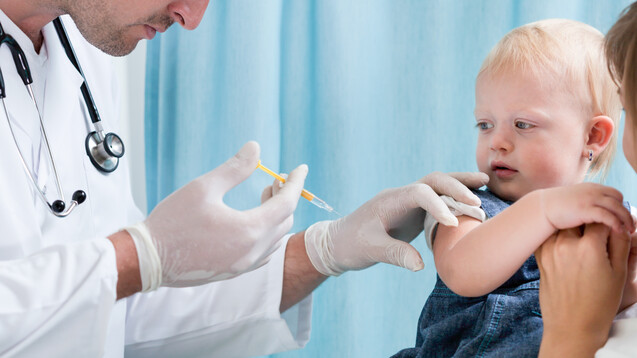
In der EU ist derzeit noch kein Corona-Impfstoff für Kleinkinder zugelassen. (s / Foto: Photographee.eu / AdobeStock)
Während viele bereits über eine vierte Corona-Impfung und damit einen zweiten Booster mit einem eventuell angepassten Corona-Impfstoff der zweiten Generation nachdenken, gibt es eine Gruppe in der Bevölkerung, die noch gar keine Impfung gegen COVID-19 erhalten hat: Kleinkinder zwischen sechs Monaten und fünf Jahren. In den USA hat die FDA nun auch die Notfallzulassung der Impfstoffe von Biontech/Pfizer und Moderna auf diese Altersgruppe erweitert.
Seit dem 24. Mai spricht sich die Ständige Impfkommission (STIKO) für eine „generelle“ Impfung von Kindern im Alter zwischen fünf und elf Jahren aus. Sie sollen zunächst allerdings nur eine Impfstoffdosis erhalten – unabhängig davon, ob sie bereits genesen sind oder noch SARS-CoV-2-naiv. Die STIKO rät „vorzugsweise“ zur Impfung mit Comirnaty (10 µg).
Damit bleibt vor allem eine Gruppe in der Bevölkerung vorerst ungeimpft: die Unter-Fünfjährigen.
Mehr zum Thema
Nur eine Dosis
STIKO: Alle fünf- bis elfjährigen Kinder gegen Corona impfen

Corona-Impfstoff von Moderna
EMA empfiehlt Zulassung von Spikevax ab sechs Jahren

Genehmigung erwartet
In den USA wohl bald Corona-Impfung für Unter-Fünfjährige
Schon Anfang Juni hieß es, dass die US-Regierung mit ersten Impfungen gegen das Coronavirus für Kinder im Alter unter fünf Jahren ab dem 21. Juni rechne. Der Coronavirus-Koordinator des Weißen Hauses, Ashish Jha, sagte, der zuständige FDA-Ausschuss werde die von den Herstellern Pfizer/Biontech und Moderna vorgelegten Daten für ihre Impfstoffe, die für Kinder ab sechs Monaten zum Einsatz kommen sollen, am 14. und 15. Juni prüfen.
Nun hat sich ein Beratergremium der US-Arzneimittelbehörde FDA tatsächlich für den Einsatz von Coronavirus-Impfstoffen bei Kindern im Alter zwischen sechs Monaten und fünf Jahren ausgesprochen: Sowohl der Impfstoff der Hersteller Biontech und Pfizer als auch das Präparat von Moderna könnten dafür zum Einsatz kommen, urteilte das Gremium am vergangenen Mittwoch nach stundenlanger Diskussion jeweils einstimmig. Die FDA selbst hat die Notfallzulassung heute entsprechend erweitert.

Der Zeitplan der STIKO
Corona-Impfung: Wie geht es weiter mit den (Klein)kindern?

Corona-Impfung für Kleinkinder kommt wahrscheinlich später
Biontech untersucht dritte Impfstoff-Dosis für die Kleinsten

Kleinkinder-Impfstoff noch in erster Jahreshälfte?
Corona-Impfstoff für Kinder von zwei bis fünf – Moderna erwartet im März Ergebnisse
Im Januar 2022 hatte der US-Hersteller Moderna mitgeteilt, im März mit den Ergebnissen seiner klinischen Studie zum Corona-Impfstoff für Kinder im Alter von zwei bis fünf Jahren zu rechnen. Falls die Daten und Gespräche mit der Aufsichtsbehörde positiv ausfielen, könnte Moderna sich dann für die Impfung um eine Notfallzulassung bemühen, hieß es. Im Februar hatten schließlich Biontech/Pfizer für ihren Corona-Impfstoff auf Anfrage der US-amerikanischen Food and Drug Administration einen Antrag auf Änderung der Notfallzulassung auf Kleinkinder gestellt. Tatsächlich bezog sich der Antrag vorerst nur auf die Zulassung der ersten beiden 3 µg-Dosen für diese Altersgruppe. Denn Daten zu einer dritten Dosis, die mindestens acht Wochen nach Abschluss der zweiten Dosis verabreicht wird, würden erst in den kommenden Monaten erwartet, hieß es.
Der „Washington Post“ ist nun zu entnehmen, dass es sich bei der aktuellen Empfehlung um drei Dosen von Biontech/Pfizer handelt. Denn offenbar sprechen Kinder im Alter zwischen zwei und fünf Jahren nicht genauso gut auf die COVID-19-Impfung von Biontech/Pfizer an wie Jugendliche und Erwachsene ab 16 Jahren und wie Kinder zwischen 6 und 24 Monaten. Deshalb war schon Ende vergangenen Jahres angekündigt worden, dass es wahrscheinlich eine dritte Impfstoff-Dosis brauchen wird.
Laut „Washington Post“ besteht die Impfung von Moderna für Kleinkinder momentan noch aus zwei Impfdosen zu je 25 µg, man untersuche aber bereits eine dritte. Es gehe zunächst darum, mit der Impfung von Babys überhaupt zu beginnen.
Bundesgesundheitsminister Karl Lauterbach begrüßte die Empfehlung der US-Arzneimittelbehörde. „Das ist eine gute Nachricht für Eltern“, schrieb der SPD-Politiker am Mittwochabend bei Twitter.
Der Impfstoff von Biontech/Pfizer war in den USA für Kinder im Alter von fünf bis elf Jahren zugelassen, der Impfstoff von Moderna für Menschen ab 18 Jahren – er darf nun auch zwischen sechs Monaten und 17 Jahren angewendet werden. Bereits am vergangenen Dienstag hatte sich das FDA-Beratergremium aber dafür ausgesprochen, den Impfstoff von Moderna auch für Kinder und Jugendliche zwischen sechs und 17 Jahren zuzulassen.
In der EU ist derzeit noch kein Corona-Impfstoff für Kleinkinder zugelassen. Die europäische Arzneimittelbehörde EMA in Amsterdam prüft zurzeit, ob der Impfstoff des Herstellers Moderna (Spikevax) auch für Kinder unter sechs Jahre zugelassen werden kann. Für den Impfstoff der Hersteller Biontech und Pfizer hat eine solche Prüfung noch nicht begonnen. Die Hersteller haben bisher nach Angaben der EMA keinen entsprechenden Antrag auf Erweiterung der Zulassung gestellt.
Dieser Text wurde am 17.06.2022 um 17:26 Uhr aktualisiert





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.