
- DAZ.online
- News
- Pharmazie
- Welche Daten gibt es bei...
AstraZeneca-Impfstoff: STIKO und EMA uneins
Welche Daten gibt es bei Älteren?
Stuttgart - 01.02.2021, 13:45 Uhr
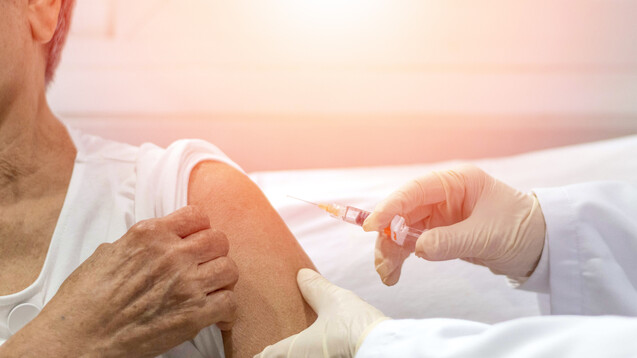
AstraZeneca berichtete Ende 2020 über positive Zwischenergebnisse zur Antikörperbildung nach Impfung mit AZD1222 – gerade auch bei älteren Menschen. (Foto: Khunatorn / stock.adobe.com)
Seit 29. Januar 2021 darf neben BNT162b2 (Comirnaty) von Biontech/Pfizer und mRNA-1273 von Moderna auch mit dem COVID-19-Impfstoff AstraZeneca in der EU geimpft werden. Die STIKO rät, nur 18- bis 64-Jährige damit zu impfen, die EMA setzt keine Altersobergrenze: Da es zuverlässige Informationen zur Sicherheit in dieser Altersgruppe gibt, könne der Impfstoff bei Älteren eingesetzt werden, sagt das CHMP. In der Tat gibt es eine Subgruppenanalyse.
Die Europäische Arzneimittelagentur EMA hat am 29. Januar die bedingte Zulassung des dritten COVID-19-Impfstoffes für die EU empfohlen, noch am selben Tag erteilte sodann die Europäische Kommission die Zulassung. Es geht um die Vakzine von AstraZeneca und der Universität Oxford: AZD1222, auch bekannt als ChAdOx1 nCoV-19. Ihr „neuer“ Name lautet nun „COVID-19-Impfstoff AstraZeneca“. Geimpft wird mit zwei Dosen im Abstand von vier bis zwölf Wochen.
EMA und STIKO unterschiedlicher Meinung
Dass sich der Humanarzneimittelausschuss positiv äußert, war erwartet worden. Nicht erwartet wurde allerdings, dass der vektorbasierte Corona-Impfstoff auch für Senioren zugelassen wird, da er nach Ansicht der EMA bei allen Menschen ab 18 Jahren eingesetzt werden kann. Warum überraschte die fehlende Altersobergrenze? Erst tags zuvor hatte die Ständige Impfkommission (STIKO) am Robert Koch-Institut (RKI) ihre Empfehlungen zur COVID-19-Impfung aktualisiert. In dem „Beschluss der STIKO zur 2. Aktualisierung der COVID-19- Impfempfehlung und die dazugehörige wissenschaftliche Begründung“ rät sie, dass AZD1222 nur bei Personen im Alter von 18 bis 64 Jahren geimpft werden soll. Sie STIKO begründet ihre Empfehlung: „Der COVID-19-Impfstoff von AstraZeneca wird aktuell aufgrund der derzeit verfügbaren Daten nur für Personen im Alter von 18 bis 64 Jahren empfohlen.“ Zur Beurteilung der Impfeffektivität bei Menschen ab 65 Jahren lägen bisher keine ausreichenden Daten vor. Abgesehen von dieser Einschränkung sieht die STIKO den dritten COVID-19-Impfstoff aber als gleichermaßen (wie Comirnaty® und mRNA-1273 von Moderna) geeignet an, um Menschen vor COVID-19 zu schützen und die Pandemie zu bekämpfen.
Wirksamkeit bei Älteren „nicht beurteilbar“
In der Tat ist den im Fachjournal „The Lancet“ veröffentlichten Forschungsergebnissen („Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK“) zu AZD1222 zufolge die Datenlage bei älteren Menschen gering, denn: Nur 12,2 Prozent der Studienteilnehmer:innen, die in die Auswertung mit einbezogen wurden, waren 55 Jahre und älter. Die Wissenschaftler:innen hinter den Impfstoff-Studien erklären somit: „Die Wirksamkeit des Impfstoffs konnte in älteren Altersgruppen nicht beurteilt werden.“
Mehr zum Thema

Dritter Impfstoff für Europa
EMA empfiehlt bedingte Zulassung für AstraZeneca-Impfstoff – auch für Senioren
Nun kennt auch die EMA diese Arbeit und die Ergebnisse, und sie räumt ein: „Es gibt noch nicht genügend Ergebnisse bei älteren Teilnehmer:innen (über 55 Jahre alt), um zu bewerten, wie gut der Impfstoff in dieser Gruppe wirkt“, es werde jedoch ein Schutz erwartet – basierend auf Erfahrungen mit anderen Impfstoffen und da in dieser Altersgruppe eine Immunantwort beobachtet wurde. Und weiter: „Da es zuverlässige Informationen zur Sicherheit in dieser Altersgruppe gibt, sind die wissenschaftlichen Experten der EMA der Ansicht, dass der Impfstoff bei älteren Erwachsenen eingesetzt werden kann.“ Weitere Informationen würden von laufenden Studien erwartet, die einen höheren Anteil älterer Teilnehmer:innen einschlössen.





















2 Kommentare
schlampige Studie?
von Kiwi am 02.02.2021 um 8:34 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Geschlechterneutralität in der Impfstofforschung
von Corona Virus am 02.02.2021 um 8:26 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.