
- DAZ.online
- News
- Apotheke
- Ist der Großhandel die ...
Arzneimittelsicherheit
Ist der Großhandel die Sicherheitslücke bei Securpharm?
Berlin - 11.09.2018, 07:00 Uhr

Während Hersteller und Apotheker jede einzelne Packung im Securpharm-System ein- und ausbuchen müssen, müssen Großhändler nur bestimmte Arzneimittel kontrollieren. Ist das eine Sicherheitslücke? ( j/ Foto: Imago)
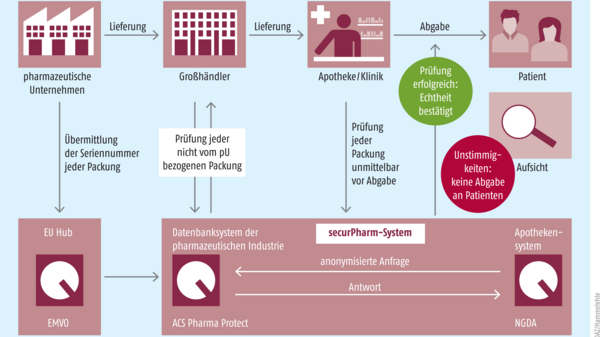
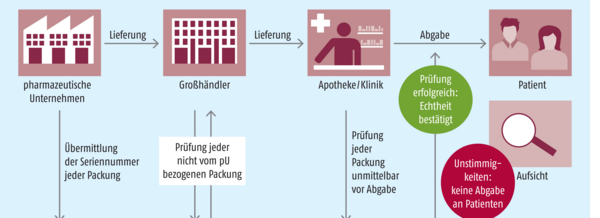
Wenn im Februar 2019 Securpharm startet, sollen gefälschte Arzneimittel hierzulande bestenfalls gar nicht mehr auftauchen. Das Securpharm-Prinzip ist einfach: Der Hersteller bucht eine Packung ins System ein, der Apotheker bucht dieselbe Packung bei der Abgabe wieder aus. So soll die Lieferkette transparenter werden. Der Großhandel hingegen muss nicht jede einzelne Packung ein- und ausbuchen. Kann man also von einer Sicherheitslücke sprechen? Die Großhändler selbst meinen, dass Skandale wie die Lunapharm-Affäre trotzdem verhindert werden könnten. Einige Apotheker scheinen das anders zu sehen, die ABDA spricht von einem „risikobasierten Ansatz“.
Gerade mit Blick auf die derzeitige Lunapharm-Affäre wird deutlich: Oft mangelt es an Transparenz in der Arzneimittel-Lieferkette. Medienberichte, erste Ergebnisse staatsanwaltschaftlicher Ermittlungen sowie der Bericht der Lunapharm-Taskforce lassen alle nur ein Bild zu: In Europa gibt es ein hochkomplexes Netzwerk aus Arzneimittelhändlern, die teils mit gestohlener Klinikware handeln und Medikamente von einem Land ins nächste verkaufen, sodass der genaue Lieferweg der Präparate bei der letzten Station in der Lieferkette oftmals nicht mehr nachvollziehbar ist.
Mit Securpharm, das aus der EU-Arzneimittelfälschungsrichtlinie entspringt, soll die Lieferkette nun transparenter werden. Das System soll die Echtheitsprüfung von Arzneimitteln ermöglichen. Am 9. Februar 2019 wird der Startschuss fallen. Dann muss jedes verifizierungspflichtige Arzneimittel (das ist grundsätzlich jedes verschreibungspflichtige) in jeder Apotheke eines EU-Mitgliedstaates sowie den EWR-Staaten auf seine Echtheit überprüft werden, ehe es an den Patienten abgegeben wird. Konkret muss der Hersteller jede Arzneimittelpackung vor der Abgabe ins Sicherheitssystem einbuchen. Bei der Abgabe in der Apotheke müssen dann zwei Sicherheitsmerkmale überprüft werden: das individuelle Erkennungsmerkmal in Form eines Data-Matrix-Codes und der Erstöffnungsschutz, der eine Vorrichtung gegen Manipulationen darstellt. Wenn beides in Ordnung ist, bucht der Apotheker die Packung per Scan aus dem System aus – das Arzneimittel gilt als sicher abgegeben.
Hersteller und Apotheker müssen alle Packungen scannen
Während Hersteller und Apotheker jede einzelne Packung ein- beziehungsweise ausbuchen und kontrollieren müssen, ist das beim Großhandel nicht der Fall. Auch die Großhändler waren am Aufbau von Securpharm natürlich maßgeblich beteiligt – jeder Großhändler musste seine Lager mit der neuen Technik ausrüsten, um Packungen zu scannen und sie somit ein- und auszubuchen. Allerdings gilt die Scan-Pflicht nur für bestimmte Arzneimittel. Was die Großhändler überprüfen müssen, ist in der Delegierten Verordnung klar geregelt. Sie müssen Arzneimittel überprüfen, …
- … die von Apotheken oder einem anderen pharmazeutischen Großhändler zurückgegeben werden oder
- … die sie von einem anderen pharmazeutischen Großhändler erhalten, bei dem es sich weder um den Hersteller noch um den Zulassungsinhaber oder Mitvertreiber des jeweiligen Arzneimittels handelt.
Heißt konkret: Alle Arzneimittel, die der Großhändler direkt vom Hersteller bezieht, müssen nicht kontrolliert werden. Der Großhandelsverband Phagro ergänzt, in welchem Fall die Grossisten ebenfalls nicht überprüfen müssen: „Dies gilt im Übrigen auch dann, wenn der pharmazeutische Unternehmer einen anderen Großhändler als Pre-Wholesaler dazwischen schaltet und diesen schriftlich beauftragt, seine Arzneimittel in seinem Namen zu lagern und zu vertreiben. Diesem Ansatz liegt der Gedanke zugrunde, dass der Hersteller nicht selbst gefälschte Arzneimittel herstellen und in den Verkehr bringen wird.“ Umgekehrt gilt die Scan-Pflicht im Großhandel beispielsweise für alle Arzneimittel, die außerhalb der EU vertrieben werden sollen oder die – etwa wegen eines Rückrufes – zurück an den Großhändler gehen.
Phagro: Track-and-Trace ohne Patientenmehrwert
Nicht alle Systembeteiligten sind mit dieser Lösung zufrieden: Hört man sich unter Apothekern um, wird des Öfteren hinterfragt, warum auf die Apotheker mehr Pflichten zukommen als auf Großhändler. Apotheker Gunnar Müller aus Nordrhein-Westfalen nahm dies kürzlich zum Anlass und schrieb einen Brief an Bundesgesundheitsminister Jens Spahn (CDU), in dem er ihn aufforderte, dass auch der Großhandel unter Securpharm alle Packungen kontrollieren solle. In seinem Brief erläutert Müller: „Nur so kann das Auftreten von einer Packung an zwei Orten (z.B. auch bei unentdecktem Diebstahl) wirksam erfasst werden.“
Ferner wies er darauf hin, wie hoch der Mehraufwand in den Apotheken durch Securpharm ist – ohne dass die Kassen die Pharmazeuten dafür vergüten: Jährlich müssen mehr als 900 Millionen Packungen in der Apotheke überprüft werden, die Apotheker müssen in höhere System- und Softwaregebühren investieren und haben einmalige Kosten durch die Einrichtung der Scanner.
Phagro: Lunapharm hätte Fälschungen entdecken müssen
Der Großhandelsverband Phagro verteidigt die Securpharm-Konstruktion und weist darauf hin, dass es sich bei Securpharm nicht um eine „Track-and-Trace-Lösung“ handelt, sondern um eine „End-to-End-Überprüfung“. Zur Erklärung: „Track-and-Trace-Kontrollen“ werden beispielsweise von Paketdienstleistern angeboten. Hier können Kunden nach Eingabe eines Verifizierungscodes jederzeit einsehen, wo sich ihr Paket gerade befindet. Der Phagro erklärte gegenüber DAZ.online aber, dass „Track-and-Trace“ „keinen Mehrwert für den Patientenschutz“ habe.
Bezogen auf die Lunapharm-Affäre
erklärt der Phagro jedoch, dass das Brandenburger Unternehmen als
pharmazeutischer Großhändler die aus Griechenland bezogenen Arzneimittel in
jedem Fall hätte überprüfen müssen, „da kein Erwerb über den pharmazeutischen Unternehmer erfolgte, sondern ein, zumindest
behaupteter, Bezug von einem vermeintlichen Großhandelserlaubnisinhaber“. Der
Phagro ist sich daher sicher: „Daher hätte Lunapharm die
Arzneimittelfälschungen entdecken müssen. (…) Der Fall Lunapharm zeigt, dass die
Einführung von Securpharm sinnvoll ist und funktionieren würde.“ Dieses Szenario setzt allerdings voraus, dass Lunapharm selbst rechtschaffen war und glaubte, die aus Griechenland bezogenen Arzneimittel seien „sauber“.
ABDA: Apotheker können Verträge mit Großhändlern abschließen
DAZ.online hat auch bei der ABDA angefragt. Im Vergleich zum Phagro sieht die Standesvertretung der Apotheker, die ebenfalls an der Einrichtung von Securpharm beteiligt ist, die Sachlage nüchterner. Auf die Frage, warum „nur“ eine „End-to-End-Überprüfung“ vorgesehen ist, erklärt ein ABDA-Sprecher: „Der ‚risikobasierte Ansatz‘, bei dem der pharmazeutische Großhandel nur stichprobenweise kontrolliert, insbesondere aber alle Packungen, die er nicht vom pharmazeutischen Unternehmer bezieht, ist im Delegierten Rechtsakt vorgegeben. Er ist auch Ausfluss eines bewussten Verzichtes auf das sogenannte ‚Track and Trace‘, den alle deutschen Stakeholder unterstützt haben.“
Die ABDA betont, dass dem Apotheker in diesem System eine wichtige Rolle zukomme. Er sei die „letzte Schutzinstanz“ in diesem System. Was den Lunapharm-Fall betrifft, hat die ABDA – ebenfalls im Gegensatz zum Phagro – offenbar wenig Hoffnungen, dass eine lückenlose Kontrolle aller Packungen den Skandal hätte verhindern können. Denn: „Sofern ein Großhändler bewusst gegen verschiedene Vorschriften verstößt, scheint es optimistisch anzunehmen, dass die Verpflichtung zur Arzneimittelverifikation ein solches Verhalten würde wirklich ‚heilen‘ können. Schließlich gibt der ABDA-Sprecher den Apothekern noch einen Tipp mit auf den Weg: „Es bleibt dem einzelnen Apotheker unbenommen, in seinen vertraglichen Regelungen mit den ihn beliefernden Großhandlungen weitergehende Überprüfungen (Verifikationen) des Lieferanten freiwillig zu vereinbaren.“
BMG: Lunapharm hätte als Importeur prüfen müssen
Auch dem Bundesgesundheitsministerium hat DAZ.online Fragen zu eventuellen Sicherheitslücken bei Securpharm gestellt. Ein Ministeriumssprecher verwies jedoch lediglich auf die Funktionsweise des „End-to-End“-Systems und fügte hinzu: „Das ‚End-to-end‘- System wird seitens der Großhändler durch risikobasierte Überprüfungen ergänzt.“ Was den Lunapharm-Fall betrifft, pflichtet das BMG dem Phagro im Ergebnis bei: „In der vorliegenden Konstellation hat Lunapharm nicht als Großhändler, sondern als pharmazeutischer Unternehmer agiert. (…) Zukünftig hat ein Hersteller parallel eingeführter oder parallel vertriebener Arzneimittel, der die Sicherheitsmerkmale vollständig oder teilweise entfernt oder überdeckt, die Echtheit des individuellen Erkennungsmerkmals zu überprüfen und dieses im Falle einer Ersetzung zu deaktivieren.“
Auch wenn einiges dafür spricht, dass die gestohlenen Arzneimittel bei Lunapharm unter Securpham-Bedingungen hätten entdeckt werden müssen – bis auch Griechenland und Italien die neuen Vorgaben zum EU-Fälschungsschutz implementiert haben müssen, wird noch einige Zeit ins Land gehen. Ausgerechnet diese beiden Länder haben eine um sechs Jahre längere Übergangsfrist für die Umsetzung. Hier können Firmen wie Lunapharm also noch bis Februar 2025 unserialisierte Arzneimittel kaufen, die sie dann ab kommendem Februar lediglich selbst serialisieren müssten.






























7 Kommentare
Sicher ?
von Michael Kuenen am 11.09.2018 um 9:00 Uhr
» Auf diesen Kommentar antworten | 3 Antworten
AW: Re: Sicher
von Christian Becker am 11.09.2018 um 9:44 Uhr
AW: Sicher
von Andreas Kronsbein am 11.09.2018 um 9:56 Uhr
AW: Sicher
von Kiwei am 11.09.2018 um 12:16 Uhr
Passt die Lösung zum Problem?
von Holger am 11.09.2018 um 8:39 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
überflüssig
von Karl Friedrich Müller am 11.09.2018 um 8:07 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: überflüssig an falscher Stelle
von Dr Schweikert-Wehner am 11.09.2018 um 15:01 Uhr
Das Kommentieren ist aktuell nicht möglich.