
- DAZ.online
- News
- Apotheke
- BfArM informiert zu ...
Europaweite Rückrufe
BfArM informiert zu Valsartan
Berlin - 06.07.2018, 11:45 Uhr
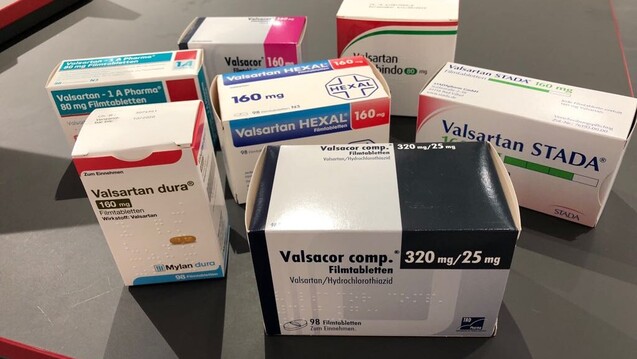
Während immer mehr Hersteller die vom BfArM angekündigten Valsartan-Rückrufe umsetzen, bleiben Fragen zu den Hintergründen noch unbeantwortet. Das BfArM informiert so weit wie möglich. (m / Foto: privat)
Der chargenbezogene Rückruf valsartanhaltiger Arzneimittel,
deren Wirkstoff von dem chinesischen Hersteller Zhejiang Huahai Pharmaceutical
produziert wurde, sorgt derzeit für Verunsicherung. Das Bundesinstitut für Arzneimittel
und Medizinprodukte hat nun einige
wichtige Fragen und Antworten zum Thema auf seiner Webseite zusammengestellt. Mit Basics hat indessen das siebte Unternehmen einen Rückruf angeordnet.
Sieben Hersteller – Dexcel, Heumann, Hormosan, Hexal, Zentiva, Aliud und Basics – haben bereits den vorsorglichen Rückruf aller oder bestimmter Chargen valsartanhaltiger Arzneimittel erklärt. Einige Hersteller gaben auch schon Entwarnung: Darunter Marktführer TAD, sowie Mylan und Novartis.
Weitere pharmazeutische Unternehmen sind noch dabei zu ermitteln, welche ihrer Chargen betroffen sind. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) geht davon aus, dass dieses Verfahren kurzfristig abgeschlossen werden kann.
Die Webseite der Arzneimittelkommission
der Deutschen Apotheker (AMK) mit den neuesten Rückrufen ist derzeit kaum bis gar nicht erreichbar. DAZ.online hält Sie jedoch auf dem neuesten Stand der Rückrufe.
Mehr zum Thema
Valsartan-Rückrufe
Hexal ruft zurück, TAD Pharma nicht betroffen
Verunreinigungen
Valsartan-Rückrufe starten – einige Rabattverträge betroffen
Die umfassenden Rückrufe sorgen für Unruhe und werfen viele Fragen auf. Einige dieser Fragen und Antworten hierauf hat das BfArM jetzt auf seiner Webseite veröffentlicht.
Eine der Fragen lautet beispielsweise: Wie sollen sich Patientinnen und Patienten verhalten, die valsartanhaltige Arzneimittel einnehmen?
Die Antwort des BfArM: Patientinnen und Patienten, die valsartanhaltige Arzneimittel einnehmen, sollen die Arzneimittel nicht ohne Rücksprache mit ihrer Ärztin oder ihrem Arzt absetzen, da das gesundheitliche Risiko eines Absetzens um ein Vielfaches höher liegt als das mögliche Risiko durch eine Verunreinigung. Ein akutes Patientenrisiko besteht nicht.
Das BfArM verspricht: Sobald weitere Erkenntnisse vorliegen, werde es unverzüglich darüber informieren und den Sachstand entsprechend ergänzen.
Basics-Rückruf
Indessen hat auch Basics als siebter Hersteller sein Kombi-Präparat zurückgerufen. Es handelt sich um folgende Chargen:
- Valsartan comp Basics 80 mg/12,5 mg, 28, 56 und 98 Filmtabletten, Ch.-B.: 2747047, 2779990, 2809127, 2881210, 2881210A, 2881210B
- Valsartan comp Basics 160 mg/12,5 mg, 28, 56 und 98 Filmtabletten, Ch.-B.: 2751697, 2768857, 2788251, 2839490, 2839490A, 2839490B, 2892567, 2907521
- Valsartan comp Basics
160 mg/25 mg, 28, 56 und 98
Filmtabletten, Ch.-B.:
2747039, 2839503, 2839507, 2839509, 2839509A, 2839509
(PZN 08472000, 08472052, 07762115, 08472135, 08472589, 07762121, 08472075, 08472081 und 07762138)
Im ursprünglichen Artikel wurde fälschlicher Weise die Formulierung „sein Mono- und sein Kombi-Präparat zurückgerufen“ verwendet. Basics ruft aber, wie aus der Auflistung hervorgeht, nur seine Kombi-Präparate zurück. Die Formulierung wurde am 16.07.2018 angepasst.





















1 Kommentar
Valsartan ratiopharm 160mg . CH.B.T17379T
von Klaus Gabata am 09.07.2018 um 16:20 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Das Kommentieren ist aktuell nicht möglich.