
- DAZ.online
- News
- Wirtschaft
- Generika und Biosimilars ...
Vorschlag der EU-Kommission
Generika und Biosimilars trotz Schutzzertifikat
Berlin - 29.05.2018, 11:00 Uhr
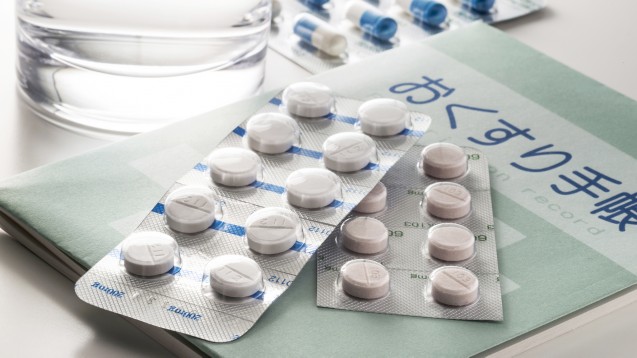
Vorschlag der EU-Kommission: Firmen sollen trotz bestehendem Schutzzertifikat Generika fürs nicht EU-Ausland produzieren dürfen. (Foto: studiopure / stock.adobe.com)
Die EU-Kommission will die Vorschriften zum geistigen Eigentum im Pharmabereich nachbessern. Sie hat einen Vorschlag vorgelegt, der es Unternehmen mit Sitz in der EU erlauben soll, bereits dann Generika oder Biosimilars herzustellen, wenn für das Original noch das ergänzende Schutzzertifikat gilt – allerdings nur für den nicht-europäischen Markt, in dem der Schutz nicht besteht.
Ergänzende Schutzzertifikate (SPC) verlängern den Patentschutz für Arzneimittel. Hintergrund für diesen besonderen Eigentumsschutz ist, dass die Patentlaufzeit, die regulär 20 Jahre beträgt, bei Arzneimitteln infolge der langen Entwicklungszeit um mehrere Jahre verkürzt ist. Daher kann der Hersteller bis zu fünf Jahre längeren Schutz beantragen – das SPC. Regelungen hierzu hat der europäische Gesetzgeber in der EU-Verordnung über das ergänzende Schutzzertifikat für Arzneimittel getroffen. Danach wirken SPC derzeit wie ein Patent: Sowohl die Vermarktung als auch die Herstellung von „Nachahmern“ ist in dieser Zeit verboten – ausgenommen ist nur die Herstellung zu Forschungszwecken. Auch eine Vorratsherstellung für den Tag des Ablaufs des Schutzzertifikats ist nicht möglich.
Mehr zum Thema
Schlappe für Gilead
Bundespatentgericht: Truvada-Schutzzertifikat ist nichtig

Absprachen über verzögerte Citalopram-Generika
Gericht bestätigt Millionen-Geldbußen
Diese Verordnung soll nun nach dem Willen der EU-Kommission eine Ausnahmeregelung bekommen: Unternehmen mit Sitz in der EU soll während der Geltungsdauer des Zertifikats erlaubt werden, eine generische oder biosimilare Version eines SPC-geschützten Arzneimittels herzustellen. Einen entsprechenden Vorschlag hat die Kommission am gestrigen Montag vorgelegt. Ausdrücklich will sie dabei die Schutzrechte des geistigen Eigentums sichern. Denn die Produktion darf ausschließlich für die Ausfuhr in ein Nicht-EU-Land geschehen, in dem der Schutz abgelaufen ist oder nie existiert hat. Dies wird als „manufacturing waiver“ bezeichnet.
Was bedeutet das für die Marktexklusivität in der EU?
„Durch die Ausnahmeregelung wird Europas Vorreiterrolle bei der pharmazeutischen Forschung und Entwicklung unterstützt“, heißt es in der Mitteilung der Kommission. Dank ihr wären die geistigen Eigentumsrechtebei der Herstellung von Arzneimitteln in Europa auch künftig weltweit am besten geschützt. Jyrki Katainen, der für Arbeitsplätze, Wachstum, Investitionen und Wettbewerbsfähigkeit zuständige Vizepräsident der Kommission, betonte: „Wir bekennen uns zu den grundlegenden Rechten und zur Dauer dieses Schutzes. Hier wird es auch künftig keine Änderungen geben“. SPC-geschützte Arzneimittel behielten ihre volle Marktexklusivität in der EU. Ganz so schnell dürften die Änderungen allerdings nicht in Kraft treten: Der Vorschlag muss nun noch durch das Europäische Parlament und auch der Europäische Rat muss darüber befinden.
Beim VfA kommt der Vorschlag nicht gut an, bei Pro Generika schon
Beim Verband forschender Pharmaunternehmen (vfa) kommt der Vorstoß nicht gut an. Hier sieht man keinen Grund, an den bestehenden Regelungen etwas zu ändern, erklärte ein Sprecher gegenüber DAZ.online. Beim Branchenverband Pro Generika ist die Stimmung besser: „Das ist ein erstes, wichtiges und vor allem überfälliges Signal“, sagt Geschäftsführer Bork Bretthauer „Das kann dazu führen, dass der Produktionsstandort Deutschland gestärkt wird und mehr Generika nach deutschen Sozial- und Umweltstandards produziert werden.“
Allerdings hätte man sich hier mehr gewünscht – nämlich die Möglichkeit, auch diejenigen Medikamente hierzulande herzustellen zu können, die am Tag nach Ablauf aller Schutzrechte für die Versorgung in Deutschland benötigt werden. Dies war im Vorfeld des Kommissionsvorschlags diskutiert, aber letztlich nicht umgesetzt worden. Bretthauer: „Anderenfalls würde ein nahezu absurder Zustand geschaffen: In Deutschland dürften dann zwar Arzneimittel hergestellt werden, die in den Export gehen. Arzneimittel aber, die nach Ablauf aller Schutzfristen in deutschen Apotheken abgegeben werden, müssten weiterhin im Ausland hergestellt werden. Das kann ernsthaft keiner wollen. Daher erwarten wir, dass die Bundesregierung auch diesen Vorschlag unterstützt.“





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.