
- DAZ.online
- DAZ / AZ
- DAZ 9/2023
- Lichtblicke beim ...
Schwerpunkt Lungenkrebs
Lichtblicke beim Lungenkarzinom
Neue Therapiemöglichkeiten verbessern die Prognose
In Deutschland erkranken jedes Jahr rund 57.000 Menschen an Lungenkrebs. Bei Männern ist das Lungenkarzinom mit rund 35.000 Fällen der zweithäufigste Tumor nach Prostatakrebs. Bei Frauen ist das Bronchialkarzinom nach Brustkrebs und Darmkrebs die dritthäufigste Krebsart mit rund 22.000 Erkrankten. Das mediane Erkrankungsalter liegt zwischen 68 und 70 Jahren; nur rund 2% der Betroffenen erkranken vor dem 50. Lebensjahr. Bei Männern ist Lungenkrebs mit rund 28.000 Verstorbenen pro Jahr die häufigste, bei Frauen mit etwa 16.500 Sterbefällen die zweithäufigste Krebs-Todesursache. Absolut betrachtet gibt es immer mehr Betroffene mit Lungenkrebs. Das liegt vor allem daran, dass mehr Menschen ein höheres Alter erreichen, in dem eine Krebserkrankung wahrscheinlicher wird. Nimmt man den Faktor „Alter“ heraus, ergibt sich ein anderes Bild: Die Zahl der erkrankten Männer nimmt seit einigen Jahren leicht ab, die der Frauen nimmt zu, was vornehmlich dem veränderten Rauchverhalten geschuldet ist [1].
Histologie
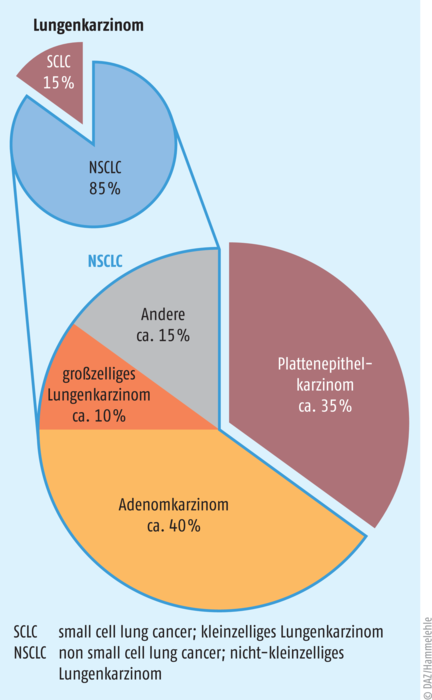
Lungenkarzinome sind primär in der Lunge entstandene, epitheliale Malignome. Sie werden in zwei große Gruppen unterteilt: In das kleinzellige (small cell lung cancer, SCLC) und das nicht-kleinzellige Lungenkarzinom (non small cell lung cancer, NSCLC). Das kleinzellige Karzinom macht rund 15% der Bronchialkarzinome aus, das nicht-kleinzellige rund 80 bis 85% (s. Abb. 1). Histologisch betrachtet gehören zu den nicht-kleinzelligen Lungenkarzinomen vor allem Adenokarzinome und Plattenepithelkarzinome sowie das großzellige/undifferenzierte Lungenkarzinom. Das kleinzellige Lungenkarzinom ist histologisch den neuroendokrinen Tumoren zuzuordnen.
Abb. 1: Histologische Einteilung der Lungenkarzinome SCLC = small cell lung cancer; kleinzelliges Lungenkarzinom NSCLC = non small cell lung cancer; nicht-kleinzelliges Lungenkarzinom, GZLK = großzelliges Lungenkarzinom
Bei Lungenkarzinomen gibt es deutliche Unterschiede in der Verteilung der Tumorstadien und in den Überlebensraten. Bei Erstdiagnose eines nicht-kleinzelligen Lungenkarzinoms liegen bei rund der Hälfte der Betroffenen bereits Fernmetastasen vor; frühe Krankheitsstadien werden lediglich bei 27% der Patienten diagnostiziert. Das SCLC zeichnet sich durch eine frühe Lymphknoten- und Fernmetastasierung aus, und nur 5% der kleinzelligen Tumore werden in Anfangsstadien erkannt. Dies spiegelt sich auch in den relativen Fünf-Jahres-Überlebensraten von unter 10% beim kleinzelligen und von rund 21% (Frauen) bzw. 15% (Männer) beim nicht-kleinzelligen Lungenkarzinom wider. Aufgrund der unterschiedlichen Malignität der Subtumorarten und des Tumorstadiums ist die Wahrscheinlichkeit einer Heilung eher für Patienten mit nicht-kleinzelligem Lungenkarzinom in frühen und teilweise in fortgeschrittenen Stadien gegeben, weniger für die Mehrzahl der Patienten im Stadium IIIB/C und IV [2]. Die Stadieneinteilung des Bronchialkarzinoms geht von der TNM-Klassifikation aus, wobei T die Tumorgröße, N die Anzahl betroffener Lymphknoten und M das Auftreten von Metastasen beschreibt. Im Stadium I ist der Tumor örtlich begrenzt, und es liegen weder Fernmetastasen noch befallene Lymphknoten vor. Das Stadium IV hingegen ist durch Fernmetastasen und Lymphknotenbefall charakterisiert.
Lernziele
In diesem Beitrag lernen Sie unter anderem,
- wie Lungenkarzinome eingeteilt werden,
- mögliche Symptome eines Bronchialkarzinoms,
- Grundzüge der Behandlung eines Bronchialkarzinoms,
- wie das nicht-kleinzellige Lungenkarzinom therapiert wird,
- wie das kleinzellige Lungenkarzinom therapiert wird,
- welche neuen Sprunginnovationen es bei zielgerichteten Therapien bei Treibermutationen gibt,
- welche Möglichkeiten die Immuncheckpoint-Inhibitoren bieten und
- wie mit immunvermittelten Nebenwirkungen umgegangen wird.
Symptome und Screening
Es gibt noch keine geeignete Methode zur Früherkennung von Lungenkrebs für die gesamte Bevölkerung. Screening asymptomatischer Risikopersonen mittels einer Niedrigdosis-Computertomografie kann Lungenkarzinome in frühen Stadien erkennen und die Lungenkrebsmortalität bei Rauchern und in noch größerem Ausmaß bei Raucherinnen senken, ist aber in den deutschsprachigen Ländern bisher noch nicht als Früherkennungsprogramm implementiert.
Die klinische Symptomatik ist beim kleinzelligen und nicht-kleinzelligen Lungenkarzinom ähnlich. Im frühen Stadium ist Lungenkrebs oft asymptomatisch. Leitsymptome wie Husten und Dyspnoe können auch erst bei fortgeschrittener Erkrankung auftreten (s. Tab. 1). Eine Besonderheit des kleinzelligen Lungenkarzinoms ist das häufige Vorkommen paraneoplastischer Syndrome, die nicht lokal durch den Tumor oder Metastasen verursacht werden [2].
Ursache | Symptome |
|---|---|
lokal tumorbedingt |
|
metastasenbedingt |
|
Allgemeinsymptome |
|
Grundzüge der Therapie
Die wichtigsten Bausteine der Behandlung sind die chirurgische Entfernung des Tumors, Bestrahlung sowie systemische und supportive Therapien. Alle Elemente werden häufig in einem multimodalen Konzept zusammengefasst. Die Behandlung erfolgt stadienabhängig unter Berücksichtigung des Allgemeinzustandes, der lungenfunktionellen Reserve und Komorbiditäten. Welche Therapie gewählt wird, hängt von den Ergebnissen der pathologischen Untersuchungen und des Lymphknotenstatus ab. Vor einer systemischen medikamentösen Erstlinien-Therapie sollen behandlungsrelevante Mutationen erfasst werden. Die Berücksichtigung histologischer, immunologischer und genetischer Marker spielt eine entscheidende Rolle bei der Auswahl einer zielgerichteten Therapie.
Risikofaktoren
- Rauchen (vor allem beim kleinzelligen Lungenkarzinom), auch Passivrauchen
- ionisierende Strahlen (hohe Umwelt-Radonbelastung, Uran-Bergbau, medizinische Strahlenexposition)
- Feinstaub
- Dieselmotorabgase
- Asbest
- Quarzstäube
- chronische Infektionen
- genetische Faktoren: Personen mit einer positiven Lungenkrebs-Anamnese bei einem oder mehreren Verwandten ersten Grades haben ein erhöhtes Erkrankungsrisiko.
Durch die Einführung der systemischen molekular-gezielten Therapie, immunologisch wirksamen Checkpoint-Inhibitoren und der multimodalen, interdisziplinären Therapie können auch Patienten mit metastasierter Erkrankung Überlebenszeiten von über fünf Jahren erreichen. Die von Fachgesellschaften erarbeiteten Behandlungsalgorithmen sind sehr komplex und werden im Folgenden nur grob skizziert – detaillierte Ausführungen finden sich etwa in der aktualisierten Leitlinie zum Lungenkarzinom [2, 3, 4].
Das kleinzellige Lungenkarzinom (SCLC) ist aufgrund der hohen Zellteilungsrate und einer raschen Wachstumsprogredienz eine Erkrankung mit meist sehr ungünstiger Prognose. Der hohe Anteil sich teilender Tumorzellen führt zwar zu einer merklichen Sensibilität des Tumors gegenüber Chemo- und Strahlentherapien und einem raschen Therapieansprechen, indes hält die Remission aufgrund einer frühzeitigen Streuung und Ausbreitung maligner Zellen meist nur kurz an. Rund zwei Drittel aller Fälle werden erst in einem weit fortgeschrittenen Stadium erkannt, in dem in der Regel keine Heilung mehr wahrscheinlich ist. Die mediane Überlebenszeit beträgt neun bis zwölf Monate; die Zwei-Jahres-Überlebensrate liegt bei 5 bis 10%. Die Therapie konzentriert sich auf eine Symptomkontrolle, Verlängerung der Überlebenszeit und Verbesserung der Lebensqualität. Behandlungsstandard ist eine systemische, medikamentöse Therapie bzw. Immun-Chemotherapie, die bei Bedarf durch strahlentherapeutische Optionen ergänzt wird; Operationen spielen nur eine marginale Rolle.
Die Behandlung des nicht-kleinzelligen Lungenkarzinoms hängt vom Tumorstadium ab. In den Stadien I und II ist eine operative Entfernung des Tumors die Standardtherapie. Je nach Tumorstadium kann durch eine postoperative Chemotherapie oder in bestimmten Fällen auch mit einer zielgerichteten Therapie eine weitere Verbesserung der Heilungschancen und des rezidivfreien Überlebens erzielt werden. In den Stadien IIIA und IIIB kann das Lungenkarzinom unter günstigen Umständen ebenfalls operativ entfernt werden, häufig ist aber ein erweiterter Behandlungsplan nötig, der Chemotherapie, Strahlentherapie mit nachfolgender Immuntherapie und/oder Operation als Therapiemöglichkeiten einschließt. Bei dem am weitesten fortgeschrittenen Stadium IV mit Fernmetastasen erfolgt bei Tumoren ohne genetische Veränderungen meistens eine Immun- bzw. Chemo-Immuntherapie. Liegen genetische Veränderungen vor, was bei rund 40% der Patienten der Fall ist, ist eine zielgerichtete Therapie gegen bestimmte Treibermutationen angezeigt [2].
Treibermutationen
Veränderungen im Genom der Lungenkrebszelle, die dem malignen Wachstum der Krebszelle zugrunde liegen, werden zusammenfassend Treibermutationen genannt. Dabei kann es sich um Mutationen im engeren Sinn (Austausch der DNA-Bausteine im Genom der Krebszelle), aber auch um den Verlust von Genabschnitten (Deletion), um Genbrüche, die zu einer Verschmelzung mit neuen Genabschnitten führen (Fusionen, Translokationen) oder um Vervielfältigungen von Genen oder Genabschnitten (Amplifikationen) handeln. Findet sich keine Mutation bei der molekularen Diagnostik in einem der untersuchten Gene, wird der Befund als Wildtyp bezeichnet.
Sprunginnovation: Zielgerichtete Therapien bei Treibermutationen
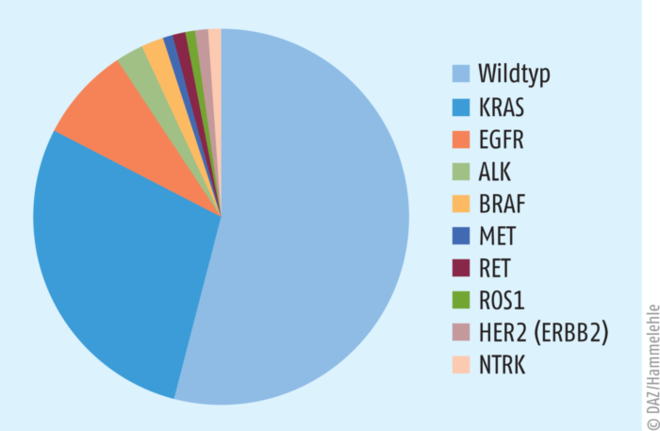
Die Behandlungserfolge bei Lungenkarzinomen erlebten in den vergangenen fünf Jahren einen deutlichen Schub nach vorne, was den zielgerichteten und immunonkologischen Therapien zu verdanken ist. Lag 2002 das mediane Überleben bei rund acht Monaten, stieg es unter einer Immuntherapie auf 26 Monate, unter einer personalisierten Therapie bei ausgewählten Gruppen auf 90 Monate an [5]. Wie kam dieser Fortschritt zustande? Um 2000 wurden die ersten Treibermutationen beim nicht-kleinzelligen Lungenkarzinom entdeckt, in den folgenden Jahren kamen weitere dazu. Da auch zielgerichtete Wirkstoffe gegen diese Treibermutationen entwickelt werden konnten, war erstmals eine stratifizierte Behandlung möglich. Die ersten Vertreter waren Erlotinib und Gefitinib (Zulassung 2009) bei EGFR-Mutationen. Derzeit können beim NSCLC zielgerichtete Wirkstoffe gegen mehrere Treibermutationen eingesetzt werden (s. Abb. 2). Da rund 40 bis 50% aller Patienten mit einem metastasierten NSCLC eine Treibermutation aufweisen, ist der Erfolg einer stratifizierten Therapie groß und das nicht-kleinzellige Lungenkarzinom gilt als eine Modellerkrankung für den Einsatz zielgerichteter Wirkstoffe [6, 7]. Treibermutationen treten am häufigsten beim Adenokarzinom, seltener beim Plattenepithelkarzinom auf. Die bei Treibermutationen eingesetzten Wirkstoffe sind meist oral einzunehmende Tyrosinkinase-Inhibitoren (s. Tab. 2).
Mutation | Charakteristik | Wirkstoffe (Beispiele) |
|---|---|---|
Wildtyp | keine genetischen Veränderungen | keine zielgerichtete Therapie möglich |
KRAS-Mutationen |
| Sotorasib |
EGFR-Mutationen (zumeist Exon-19-Deletionen, L858R-Mutation) | gehäuft bei Frauen und Nierauchern mit Adenokarzinom | Erlotinib, Gefitinib, Afatinib, Osimertinib |
ALK-Translokationen | fast ausschließlich bei Adenokarzinomen, gehäuft bei jüngeren Patienten und Nierauchern | Crizotinib, Alectinib, Brigatinib, Lorlatinib, Ceritinib, Ensartinib |
BRAF-Mutationen (BRAF V600-Mutationen) | fast ausnahmslos bei Adenokarzinomen | Dabrafenib |
MET-Mutation | meist Adenokarzinome | Tepotinib |
RET-Translokationen | bei Adenokarzinomen und gehäuft, aber nicht ausschließlich, bei Nierauchern | Selpercatinib, Pralsetinib |
ROS1-Translokationen | bei Adenokarzinomen, gehäuft bei jüngeren Patienten und Nierauchern | Crizotinib (kombinierter ALK-, ROS1-, c-MET-Inhibitor), Entrectinib (kombinierter ALK-, ROS1-, Tropomyosin-Rezeptorkinase[TRK]-Inhibitor |
HER2-Amplifikationen und Mutationen | vor allem bei Adenokarzinomen | Trastuzumab, Trastuzumab / Pertuzumab, Antikörperkonjugate mit Trastuzumab (teilweise off-label), spezifische Inhibitoren in der klinischen Prüfung |
NTRK-Mutationen | selten | Larotrectinib (kombinierter TRK-, ALK- und ROS1-Inhibitor) |
Eine molekularbasierte zielgerichtete Behandlung ist beim kleinzelligen Lungenkarzinom derzeit nicht möglich. Man weiß zwar, dass auch das kleinzellige Lungenkarzinom aus stratifizierbaren Untergruppen besteht, die durch molekulare Veränderungen charakterisiert sind, bislang ist indes nur eine Treibermutation (Translokation des Gens für den FGFR 1) beschrieben, für die es derzeit keine zugelassene Therapiemöglichkeit gibt [8].
Nicht für alle diese genetischen Aberrationen ist eine zielgerichtete Therapie bereits in der Erstlinie zugelassen. Auch gilt bislang die Zulassung nur für das fortgeschrittene Krankheitsstadium; mit Zulassungen zur Behandlung im frühen/kurativen Stadium ist zu rechnen. Eine molekulare Testung vor Beginn der Erstlinien-Therapie ist Voraussetzung.
Abb. 2: Treibermutationen beim nicht-kleinzelligen Lungenkarzinom (nach Informationen des nationalen Netzwerks Genomische Medizin [nNGM] Lungenkrebs, https://nngm.de/)
Sprunginnovation: Immuntherapie
Lange Zeit waren sämtliche Versuche, die körpereigene Immunantwort gegen Tumorzellen für eine wirksame Lungenkrebstherapie zu nutzen, erfolglos. Erst mit der Einführung der Immuncheckpoint-Inhibitoren ergaben sich für die Therapie des kleinzelligen und des nicht-kleinzelligen Lungenkarzinoms neue, wirksame Therapieansätze (s. Tab. 3).
Wirkstoff | Target | Handelsname |
|---|---|---|
Atezolizumab | PD-L1 | Tecentriq® |
Cemiplimab | PD-1 | Libtayo® |
Durvalumab | PD-L1 | Imfinzi® |
Ipilimumab | CTLA-4 | Yervoy® |
Nivolumab | PD-1 | Opdivo® |
Pembrolizumab | PD-1 | Keytruda® |
Die Immuntherapie wird beim nicht-kleinzelligen Lungenkarzinom im metastasierten Stadium eingesetzt, wenn keine therapierbaren Treibermutationen vorliegen. Bildet mindestens die Hälfte der Tumorzellen den Programmed Death-Ligand 1 PD-L1 (PD-L1 > 50%), wird in der Ersttherapie eine Immuntherapie mit einem Checkpoint-Inhibitor angeboten, bei geringer PD-L1-Expression in Kombination mit einem Zytostatikum als Immun-Chemotherapie. Teilweise wird die Immuntherapie bereits im adjuvanten Stadium eingesetzt, so etwa Atezolizumab beim nicht-kleinzelligen Lungenkarzinom [9, 10].
Beim kleinzelligen Lungenkarzinom konnte dank einer kombinierten Chemo-Immuntherapie erstmals ein jahrzehntelanger therapeutischer Stillstand überwunden und das Gesamtüberleben um rund 30% verlängert werden. Die Kombination aus einem Platin-Derivat (Cisplatin oder Carboplatin) mit Etoposid und einem PD-L1-Inhibitor (Atezolizumab oder Durvalumab) ist seitdem Standard in der Erstlinien-Therapie des kleinzelligen Lungenkarzinoms im fortgeschrittenen Stadium [10, 11].
Warnsymptome
Tritt unter einer Therapie mit Immunonkologika eines dieser Symptome auf, sollte dringend der Arzt konsultiert werden:
- Fieber: > 38 °C
- Lunge: Atemnot, erschwertes Atmen oder Schmerzen beim Atmen
- Blase: Blasenkrämpfe, Schmerzen beim Wasserlassen oder Blut im Urin
- Nerven: Lähmungserscheinungen, Krampfanfälle oder akute Schmerzen
- Magen-Darm-Trakt: Durchfall (> sechsmal / Tag oder schwere Krämpfe), Blut im Stuhl, Erbrechen (> fünfmal / Tag)
- Haut: Gelbsucht
Therapieerfolg nicht sicher vorhersehbar
Ein Therapieerfolg für den einzelnen Patienten lässt sich derzeit nicht sicher vorhersagen. Faktoren wie eine hohe Tumorlast, rasch progredientes Tumorwachstum sowie schlechter Allgemeinzustand weisen eher auf ein schwaches Therapieansprechen hin. Zudem geht man davon aus, dass Checkpoint-Inhibitoren ausreichend Zeit brauchen, um ihre Wirksamkeit entfalten zu können. Eine Immuntherapie kann anfänglich auch das Tumorvolumen vergrößern. Durch das Einwandern von Immunzellen in die Tumorregion kann in bildgebenden Verfahren eine Vergrößerung beobachtet werden, die jedoch nicht Ausdruck einer echten Tumorprogression ist. Um zu vermeiden, dass das Phänomen einer sogenannten Pseudoprogression zum vorzeitigen Therapieabbruch führt, wurden spezifische Bewertungskriterien entwickelt. Diese Immune-related-RECIST-Kriterien (iRECIST) ermöglichen die Beurteilung eines Therapieerfolgs trotz anfänglicher Tumorvergrößerung [12, 13, 14].
Pharmazeutische Dienstleistung
In Apotheken kann unter bestimmten Voraussetzungen die Beratung eines Patienten unter einer oralen Krebstherapie als pharmazeutische Dienstleistung angeboten werden. Lesen Sie dazu in dieser DAZ auf S. 54 den Beitrag Jungmayr P. „Lungenkrebspatienten in der Apotheke – Was bei der pharmazeutischen Beratung zu Oralia zu beachten ist.“
Immunvermittelte Nebenwirkungen
Die unter einer Immuntherapie auftretenden Nebenwirkungen unterscheiden sich von denjenigen unter einer Chemotherapie. Die Aufhebung der Blockade des Immunsystems kann zu zahlreichen Autoimmunreaktionen und unkontrollierten Immunreaktionen gegen körpereigenes Gewebe führen. Dies kann unter anderem zu Hautreaktionen, Diarrhö und Kolitis, Pneumonitis, Hepatitis, Myokarditis, Nephritis, muskuloskelettalen und endokrinen Funktionsstörungen (Schilddrüse, Nebennieren, Hypophyse, Pankreas), hämatologischen und okulären Nebenwirkungen sowie Auswirkungen auf das ZNS führen [15]. Diese immune-related adverse events (irAE) werden in verschiedene Schweregrade unterteilt, und Leitlinien [16] geben explizite Anweisungen, wie im Einzelfall zu verfahren ist und wann eine Behandlung unterbrochen oder vollständig abgesetzt werden muss.
Die autoimmunen Reaktionen treten mit unterschiedlicher Latenz auf und sind abhängig vom eingesetzten Wirkstoff. Effekte an Haut (Exanthem), Darm (Diarrhö) und Lunge (Pneumonitis) sind im Allgemeinen relativ früh zu beobachten (ein bis vier Monate), Nebenwirkungen auf die Schilddrüse nach etwa sechs Monaten, unerwünschte Effekte an Niere und Zentralnervensystem treten dagegen erst nach längerer Therapiedauer auf (über neun Monate). Zu beachten ist auch, dass gelegentlich autoimmune Reaktionen auch lange nach Absetzen der Immunonkologika manifest werden.
Pharmazeutische Dienstleistungen – So gelingt die Umsetzung in der Apotheke
Seit Juni 2022 werden fünf Pharmazeutische Dienstleistungen honoriert. Nun gilt es, diese flächendeckend in den Apotheken anzubieten. Mitarbeitermangel, hoher bürokratischer Aufwand und Unsicherheit bei der effizienten Etablierung sind Hemmnisse, über die Kollegen berichten, die noch nicht damit begonnen haben. Die pharmazeutischen Dienstleistungen aber bieten eine hervorragende Chance, sich heilberuflich zu positionieren. Diese sollte genutzt werden, um den Arbeitsplatz Apotheke für den Nachwuchs attraktiv zu machen und die Kunden an die Vorort-Apotheke zu binden. Wie kann die Motivation des gesamten Apothekenteams gelingen? Wie können Arbeitsabläufe optimiert werden, so dass die Dienstleistungen und ihre Abrechnung praxisgerecht umgesetzt werden können? Wie lassen sich Patienten dafür interessieren und wie wird der Nutzen der pDL patientengerecht kommuniziert? Am Freitag, den 5. Mai 2023, wird Dr. Katja Renner auf der Interpharm in Göttingen an Beispielen aus dem eigenen Apothekenalltag die Dienstleistungen erläutern.
Weitere Informationen zur Interpharm finden Sie auf www.interpharm.de
Aufklärung der Patienten
Patienten, die eine immunonkologische Therapie erhalten, müssen über mögliche Nebenwirkungen aufgeklärt und geschult sowie regelmäßig untersucht werden. Im Zentrum steht dabei die Evaluation spezifischer Symptome einer endokrinen Insuffizienz, Fragen nach Darmfunktion (Diarrhö), Übelkeit, Schwindel, Husten, Dyspnoe, Fieber, Pruritus. Die Inspektion der Haut ist obligat. Regelmäßig sollten Blutbild, Schilddrüsenwerte und Leberwerte kontrolliert werden [17]. |
Interessenkonflikte
Die Autorin versichert, dass keine Interessenkonflikte bestehen.
Literatur
[1] Krebs in Deutschland – Lungenkrebs. Krebs in Deutschland für 2017/2018, 13. Ausgabe, Robert Koch-Institut, Berlin 2021, www.krebsdaten.de/Krebs/DE/Content/Publikationen/Krebs_in_Deutschland/kid_2021/kid_2021_c33_c34_lunge.pdf?__blob=publicationFile
[2] Griesinger F, Absenger G, Bleckmann A et al. Lungenkarzinom, nicht-kleinzellig (NSCLC). Stand: November 2022, Deutsche Gesellschaft für Hämatologie und Medizinische Onkologie e. V., www.onkopedia.com/de/onkopedia/guidelines/lungenkarzinom-nicht-kleinzellig-nsclc/@@guideline/html/index.html
[3] Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms. Stand Dezember 2022, S3-Leitlinie, Leitlinienprogramm Onkologie, AWMF-Registernummer 020/007OL
[4] Ettinger DS et al. Non-Small Cell Lung Cancer, Version 3.2022, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw 2022;20(5):497-530, doi: 10.6004/jnccn.2022.0025, PMID: 35545176
[5] Griesinger F. Moderner Therapiealgorithmus Lungenkrebs. Vortrag gehalten am 15. November 2022 im Rahmen des 35. Deutschen Krebskongresses, Berlin, 13. bis 16. November 2022
[6] Reinmuth N. Molekular basierte Behandlungsstrategien beim NSCLC mit Treiberalterationen. Trillium 2022;3, www.trillium.de
[7] Tan AC et al. Targeted Therapies for Lung Cancer Patients With Oncogenic Driver Molecular Alterations. J Clin Oncol 2022;40(6):611-625, doi: 10.1200/JCO.21.01626, Epub 5. Januar 2022, PMID: 34985916
[8] Treibermutationen beim Lungenkrebs. Informationen des Netzwerk Genomische Medizin (NGM) Lungenkrebs, https://ngm-cancer.com/molekularpathologie/treibermutationen-beim-lungenkrebs/
[9] Reck M. Immuntherapeutische Strategien beim fortgeschrittenen nicht-plattenepithelialen NSCLC ohne therapierbare Treiberalterationen. Trillium 2022;3, www.trillium.de
[10] Frost N et al. Lung Cancer in Germany. J Thorac Oncol 2022;17(6):742-750, doi: 10.1016/j.jtho.2022.03.010, PMID: 35623674
[11] Hoffknecht P. Metastasiertes kleinzelliges Lungenkarzinom: neue Behandlungsoptionen und Perspektiven für die erste Behandlungslinie. Trillium 2022;3, www.trillium.de
[12] Persigehl T et al. iRECIST: how to do it. Cancer Imaging 202;20:2, https://doi.org/10.1186/s40644-019-0281-x
[13] Schneider H et al. Monitoring von Immuntherapien. Radiologe 202;60:711–720, https://doi.org/10.1007/s00117-020-00726-x
[14] Zander H et al. Checkpointinhibitoren in der Tumortherapie [Checkpoint inhibitors for cancer therapy]. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2020;63(11):1322-1330, doi: 10.1007/s00103-020-03221-9, Epub 1. Oktober 2020
[15] Braun GS et al. Nebenwirkungen neuer onkologischer Immuntherapien [Side effects of novel cancer immunotherapies]. Nephrologe 2020;15(3):191-204, doi: 10.1007/s11560-020-00424-8, Epub 29. April 2020
[16] Schneider BJ et al. Management of Immune-Related Adverse Events in Patients Treated With Immune Checkpoint Inhibitor Therapy: ASCO Guideline Update. J Clin Oncol 2021;39(36):4073-4126, doi: 10.1200/JCO.21.01440, Epub 1. November 2021, Erratum in: J Clin Oncol 2022;40(3):315, PMID: 34724392
[17] Thomssen C. Nebenwirkungsmanagement immunonkologischer Therapien – was gibt es zu beachten? Gynäkologe 2022;55:344–350, https://doi.org/10.1007/s00129-022-04941-6
Zum "Schwerpunkt Lungenkrebs" gehört neben diesem auch der Beitrag: "Lungenkrebspatienten in der Apotheke: Was bei der pharmazeutischen Beratung zu Oralia zu beachten ist.".























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.