
- DAZ.online
- DAZ / AZ
- DAZ 41/2023
- Gene per RNA ausschalten
Genetik
Gene per RNA ausschalten
Wie RNA-Interferenz funktioniert und wo sie eingesetzt wird
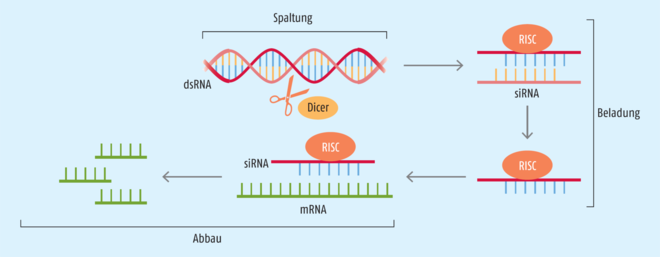
Um Gene stillzulegen gibt es verschiedene Möglichkeiten. Eine davon ist es, die Übersetzung der Messenger-RNA (mRNA) in ein Protein zu unterbinden. Das passiert bei der RNA-Interferenz. Natürlicherweise ist der Prozess der RNA-Interferenz z. B. wichtig, um Viren abzuwehren: Die exogene, virale RNA wird dadurch abgebaut, und die Replikation und Translation der fremden Erbinformation im Organismus wird unterbunden, sodass sich die Viren nicht vermehren können. Auch endogene RNA wird mittels RNA-Interferenz stillgelegt, um die Expression von Genen zu regulieren. Zur Erinnerung: Um Proteine zu synthetisieren, wird im Zellkern zunächst eine einzelsträngige RNA als Kopie eines Gen-Transkripts erstellt, das in der Desoxyribonukleinsäure (DNA) codiert ist (Transkription). Diese prä-mRNA wird zu einer reifen mRNA weiterverarbeitet und aus dem Zellkern ins Cytoplasma befördert. Dort findet an den Ribosomen die Übersetzung der mRNA in ein Protein statt (Translation). Die mRNA liegt dabei für die Translation einzelsträngig vor. Doppelsträngige RNA-Fragmente hingegen sind die Grundlage für den Prozess der RNA-Interferenz, der genutzt wird, um die Translation zu verhindern. Dabei sind doppelsträngige small interfering RNA- (siRNA) oder Micro-RNA-Moleküle (miRNA) entscheidend. Man differenziert diese beiden RNA-Fragmente unter anderem aufgrund ihrer Vorläufermoleküle: siRNA-Moleküle entstehen aus großen doppelsträngigen RNA-Strängen, die von außerhalb in die Zelle gelangen z. B. durch Viren; miRNA-Moleküle entstehen endogen aus Vorläufer-Ribonukleinsäure, für die genomische DNA codiert, z. B. um die Genregulation zu steuern. Wie der Prozess der RNA-Interferenz abläuft, zeigt Abbildung 1:
- Im ersten Schritt kürzt das Enzym Dicer lange doppelsträngige RNA zu den circa 23 Nukleotid-langen siRNA- bzw. miRNA-Fragmenten im Cytoplasma.
- Im zweiten Schritt binden die siRNA- oder miRNA-Moleküle an bestimmte Proteine im sogenannten RISC-Komplex (RNA-induced silencing complex). Dort spaltet die Endonuclease Argonaut 2 den RNA-Doppelstrang in Einzelstränge, von denen einer abgebaut wird und der Leitstrang im Komplex verbleibt.
- Die RNA-Sequenz im aktivierten RISC-Komplex kann nun spezifisch an komplementäre mRNA im Cytoplasma binden. In Folge werden die gebundenen Ziel-mRNA-Moleküle im RISC-Komplex abgebaut, und die Translation der mRNA in die entsprechenden Proteine ist unterbunden [1, 2].
Beladung: Die Fragmente interagieren mit dem RISC-Komplex (orange). Dort wird ein Strang (gelb) der RNA abgebaut, der Leitstrang (blau) verbleibt im Komplex.
Abbau: Der Leitstrang im RISC-Komplex bindet komplementäre mRNA-Moleküle (grün) im Cytoplamsa, die dann abgebaut werden. Die Translation der Proteine ist unterbunden.
siRNA: small interfering RNA, RISC: RNA-induced silencing complex (modifiziert nach [15])
Wie kommt die siRNA an den Wirkort?
SiRNA-Moleküle können nach Abwandlung auch von außen in den menschlichen Körper eingebracht werden und lassen sich therapeutisch nutzen. Theoretisch könnte siRNA gegen alle Erkrankungen eingesetzt werden, bei denen schädliche Proteine beteiligt sind. Das macht sie als Therapieansatz so interessant, denn siRNA kann alle Proteine einfach und sehr spezifisch adressieren. Allerdings gibt es viele Eigenschaften, die eine siRNA erfüllen muss, damit die RNA-Interferenz als therapeutisches System funktionieren kann. Ein Problem ist die Stabilität von RNA, sie wird im Blut innerhalb von wenigen Minuten abgebaut. Um das zu verhindern, werden die Moleküle chemisch verändert z. B. durch Methylierung an der 2'-Position der Ribose.
Damit die siRNA-Moleküle in die Zellen aufgenommen werden, in denen sie die Translation verhindern sollen, gibt es verschiedene Möglichkeiten. Eine ist die Verpackung der siRNA in Lipidnanopartikel. Diese ahmen Biomembranen nach und interagieren mit Lipoproteinen, wodurch die siRNA-Moleküle in die Zellen aufgenommen werden (z. B. Patisiran, s. Tab.). Eine andere Möglichkeit, um siRNA an ihren Wirkort zu bringen, ist die Verknüpfung der siRNA mit einem Liganden oder Antikörper. So bewirkt die Konjugation mit N-Acetyl-Galactosamin (GalNAc), dass siRNA-Moleküle über den Liganden an Asialoglycoprotein-Rezeptoren auf Hepatozyten binden und in diese geschleust werden (z. B. Givosiran, Inclisiran, Lumasiran und Vutrisiran, s. Tab.). Weitere Probleme, die durch das Design der siRNA beeinflusst werden können, sind die Auswahl des richtigen Leitstrang im RISC-Komplex, die Minimierung von Off-Target-Effekten und die Vermeidung von Immunreaktionen [3, 18].
Im Gegensatz zu siRNA- paaren sich miRNA-Moleküle mit der Ziel-mRNA weniger spezifisch. Die miRNA muss nur teilweise komplementär zu ihrer Ziel-mRNA sein, um mit dieser zu interferieren. So adressiert eine miRNA unterschiedliche mRNA-Stränge. Um miRNA therapeutisch zu nutzen, gibt es andere Ansätze (s. Kasten „Kann auch Micro-RNA therapeutisch eingesetzt werden?“).
Kann auch Micro-RNA therapeutisch eingesetzt werden?
In der Forschung werden bereits auch Interventionen auf Micro-RNA-Basis erprobt. Dabei gibt es zwei Ansätze:
- Beim miRNA-Antagonismus wir mit synthetischen einzelsträngigen RNA-Fragmenten, sogenannte miRNA-Antagonisten, die Wirkung der endogenen Micro-RNA-Stränge gehemmt. Therapeutische Antagomere könnten gegen krankheitsverursachende miRNA-Moleküle eingesetzt werden z. B. gegen onkogene miRNA, die in Karzinomzellen überexprimiert wird, oder gegen miRNA, die zur Herzinsuffizienz führt. Beispielsweise wird das synthetische Oligonukleotid CDR132L als Antagomer gegen die Micro-RNA-132 klinisch erprobt, die nach einem Herzinfarkt zum pathologischen Remodeling führt.
- Bei der miRNA-Ersatztherapie sollen miRNA-Moleküle, die in kranken Zellen herunterreguliert oder vollständig verloren sind, wiederhergestellt werden, z. B. um Tumorsuppressor-miRNA zu ersetzen [3].
Welche RNAi-Therapeutika sind zugelassen?
RNA-Interferenz wird zunehmend therapeutisch eingesetzt. Bisher gibt es fünf zugelassene RNAi-Therapeutika, alle zielen auf die Stilllegung von mRNA in Leberzellen ab und werden parenteral verabreicht: Inclisiran wird bei Patienten mit einer primären Hypercholesterolämie oder gemischten Dyslipidämie eingesetzt, bei denen mit anderen lipidsenkenden Therapeutika kein ausreichender Effekt erzielbar ist oder Statine kontraindiziert sind. Die weiteren zugelassenen siRNA-Moleküle werden gegen seltene Indikationen eingesetzt; Givosiran gegen die akute hepatische Porphyrie, Lumasiran gegen die primäre Hyperoxalurie Typ 1, Patisiran und Vutrisiran gegen die hereditäre Transthyretin-Amyloidose. In folgendem Text und Abbildung 2 wird näher auf die Arzneimittel und Wirkmechanismen eingegangen.
Abb. 2: Zugelassene RNAi-Therapeutika und deren Wirkmechanismen; LNP: Lipidnanopartikel, siRNA: small interfering RNA, GalNAc: N-Acetyl-Galactosamin, RISC: RNA-induced silencing complex (modifiziert nach [3]).
Givosiran (Givlaari®) wird bei Patienten mit der seltenen Erkrankung akute hepatische Porphyrie (Prävalenz: 1 : 75.000) eingesetzt. Betroffene leiden unter einem von vier vererbten Enzymdefekten in der Häm-Biosynthese. Häme sind entscheidend für die Sauerstoffaufnahme in den Körper, sie bestehen aus einem zentralen Eisen-Ion und einem Gerüst eines Porphyrin-Moleküls. Aufgrund der gestörten Häm-Synthese ist bei den Patienten ein weiteres Enzym in Leberzellen hochreguliert, das für den ersten Schritt der Häm-Synthese verantwortlich ist, die sogenannte Aminolävulinsäure-Synthase-1 (ALAS1). Der Anstieg von ALAS1 führt zu einer ausreichenden Produktion des Blutfarbstoffs Häm, aber auch zum Anstieg der toxischen Zwischenprodukte Aminolävulinsäure und Porphobilinogen. Diese Proteine sind für Nervenzellen schädlich und können lebensbedrohliche Attacken auslösen sowie langfristige Komplikationen. Treten diese neuroviszeralen Attacken auf, leiden Patienten unter anderem über mehrere Tage an Leibschmerzen, neurologischen Symptomen wie Muskelschwäche und Krämpfen sowie psychischen Symptomen. Die siRNA Givosiran bindet an die mRNA des Enzyms ALAS1 in Leberzellen und sorgt dafür, dass die ALAS1-mRNA abgebaut und die Enzymproduktion gestoppt wird. In der Folge sinken die Spiegel der toxischen Proteine um nahezu 95%, und die Attacken gehen zurück sowie auch andere Manifestationen der Erkrankung [4, 6, 9].
Inclisiran (Leqvio®) ist ein Arzneimittel, das gegen Hypercholesterolämie und Dyslipidämie eingesetzt werden kann. Die siRNA bindet an die mRNA des Liganden Proproteinkonvertase Subtilisin/Kexin Typ 9 (PCSK9) und leitet deren Abbau ein. Physiologisch hat PCSK9 die Aufgabe, an LDL-Cholesterol-Rezeptoren (LDL: Low density lipoprotein) auf Hepatozyten zu binden und dadurch den Abbau der Rezeptoren für LDL-Cholesterol einzuleiten. Durch die Interferenz der siRNA mit der mRNA von PCSK9 wird weniger des Proteins PCSK9 synthetisiert. Infolge der verminderten Konzentration des Liganden PCSK9 werden weniger LDL-Cholesterol-Rezeptoren abgebaut und verbleiben auf den Hepatozyten. So kann mehr LDL-Cholesterol über die Rezeptoren in die Leberzellen aufgenommen werden und die LDL-Cholesterol-Blutspiegel sinken. Indiziert ist Inclisiran bei erwachsenen Patienten mit primärer, heterozygot familiärer und nicht familiärer Hypercholesterolämie oder gemischter Dyslipidämie zusätzlich zu einer diätetischen Therapie, wenn die LDL-Cholesterol-Zielwerte unter alleiniger Statin-Therapie nicht erreicht werden. Die siRNA wird mit Statinen oder einer lipidsenkenden Therapie kombiniert. Innerhalb von einem Monat können nach der Applikation von Inclisiran die LDL-Cholesterol-Blutspiegel über mindestens sechs Monate anhaltend um 50 bis 55% gesenkt werden. Dabei muss die siRNA in der Erhaltungsphase nur alle sechs Monate injiziert werden, allerdings von medizinischem Fachpersonal [4, 10]. Erst vor Kurzem wurden neue Langzeitdaten aus der offenen Extensionsstudie ORION-8 zu Inclisiran veröffentlicht. Die Ergebnisse zeigten, dass bei zusätzlicher Behandlung mit Inclisiran zu einer Statin-Therapie die LDL-Cholesterol-Werte über einen Zeitraum von bis zu mehr als sechs Jahren gesenkt werden konnten. Die Langzeitsicherheit aus den zuvor durchgeführten klinischen Studien wurde bestätigt [16].
Lumasiran (Oxlumo®) ist eine siRNA, die den Abbau der mRNA des Proteins der Glykolat-Oxidase initiiert. In der Folge sinken Oxalat-Spiegel von Patienten mit der autosomal-rezessiv vererbten Erkrankung primäre Hyperoxalurie Typ 1 (Prävalenz: 1 bis 3 : 1.000.000). Bei dieser Erkrankung schädigt eine Überproduktion von Oxalat die Niere und andere Organe. Grund der Überproduktion von Oxalat ist eine Mutation im Leberenzym Alanin-Glyoxylat-Aminotransferase, die Glyoxylat normalerweise in Glycin umwandelt. Weil das defekte Enzym Glyoxylat nicht metabolisieren kann, wird Glyoxylat vermehrt durch die Lactat-Dehydrogenase in Oxalat umgewandelt und lagert sich in Form von Calciumoxalat-Kristallen in verschiedenen Geweben ab, unter anderem in den Harnwegen und den Nieren, was zur Bildung von Harnsteinen und letztendlich Nierenversagen führt. Die siRNA Lumasiran interferiert mit der mRNA des Enzyms Glykolat-Oxidase, einem Enzym, das für einen vorgeschalteten Reaktionsschritt der Oxalat-Produktion verantwortlich ist – es wird also nicht das mutierte Protein adressiert, das für die Krankheit verantwortlich ist. Durch die Stilllegung der Expression der Glykolat-Oxidase sinken die pathologischen Oxalat-Spiegel [4, 11].
Patisiran (Onpattro®) und Vutrisiran (Amvuttra®) sind RNAi-Therapeutika, die zur Behandlung der hereditären Transthyretin-Amyloidose (Prävalenz: 1 : 1.000.000) eingesetzt werden können, bei Patienten mit Polyneuropathie der Stadien 1 oder 2. Die Erkrankung entsteht aufgrund einer autosomal-dominant vererbten Mutation im Transportprotein Transthyretin. Wegen der Mutation ist Transthyretin fehlerhaft gefaltet und akkumuliert zu Amyloidfibrillen. Diese lagern sich im Nervensystem, Herzen, Gastrointestinaltrakt, Knochenmark sowie in den Augen, Nieren und der Schilddrüse ab. Es entwickeln sich Polyneuropathien mit Lähmungen und Krämpfen, Kardiomyopathien bis zum Herzversagen, schwere Verdauungsstörungen und andere Symptome wie Sehstörungen, Nierenfunktionsstörungen und Demenz. Physiologisch wird Transthyretin in der Leber gebildet und transportiert Schilddrüsenhormone und Vitamin A. Die siRNA-Moleküle in Patisiran und Vutrisiran interferieren mit der Transthyretin-mRNA und leiten ihren Abbau ein, dabei wird nicht nur die mRNA der mutierten, für die Krankheit verantwortlichen Proteine abgebaut, sondern auch die der nicht mutierten. Insgesamt wird eine mehr als 80%ige langfristige Reduktion der Transthyretin-Serum-Spiegel erzielt. Eine unerwünschte Wirkung der Therapie ist es, dass der Vitamin-A-Transport gestört ist und die Vitamin-A-Spiegel im Serum der Patienten verringert sind. Vitamin A sollte deshalb bei Anwendung dieser Therapeutika supplementiert werden. Die beiden Wirkstoffe Patisiran und Vutrisiran unterscheiden sich in ihrer Applikationsform und der Art, wie die siRNA in die Zelle aufgenommen wird . Die siRNA in Patisiran ist in Lipidnanopartikel verpackt und wird als Infusion verabreicht, Vutrisiran wird subkutan injiziert und gelangt über den Liganden N-Acetyl-Galactosamin (GalNAc) in die Zelle [4, 12, 13].
Wirkstoffname (Präparat, Zulassung) | Indikation | Dosierungen/Hinweise |
|---|---|---|
Givosiran (Givlaari®, 2020) | akute hepatische Porphyrie; ab 12 Jahren |
|
Inclisiran (Leqvio®, 2020) | primäre Hypercholesterolämie oder gemischte Dyslipidämie; ab 18 Jahren |
|
Lumasiran (Oxlumo®, 2020) | primäre Hyperoxalurie Typ 1; alle Altersgruppen |
|
Patisiran (Onpattro®, 2018; Verlängerung: 2023) | hereditäre Transthyretin-Amyloidose, bei Patienten mit Polyneuropathien der Stadien 1 oder 2; ab 18 Jahren |
|
Vutrisiran (Amvuttra®, 2022) | hereditäre Transthyretin-Amyloidose, bei Patienten mit Polyneuropathien der Stadien 1 oder 2; ab 18 Jahren |
|
Was steckt in der Pipeline?
Die bereits zugelassenen fünf RNAi-Therapeutika beweisen, dass RNA-Interferenz eine Chance ist, um gezielte Therapien zu entwickeln. Darüber hinaus ist das Potenzial der Technologie noch lange nicht ausgeschöpft. In der Pipeline befinden sich viele Wirkstoffe, die neue Therapieoptionen ermöglichen könnten. Zum Beispiel könnte siRNA auch gegen das metabolische Syndrom oder Hypertonie eingesetzt werden. Vor Kurzem wurden Studienergebnisse einer Phase-II-Studie (KARDIA-1) zum Wirkstoff Zilebesiran veröffentlicht zur Behandlung von Bluthochdruck. Die siRNA interferiert mit der mRNA von Angiotensinogen, das in der Leber produziert wird und blutdruckerhöhend im System der Renin-Angiotensin-Aldosteron-Kaskade wirkt. Die Ergebnisse zeigen, dass durch die subkutane Injektion von Zilebesiran der mittlere systolische Blutdruck von Hypertonikern dauerhaft über 24 Stunden gesenkt werden kann. Durch eine Applikation von 300 oder 600 mg konnte eine Senkung des Blutdrucks von mehr als 15 mmHg erreicht werden (p < 0,0001). Auch nach sechs Monaten war die Senkung des Blutdrucks anhaltend. Schafft es Zilebesiran zur Zulassung, könnte es möglich sein, Hypertonie durch eine viertel- oder halbjährliche Injektion zu behandeln. Neben Zilebesiran gibt es einige weitere RNAi-Therapeutika in der Entwicklung, manche haben bereits die klinischen Studien der Phase III erreicht, darunter:
- Fitusiran. Die siRNA bindet an die mRNA von Antithrombin, das normalerweise Thrombin proteolytisch abbaut. Die verminderte Translation von Antithrombin führt zu einer erhöhten Thrombin-Konzentration und einer verstärkten Gerinnung. Die siRNA wird gegen Hämophilie A und B entwickelt, eine Blutungsstörung mit Mutationen in den Genen der Gerinnungsfaktoren VIII bzw. IX.
- Nedosiran zielt auf die mRNA der hepatischen Lactat-Dehydrogenase ab, dadurch sinken die Oxalat-Produktion und Spiegel. Anfang Oktober 2023 wurde die siRNA für die Behandlung der primären Hyperoxalurie Typ 1 durch die FDA zugelassen.
- Tivanisiran ist gegen die mRNA des Transient-Rezeptor-Potential-Kationenkanals der Subfamilie V gerichtet. Dieser Rezeptor spielt eine wichtige Rolle in verschiedenen Signalwegen, darunter auch die Schmerzsignaltransduktion. Tivanisiran wird für die Behandlung von Augenschmerzen und trockenen Augen erprobt [3, 5, 7, 8]. |
Literatur
[1] Meister G. Steuerung der Proteinproduktion durch kleine RNA-Moleküle. Information der Max-Planck-Gesellschaft, Steuerung der Proteinproduktion | Max-Planck-Gesellschaft (mpg.de)
[2] RNA-Interferenz. Information der Seite Pflanzenforschung.de
[3] Traber GM, Yu A. RNAi-Based Therapeutics and Novel RNA Bioengineering Technologies. Journal of Pharmacology and Experimental Therapeutics 2023;384(1):133-154
[4] Fachinformationen der genannten Präparate
[5] RNA-Interferenz stoppt Angiotensinogenproduktion und senkt Blutdruck. Artikel vom 31. Juli 2023 des Aerzteblatts, www.aerzteblatt.de/nachrichten/144767/RNA-Interferenz-stoppt-Angiotensinogenproduktion-und-senkt-Blutdruck?rt=c631a3a05259f71cfe268d1ec45ebf0b
[6] Akute hepatische Porphyrie. Information von Alnylam Pharmaceuticals, www.alnylam.de/wp-content/uploads/pdfs/DE-AHP-Disease-Backgrounder.pdf
[7] Roche and Alnylam report positive topline results from Phase 2 study KARDIA-1 of zilebesiran, an investigational RNAi therapeutic in development to treat hypertension in patients at high risk of cardiovascular disease. Presseinformation von Roche vom 7. September 2023.
[8] Fitusiran. Information auf DocCheck Felxikon, Stand: April 2023, https://flexikon.doccheck.com/de/Fitusiran
[9] Neubeck M. Givosiran. Artikel auf DAZ.online vom 15. April 2020
[10] Neubeck M. Inclisiran. Artikel auf DAZ.online vom 1. Februar 2021
[11] Neubeck M. Lumasiran. Artikel auf DAZ.online vom 1. Januar 2021
[12] Neubeck M. Patisiran. Artikel auf DAZ.online vom 1. Oktober 2028
[13] Neubeck M. Vutrisiran. Artikel auf DAZ.online vom 3. Januar 2023
[14] Oetzel S. RNA mit großem therapeutischem Potenzial. DAZ 2021;11:56-63
[15] Abdellatef E et al. Tuning Beforehand: A Foresight on RNA Interference (RNAi) and In Vitro-Derived dsRNAs to Enhance Crop Resilience to Biotic and Abiotic Stresses. International Journal of Molecular Sciences 2021;22(14):7687
[16] ESC-Kongress 2023: Aktuelle Daten zum Cholesterinsenker. Information der Novartis Pharma GmbH, Stand: 30. August 2023, www.novartis.com/de-de/medien/pressemitteilungen/esc-kongress-2023-aktuelle-daten-zum-cholesterinsenker
[17] EU-zugelassene therapeutische Medikamente auf Basis von RNA oder DNA. Information des Verband Forschender Arzneimittelhersteller e.V., Stand: September 2023, www.vfa.de/de/arzneimittel-forschung/datenbanken-zu-arzneimitteln/zugelassene-rna-oder-dna-basierte-therapeutika
[18] Lam JKW et al. siRNA Versus miRNA as Therapeutics for Gene Silencing. Mol Ther Nucleic Acids 2015; 4(9):e252























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.