
- DAZ.online
- DAZ / AZ
- DAZ 10/2023
- Schattendasein der SARS-...
COVID-19
Schattendasein der SARS-CoV-2-Antikörper
Warum die neutralisierenden monoklonalen Antikörper kaum eingesetzt wurden
Hört es sich rückblickend nicht utopisch an? Im Frühjahr 2021, mitten in der COVID-19-Pandemie, noch bevor große Teile der Bevölkerung zweifach geimpft waren, lagen wirksame Arzneimittel zur Verhinderung eines schweren Verlaufs vor. Die Rede ist von SARS-CoV-2 neutralisierenden monoklonalen Antikörpern (monoclonal antibodies, mAbs). Diese hätten alsbald nach einem Corona-Ausbruch in einem Altenpflegeheim allen bis dato nicht nachweislich infizierten Bewohnern als Post-Expositionsprophylaxe (PEP) angeboten werden können. Idealerweise hätten sich so viele dieser vulnerablen Personen vor einer Übertragung schützen können. Dadurch wäre es wahrscheinlich möglich gewesen, das Infektionsgeschehen in der Pflegeeinrichtung einzudämmen. Und diejenigen, die es „erwischt“ hatte, hätten nach individueller Nutzen-Risiko-Abwägung zeitnah eine Infusion mit monoklonalen Antikörpern bekommen können. Immer mit dem Ziel, die Viruslast im Körper effektiv zu reduzieren, hierdurch eine klinische Verbesserung zu erzielen und schwere Krankheitsverläufe inklusive Hospitalisierung und Tod abzuwenden. Erwähnenswert ist an dieser Stelle, dass in den Jahren 2020 und 2021 laut aktuellem Barmer-Pflegereport fast jeder zweite COVID-19-Verstorbene in Deutschland zuvor in einer Pflegeeinrichtung gewohnt hat [13]. In einem anderen Szenario hätte man monoklonale Antikörper halbjährlich als Prä-Expositionsprophylaxe (PrEP) geben können. Diese Art der passiven Immunisierung war eine Option für seronegative Personen mit fehlendem Impfansprechen, beispielsweise bedingt durch eine immunsuppressive Therapie oder eine hämato-onkologische Grunderkrankung. Doch auch ganz grundlegend hätten geimpfte ebenso wie ungeimpfte Personen mit einem erhöhten Risiko, schwer an COVID-19 zu erkranken, wie etwa ein 70-Jähriger mit Übergewicht und Herz-Kreislauf-Erkrankungen, mit den SARS-CoV-2 neutralisierenden monoklonalen Antikörpern nach einem Risikokontakt vorsorglich geschützt (Post-Expositionsprophylaxe) oder bei einer Infektion therapiert werden können. Aktuell spielen diese Überlegungen für die medizinische Versorgung keine Rolle, da EMA und FDA vermelden, dass die zugelassenen Antikörperpräparate gegen die derzeit zirkulierenden Virus-Varianten eine mangelnde Neutralisationsfähigkeit aufweisen [1, 2]. Doch wieso wurden monoklonale Antikörper gegen SARS-CoV-2 in der Vergangenheit nicht oder nur selten eingesetzt, obwohl sie wirksam waren?
Teure Cocktails
Zunächst waren die Erwartungen hoch – zur Erinnerung: (Vor-)eilig sicherte sich der Bund im Januar 2021 400 Millionen Euro teure Kontingente des mAb-Cocktails Casirivimab/Imdevimab (mittlerweile zugelassen als Ronapreve®) und von Bamlanivimab (Zulassungsantrag derweil zurückgezogen). Hierdurch sollte die Behandlung von 186.000 Patienten ermöglicht werden. Dass die Wirkstoffe zum Zeitpunkt ihres Einkaufs weder in der EU zugelassen waren, noch eine wissenschaftliche Empfehlung des Ausschusses für Humanarzneimittel (CHMP) bei der EMA vorlag, störte offenbar die Einkäufer nicht. Vermutlich waren Studienergebnisse über eine vielversprechende Wirksamkeit in der Prä-Expositionsprophylaxe und der Therapie zu verlockend gewesen. Zu Bamlanivimab musste im weiteren Verlauf Etesevimab als Kombinationspartner nachgeordert werden, da man sich der Wirksamkeit der Monotherapie nicht sicher war. Seit Ende Januar 2022 ist außerdem das zur COVID-19-Therapie zugelassene monoklonale Antikörper-Präparat Xevudy® (Sotrovimab) in Deutschland verfügbar. Die Bundesregierung kaufte davon über 50.000 Dosen. Mit der Kombination aus Tixagevimab und Cilgavimab (Evusheld®) kam Ende Februar 2022 ein Präparat mit verlängerter Halbwertszeit hinzu, welches – wie Ronapreve® – sowohl zur Therapie als auch für die Prä-Expositionsprophylaxe zugelassen ist (Hinweis: Ronapreve® ist zudem auch für die PEP zugelassen). Das Bundesministerium für Gesundheit (BMG) verlautbarte seinerzeit, dass hiervon „begrenzte Kontingente“ zur Verfügung gestellt wurden. Zum jetzigen Zeitpunkt ist allerdings keines der Präparate mehr wirksam. Auch zu dem zuletzt verbliebenen Hoffnungsträger Evusheld® wurden nun die Empfehlungen der STIKO weiter eingegrenzt. Aufgrund unzureichender In-vitro-Neutralisationskapazität gegenüber den aktuell zirkulierenden Varianten und Sublinien soll er nur noch in begründeten Einzelfällen für bestimmte Hochrisikopersonen zur Prä-Expositionsprophylaxe in Betracht kommen. Dabei wird von der STIKO eine Off-Label-Dosierung von jeweils 300 mg der beiden Antikörper zur Prä-Expositionsprophylaxe empfohlen (die in der EU zugelassene Dosierung zur Vorbeugung beträgt jeweils 150 mg) [14].
Wettlauf gegen die Zeit
Als besonders herausfordernd erwies sich vor allem das scharf begrenzte Zeitfenster, in dem monoklonale Antikörper bei COVID-19 verabreicht werden durften. Denn mit der passiven Immunisierung sollten lediglich Patienten ab zwölf Jahren mit einem erhöhten Risiko für einen schweren COVID-19-Verlauf behandelt werden, die in einem frühen Stadium der Erkrankung waren. Die Gabe durfte nicht später als (fünf bis) sieben Tage nach Symptombeginn erfolgen, in der Regel befand sich der Patient daher im ambulanten Bereich. Die rechtzeitige Behandlung ist deshalb wichtig, da die Therapie nur anspricht, bevor das immunologische Geschehen aus dem Ruder gelaufen ist und man die Virusreplikation besonders früh eindämmen möchte. Verzögerungen sind dementsprechend unerwünscht, konnten aber eintreten. Zum Beispiel wenn frühe Symptome als wenig bedrohlich eingeschätzt wurden oder das Ergebnis des PCR-Tests zur Sicherung der Diagnose noch ausstand. Auch eine in Anspruch genommene infektiologische Beratung konnte zu Verzögerungen führen oder es erfolgte zunächst eine serologische Überprüfung der gegebenenfalls vorhandenen Immunantwort. Für behandelnde Ärzte war es zudem umständlicher als sonst, an das jeweilige Präparat zu gelangen. Hintergrund ist die anfängliche zentrale Beschaffung der monoklonalen Antikörper durch das BMG: Da sie nicht über den normalen Vertriebsweg, sondern nur über bestimmte Krankenhaus-, beziehungsweise krankenhausversorgende Apotheken verteilt wurden, musste das kühlkettenpflichtige Präparat von einem Bevollmächtigten der Arztpraxis dort selbst abgeholt, oder eine öffentliche Apotheke mit der Abholung beauftragt werden. Diese Aspekte trugen sicherlich dazu bei, dass sich die Therapie mit monoklonalen Antikörpern zu einem Wettlauf gegen die Zeit entpuppte, jedoch musste das Rennen auch erst einmal angetreten werden [3].
Hohe Hürden
Neben den logistischen Hürden und der zeitnahen Applikation gab es viele weitere Gründe, warum Arztpraxen Abstand genommen haben, SARS-CoV-2 neutralisierende monoklonale Antikörper zur Therapie oder Prophylaxe bei COVID-19 einzusetzen. Sicherlich sind der Dokumentations- und Meldeaufwand sowie rechtliche Bedenken im Fall nicht zugelassener Präparate auch abschreckend gewesen. Vielleicht waren die Ärzte auch unsicher oder wussten nicht genug über die Wirksamkeit und Sicherheit der neuen Arzneimittel. Es scheint, als hätte es generelle Berührungsängste gegenüber der Therapieform gegeben. Eine weitere Hürde war der mit der Verabreichung verbundene hohe Zeitaufwand in einem ohnehin ausgelasteten, von COVID-19-Impfungen dominierten System. Dabei muss bedacht werden, dass es sich bei der Gabe von SARS-CoV-2 neutralisierenden monoklonalen Antikörpern bei COVID-19 um eine ärztliche Tätigkeit handelt, die nicht delegiert werden kann. Zudem durften andere Patienten der Praxis nicht gefährdet werden, so benötigte man zum Beispiel einen separaten Eingang und getrennte Räumlichkeiten [3]. Nicht immer war die räumliche und personelle Infrastruktur hierfür gegeben. Auch die hohen Anforderungen an Infektionsschutz- und Hygienemaßnahmen waren eine Zusatzbelastung. Beim therapeutischen Einsatz von SARS-CoV-2 neutralisierenden monoklonalen Antikörpern braucht es eine eingehende Diagnostik, ausführliche Aufklärungsgespräche, die Applikation an sich und in der Regel eine einstündige Nachbeobachtungszeit. Folglich hat auch das Personal viel Kontakt mit infektiösen Personen und muss entsprechend geschützt werden. Zunächst mussten die Präparate auch als circa einstündige Infusion verabreicht werden, erst später bot sich zeitsparend die Möglichkeit zur Kurzinfusion, zur subkutanen Anwendung (Ronapreve®) oder zur intramuskulären Gabe (Evusheld®). Professor Martin Scherer, Präsident der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM), gab gegenüber dem Deutschen Ärzteblatt einen weiteren Punkt zu bedenken: Die Therapie sollte unter Bedingungen erfolgen, die eine schnelle Behandlung einer Infusionsreaktion oder einer allergischen Reaktion möglich machen. Daher sei aus seiner Sicht der Einsatz für eine reguläre vollversorgende Hausarztpraxis nicht praktikabel und sollte spezialisierten Einrichtungen vorbehalten bleiben [4].
Antikörper-Ambulanzen
Um die Versorgung mit monoklonalen Antikörpern zu verbessern und den ambulanten Bereich zu entlasten, eröffneten viele Krankenhäuser sogenannte Antikörper-Ambulanzen. Nach Terminabsprache durch den Patienten selbst oder den behandelnden Arzt konnten hier frisch mit SARS-CoV-2-Infizierte, die ein erhöhtes Risiko für einen schweren COVID-19-Verlauf aufwiesen, vorstellig werden und eine Therapie mit monoklonalen Antikörpern erhalten. Das Robert Koch-Institut (RKI) entwickelte eigens ein Postleitzahlen-Tool, um die Suche nach Krankenhäusern beziehungsweise Ansprechpartnern zu erleichtern, die an der Versorgung mit monoklonalen Antikörpern teilnehmen (s. Kasten „Wer und Wo?“). Den niedergelassenen Ärzten, die monoklonale Antikörper bei COVID-19 nicht anwenden konnten oder wollten, kam an dieser Stelle eine wichtige Lotsenfunktion zu. Doch die Nachfrage war mau, wie Prof. Dr. Leif Erik Sander, Klinikdirektor Infektiologie an der Berliner Charité, im Rahmen eines Symposiums ernüchtert feststellen musste: „Wir haben an der Charité im April 2021 eine Antikörper-Ambulanz eingerichtet, in einem separaten Gebäude. Es gab auch extra eine Hotline, bei der Ärzte im Falle von Rückfragen und zur Terminvergabe anrufen konnten. Wir haben ehrlich gesagt damit gerechnet, dass wir da überrannt werden. Dann mussten wir die Ambulanz nach ein paar Monaten schließen, weil keiner kam. Das war sehr frustrierend, dabei hatten wir die Ärztekammern informiert und hätten den niedergelassenen Kolleginnen und Kollegen die Behandlung abgenommen“ [5].
Wer und Wo?
Das Robert Koch-Institut stellt Listen und Tools zur Verfügung, damit sich Patienten und Heilberufler über die Versorgung mit monoklonalen Antikörpern informieren können. Um dorthin zu gelangen, geben Sie bitte die Webcodes direkt in die Suchmaske auf DAZ.online ein.
- Liste der bevorratenden Apotheken für monoklonale Antikörper (Webcode: N2ZK5) [9]
- Postleitzahlen-Tool zur Suche nach Ansprechpartnern zur Therapie mit monoklonalen Antikörpern in Krankenhäusern (Webcode: E5YX8) [10]
- Liste der Krankenhäuser/Ansprechpartner, die an der Versorgung mit monoklonalen Antikörpern teilnehmen (Webcode: G9PM2) [11]
Wenig beachtete Ladenhüter
Professor Sander sprach auch an, dass man bei monoklonalen Antikörpern unberechtigterweise an eine Last-Line-Therapie denken würde [5]. Dass sie aber sehr gut wirksam und verträglich waren, sei seiner Meinung nach offenbar bei einem großen Teil der Ärzteschaft nicht angekommen. Vielleicht mangelte es auch an öffentlicher Aufklärung und überregionalen Informationskampagnen zu dieser Therapieoption. Man kann den Eindruck gewinnen, dass die monoklonalen Antikörper von Beginn an im Schatten der COVID-19-Impfungen, für die intensiv „geworben“ wurde, standen. Der „Stern“ berichtete, dass bis zum 19. November 2021 hierzulande nur 8000 Infusionen verabreicht wurden, weshalb in der Zeitschrift von einem „Antikörper-Skandal“ die Rede war [7]. Wie viele der zentral beschafften Dosen zur Anwendung kamen, wollte die DAZ nun direkt vom BMG wissen. Laut Auskunft einer Sprecherin wurden von 255.000 zentral beschafften Therapieeinheiten bislang rund 140.000 an die Stern- und Satelliten-Apotheken ausgeliefert. Unklar bleibt, wie viele dort tatsächlich abgerufen oder ungenutzt verfallen sind. Eigentlich müsste diese Information aber vorliegen, da ein Teil der bürokratischen Hürden für Ärzte darin bestand, jede Anwendung verpflichtend an das Paul-Ehrlich-Institut zu melden. Konkret wurde man aber bei der Anzahl gespendeter Therapieeinheiten: Rund 60.000 seien an andere Staaten abgegeben worden, so die Sprecherin [6]. Rechnet man nach, so ergibt sich, dass von 255.000 Therapieeinheiten 55.000 ein gänzlich unbekanntes Dasein fristen (255.000 - 140.000 - 60.000 = 55.000).
Fehlende finanzielle Anreize?
War die Vergütung für den Aufwand nicht hoch genug? Ist auch Geld ein Grund, warum monoklonale Antikörper nicht häufiger eingesetzt wurden? Immerhin wurde die extrabudgetäre Anwendung zentral beschaffter monoklonaler Antikörper zur Therapie einer SARS-CoV-2-Infektion mit 360 Euro (vor März 2022 sogar mit 450 Euro) durch die gesetzliche Krankenversicherung und andere Kostenträger vergütet. Im Falle einer prophylaktischen Gabe konnten Ärzte 150 Euro plus 60 Euro Zuschlag für einen Hausbesuch abrechnen. Entsprechende Regelungen finden sich in der Monoklonale-Antikörper-Verordnung (MAKV), die auch die Anspruchsvoraussetzungen sowie die Bereitstellung dieser Arzneimittel beinhaltet [8]. In Anbetracht der zurückhaltenden Nutzung waren die Pauschalen scheinbar nicht attraktiv genug, um die Hürden bei der Behandlung von Risikopatienten mit monoklonalen Antikörpern gegen COVID-19 bzw. der Prophylaxe zu nehmen.
Das Virus weicht aus
Mittlerweile ist es in der öffentlichen Debatte noch ruhiger um neutralisierende monoklonale Antikörper gegen SARS-CoV-2 geworden. Grund hierfür ist der alles entscheidende Wettlauf in dieser Pandemie: die Virusevolution. Die Stärke dieser hochspezifischen monoklonalen Antikörper ist es, antigene Oberflächenstrukturen (Epitope) passgenau zu erkennen. Diese Eigenschaft ist gleichzeitig ihre Achillesferse, wenn Fluchtmutationen auftreten. Während Blockbuster unter den monoklonalen Antikörpern wie Adalimumab und Co. nicht von veränderlichen Zielen betroffen sind, ist dies bei neutralisierenden Antikörpern gegen Erreger von Infektionskrankheiten grundsätzlich zu befürchten. So wurde es für die am Markt befindlichen monoklonalen Antikörper mit zunehmender Veränderung der Epitope auf dem Spike-Protein schwierig bis unmöglich, die neuen Virusvarianten als ihr Zielobjekt zu identifizieren. Alle bisher zugelassenen SARS-CoV-2-neutralisierenden Antikörper binden an unterschiedlichen Stellen der rezeptorbindenden Domäne (Receptor-Binding Domain, RBD) des Spike-Proteins. Gerade dieses wurde im Laufe der Virusevolution zahlreichen Mutationen unterworfen, was zu deutlichen Veränderungen in der RBD geführt hat und sich unweigerlich auf die Antigenität auswirkte. Das war vor allem nach dem Aufkommen der Omikron-Variante und ihrer Sublinien ein Problem, analog den COVID-19-Impfstoffen. Die Omikron-Sublinien sind durch eine sehr starke Immunflucht geprägt (Immune-Escape-Varianten).
Aus dem Schatten ins Licht?
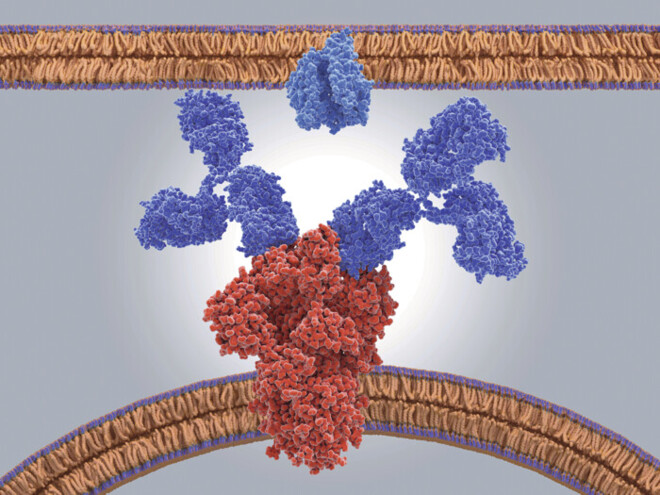
Ein Forscherteam aus Boston hat einen Antikörper identifiziert, der alle bisher gängigen Varianten von SARS-CoV-2 neutralisieren kann. Dazu spritzten sie Mäusen mit humanisiertem Genom Immunogene des Spike-Proteins des Wuhan-Stamms. Die Mäuse produzierten neun verschiedene B-Zell-Linien. Der aus einer Linie exprimierte monoklonale Antikörper SP1-77 zeigte sich in verschiedenen Neutralisationstests als potent gegen alle bisher bekannten Pseudovirus-Varianten. SP1-77 bindet nicht an der ACE2-Rezeptorbindestelle, sondern an der gegenüberliegenden Seite. Die meisten Mutationen der SARS-CoV-2 Varianten liegen außerhalb dieses Bereichs. Der Antikörper blockiert durch seine Bindung die Membranfusion von Wirtszelle und Virus anstatt die Bindung des Virus an die Wirtszelle zu verhindern. Durch diesen Mechanismus unterscheidet er sich von bisher bekannten Antikörpern. Bestätigen sich die Ergebnisse in vivo, dann hat der Antikörper das Potenzial gegen aktuelle und neue Varianten alleine oder in Kombination mit anderen Antikörpern eingesetzt zu werden. Außerdem könnten die Ergebnisse Hinweise für ein mögliches Target für künftige Impfstoffe liefern [12].
Wie geht es weiter?
Bei der Suche nach wirksamen therapeutischen Antikörpern gegen SARS-CoV-2 sind konservierte Regionen des Zielmoleküls interessant, da sie nicht leicht veränderlich sind. Ziel vieler Forschungsgruppen ist es, breitneutralisierende Antikörper zu finden, die auch gegen Immune-Escape-Varianten wirksam bleiben). Um Resistenzen zu verhindern, setzt man ferner auf Antikörper-Kombinationen, die an verschiedene, nicht überlappende Epitope des Antigens binden. So könnte man bei Mutationen einer „Andockstelle“ noch auf eine Neutralisationsaktivität über andere Epitope hoffen. Einen zukunftsgerichteten Blick über das dynamische Feld der Entwicklung monoklonaler Antikörper bei COVID-19 lesen Sie in unserem Interview mit dem Antikörperexperten Professor Florian Klein von der Universitätsklinik Köln. Sofern wieder wirksame Optionen vorhanden sind, sollte das Wissen um den Nutzen einer passiven Immunisierung bei Ärzten wie Patienten verbreitet und die mühsam aufgebaute Infrastruktur der Antikörper-Ambulanzen stärker wahrgenommen werden. |
Literatur
[1] ETF warns that monoclonal antibodies may not be effective against emerging strains of SARS-CoV-2. Pressemitteilung der EMA vom 9. Dezember 2022, www.ema.europa.eu/en/news/etf-warns-monoclonal-antibodies-may-not-be-effective-against-emerging-strains-sars-cov-2
[2] Coronavirus (COVID-19) Update: FDA Limits Use of Certain Monoclonal Antibodies to Treat COVID-19 Due to the Omicron Variant. Pressemitteilung der FDA vom 24. Januar 2023, www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-limits-use-certain-monoclonal-antibodies-treat-covid-19-due-omicron
[3] Böbel M. Ambulante Gabe von monoklonalen Antikörpern in der Frühphase von COVID-19: ein Erfahrungsbericht aus der Hausarztpraxis/Corona-Schwerpunkt-Praxis. Information des Robert Koch-Institut (RKI) vom 25. Februar 2022, www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/COVRIIN_Dok/Erfahrungsbericht_Monoklonale_AK.pdf?__blob=publicationFile
[4] Richter-Kuhlmann E. Monoklonale Antikörper gegen COVID-19: Potenzial bisher nicht ausgeschöpft. Dtsch Arztebl 2021;118(47):A-2209/B-1822
[5] COVID-19: Rückblick und Ausblick. 37. Wissenschaftliches Symposium der Walter-Siegenthaler-Gesellschaft vom 4. bis 5. November 2022 in Köln
[6] Schriftliche Kommunikation mit dem Bundesministerium für Gesundheit (BMG) vom 3. März 2023
[7] Simon N. Der Antikörper-Skandal: Deutschland kaufte hochwirksame Therapien – doch sie werden kaum genutzt. Artikel des „Stern“ vom 1. Dezember 2021, www.stern.de/gesundheit/der-antikoerper-skandal--effektive-corona-therapien-verfallen-30977880.html
[8] Verordnung zur Vergütung der Anwendung von Arzneimitteln mit monoklonalen Antikörpern (Monoklonale-Antikörper-Verordnung – MAKV). Ausfertigung des Bundesministerium der Justiz am 21. April 2021, www.gesetze-im-internet.de/makv/BJNR611210021.html
[9] Bevorratende Apotheken für monoklonale Antikörper (Stern- und Satellitenapotheken (beauftragte Stellen nach § 2 Absatz 1 MedBVSV)). Information des Robert Koch-Institut (RKI) vom 6. April 2022, www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/Therapie/Stern-Satellitenapotheken.pdf?__blob=publicationFil
[10] Postleitzahlen-Tool zur Suche nach Ansprechpartnern zur Therapie mit monoklonalen Antikörpern in Krankenhäusern. Information des Robert Koch-Institut (RKI), Stand Juni 2022, www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/Therapie/Ansprechpartner-MAK.html
[11] Ansprechpartner zur Therapie mit monoklonalen Antikörpern in Krankenhäusern. Information des Robert Koch-Institut (RKI) vom 13. Juni 2022, www.rki.de/DE/Content/InfAZ/N/Neuartiges_Coronavirus/Therapie/Liste_KH.html
[12] Luo S, Zhang J, Kreutzberger AJB et al. Lite An antibody from single human VH-rearranging mouse neutralizes all SARS-CoV-2 variants through BA.5 by inhibiting membrane fusion. Sci Immunol 2022; 7(76), doi: 10.1126/sciimmunol.add5446
[13] Rothgang H und Müller R. Barmer Pflegereport 2022. www.barmer.de/resource/blob/1142760/9ec71d5ae2f750239f74532a33d14490/barmer-pflegereport-2022-bifg-data.pdf
[14] Epidemiologisches Bulletin: Wissenschaftliche Begründung der STIKO zur Aktualisierung der Empfehlung zur SARS-CoV-2-Prä-Expositionsprophylaxe mit Tixagevimab/Cilgavimab (Evusheld). Information des Robert Koch-Institut (RKI), Stand: Februar 2023, edoc.rki.de/bitstream/handle/176904/10772/EB-8-2023-3_Evusheld.pdf?sequence=1&isAllowed=y























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.