
- DAZ.online
- DAZ / AZ
- DAZ 8/2021
- Damit kein Auge trocken ...
Beratung
Damit kein Auge trocken bleibt
Neue Erkenntnisse zur Pathogenese und Therapie der Keratokonjunktivitis sicca
In Deutschland leidet mittlerweile jeder zweite bis dritte Patient einer ophthalmologischen Praxis unter einer Keratokonjunktivitis sicca und assoziierten Symptomen [1]. Genaue epidemiologische Zahlen sind schwierig zu ermitteln, denn viele Betroffene greifen zur Selbstmedikation ohne augenärztliche Kontrolle. Längst gilt das trockene Auge nicht mehr als reine Befindlichkeitsstörung, sondern als multifaktorielle, ernst zu nehmende entzündliche Erkrankung der Augenoberfläche. Typische Symptome sind oft unspezifisch und umfassen Benetzungsstörungen, Trockenheits- und Fremdkörpergefühl, Brennen, Stechen, Juckreiz und Lichtempfindlichkeit. Vor allem im Anfangsstadium kann es durch den chronischen Reizzustand zunächst zu einer reflektorischen Hypersekretion kommen, was für viele Patienten verwirrend ist. Ansonsten finden sich neben einer charakteristischen Bindehautrötung sowie einer Schädigung der Augenoberfläche mit punktförmigen Epitheldefekten oft auch temporale lidkantenparallele konjunktivale Falten. Der am unteren Lidrand stehende Tränensee (Tränenmeniskus) ist reduziert. Hinzu treten häufig Zeichen einer Meibomdrüsendysfunktion (MDD) mit verdickten Lidrändern. Die Ausführungsgänge der Meibomdrüsen sind verstopft mit oft trübem, eingedicktem Drüsensekret, das sich nur mit erheblichem Druck auf das Unterlid ausstreichen lässt. Die infolge der Meibomdrüsendysfunktion mangelhafte Lipidschicht des Tränenfilms verursacht eine erhöhte Tränenverdunstung. In mittelschweren bis schweren Fällen kommt es darüber hinaus zu erheblicher Schädigung der Augenoberfläche, zu massiven Schmerzen und Einschränkungen in der täglichen Lebensführung, auch ergaben Studien eine signifikante Assoziation der Erkrankung mit Depressionen [2, 3, 4].
Klassifikation und Schweregrade
Klinisch wird die Keratokonjunktivitis sicca nach wie vor in zwei Hauptkategorien eingeteilt: eine hyposekretorische Form mit verminderter oder ausbleibender Tränenproduktion und eine hyperevaporative Störung, also eine vermehrte Verdunstung des Tränenfilms. Beide können kontinuierlich ineinander übergehen und Mischformen bilden. Bei 80% der Patienten ist die Lipidphase des Tränenfilms verändert, nur bei 15% die wässrige Phase, die restlichen 5% ergeben sich aus Muzinstörungen. Eingeteilt wird das trockene Auge in vier Schweregrade (mild, moderat, schwer, äußert schwer), wobei die Symptome nicht immer mit den tatsächlichen klinischen Befunden korrelieren. Einige Patienten haben starke Symptome ohne wesentliche klinische Zeichen, während andere mit visusbedrohenden Komplikationen nur ein geringes Beschwerdebild zeigen. Diese Diskrepanz lässt sich zumindest teilweise anhand physiologischer Mechanismen erklären. Zu Beginn oder bei milder Erkrankung tritt häufig eine Hyperalgesie auf, die zu deutlichen Schmerzen oder okulären Symptomen führt, ohne dass bereits eine Gewebsschädigung vorliegt. Bei schweren Fällen oder chronischer Erkrankung besteht dagegen eine verminderte Hornhautsensibilität und zuweilen auch eine Beschädigung sensorischer Neurone der Kornea, so dass die Patienten ihre Symptome als weniger schwer empfinden [2, 3].
Schlüsselmechanismen der Pathophysiologie
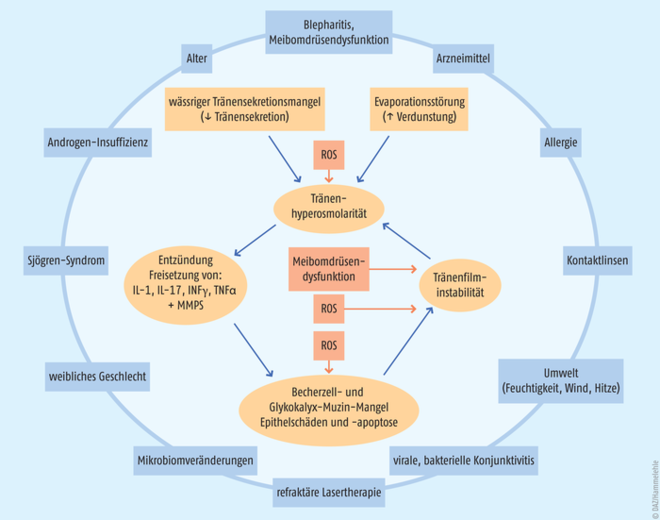
In den letzten Jahren haben sich die Kenntnisse zur Entstehung des trockenen Auges beständig fortentwickelt. Während Tränenstörungen immer noch klassifiziert werden durch mangelnde Tränensekretion oder erhöhte Verdunstung der Tränenflüssigkeit, weisen die Patienten in der Realität zahlreiche Risikofaktoren auf und zeigen mehr als eine pathologische Störung (s. Abb. 1). Vor allem Tränenfilminstabilität, Hyperosmolarität, Entzündung und Beschädigung der Augenoberfläche sowie neurosensorische Anomalien spielen eine entscheidende Rolle. Primär führt eine Dysfunktion der Meibomdrüsen zu einem Lipidmangel und damit zu einer erhöhten Verdunstung sowie einer resultierenden Hyperosmolariät der Tränen. Diese löst eine Entzündungsreaktion in den Oberflächenzellen von Hornhaut und Bindehaut aus: Proinflammatorische Zytokine (z. B. IL-β, IL-6, TNF-α) und Matrix-Metalloproteinasen (MMP-3, MMP-9) führen zu fortlaufender Aktivierung und Einwanderung von Abwehrzellen, vor allem von CD4+-T-Zellen in die Bindehaut und antigenpräsentierenden Zellen in die Hornhaut. Daraufhin werden vermehrt Th1- und Th17-Zellen gebildet, die in der Folge Interferon γ bzw. Interleukin 17 sezernieren, die als kritische Zytokine bei trockenem Auge identifiziert wurden. IL-17 bewirkt Störungen in der Hornhautbarriere und Lymphangiogenese. Interferon γ führt zu einem Rückgang der Becherzellen sowie zur Hochregulation von Chemokinzeptoren und Zelladhäsionsmolekülen, welche den erhöhten Eintritt von Immunzellen in das Gewebe der Augenoberfläche fördern. Insgesamt verursachen die Entzündungsprozesse Epithelschäden und Apoptose, vor allem der Muzin-produzierenden Becherzellen in der Bindehaut, was wiederum die Tränenfilminstabilität verstärkt. Es kommt zu einer erhöhten Osmolarität und zu ausgeweiteten inflammatorischen Prozessen, bis schließlich ein Circulus vitiosus von Oberflächenschädigung und Entzündung entsteht und die Erkrankung weiter fortschreitet. Der chronische Reizzustand am Auge sensibilisiert korneale Nozizeptoren, durch eine Fehlregulation des sensorischen Nervensystems treten zusätzlich Schmerzen auf [2, 5, 6].
Risikofaktoren
Zahlreiche Triggerfaktoren begünstigen die Entstehung der Erkrankung. Beispielsweise setzen reaktive Sauerstoffspezies (ROS) an verschiedenen Stellen die pathologische Kaskade in Gang. Sie erhöhen die Instabilität des Tränenfilms sowie die Osmolarität und schädigen die Becherzellen [8]. Zu den weiteren auslösenden Faktoren zählen vor allem zunehmendes Lebensalter, weibliches Geschlecht, postmenopausale Östrogentherapie, refraktive Chirurgie der Hornhaut, hämopoetische Stammzelltransplantation, Bestrahlung, Vitamin-A-Mangel, Hepatitis C sowie Androgeninsuffizienz. Hinzu kommt die Einnahme bestimmter Medikamente (z. B. Antihistaminika, tricyclische Antidepressiva, SSRI, Diuretika, Betablocker, Isotretinoin, Anticholinergika) sowie eine medikamentöse Augentropfentherapie (Antiglaukomatosa: adrenerge Substanzen, Betablocker, Cholinergika, Carboanhydrasehemmer, Prostaglandine oder Antiallergika, Lokalanästhetika, nichtsteroidale Antirheumatika) oder Konservierungsmittel in Augentropfen. Auch Erkrankungen wie ein Sjögren-Syndrom, Diabetes mellitus oder Rosazea, Umwelteinflüsse (z. B. niedrige Luftfeuchtigkeit), lang anhaltende Bildschirmarbeit mit reduzierter Lidschlagfrequenz und das Tragen von Kontaktlinsen können ein trockenes Auge verstärken [3, 4].
Diagnostik des trockenen Auges
Vor der Diagnosestellung ist eine umfassende Anamnese unerlässlich. Wichtig dabei sind Fragen nach Zeit, Ort und Tagesabhängigkeit der Symptome, Arbeitsplatzbelastung, Tragen von Kontaktlinsen, Allgemeinerkrankungen sowie Medikamenten. Hilfe hierbei bieten standardisierte Fragebögen (z. B. OSDI: Ocular Surface Disease Index, DEQ-5: Dry Eye Questionaire oder SPEED: Standard Patient Evaluation Eye Dryness). Daneben stehen zahlreiche Testverfahren zur Verfügung, etwa Untersuchung der Lider (Lidschlagfrequenz, Lidstellung, Lidschluss, Lidrand), Erfassung der Lidrand-parallelen konjunktivalen Falten zur Einschätzung des Gewebeumbaus durch Entzündungsvorgänge, Vitalfärbungen der Binde- und Hornhaut, Bestimmung der Hornhautsensibilität, Untersuchung des Tränenfilms (Tränenfilmmeniskus zur Analyse des Tränenvolumens, Tränenfilmaufreißzeit als Maß der Stabilität des Tränenfilms) sowie der Schirmer-Test, welcher die Sekretionsleistung der Tränendrüse ermittelt. Als Zusatzuntersuchung kann eine Messung der Osmolarität des Tränenfilms erfolgen, eine Bestimmung der Matrix-Metalloproteinase-9 als Biomarker für Diagnose und Therapieverlauf oder eine Meibographie zur optischen Bestimmung der Drüsenstruktur im Augenlid. Unbedingt erforderlich ist eine Abgrenzung des trockenen Auges zu anderen Oberflächenerkrankungen wie Allergien oder Infektionen sowie der serologische Ausschluss eines Sjögren-Syndroms. Insgesamt sollten in der klinischen Praxis stets nur so viele Tests eingesetzt werden, bis eine zuverlässige Klassifizierung der Benetzungsstörung möglich ist. Nicht alle Untersuchungen sind unbedingt bei jedem Patienten notwendig. Generell sollte mit nicht-invasiven Verfahren begonnen werden, ehe invasive Maßnahmen folgen [1, 2, 3].
Therapie: Step by step
Die Therapie des trockenen Auges erfolgt nach einem Stufenplan (s. Abb. 2) und richtet sich nach dem jeweiligen Schweregrad. Allerdings sollten die verschiedenen Optionen einer Therapiestufe nicht „automatisiert“ eingesetzt werden, sondern sich stets an den individuellen Patientenbedürfnissen orientieren [9].
Abb. 2: Management und Behandlung des trockenen Auges – Stufenschema nach [10]; Kombinationen verschiedener Stufen sind möglich, auch können innerhalb jeder Stufe mehrere Optionen gleichzeitig in Erwägung gezogen werden.
Stufe 1
Jede Behandlung des trockenen Auges sollte mit einer Information des Patienten über Ursachen, Verlauf und grundsätzliche therapeutische Möglichkeiten beginnen. Daneben ist das Wissen um die Risikofaktoren nützlich, um diese möglichst zu vermeiden. Weiterhin ist zu hinterfragen, ob die Augenbeschwerden durch eine Pharmakotherapie bedingt sein könnten. Dann gilt es abzuwägen, welchen Stellenwert die auftretende Störung der Augenoberfläche hat und ob sich die Medikamente umstellen lassen. Zudem ist den Betroffenen eine Omega-3-Fettsäure-reiche Ernährung anzuraten. Omega-3-Fettsäuren blockieren proinflammatorische Eicosanoide und reduzieren Zytokine, sind also antientzündlich wirksam. Eine Metaanalyse ergab darüber hinaus, dass eine Supplementierung mit Omega-3-Fettsäuren (z. B. Omega3-Loges® pflanzlich, Norsan Omega-3 Kapseln) im Vergleich zur Kontrollgruppe zu einer signifikant verlängerten Tränenfilmaufreißzeit und signifikant besseren Ergebnissen im Schirmer-Test führte [2, 8, 11].
Lidrandhygiene: Ein weiterer Therapiebaustein ist die regelmäßige, zweimal täglich durchgeführte Lidrandpflege, mit der vor allem eine Verbesserung der Meibomdrüsenfunktion erreicht werden kann. Sie gliedert sich in die drei wesentlichen Schritte Wärmeapplikation, Lidmassage und Reinigung der Lidkanten. Durch Wärmebrillen oder Gelmasken (z. B. Posiforlid® Augenmaske, Meibopatch® erwärmbare Augenmaske) lässt sich das verhärtete Sekret aufweichen und mit einem angefeuchteten Wattestäbchen in Richtung der Lidrandkante ausstreichen. Anschließend werden die Lidränder mit einem in Reinigungslotion getränkten Wattepad bzw. gebrauchsfertigen Reinigungstüchern (z. B. Blephaclean®, Blephacura®) sanft abgerieben. Bei einem verstärkten Befall mit Demodex-Milben ist ein Behandeln der Lidränder mit Teebaumöl-Präparaten (Wirkstoff: Terpinen-4-ol) angezeigt. In diesem Stadium II sind auch intensivere, physikalische Varianten in der ärztlichen Praxis angebracht, wie die maschinelle abrasive Lidrandreinigung (z. B. BlephEx®), die automatisierte maschinelle Lidwärmung mit gleichzeitiger Meibomdrüsenexpression (z. B. LipiFlow®) und die intensive Lichttherapie (E-Eye® Intense Pulsed Light Therapy), die vor allem bei einer okulären Rosazea empfohlen wird [1, 2].
Künstliche Tränen: Tränenersatzmittel bilden die Basistherapie bei allen Schweregraden des trockenen Auges und sollten grundsätzlich parallel zu jeder weiteren Behandlung angewendet werden. Ein wichtiger Effekt beim Tränenersatz ist die Reduktion der Scherkräfte beim Blinzeln. Hierdurch wird der mechanisch bedingte Entzündungsschub gedämpft. Außerdem erhöhen Tränenersatzmittel die Tränenfilmstabilität und können über ihre symptomlindernde Wirkung auch die Lebensqualität der Patienten steigern. Es steht eine Vielzahl von Präparaten auf Basis von Polyvinylalkoholen, Polyvidonen, Hydroxypropyl-Guar, Zellulosederivaten und Hyaluronsäure zur Verfügung. Gleichzeitig enthaltene Osmoprotektiva (z. B. L-Carnitin und Erythritol in Optive®, Trehalose in Thealoz® Duo) wirken zusätzlich antiinflammatorisch [1, 9]. Je nach Schweregrad werden niedrig-visköse Präparate bis hin zu hochviskösen Gelen und Salben eingesetzt. Patienten, die mehrfach täglich über einen längeren Zeitraum auf Tränenersatzmittel angewiesen sind, sollten unbedingt konservierungsmittelfreie Produkte benutzen. Bei der hyperevaporativen Keratokonjunktivitis sicca mit Meibomdrüsendysfunktion muss mithilfe der künstlichen Tränen außerdem eine Lipidsubstitution erfolgen. Geeignete Formulierungen enthalten mittelkettige Triglyceride (z. B. Artelac® Lipids), Omega-3-Fettsäuren (z. B. EvoTears® Omega, VisuEvo®), Rizinusöl (z. B. Optive® plus, Hylo-Vision® SafeDrop® Lipocur®) oder Phospholipide kombiniert mit Paraffinöl (z. B. Cationorm® MD sine, Systane® Complete). Geeignet sind auch komplett wasserfreie Augentropfen, etwa mit dem Wirkstoff Perfluorohexyloctane (EvoTears®). Alternativ bieten sich liposomale Augensprays auf Basis von Sojalecithin an (z. B. LipoNit® sensitive, TearsAgain® sensitive), die auf das geschlossene Lid appliziert werden.
Stufe 2
Antientzündliche Therapie: Bereits bei einem moderaten trockenen Auge besteht eine (oft subklinische) Entzündungsreaktion im Bereich der Augenoberfläche und der Tränendrüse. Um den Circulus vitiosus von Oberflächenschädigung und Entzündung zu durchbrechen, ist hier eine antientzündliche Therapie notwendig. Die Behandlung erfolgt vor allem topisch, wobei Corticosteroide zwar die Produktion proinflammatorischer Zytokine verringern, wegen der Gefahr eines erhöhten Augeninnendrucks oder Katarakts jedoch maximal kurzzeitig verwendet werden sollten.
Das Makrolid-Antibiotikum Azithromycin (z. B. Azyter® Augentropfen) wird aufgrund seiner antientzündlichen Wirkung im Off-Label-Use bei Blepharitis und Meibomdrüsendysfunktion eingesetzt. Es reduziert die Entzündungsreaktion um die Ausführungsgänge der Meibomdrüsen herum und führt zu einer Lipidanreicherung im Tränenfilm.
Das Immunsuppressivum Ciclosporin A greift in die T-Zell-Aktivierung ein und hemmt so die Produktion proinflammatorischer Zytokine. Darüber hinaus kommt es zur vermehrten Bildung von Tränenflüssigkeit. Ciclosporin-A-Tropfen sind als Fertigprodukt verfügbar (Ikervis® 0,1%) oder können in verschiedenen Formulierungen in der Apotheke hergestellt werden.
Die weiteren Calcineurin-Inhibitoren Tacrolimus (Protopic®) und Pimecrolimus (Elidel®) werden als Hautsalbe bei therapieresistenter Blepharokeratokonjunktivitis ein- bis zweimal täglich auf die Lider appliziert [3, 11]. Zudem ergab eine Studie mit topischen 0,03%-igen Tacrolimus-Augentropfen verbesserte Tränenfilmstabilität und Augenoberflächenparameter bei Patienten mit entzündlichem oder Sjögren-Syndrom-assoziiertem trockenen Auge [12].
Bei obstruktiver Meibomdrüsendysfunktion sind oft orale Tetracycline wirksam, vor allem dann, wenn gleichzeitig eine Rosazea der Gesichtshaut vorliegt. Empfohlen wird eine niedrige Dosis von 40 mg bis 50 mg Doxycyclin pro Tag (z. B. Oraycea®) über einen Anwendungszeitraum von sechs Monaten. Diese Dosierung liegt unterhalb der antibiotischen Wirkschwelle, so dass die antientzündliche und sekretnormalisierende Wirkung dominiert. Doxycyclin reduziert die Synthese und Aktivität von Matrix-Metalloproteinasen sowie die Produktion von Interleukin 1 und Tumor-Nekrose-Faktor im Kornea-Epithel, die Kollagenase-Aktivität und die B-Zell-Aktivierung [11].
Eine nichtmedikamentöse Behandlungsform ist der temporäre Verschluss der Tränenpünktchen mit Punctum Plugs, kleinen Kollagen- oder Silikonstöpseln. Über eine Verzögerung der Tränendrainage soll so eine bessere Befeuchtung des Auges erreicht werden. Die häufigste „Komplikation“ ist ein Verlust des Plugs [3, 11].
Stufe 3
Autologe Serumaugentropfen: Liegt eine schwere Ausprägung des trockenen Auges vor, kann unter anderem die Anwendung von autologen Serumaugentropfen erwogen werden. Die Inhaltsstoffe werden aus dem Blutserum der Patienten gewonnen und später in einer Kochsalzlösung verdünnt. Sie wirken als Tränenersatz und antiinflammatorisch. Die Anwendung erfolgt fünfmal täglich bis stündlich. Eigenserumaugentropfen unterliegen in Deutschland nicht nur dem Arzneimittel-, sondern auch dem Transfusionsgesetz, eine Herstellungserlaubnis ist notwendig [1, 13].
Kontaktlinsen: In schweren Fällen besteht die Möglichkeit, die Oberfläche der Kornea mithilfe von Kontaktlinsen zu schützen und zu befeuchten. Verschiedene Linsenarten werden verwendet, z. B. aus Silikonkautschuk oder harte gasdurchlässige Sklerallinsen. Die Hornhautoberfläche wird bei diesem Linsentyp dauerhaft in einem feuchten Reservoir eigener Tränen „gebadet“ und von mechanischer Belastung durch den Lidschlag abgeschirmt, was die Regeneration der Oberfläche verbessert [3, 11].
Eine weitere Option sind Arzneistoffe, die die Flüssigkeits- bzw. die Muzinsekretion fördern. Mithilfe dieser Eigenschaft können sie dazu beitragen, den Tränenfilm zu stabilisieren und einer Entzündung der Augenoberfläche entgegenzuwirken. Das Muzin-Sekretagogum Diquafosol ist ein P2Y2-Rezeptor-Agonist, der durch die Aktivierung von Chlorid-Kanälen eine drüsenunabhängige Sekretion von Muzin und Wasser induziert. In Japan ist eine topische Formulierung dieses Wirkstoffs seit einigen Jahren für die Behandlung des trockenen Auges zugelassen (Diquas® Ophthalmic Solution 3%), ebenso das Quinolon-Derivat Rebamipide (Mucosta® Ophthalmic Solution 2%). In Deutschland erfolgt eine entsprechende Therapie mit diesen Wirkstoffen im Off-Label-Use im Stadium II. Weitere, systemische Sekretagoga sind die cholinergen Agonisten Cevimelin (Evoxac®, in Europa nicht zugelassen) und Pilocarpin (Salagen®). Beide Wirkstoffe werden beim Sjögren-Syndrom eingesetzt, sie zeigten aber auch positive Effekte beim trockenen Auge. Allerdings muss bei der systemischen Anwendung mit einer Reihe von Nebenwirkungen gerechnet werden, wie Schwitzen, Rhinitis, Schwindel, gastrointestinalen Beschwerden und Kopfschmerzen [1, 11].
Auf einen Blick
- Das trockene Auge gilt nicht mehr als reine Befindlichkeitsstörung, sondern als multifaktorielle, entzündliche Erkrankung der Augenoberfläche.
- Typische Symptome umfassen Benetzungsstörungen, Trockenheits- und Fremdkörpergefühl, Rötung, Brennen, Stechen, Juckreiz und Lichtempfindlichkeit, häufig auch verklebte, entzündete Lidränder.
- Zu den zentralen Krankheitsmechanismen zählen vor allem Tränenfilminstabilität, Hyperosmolarität, Entzündung und Beschädigung der Augenoberfläche sowie neurosensorische Anomalien.
- Zahlreiche extrinsische und intrinsische Triggerfaktoren begünstigen die Entstehung der Erkrankung.
- Die Therapie erfolgt nach einem Stufenplan und richtet sich nach dem jeweiligen Schweregrad.
- Tränenersatzmittel bilden die Basis, ein weiterer Therapiebaustein ist die regelmäßige Lidrandpflege, bestehend aus Wärmeapplikation, Lidmassage und Reinigung der Lidkanten.
- Eine antientzündliche Behandlung erfolgt topisch mit Azithromycin- oder Ciclosporin-Augentropfen oder oral mit Tetracyclinen.
Stufe 4
Für sehr schwere Ausprägungen des trockenen Auges stehen chirurgische Therapieoptionen zur Verfügung. Hierzu zählen neben einem Verschluss der Tränenpünktchen durch Kauterisierung vor allem die chirurgische Korrektur von Fehlstellungen des Augenlides. Bei therapieresistenten Oberflächenstörungen kann eine Amnionmembran-Abdeckung erfolgen, zusätzlich eine Tarsorrhaphie, also eine operative Verkleinerung der Lidspalte durch eine temporale Vernähung des Ober- und Unterlides. Eine selten angewandte und aufwändige Maßnahme ist eine Transplantation von Speicheldrüsen als Tränendrüsenersatz, die jedoch im Langzeitverlauf zu Hornhautödem und exzessivem Tränen führen kann [11].
Fazit und Ausblick
Die Therapie des trockenen Auges hat sich von ausschließlicher Tränenersatztherapie zu einer differenzierten Stufenplanbehandlung entwickelt. Aktuelle Forschungsschwerpunkte befassen sich mit der Pathophysiologie, neuen diagnostischen Verfahren und innovativen Therapiekonzepten.
Wirksamkeit bei trockenem Auge zeigte beispielsweise auch der humane Interleukin-1-Rezeptor-Antagonist Anakinra - eingesetzt als Augentropfen 2,5%, dreimal täglich [14] - sowie der von der FDA zugelassene Arzneistoff Lifitegrast. Dieser Antagonist des Leukozyten-Integrins LFA-1 (Xiidra® Ophthalmic Solution 5%, zweimal täglich) greift in immunologische Entzündungsprozesse des Auges ein, indem er die Interaktion zwischen Integrin LFA-1 und seinem Liganden ICAM-1 blockiert. Außerdem in den USA zugelassen ist ein intranasales Gerät zur Stimulation des nasolakrimalen Reflexes (TruetearTM), das für eine erhöhte Tränensekretion, eine Senkung der Tränenfilmosmolarität sowie eine gesteigerte Lipid- und Muzinsekretion sorgen soll [1]. Als weitere antientzündlich wirkende Substanzen werden zurzeit Neurokinin-1-Rezeptor-Antagonisten erforscht [15]. Zudem könnten auch antiinflammatorisches Curcumin und Probiotika eine zukünftige Therapieoption bei trockenem Auge sein [8]. |
Literatur
[1] Blick zurück nach vorn! Entzündliche Erkrankungen der Augenoberfläche. 25 Jahre Berliner Immunologie-Seminar, 1. Juni 2019, Charité-Universitätsmedizin Berlin, Augenklinik Campus Virchow Klinikum; www.bis-augen.info; Skript_BIS_2019 (1).pdf
[2] TFOS DEWS II – Report 2017. Informationen der Tear Film and Ocular Surface Society Boston (TFOS), www.tfosdewsreport.org/report-tfos_dews_ii_report/36_36/de/, Abruf: 30. Januar 2021
[3] Messmer EM. The pathophysiology, diagnosis and treatment of dry eye disease. Dtsch Ärztebl Int 2015;112: 71–82, doi: 10.3238/arztebl.2015.0071
[4] Kaercher T. Das trockene Auge – Diagnostik und Klassifikation. CME-Fortbildung für Ärzte, mit Unterstützung der Santen GmbH, München, Stand: März 2016, https://studylibde.com/doc/3096979/das-trockene-auge-–-diagnostik-und-klassifikation
[5] Chauhan S, Dana R. Role of Th17 cells in the immunopathogenesis of dry eye disease. Mucosal Immunol 2009;2:375–376, https://doi.org/10.1038/mi.2009
[6] Baudouin C et al. Role of Hyperosmolarity in the Pathogenesis and Management of Dry Eye Disease: Proceedings of the OCEAN Group Meeting. The Ocular Surface 2013;11(4):246-258
[7] Pflugfelder SC, de Paiva CS. The Pathophysiology of Dry Eye Disease: What We Know and Future Directions for Research. Ophthalmology 2017;124(11):4-13, doi: 10.1016/j.ophtha.2017.07.010
[8] Heidari M et al. Das trockene Auge: Neue Ansätze für Diagnostik und Therapie. Kompass Ophthalmol 2020;6:64–75, doi: 10.1159/000507467
[9] Trockenes Auge. Leitlinie des Berufsverbands der Augenärzte Deutschland e. V. (BAV) und der Deutschen Ophthalmologischen Gesellschaft (DOG), Stand: März 2019, www.dog.org/wp-content/uploads/2019/05/Leitlinie_Sicca_2019.pdf,
[10] Dry eye redefined: TFOS Dews II Report. Informationen der Tear Film and Ocular Surface Society Boston (TFOS), www.tfosdewsreport.org/report-management_und_therapie/147_36/de/; Abruf: 30. Januar 2021
[11] Kaercher T. Das trockene Auge – Therapie. CME-Fortbildung für Ärzte, mit Unterstützung der Santen GmbH, München, Stand: September 2016, https://studylibde.com/doc/5651024/das-trockene-auge-–-therapie
[12] Moscovici BK et al. Treatment of Sjögren‘s syndrome dry eye using 0.03% tacrolimus eye drop: Prospective double-blind randomized study. Cont Lens Anterior Eye 2015;38(5): 373-378.
[13] Pan Q et al. Autologous serum eye drops for dry eye. Cochrane Database of Systematic Reviews 2017(2), doi: 10.1002/14651858.CD009327.pub3
[14] Amparo F et al. Topical interleukin 1 receptor antagonist for treatm ent of dry eye disease: A randomized clinical trial, JAMA Ophthalmol 2013;131(6):715-723, doi: 10.1001/jamaophthalmol.2013.195
[15] Man Y et al. Neurokinin-1 Receptor Antagonism Ameliorates Dry Eye Disease by Inhibiting Antigen-Presenting Cell Maturation and T Helper 17 Cell Activation, Am J Pathol 2020;190(1):125-133, doi: 10.1016/j.ajpath.2019.09.020
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.