
- DAZ.online
- DAZ / AZ
- DAZ 8/2021
- Adenovirale ...
Pandemie Spezial
Adenovirale Vektorimpfstoffe unter der Lupe
Das Potenzial und die Herausforderungen viraler „Genfähren“
Die Impfstoffentwicklung begann umgehend, als die ersten genetischen SARS-CoV-2-Genome im Januar 2020 sequenziert und veröffentlicht worden waren. Mittlerweile sind weltweit über 180 Impfstoffkandidaten gegen das Coronavirus in Entwicklung, welche meist auf dem SARS-CoV-2-Spike-Protein basieren [Krammer F, 2020]. Das Spike-Protein befindet sich auf dem Virion und leitet die zelluläre Infektion durch Bindung an den zellulären SARS-CoV-2-Rezeptor ACE2 ein. Spike-basierte Impfstoffe eignen sich daher, um virusneutralisierende Antikörper zu induzieren und auf diese Weise eine virale Infektion zu verhindern oder stark abzumildern. Bereits im Sommer 2020 konnten erste erfolgversprechende klinische Studien zeigen, dass mRNA- und Adenovirusvektor-basierte Impfungen häufig hohe anti-Spike-spezifische IgG-Antikörpertiter induzieren – oftmals höher als nach einer natürlichen SARS-CoV-2-Infektion. Diese Antikörperantworten neutralisierten das Virus in vitro, ein erstes wichtiges Signal dafür, dass eine Immunisierung mit solchen Impfstoffkandidaten möglich sein sollte [Jackson LA et al., 2020, Mulligan MJ et al., 2020, Logunov DY et al., 2020]. In etwa zeitgleich konnte in einem für die Europäische Arzneimittel-Agentur (EMA) relevanten Infektionsmodell gezeigt werden, dass solche impfinduzierten, neutralisierenden Antikörperantworten in Makaken mit einem Schutz der unteren Atemwege vor einer SARS-CoV-2-Virusinfektion korrelieren [Mercado NB et al., 2020]. Kurze Zeit später wurden ähnlich hohe Antikörper- und T- Zellantworten auch für eine weitere Adenovirusvektor-basierte Impfung mit ChAdOx1 nCoV-19 (AstraZeneca/Universität Oxford) gezeigt [Folegatti PM et al., 2020]. Russische Behörden ließen – vermutlich basierend auf den von Logunov dann publizierten Daten – ihren Adenovirus-basierten Impfstoff Sputnik V bereits im Sommer 2020 zu, noch bevor erste klinische Effizienzdaten vorliegen konnten. Bis Ende Januar 2021 wurde dann von einer ganzen Reihe an Impfstoffkandidaten eine Schutzwirkung vor COVID-19 in Größenordnungen von 50% bis 95% bekannt gegeben. Drei Impfstoffe, ein mRNA-Impfstoff der Firmen Biontech/Pfizer, ein mRNA-Imfpstoff von Moderna und der Adenovirusvektor-basierte Impfstoff von AstraZeneca, erhielten schließlich auch in der Europäischen Union (EU) von der EMA eine bedingte Zulassung. Mit der bedingten Zulassung eines weiteren Adenovirusvektor-basierten Impfstoffes von Janssen/Johnson&Johnson wird in Kürze gerechnet. Während mRNA-basierte Impfstoffe mit ca. 95% Effizienz vor einer COVID-19-Erkrankung schützen sollen, zeigte sich bei den Adenovirus-basierten Impfstoffen Schutzwirkungen zwischen 70% und 92% [Logunov DY et al., 2021, Voysey M et al., 2020].
Pluspunkte für vektorbasierte Impfstoffe
Ein Vorteil von vektorbasierten gegenüber mRNA-basierten Impfstoffen ist, dass es bereits über mehr als zwei Jahrzehnte klinische Erfahrungen mit ihnen gibt und sie sich in den dazu durchgeführten Studien weitestgehend als sehr sicher erwiesen haben. Sie wurden teilweise bereits in frühem Kindesalter getestet. Auch ihre im Vergleich zu den mRNA-Impfstoffen größere Thermostabilität und einfachere Handhabung sprechen für solche Impfstoffe.
Vor allem adenovirale Vektoren weisen eine Reihe von wünschenswerten Eigenschaften auf, die sie für Impfstoffanwendungen besonders prädestinieren. Ihr Genom ist stabil und leicht zu manipulieren. Sie können unter Verwendung verschiedener komplementärer Zelllinien, die den Verfahren der guten klinischen Praxis (GCP) entsprechen, amplifiziert und zu hohen Titern hergestellt werden. Bisher wurden unterschiedliche adenovirale Vektoren in zahlreichen klinischen Studien am Menschen und unterschiedlichen Zielpopulationen getestet (n >130, clinicaltrials.gov, other terms „adenovirus vaccines“, „completed“ or „recruiting“), mit einer insgesamt hervorragenden Bilanz hinsichtlich ihrer Sicherheit und Immunogenität [Coughlan L, 2020].
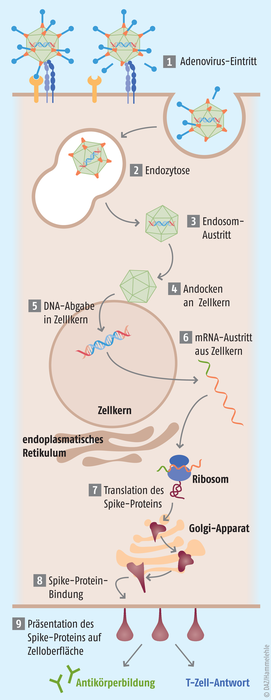
Abb.: Adenovirus-basierte Vektorimpfstoffe, die eine Immunantwort gegen das SARS-CoV-2-SPIKE-Protein induzieren.
Das Prinzip der viralen Vektoren
Virale Vektoren wie auch mRNA-Impfstoffe ermöglichen es, Impfantigene in vivo (= im Körper) zu exprimieren, um so eine Impfantigen-spezifische adaptive Immunantwort zu induzieren (Abb.). Dies geschieht im Kontext der natürlichen, angeborenen Immunantwort gegen den viralen Impfvektor (bzw. gegen die mRNA-Impfung), was als natürliches Adjuvans wirken. Adjuvanzien verstärken eine impfinduzierte Immunantwort auf unspezifische Art und Weise. So werden die Virusproteine nach Impfung durch dieselbe zelluläre Proteinexpressionsmaschinerie im endoplasmatischen Retikulum und im Golgi-Apparat prozessiert wie während einer natürlichen Virusinfektion. Die Glykosylierungsmuster von impfkodierten Immunogenen und solchen, die im Rahmen einer bestimmten natürlichen Virusinfektion entstehen, sind deswegen sehr ähnlich bis identisch. Dies ist wichtig, da die Immunogenizität eines Proteins stark vom Glykosylierungsmuster beeinflusst werden kann. Auch die Proteinstruktur und Aminosäuresequenz kann man durch gezieltes Impfstoffdesign – zum Beispiel durch Einführen bestimmter Punktmutationen – modulieren und optimieren. So basieren viele der aktuellen SARS-CoV-2-RNA- und vektorbasierten Impfstoffe auf einer stabilisierten Spike-Proteinvariante, bei der die Gensequenz so modifiziert wurde, dass
- die In-vivo-Expression durch sogenannte Codon-Optimierung für den Menschen verbessert wurde sowie
- das virale Spike-Protein durch Mutation der Furin-Schnittstelle in voller Länge stabil hergestellt und die Proteinstruktur durch zwei „Prolin-Mutationen“ noch zusätzlich in einer „Prä-fusions“-Struktur stabilisiert wurde [Wrapp D et al., 2020, Pallesen J et al., 2017]. Auf diese Weise gleicht das Spike-Immunogen der natürlichen viralen Spike-Proteinvariante auf dem SARS-CoV-2-Virion vor der Zellinfektion nicht nur in der Aminosäuresequenz, sondern auch in der Proteinstruktur und im Glykosylierungsmuster. Durch Punktmutationen in der Immunogensequenz werden zum Beispiel auch in therapeutischen HP-16-Impfstoffen onkogene Proteinbereiche der Impfantigene E6 und E7 gezielt unschädlich gemacht. Dass solches Immunogendesign entscheidend zur Wirksamkeit von SARS-CoV-2-Impfungen beitragen kann, wurde in einem wegweisenden Experiment gezeigt: Makaken wurden mit verschiedenen Ad26-kodierenden-Spike-Proteinvarianten gegen SARS-CoV-2 geimpft, welche sich im genauen Spike- Immunogendesign unterschieden. Diese Proteinvarianten unterschieden sich unter anderem darin, ob sie – wie oben beschrieben – stabilisiert waren, ob sie zellmembranständig exprimiert werden, oder nach Deletion der Transmembran- und zytoplasmatischen Domäne von der Zelle sekretiert wurden. Lediglich die oben erwähnte „zwei Prolin-stabilisierte“, zellmembranständige Immunogenvariante schützte die Affen komplett vor einer SARS-CoV-2-Infektion der unteren Atemwege und genau diese Variante ist wie nun bekannt auch im Menschen hochwirksam [Mercado et al., 2020].
Natürlicher Selektionsdruck begünstigt bei vielen RNA-Viren die Bildung von „Immun-Escapemutationen“ welche die Immunerkennung abschwächen und auch die Impfwirkung beeinträchtigen können. Besonders ausgeprägt ist dies bei HIV, jedoch scheint die Immunerkennung und Impfwirksamkeit auch bei bestimmten SARS-CoV-2-Varianten wie der südafrikanischen Variante B.1.351 beeinträchtigt zu sein. Eine besonders breite Immunerkennung des Virus und seiner Varianten durch das adaptive Immunsystem ist in solchen Fällen höchst wünschenswert. Eine Strategie ist es hier, mit Hilfe des Computers Mosaik-Immunogen-Sequenzen so zu designen, dass die Immunerkennung verschiedener Virusvarianten optimiert wird [Barouch DH et al., 2018]. Abgesehen davon könnten mehrere Immunogenvarianten in einem Vektor – polycistronisch - oder in mehreren Vektoren gleichzeitig verimpft werden [Kibuuka H et al., 2010].
Vielfältige virale Impfvektoren
Es gibt eine Vielzahl an verschiedenen Viren, die sich zur Herstellung von viralen Impfvektoren eignen [Afrough B et al., 2019, Kimpel J, Geldmacher C, 2019]. Verschiedene Faktoren beeinflussen die Wahl eines bestimmten viralen Vektors für eine spezifische klinische Anwendung oder Impfung. Wichtig sind die Kapazität des Impfvektors für fremde „transgene“ Impfantigene, nachgewiesene genetische Stabilität, sowie Daten zur Toxizität/Biodistribution und Wirksamkeit in einem oder mehreren relevanten Tiermodellen nach Impfung. Daten zu diesen wichtigen Parametern müssen von den regulatorischen Behörden begutachtet werden, bevor eine neue experimentelle Impfung erstmals in Menschen getestet werden darf. Soweit vorhanden sind Daten zum klinischen Sicherheitsprofil eines Vektors natürlich extrem wünschenswert, ebenso klinische Daten zur Qualität, Quantität, Dauer und antiviralen Effizienz der induzierten Immunreaktion. Des Weiteren spielen Kosten der Produktion und gegebenenfalls bereits vorhandene vektorspezifische Immunantworten in der Zielpopulation eine Rolle für die Auswahl eines bestimmten Vektors (siehe unten).
Virale Impfvektoren können entweder replikationskompetent sein, wie der 2019 in der EU zugelassene Ebolavirus- Impfstoff VSV-ZEBOV (Handelsname; Ervebo® von Merck). Sie sind jedoch meist replikationsinkompetent, wie die adenoviralen und pockenviralen Vektoren aus der Impfstoffkombination aus Zabdeno (Ad26.ZEBOV) und Mvabea (MVA-BN-Filo), welche kürzlich in der EU als Impfstoffe gegen Ebola zugelassen wurden. Impfvektoren können auf RNA- (z. B. VSV oder Masernviren) oder auf DNA-Viren (z. B. Pockenviren oder Adenoviren) basieren, eine Hülle haben (z. B. VSV oder Pockenviren) oder auch unbehüllt sein (z. B. Adenoviren), zur Transfektion des Zellkerns (z. B. adenovirale Vektoren) oder auch nur des Zytoplasmas (z. B. sämtliche RNA-Viren und Pockenviren) führen.
Adenovirale Vektoren
Adenovirale Vektoren werden seit mehr als 20 Jahren klinisch charakterisiert und erweisen sich seither als hochimmunogen – sowohl zur Induktion von T-Zell- als auch von Antikörper-vermittelten adaptiven Immunantworten gegen das transgene Immunogen. Die solchen Vektoren zugrunde liegenden ikosaedrischen Adenoviren sind unbehüllt (Abb.). Über 300 unterschiedliche Adenovirustypen wurden bisher beschrieben. Das Viruskapsid besteht aus drei Hauptstrukturproteinen: dem Faserprotein, dem Penton- und dem Hexonprotein und beinhaltet ein doppelsträngiges DNA-Genom von 26 bis 45 kb.
Besonders rekombinante-Adenovirus-5(rAd5)-basierte Vektoren sind gut charakterisiert und kamen bisher vor allem in der HIV-Impfstoffforschung, aber auch als Ebola-Impfung zum Einsatz, da sie auch eine starke zelluläre Immunantwort induzieren können. Der klassische Eintrittsweg dieser rAd5-basierten Vektoren wird durch Bindung der Faserknopfdomäne an den Coxsackie- und Adenovirus-Rezeptor (CAR) vermittelt, welche die Virusinternalisierung initiiert. Ad5-basierte Vektoren haben einen breiten Gewebetropismus, da der CAR-Rezeptor in unterschiedlichen Geweben exprimiert wird. rAD5-Vektoren können replizierende und nichtreplizierende Zellen infizieren. Über Rezeptornutzung und Tropismus seltenerer oder nicht menschlicher Adenovirustypen ist jedoch weniger bekannt [Coughlan L, 2020]. Auch weitere zelluläre Rezeptoren können eine zelluläre Infektion durch Adenoviren ermöglichen, zum Beispiel auf professionellen antigenpräsentierenden Zellen wie den sogenannten dendritischen Zellen, die für die Initiierung einer adaptiven T-Zellantwort und daraus resultierender Immunität von zentraler Bedeutung sind. Nach dem Entweichen aus den intrazellulären Endosomen wird das Virion über das Zellskelett zum Zellkern transportiert, wo die virale DNA freigesetzt und die Transgenexpression ermöglicht wird. Die Gefahr einer malignen Transformation durch Vektor-DNA-Integration wird als extrem gering eingeschätzt [Jötten F, 2021].
Rekombinante Adenovirus(rAd)-Vektoren werden durch eine Deletion des essenziellen viralen Gens E1 replikationsinkompetent gemacht. Eine weitere Deletion der E3-Region ermöglicht es, heterologe Transgene (immunogene Bereiche eines bestimmten Krankheitserregers) von bis zu ~ 7,5 kbp mittels Standardklonierungsverfahren einzusetzen um sie dann in vivo zu exprimieren. Ein Beispiel wäre das ca. 3,5 kb große SARS-CoV-2-Spike-Gen, oder auch polycistronische Genkassetten. Letztere sind aus mehreren Genen zusammengesetzt und können für weitere Antigene eines Krankheitserregers kodieren.
Von den bisher beschriebenen humanen und nicht humanen Adenovirustypen, werden im Moment vor allem die humanen Adenoviren Typen 5, 26 sowie der von Schimpansenviren abgeleitete Vektor ChAdY25 (=ChAdOx1) als Vektoren in zugelassenen Impfstoffen genutzt. Es gibt jedoch eine Reihe von weiteren adenoviralen Vektoren, welche bereits in klinischen Studien getestet werden.
Immunogenizität und Seroprävalenz bestimmen Auswahl
Die Auswahl eines bestimmten Adenovirustypen wird maßgeblich von der Immunogenizität und der Seroprävalenz in der Bevölkerung bestimmt. Die Seroprävalenz bezeichnet die Prozentzahl der Personen, welche bereits Antikörper gegen einen Adenovirustyp haben.
rAd5-basierte Impfungen (z. B. Sputnik V, Russland; Convidicea, China) zeichnen sich durch eine hohe Kapazität zur Induktion Antigen-spezifischer T-Zell- als auch Antikörperantworten aus [Abbink P et al., 2007] und gelten deswegen als „Immunogenizitäts“-Maßstab für weitere Ad-basierte Vektoren. Ein Nachteil der Ad5-basierten Vektoren ist jedoch eine vergleichsweise hohe Seroprävalenz von anti-Ad5-spezifischen Antikörpern in weiten Teilen der globalen Bevölkerung, welche sich negativ auf die Impfreaktion auswirken kann und auch auf die Impfungssicherheit (siehe unten). So haben in den meisten globalen Regionen mehr als 50% der untersuchten Bevölkerung nachweisbare Anti-Ad5-Antikörpertiter im Serum – zum Teil auch hohe Titer. Aus diesen Gründen werden eine Reihe von weiteren humanen und nicht-humanen Adenovirentypen auf Eignung zum Impfvektor getestet [Abbink P et al., 2007, Barouch DH et al., 2011, Coughlan L, 2020]. Aufgrund der vergleichsweise niedrigen globalen Seroprävalenz gepaart mit starker Immunogenizität im Menschen gehören Ad26-basierte Vektorimpfstoffe im Moment zu den vielversprechendsten Adenovirus-basierten Impfstoffen. Sie wurden oder werden derzeit gegen Ebola, SARS-CoV-2 (Ad26.COV2., Janssen/Johnson&Johnson USA) und HIV entwickelt. Auch Schimpansen-Adenoviren-basierte Vektoren, wie der ChadOx1 (AZD1222, AstraZeneca), sind prinzipiell vielversprechend, da es gegen diese keine vorbestehende Immunität im Menschen geben sollte und im Menschen eine starke immunogen-spezifische T-Zellantwort induziert wird [Folegatti PM et al., 2020].
Problem: vektorspezifische Immunantworten
Wie sich präexistierende vektorspezifische Antikörper auf die induzierte Immunantwort gegen das transgene Immunogen auswirken, ist Gegenstand intensiver Forschung. Der Einfluss von vorbestehenden rAd5-neutralisierenden Antikörpertitern auf die impfinduzierten Immunantworten im Menschen wurde meist im Kontext von HIV-Impfstudien untersucht. Diese hatten einen negativen Effekt auf die impfinduzierte HIV-spezifische Immunantwort, vor allem dann, wenn lediglich rAd5-HIV verimpft wurde und hohe Anti-rAd5-Titer vorlagen [Kibuuka H et al., 2010]. Präexistierende anti-Ad5-spezifische Antikörper hatten jedoch noch einen weiteren, unerwarteten Effekt. In den Phase-IIb/III-Studien „Step“- und „Phambili“ kam es zu vermehrten HIV-Infektionen [Gray G et al., 2010] mit einem drei- bis vierfach höheren Risiko in unbeschnittenen, geimpften Männern versus Placebo. Dieses rAD5-impfassoziierte HIV-Risiko betraf ausschließlich Männer [Moodie Z et al., 2015], und vor allem solche, die vor Immunisierung höhere Anti-Ad5-Titer hatten. Dieses Potenzial, möglicherweise die HIV-Empfänglichkeit bei männlichen Impfstoffempfängern zu erhöhen, konnte durch vorherige klinische Studien der Phase I/IIa nicht vorhergesagt werden. In großen Phase-IIb- und -III-HIV-Impfstoffstudien werden in der Regel ausschließlich Probanden mit einem Hochrisikoprofil für HIV-Infektionen rekrutiert. Deswegen mag dieses Ergebnis für Frauen und auch für viele Männer mit geringem HIV-Risikoprofil nicht besonders relevant sein. Dennoch muss bei der Anwendung von aktuellen Ad5-basierten Impfstoffen gegen SARS-CoV-2 – wie dem russischem Sputnik-Impfstoff – berücksichtigt werden, dass diese möglicherweise das Risiko für HIV-Infektionen in Männern erhöhen könnten. Inwiefern dies auch für weitere Adenovirus-basierte Vektoren gelten könnte, ist nicht bekannt und sollte nach Zulassung solcher Impfstoffe weiter untersucht werden. Es gibt eine Reihe von Studien und Erklärungsversuchen für dieses Phänomen, unter anderem dass präexistierende Adenovirus-spezifische T-Helferzellen durch die Impfung aktiviert wurden und dadurch leichter von HIV infiziert werden konnten [Buchbinder SP et al., 2020].
Niedrige präexistierende Ad26-spezifische Antikörper-Spiegel scheinen im Tiermodell keinen besonders negativen Einfluss auf die Immunantwort gegen Ad26-kodierte Immunogene zu haben [Barouch DH, Vaccine 2011]. Auch wurde bisher kein deutlicher Einfluss der natürlichen oder vektorinduzierten vorbestehenden Immunität gegen Ad26 auf die Immunogenität des Impfstoffs beobachtet. Ergebnisse aus klinischen Studien, in denen die wiederholte Verabreichung von Ad26-basierten Impfansätzen bewertet wurde, zeigten zudem, dass eine zweite oder nachfolgende Dosis des Studienimpfstoffs die humoralen und zellulären Immunantworten deutlich verstärken konnte [Custers et al., 2020]. Um das Problem der vektorspezifischen Immunantwort zu umgehen, werden virale Vektoren auch häufig in heterologen Prime-/Boost-Kombinationen verwendet, weil eine zweite Impfung mit replikationsinkompetenten Impfvektoren die Immunität gegen das Zielpathogen weiter verbessert. Dabei kann der Kombinationspartner entweder ein weiterer viraler Vektor sein, oder es können nicht-virale Impfstoffe (DNA, RNA, Protein, Peptide) verwendet werden [Kimpel J, Geldmacher C, 2019].
Auf einen Blick
- Virale Vektoren werden zum gezielten Einschleusen von genetischer Information eingesetzt.
- Impfvektoren können auf RNA- (z. B. VSV oder Masernviren) oder auf DNA-Viren (z. B. Pockenviren oder Adenoviren) basieren, eine Hülle haben (z. B. VSV oder Pockenviren) oder auch unbehüllt sein (z. B. Adenoviren), zur Transfektion des Zellkerns (z. B. adenovirale Vektoren) oder auch nur des Zytoplasmas (z. B. sämtliche RNA-Viren und Pockenviren) führen.
- Adenovirale Vektoren weisen ein stabiles Genom auf und sind leicht zu manipulieren. Unterschiedliche adenovirale Vektoren wurden in zahlreichen klinischen Studien am Menschen erfolgreich getestet.
- Für die Immunisierung gegen SARS-CoV-2 werden die humanen Adenoviren Typen 5 (Sputnik V) und 26 (Johnson&Johnson) sowie der von Schimpansenviren abgeleitete Vektor ChAdY25 (=ChAdOx1) (AstraZeneca) genutzt.
- Für den Erfolg einer Immunisierung mit adenoviralen Vektoren sollte das Immunsystem nach Möglichkeit noch nicht mit dem als Vektor genutzten Virus in Kontakt gekommen sein.
- Vor diesem Hintergrund spielen vektorspezifische Immunantworten eine Rolle. Sie können sich bei Verwendung des gleichen Vektors für die Zweitimpfung negativ auswirken. Durch Verwendung unterschiedlicher Vektoren für die Prime- und Boosterimmunisierung (Sputnik V) kann das Problem umgangen werden. Ungeachtet dessen ist eine Boosterimpfung mit dem gleichen Vektor immer noch besser für die Höhe der Immunogen-spezifischen Immunantwort als keine, auch wenn Vektor-spezifische Immunität besteht.
Fazit
Die Fortschritte auf dem Forschungsgebiet der vektorbasierten Impfstoffe während der letzten zwei Dekaden sind wirklich bemerkenswert und beruhen zu einem Teil auf der HIV- und Ebola-Impfstoffforschung. Dies bildete eine gute Grundlage für die vergleichsweise schnelle Entwicklung und Zulassung von vektorbasierten SARS-CoV-2-Impfungen. Wichtige Bereiche der Impfstoffforschung beinhalten gezieltes Vektor- und Immunogendesign sowie die darauffolgende präklinische und klinische Charakterisierung solch optimierter Impfungen in Bezug auf Sicherheit und Immunogenizität. Eine gute internationale Zusammenarbeit zwischen akademischen Institutionen, der forschenden Industrie und der regulatorischen Behörden ist hier von großer Bedeutung. Eine Verbesserung der gesetzlichen Rahmenbedingungen in Europa wäre sehr wünschenswert; so behindert z. B. die Datenschutz-Grundverordnung (DSGVO) in ihrer derzeitigen Form häufig die nationale und internationale wissenschaftliche Kollaboration, indem Datenaustausch selbst verschlüsselter Probandendaten verboten bzw. stark erschwert wird (wenn nicht von vorneherein geplant).
Ein vektorbasierter Impfstoff spielte bereits bei der Eindämmung der großen Ebola-Epidemie im Ost-Kongo von 2018/19 inmitten eines schwelenden, kriegerischen Konflikts eine wichtige Rolle – ein sehr schwieriges Unterfangen. Jetzt kommt vektor- und RNA-basierten Impfungen im globalen Kampf zur Eindämmung der SARS-CoV-2-Epidemie eine zentrale Rolle zu. Erstmals werden Millionen von Menschen in der ganzen Welt mit solchen Impfstoffen geimpft. Post-Marketing-Studien kommt nun eine wichtige Bedeutung zu, um Effizienz gegen bestimmte Virusmutanten zu studieren, sowie seltene Nebenwirkungen zu identifizieren. Die Schnelligkeit der Entwicklung gepaart mit der nun nachgewiesenen hohen Effizienz dieser Impfstoffe gegen COVID-19 zeigt, wie wichtig die neuartigen Impfstoffe in pandemischen Situationen neuartigere Erreger sein können und dass sich Investitionen in die Impfstoffforschung und Produktionskapazität in Europa und anderswo höchstgradig auszahlen. |
Literatur
Abbink P et al. Comparative seroprevalence and immunogenicity of six rare serotype recombinant adenovirus vaccine vectors from subgroups B and D. J Virol, 2007;81:4654-63
Afrough B, Dowall S, Hewson R. Emerging viruses and current strategies for vaccine intervention. Clin Exp Immunol, 2019;196:157-166
Barouch DH et al. International seroepidemiology of adenovirus serotypes 5, 26, 35, and 48 in pediatric and adult populations. Vaccine, 2011;29:5203-9
Barouch DH et al. Evaluation of a mosaic HIV-1 vaccine in a multicentre, randomised, double-blind, placebo-controlled, phase 1/2a clinical trial (Approach) and in rhesus monkeys (NHP 13-19). Lancet, 2018;392:232-243
Buchbinder SP et al. Use of adenovirus type-5 vectored vaccines: a cautionary tale. Lancet, 2020;396:e68-e69
Coughlan L. Factors Which Contribute to the Immunogenicity of Non-replicating Adenoviral Vectored Vaccines. Front Immunol, 2020;11:909
Custers J et al. Vaccines based on replication incompetent Ad26 viral vectors: Standardized template with key considerations for a risk/benefit assessment. doi: 10.1016/j.vaccine.2020.09.018 [Epub ahead of print] PMCID: PMC7532807
Folegatti PM et al. Safety and immunogenicity of the ChAdOx1 nCoV-19 vaccine against SARS-CoV-2: a preliminary report of a phase 1/2, single-blind, randomised controlled trial. Lancet, 2020;396:467-478
Gray G, Buchbinder S, Duerr A. Overview of STEP and Phambili trial results: two phase IIb test-of-concept studies investigating the efficacy of MRK adenovirus type 5 gag/pol/nef subtype B HIV vaccine. Curr Opin HIV AIDS, 2010;5:357-61
Jackson LA et al. An mRNA Vaccine against SARS-CoV-2 - Preliminary Report. N Engl J Med, 2020;383:1920-1931
Jötten F. Wird Adenovirus-DNA ins Genom eingebaut? Spektrum.de 17.02.21. www.spektrum.de/news/vektor-impfstoff-wird-adenovirus-dna-ins-genom-eingebaut/1835725#Echobox=1613545962?utm_source=pocket-newtab-global-de-DE
Kibuuka H et al. A phase 1/2 study of a multiclade HIV-1 DNA plasmid prime and recombinant adenovirus serotype 5 boost vaccine in HIV-Uninfected East Africans (RV 172). J Infect Dis, 2010;201:600-7
Kimpel J, Geldmacher C. Desing und Funktionsweise von Vektorbasierten Impfstoffen. Trillium 2019, Nr. 3
Krammer F. SARS-CoV-2 vaccines in development. Nature, 2020;586:516-527
Logunov DY et al. Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet 2021
Logunov DY et al. Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia. Lancet, 2020;396:887-897
Mercado NB et al. Single-shot Ad26 vaccine protects against SARS-CoV-2 in rhesus macaques. Nature, 2020;586:583-588
Moodie Z et al. Continued Follow-Up of Phambili Phase 2b Randomized HIV-1 Vaccine Trial Participants Supports Increased HIV-1 Acquisition among Vaccinated Men. PLoS One, 10, e0137666, 2015
Mulligan MJ et al. . Phase I/II study of COVID-19 RNA vaccine BNT162b1 in adults. Nature, 2020;586:589-593
Pallesen J et al. Immunogenicity and structures of a rationally designed prefusion MERS-CoV spike antigen. Proc Natl Acad Sci U S A, 2017;114:E7348-E7357
Voysey M et al. Safety and efficacy of the ChAdOx1 nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four randomised controlled trials in Brazil, South Africa, and the UK. Lancet 2020, doi: 10.1016/S0140-6736(20)32661-1
Wrapp D et al. Cryo-EM structure of the 2019-nCoV spike in the prefusion conformation. Science, 2020;367:1260-1263
Weitere Beiträge des Pandemie Spezials in DAZ 2021, Nr. 8
- Mit Fakten gegen Mythen: Wissenswertes rund um die SARS-CoV-2-Antigen-Schnelltests in Apotheken
- Impfreaktionen wie erwartet: Das Paul-Ehrlich-Institut gibt in Sachen AstraZeneca-Impfstoff Entwarnung
- Nicht jeder ist für eine Impfung geeignet: Was vor einer COVID-19-Impfung zu beachten ist
- Corona-Ticker: Neues zu SARS-CoV-2 in Kürze























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.