
- DAZ.online
- DAZ / AZ
- DAZ 26/2021
- Das Sehvermögen erhalten
Diabetes mellitus
Das Sehvermögen erhalten
Diabetes-Komplikationen am Auge sind therapierbar – wenn man sie rechtzeitig erkennt
Bei chronisch hohen Blutzuckerwerten infolge eines noch unerkannten oder ungenügend eingestellten Diabetes reagiert Glukose nichtenzymatisch mit verschiedenen Proteinen wie Hämoglobin und Gefäßproteinen (Glykierung). Dies führt zur Veränderung der Struktur und Funktion der betroffenen Eiweiße und ist ein wichtiger Ausgangspunkt für pathologische Veränderungen (Mikroangiopathien) der terminalen Blutgefäße in den Nieren und in der Netzhaut des Auges (Retina). Neben einer Hyperglykämie sind noch weitere Risikofaktoren für diabetische Netzhautveränderungen wie Sauerstoffmangel oder Entzündungen bekannt.
Endstation Makulaödem
Typisch für Netzhaut-Mikroangiopathien sind vor allem eine gesteigerte Kapillarpermeabilität, Kapillarverschlüsse und eine Neubildung retinaler Gefäße. Bei diesen Veränderungen, die unter dem Begriff diabetische Retinopathie zusammengefasst werden, unterscheidet man proliferative und nichtproliferative Stadien, die in unterschiedlichen Schweregraden auftreten können. Eine nichtproliferative Retinopathie ist gekennzeichnet durch Störungen der inneren Blut-Retina-Schranke und den Verschluss von Retinagefäßen. Dagegen kommt es bei der proliferativen diabetischen Retinopathie infolge der Ausschüttung von Wachstumsfaktoren zur Neubildung von brüchigen Gefäßen, die ein hohes Blutungsrisiko aufweisen. Wenn der Augenarzt bei der Untersuchung des Augenhintergrundes feststellt, dass von den pathologischen Veränderungen auch die Macula lutea (gelber Fleck), der Ort des schärfsten Sehens in der Retina, betroffen ist, lautet die Diagnose diabetische Makulopathie. Ein diabetisches Makulaödem entsteht, wenn im Bereich der Macula lutea Flüssigkeit aus den Diabetes-geschädigten Blutgefäßen austritt. Es kommt zu Schwellungen und gegebenenfalls Ablagerungen von Lipiden (harte Exsudate). Ein Makulaödem ist die häufigste Ursache für den Sehschärfeverlust bei Diabetikern. Sie kann bis zur Erblindung führen. In etwa 60% der Fälle sind beide Augen betroffen.
Lernziele
In diesem Beitrag erfahren Sie,
- welche Ursachen zu diabetischen Netzhautveränderungen führen,
- welche Symptome typisch für diabetische Netzhautveränderungen sind,
- mit welchen diagnostischen Methoden die Netzhaut untersucht werden kann,
- welche Arzneimittel und weitere Behandlungsverfahren eingesetzt werden,
- welche Nebenwirkungen dabei auftreten können,
- welche Wirkstoffe gegen das diabetische Auge derzeit in Studien geprüft werden.
Typische Symptome
Der Sehverlust bei diabetischen Netzhautkomplikationen entwickelt sich meistens schleichend und ist nicht mit Schmerzen verbunden. Eine Ausnahme bildet die Glaskörperblutung, bei der die Seheinschränkung abrupt einsetzt und weitere Beschwerden wie eine rötliche Verfärbung des Gesichtsfeldes auftreten. Glaskörperblutungen zählen neben Netzhautablösungen zu den schweren Komplikationen einer proliferativen diabetischen Retinopathie.
Warnzeichen, die auf Netzhautkomplikationen hindeuten und eine zeitnahe Vorstellung beim Augenarzt erfordern, sind vor allem:
- Verschwommensehen und verzerrtes Sehen
- Sehverschlechterungen, die nicht durch eine Brille behoben werden können
- Störungen des Farbensehens
- Leseschwierigkeiten
- Rußregen (bei Glaskörperblutungen)
Von diesen Symptomen abzugrenzen sind Sehstörungen, die auf Blutzuckerschwankungen zurückzuführen sind. Dabei variiert die Brechkraft der Augenlinsen durch unterschiedliche Quellzustände infolge osmotischer Effekte. Wenn Diabetiker über eine zunehmende Blendempfindlichkeit, ein verringertes Kontrastsehen oder Doppel- oder Mehrfachbilder berichten, deutet das nicht auf Retinaveränderungen, sondern auf einen Katarakt (grauer Star) hin. Von dieser Linsentrübung sind Diabetiker in der Regel früher betroffen als Nichtdiabetiker. Es wird deshalb empfohlen, dass Patienten direkt nach einer Diabetes-Diagnose einen Augenarzt konsultieren und anschließend die vereinbarten Kontrolltermine konsequent wahrnehmen.
Diagnostik und Therapiemonitoring
Zusätzlich zur herkömmlichen Untersuchung der Netzhaut nach medikamentöser Pupillenweitstellung stehen heute weitere, hochauflösende Methoden zur Diagnostik, Verlaufsbeobachtung und zum Therapiemonitoring zur Verfügung. Die optische Kohärenztomografie (OCT) ermöglicht eine genaue Analyse des Netzhautödems, weil sie eine Darstellung ähnlich wie bei einem histologischen Schnitt erlaubt. Mithilfe der Fluoreszein-Angiografie lassen sich diabetische Gefäßveränderungen wie Mikroaneurysmen und Mikroperfusionsstörungen sowie Gefäßleckagen gut erkennen.
Anti-VEGF-Therapie: Mittel der ersten Wahl
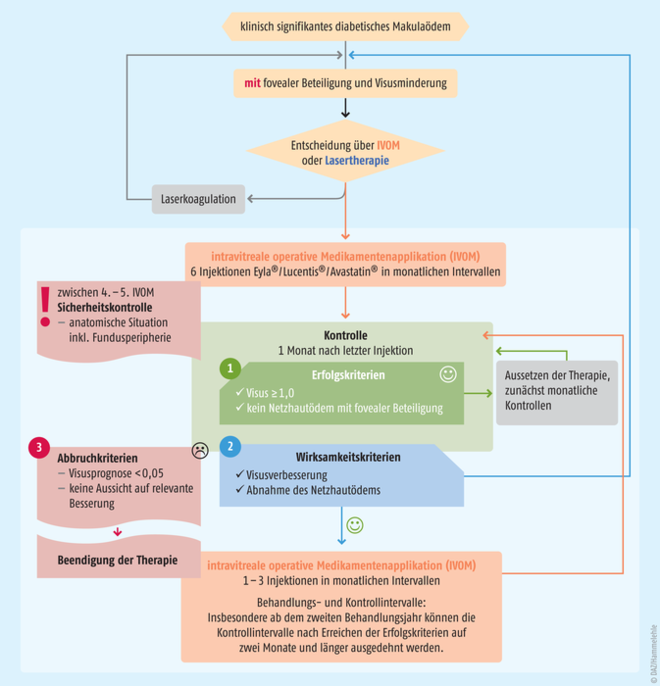
Lange Zeit war die Lasertherapie der Standard bei diabetischen Netzhautveränderungen. Sie kommt auch heute noch zum Einsatz, zum Beispiel wenn sich die Gefäßleckagen mit dem Laser gut erreichen lassen oder wenn dem Patienten die häufigen Behandlungs- und Kontrolltermine bei einer intravitrealen operativen Medikamentenapplikation (IVOM) nicht zuzumuten sind. Die Visusergebnisse sind bei der Lasertherapie nicht so gut wie bei einer IVOM. Ein weiterer Nachteil ist, dass Sehzellen und das retinale Pigmentepithel durch die Laserbehandlung dauerhaft geschädigt werden können. Dank der Einführung der intravitreal zu applizierenden VEGF-Inhibitoren und Steroiden wurde nicht nur das Therapiespektrum erweitert, sondern auch eine individuellere Behandlung ermöglicht. Wenn das diabetische Makulaödem die Fovea, die Sehgrube im Zentrum der Netzhaut, erreicht hat, sind Anti-VEGF-Medikamente die erste Wahl (s. Abb. 1).
Abb. 1: Behandlungs- und Kontrollintervalle Insbesondere ab dem zweiten Behandlungsjahr können die Kontrollintervalle nach Erreichen der Erfolgskriterien auf zwei Monate und länger ausgedehnt werden. [nach: Therapie des diabetischen Makulaödems. Stellungnahme der DOG, DRG und BVA, 2019]
Angiogenesehemmung durch VEGF-Blockade
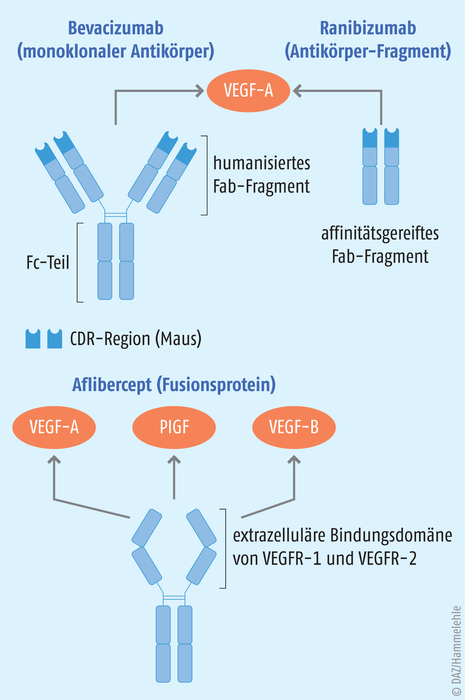
Die medikamentöse Therapie diabetischer Netzhautkomplikationen richtet sich hauptsächlich gegen den Gefäßwachstumsfaktor VEGF (Vascular Endothelial Growth Factor) sowie weitere Faktoren wie PlGF (Placental Growth Factor) und Ang-2 (Angiopoietin 2, siehe unten). Neben den zugelassenen Substanzen Aflibercept und Ranibizumab wird Bevacizumab off label eingesetzt (s. Abb. 2). Alle drei Wirkstoffe werden intravitreal (durch Injektion in den Glaskörper) verabreicht.
- Ranibizumab ist ein rekombinantes humanisiertes monoklonales Antikörperfragment gegen VEGF-A. Es bindet mit hoher Affinität an Isoformen wie VEGF-A110 , VEGF-A121 und VEGF-A165 und verhindert dadurch deren Bindung an die Rezeptoren für Wachstumsfaktoren der VEGF-Familie VEGFR-1 und VEGFR-2 auf der Oberfläche von Endothelzellen.
- Aflibercept ist ein rekombinantes Fusionsprotein aus Fragmenten der extrazellulären Domänen der humanen VEGF-Rezeptoren 1 und 2 und dem Fc-Fragment des humanen IgG1. Aflibercept wirkt als löslicher Köderrezeptor, der VEGF-A und -B sowie den ebenfalls zur VEGF-Familie gehörenden Plazenta-Wachstumsfaktor PlGF (Placental Growth Factor) mit höherer Affinität als deren natürliche Rezeptoren an Endothelzellen bindet.
- Auch der rekombinante humanisierte monoklonale Antikörper Bevacizumab bindet an VEGF und hemmt dadurch dessen Interaktion mit den Rezeptoren VEGFR-1 und VEGFR-2 auf der Oberfläche von Endothelzellen. Bevacizumab ist für verschiedene Tumorarten (z. B. Mamma- und Kolonkarzinom), jedoch nicht für ophthalmologische Indikationen zugelassen. Bei der neovaskulären altersabhängigen Makuladegeneration (nAMD) und dem diabetischen Makulaödem (DMÖ) ist Bevacizumab jedoch ähnlich wirksam wie die anderen beiden Arzneistoffe und wird daher off label eingesetzt.
Abb. 2: Angiogenesehemmer, die bei diabetischen Retinopathien eingesetzt werden, binden und inaktivieren spezifisch vaskuläre endotheliale Wachstumsfaktoren (VEGF) (Bevacizumab und Ranibizumab), Aflibercept zusätzlich den Placental Growth Factor (PlGF).
Intravitreale Applikation von Steroiden
Eine weitere Option zur Behandlung des diabetischen Makulaödems sind intravitreale Steroide. Derzeit zugelassen sind intraokuläre Implantate mit Dexamethason bzw. Fluocinolon (s. Tab.). Off label werden intravitreale Injektionen mit Triamcinolonacetonid (Volon A®) eingesetzt. Die Steroid-Implantate besitzen eine deutlich längere Wirkungsdauer als die Anti-VEGF-Therapeutika. So wird eine Wiederholungsbehandlung mit dem Dexamethason-Implantat Ozurdex® erst nach etwa sechs Monaten empfohlen, das Iluvien®-Implantat setzt bis zu 36 Monate lang Fluocinolonacetonid frei. Die geringere Zahl von intravitrealen Injektionen bei Depot-Steroiden im Vergleich zu Anti-VEGF-Wirkstoffen ist für die Adhärenz der Patienten vorteilhaft. Ein Nachteil der Steroide sind Nebenwirkungen wie ein Anstieg des Augeninnendrucks oder Linsentrübungen, die wiederum häufigere Kontrolluntersuchungen beim Augenarzt erfordern. Intravitreale Steroide sind daher nur Mittel der zweiten Wahl bei unzureichendem oder fehlendem Ansprechen auf VEGF-Inhibitoren.
Wirkstoff | Präparat | Indikationen am Auge | Hersteller |
|---|---|---|---|
Anti-VEGF-Wirkstoffe | |||
Aflibercept | Eylea® Injektionslösung in einer Fertigspritze |
| Bayer AG |
Bevacizumab | Avastin® Konzentrat zur Herstellung einer Infusionslösung | keine (Off-Label-Einsatz | Roche Pharma AG |
Ranibizumab | Lucentis® Fertigspritze |
| Novartis Pharma GmbH |
Steroide | |||
Dexamethason | Ozurdex®intravitreales Implantat |
| Allergan GmbH |
Fluocinolonacetonid | Iluvien®intravitreales Implantat im Applikator |
| Alimera Sciences |
Ergebnisse aus Studien mit Anti-VEGF-Therapeutika
Die Effektivität einer Behandlung des diabetischen Makulaödems mit Aflibercept, Bevacizumab bzw. Ranibizumab ist in zahlreichen Studien, darunter auch direkten Vergleichsstudien, untersucht worden. Eine 2015 publizierte Vergleichsstudie mit 660 Erwachsenen mit einem mittleren Alter von 61 Jahren hatte gezeigt, dass alle drei Wirkstoffe nach einem Jahr Behandlung das Sehvermögen nicht nur erhalten, sondern zum Teil verbessern können. Wird ein Makulaödem erfolgreich behandelt, bedeutet dies für die Patienten oft einen deutlichen Zugewinn an Lebensqualität, zum Beispiel wenn sie wieder ohne Lupe lesen können oder ihre Fahrtüchtigkeit wiedererlangen. Wenn das Sehvermögen der Patienten nur gering eingeschränkt war, gab es in den Studien keine wesentlichen Unterschiede zwischen den drei Wirkstoffen. Bei bereits stark eingeschränktem Visus war Aflibercept nach einem Jahr effektiver als Bevacizumab und Ranibizumab. Nach zwei Behandlungsjahren war die Visusverbesserung in dieser Subgruppe mit schlechteren Ausgangswerten unter Bevacizumab signifikant geringer als unter Aflibercept und Ranibizumab. Zu den Nebenwirkungen, die nach der Anwendung der VEGF-Inhibitoren beobachtet wurden, zählen beispielsweise Augenschmerzen, Einblutungen in den Glaskörper und die Bindehaut oder vorübergehend verminderte Sehschärfe.
Aktuelle Daten zur Prävalenz
Zur Häufigkeit diabetischer Folgeerkrankungen des Auges gibt es zahlreiche Erhebungen und Schätzungen. Eine Arbeitsgruppe unter Leitung der Augenklinik des Universitätsklinikums Bonn hatte im vergangenen Jahr eine Metaanalyse zur Prävalenz und Inzidenz des diabetischen Auges in Europa veröffentlicht. Dafür wurden 35 Prävalenz- und vier Inzidenz-Studien ausgewertet. Die Prävalenz der diabetischen Retinopathie betrug 25,7%, die des diabetischen Makulaödems 3,7%. Dabei lag die Prävalenz der diabetischen Retinopathie unter Typ-1-Diabetikern mit 54,4% deutlich höher als unter Typ-2-Diabetikern (25,0%). Aufgrund der Auswertungen schätzten die Wissenschaftler, die sich in Europa die Fallzahlen bei diabetischen Augenerkrankungen von gegenwärtig 6,4 Millionen bis zum Jahr 2050 auf 8,6 Millionen erhöhen werden.
Mögliche Dosierungsschemata
Beim diabetischen Makulaödem beträgt die empfohlene Aflibercept-Dosis 2 mg. Es wird in der Regel mit fünf aufeinanderfolgenden monatlichen Injektionen begonnen, gefolgt von einer Injektion alle zwei Monate. Zwischen den einzelnen Injektionen ist keine Verlaufskontrolle notwendig. Je nach Befund kann das Behandlungsintervall nach den ersten zwölf Monaten verlängert werden (Treat-and-Extend-Dosierungsschema). Wenn sich der funktionelle und/oder morphologische Befund des Patienten verschlechtert, kann der Arzt das Behandlungsintervall wieder verkürzen. Bei Ranibizumab werden pro Dosis 0,5 mg alle vier Wochen verabreicht, bei Bevacizumab 1,25 mg. Der weitere Ablauf kann ähnlich wie bei Aflibercept nach dem Treat-and-Extend-Schema erfolgen. Bei Patienten, bei denen sich die Schwellungen nach den ersten zwei bis drei Injektionen nicht genügend zurückbildet haben, warten Augenärzte meistens ab, da nach weiteren Injektionen häufig eine Abnahme des Makulaödems eintritt. Auch ein Wechsel auf einen anderen VEGF-Inhibitor oder ein Steroid ist möglich. Wenn die Befunde ergeben, dass der Patient nicht von einer weiteren Behandlung profitiert, sollte die Therapie beendet werden.
Blick in die Zukunft: höhere Aflibercept-Dosierung und zwei neue Antikörper
Auf dem Gebiet der gegen diabetische Makulaödeme gerichteten Therapeutika sind in naher Zukunft einige Veränderungen zu erwarten. So wird derzeit in zwei Phase-III-Studien eine höherdosierte Aflibercept-Formulierung von 8 mg zur intravitrealen Injektion geprüft. Dadurch könnten die Behandlungsintervalle weiter verlängert werden.
Im Februar 2020 wurde der monoklonale, gegen den vaskulären endothelialen Wachstumsfaktor A (VEGF-A) gerichtete Antikörper Brolucizumab (Beovu®) zur Behandlung der neovaskulären altersabhängigen Makuladegeneration zugelassen. Es handelt sich um ein humanisiertes Einzelketten-Antikörperfragment (single-chain antibody fragment, scFv). Brolucizumab wird derzeit auch in der Indikation diabetisches Makulaödem geprüft.
Diabetisches Retinopathie-Screening mit künstlicher Intelligenz
Zukünftig könnten in Allgemeinarzt- oder Diabetes-Schwerpunktpraxen Geräte stehen, die mithilfe von Künstlicher Intelligenz eine diabetische Retinopathie frühzeitig erkennen. In den USA sind solche Geräte bereits zugelassen. Ein auf der Technologie EyeArt® basierendes Kamerasystem der Firma Eyenuk Inc., das mithilfe eines mathematischen Algorithmus bei Patienten ohne medikamentöse Pupillenerweiterung eine Retinopathie erkennen kann, ist bereits im Diabeteszentrum Bad Mergentheim installiert worden.
Mit Faricimib befindet sich ein weiterer neuer Antikörper in der letzten Phase der klinischen Entwicklung. Es handelt sich dabei um einen bispezifischen Antikörper, der zusätzlich zum endothelialen Wachstumsfaktor VEGF-A auch gegen Angiopoietin 2 (Ang-2) gerichtet ist. Ang-2 ist ein Gegenspieler von Angiopoietin-1 (Ang-1), das in der gesunden Netzhaut nach Bindung an seinen Rezeptor Tie-2 die Blutgefäße stabilisiert und Entzündungen entgegenwirkt. Unter Stressbedingungen, zum Beispiel bei Sauerstoffmangel oder erhöhten Blutzuckerspiegeln, werden Ang-2 und VEGF-A verstärkt produziert. Ang-2 verdrängt Ang-1 von seinem Rezeptor, es kommt zur Destabilisierung von Blutgefäßen mit Leckage-Bildung und damit zu Flüssigkeitsansammlungen und Entzündungen in der Netzhaut. Gemeinsam fördern Ang-2 und VEFG-A die Entstehung des diabetischen Makulaödems und der altersabhängigen Makuladegeneration.
Indem Faricimib sowohl Ang-2 als auch VEGF-A hemmt, können Leckagen und Entzündungen möglicherweise besser reduziert werden als durch die alleinige Hemmung des VEGF-Signalwegs. In den bisherigen klinischen Studien war Faricimib dem rekombinanten Fusionsprotein Aflibercept nicht unterlegen. Durch die synergistische Wirkung von Faricimib könnte es möglich werden, die Häufigkeit der erforderlichen intravitrealen Injektionen zu reduzieren. In klinischen Studien konnten die Behandlungsintervalle ohne Sehschärfenverlust bis auf vier Monate verlängert werden.
Zusammenarbeit der Fachärzte notwendig
Das diabetische Auge steht in engem Zusammenhang mit weiteren Erkrankungen. Die ärztlichen Fachgesellschaften sind sich deshalb darin einig, dass diabetische Retinopathien nicht vom Augenarzt allein, sondern in enger Zusammenarbeit mit anderen Fachdisziplinen behandelt werden sollten. Beispielsweise ist ein erhöhter Blutdruck nicht nur ein Risikofaktor für die Entstehung des diabetischen Makulaödems, sondern auch für ein schlechteres Ansprechen auf dessen Behandlung. Auch mit weiteren Diabetes-Komplikationen wie der diabetischen Nephropathie sowie mit peripheren arteriellen Erkrankungen wie Schlaganfällen sind diabetische Retinopathien eng verknüpft. |
Literatur
Bayer kündigt Phase-III-Studien mit neuer 8 mg Aflibercept-Formulierung an. Pressemeldung vom 10. Februar 2020, www.media.bayer.de/baynews/baynews.nsf/id/2D9780B064CFF6A9C12585070033856A?open&ref=irrefndcd, Abruf am 20. April 2020
Der innovative bispezifische Antikörper Faricimab von Roche ermöglicht lange Therapieintervalle bei Patienten mit DMÖ und nAMD. Medienmitteilung der Roche Pharma AG vom 22. Februar 2021, www.roche.de
Ergänzende Stellungnahme zur Therapie der proliferativen diabetischen Retinopathie. Stellungnahme der Deutschen Ophthalmologischen Gesellschaft, der Retinologischen Gesellschaft und des Berufsverbandes der Augenärzte Deutschlands, Stand November 2019
Eyenuk, Inc. expands into Germany with launch of EyeArt® Artificial Intelligence Eye Screening for diabetic retinopathy. Meldung vom 5. Oktober 2018, www.eyenuk.com/en/articles/news/eyenuk-inc-expands-into-germany-with-launch-of-eyeart-artificial-intelligence-eye-screening-for-diabetic-retinopathy/, Abruf am 21. April 2021
Fachinformationen der genannten Produkte
Furino C et al. Intravitreal Therapy for Diabetic Macular Edema: An Update. J Ophthalmol 2021, https://doi.org/10.1155/2021/6654168
Geisslinger G, Menzel S, Gudermann T, Hinz B, Ruth P, Mutschler E Arzneimittelwirkungen. Pharmakologie – Klinische Pharmakologie – Toxikologie. 11., völlig neu bearbeitete Auflage, Wissenschaftliche Verlagsgesellschaft Stuttgart 2020
Intravitreale Therapie des visusmindernden Makulaödems bei retinalem Venenverschluss. Stellungnahme des Berufsverbandes der Augenärzte Deutschlands, der Deutschen Ophthalmologischen Gesellschaft und der Retinologischen Gesellschaft, Stand April 2018
Korobelnik JF et al. Intravitreal aflibercept for diabetic macular edema. Ophthalmology 2014; online publiziert am 8. Juli 2014, doi: 10.1016/j.ophtha.2014.05.006
Li JQ et al. Prevalence, incidence and future projection of diabetic eye disease in Europe: a systematic review and meta-analysis. Eur J Epidemiol 2020;35:11–23
Nationale VersorgungsLeitlinie „Prävention und Therapie von Netzhautkomplikationen bei Diabetes“, Langfassung, 2. Auflage 2015, Version 2, AWMF-Register-Nr.: nvl-001b, derzeit in Überarbeitung
Pearce I et al. Association between diabetic eye disease and other complications of diabetes: Implications for care. A systematic review. Diabetes Obes Metab 2019;21(3):467-478, doi:10.1111/dom.13550.
Spital G. Therapie des diabetischen Makulaödems. Der Diabetologe 2018,14:577–589
Therapie des diabetischen Makulaödems. Stellungnahme der Deutschen Ophthalmologischen Gesellschaft, der Retinologischen Gesellschaft und des Berufsverbandes der Augenärzte Deutschlands, Stand August 2019
Wells JA et al. Aflibercept, bevacizumab, or ranibizumab for diabetic macular edema. Two-year results from a comparative effectiveness randomized clinical trial. Ophthalmology 2016; 123(6):1351-1359
Wells JA et al. Diabetic Retinopathy Clinical Research Network. Aflibercept, bevacizumab, or ranibizumab for diabetic macular edema. N Engl J Med. 2015; 372(13):1193–203
Interessenkonflikte
Die Autorin versichert, dass keine Interessenkonflikte bestehen.























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.