
- DAZ.online
- DAZ / AZ
- DAZ 13/2021
- Mehr als ein Frü...
Pharmakognosie
Mehr als ein Frühlingsbote
Das Schneeglöckchen ist auch Giftpflanze und Arzneistofflieferant
Noch während der letzte Schnee schmilzt, blüht es schon. Das Gemeine Schneeglöckchen Galanthus nivalis zählt zu den bekanntesten Frühlingsboten (Abb. 1). Die linealen, graugrünen Blätter und die hängende weiße Blüte verleihen dieser Pflanze ein charakteristisches Aussehen [1]. Das Aussehen der Blüte drückt sich auch in dem Gattungsnamen Galanthus aus, welcher aus den altgriechischen Wörtern gala für Milch und anthos für Blüte besteht [2]. Das Schneeglöckchen bildet, wie viele Pflanzen aus der Familie Amaryllidaceae (Amaryllisgewächse), eine Zwiebel als Überdauerungsorgan [1]. Die ganze Pflanze, besonders aber die Zwiebel, ist reich an einer ganz besonderen Gruppe sekundärer Pflanzenstoffe, den Amaryllidaceen-Alkaloiden [3]. Neben dem Hauptinhaltsstoff Galantamin sind Haemanthamin, Galantin, Lycorin und Narciclasin enthalten [1]. Außer dem Gemeinen Schneeglöckchen sind einige weitere Arten im Blumenhandel und vielfach in den Vorgärten zu finden. Sie haben ähnliche Inhaltsstoffe. Viele Amaryllidaceen-Alkaloide sind pharmakologisch aktiv und deshalb auch der Grund, warum das Schneeglöckchen giftig ist. Vergiftungssymptome sind Übelkeit, Erbrechen, Durchfall und Pupillenverengung [2].
Abb. 1: Galanthus nivalis Der bekannteste Frühlingsbote blüht oft schon, während der letzte Schnee schmilzt. Charakteristisch für die Pflanze sind die hängenden, weißen Blüten.
Amaryllidaceen-Alkaloide
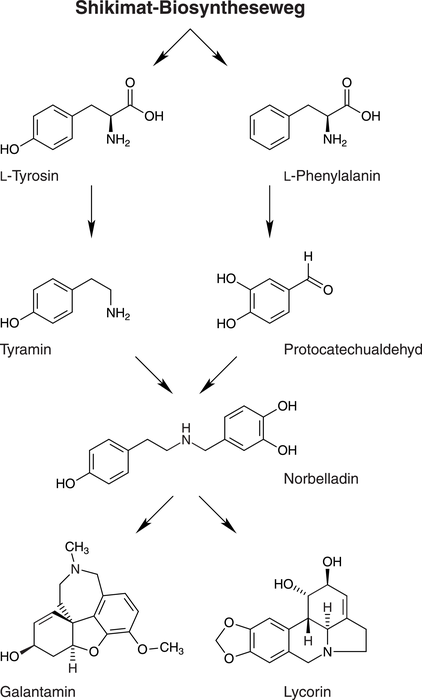
Die Gruppe der Amaryllidaceen-Alkaloide besteht aus 150 bis 300 verschiedenen Substanzen, die fast ausschließlich in der Familie der Amaryllisgewächse vorkommen [3, 4]. Biosynthetisch leiten sie sich von N-Benzyl-N-β-phenylethylamin ab, welches aus den Aminosäuren Tyrosin und Phenylalanin gebildet wird (Abb. 2) [5]. Zu den verbreitetsten Amaryllidaceen-Alkaloiden zählen neben Galantamin und Lycorin auch Pretazettin und Haemanthamin [3, 4]. Viele Amaryllidaceen-Alkaloide sind toxisch und besitzen eine ausgeprägte insektizide Wirkung [4]. Den Pflanzen dienen die Alkaloide als Fraßschutz gegen Evertebraten und Vertebraten. Pharmazeutisch bedeutsam hingegen ist Galantamin [3].
Abb. 2: Biosynthesewege von Amaryllidaceen-Alkaloiden Über den Shikimat-Biosyntheseweg können Pflanzen die aromatischen Aminosäuren L-Phenylalanin/L-Tyrosin selbst synthetisieren. Die Umwandlungsprodukte Tyramin und Protocatechualdehyd kondensieren zu einer Schiff’schen Base, welche zu Norbelladin hydriert wird. Die anschließende Bildung weiterer Ringsysteme erfolgt meist durch oxidative Kopplung.
Galantamin und Morbus Alzheimer
Galantamin ist das einzige pharmazeutisch verwendete Amaryllidaceen-Alkaloid [5]. Die Substanz wird verwendet zur symptomatischen Behandlung von leichter bis mittelschwerer Alzheimer-Demenz [3, 5, 13]. Alzheimer ist die häufigste Form der Altersdemenz [1]. Typische Symptome sind Gedächtnisverlust, Verlust der Urteilsfähigkeit und Verlust der Orientierung [16]. In Deutschland leiden ca. 1,6 Mio. Menschen an Alzheimer, jedes Jahr kommen 300.000 Neuerkrankungen hinzu [17]. Alzheimerdemenz ist eine progressiv neurodegenerative Erkrankung, die zu einem Verlust von Nervenzellen führt [16]. Pathophysiologisch charakteristisch sind eine Beeinträchtigung der cholinergen Erregungsübertragung und ein Mangel von Acetylcholin in bestimmten Gehirnregionen [1, 9].
Ein therapeutischer Ansatz besteht darin, die Konzentration von Acetylcholin im Gehirn zu erhöhen [1]. Acetylcholin wird durch das Enzym Acetylcholinesterase inaktiviert, daher bietet sich dieses Enzym als pharmakologisches Target an. Acetylcholinesterasehemmer sind die am häufigsten verschriebene Gruppe von Antidementiva [16]. In den letzten zehn Jahren sind die Verschreibungen aus dieser Arzneistoffgruppe um 30% gestiegen. Hinter Donepezil und Rivastigmin ist Galantamin der am dritthäufigsten verschriebene Acetylcholinesterasehemmer. 2019 wurden in Deutschland 7,1 Mio. Tagesdosen (DDD) Galantamin verordnet [16].
Galantamin ist ein reversibler Hemmer der Acetylcholinesterase, welcher 2001 unter dem Handelsnamen Reminyl® in Deutschland zugelassen wurde [5]. Die antidementive Wirkung von Galantamin ist dosisabhängig. Daher ist bei der Therapie die höchste verträgliche Dosis anzustreben [9]. Nebenwirkungen treten hauptsächlich bei Therapiebeginn auf; typisch sind Übelkeit, Erbrechen und Durchfall [3] (s. Kasten „Unerwünschte Wirkungen“). Um die Verträglichkeit zu steigern, wird die Dosierung über mehrere Wochen eingeschlichen [9].
Unerwünschte Wirkungen
Unter Acetylcholinesterasehemmern zur Behandlung von Alzheimerdemenz treten sehr häufig (> 1/10) unten stehende Nebenwirkungen auf [18]. Die unerwünschten Wirkungen werden vor allem zu Therapiebeginn beobachtet und äußern sich meistens in unspezifischen gastrointestinalen Beschwerden.
Donepezil
- Übelkeit
- Diarrhöe
- Kopfschmerzen
Galantamin
- Übelkeit
- Erbrechen
Rivastigmin
- Übelkeit
- Erbrechen
- Diarrhöe
- Schwindel
- Appetitlosigkeit
Bei Rivastigmin beziehen sich die Angaben auf orale Arzneiformen. Bei transdermaler Applikation sind mildere Nebenwirkungen zu erwarten.
Neben der Hemmung der Acetylcholinesterase ist Galantamin ein allosterisch potenzierender Ligand an postsynaptischen nicotinischen Acetylcholin-Rezeptoren, was die Wirkung von Acetylcholin zusätzlich steigern soll [4, 9]. Zusätzlich soll die Empfindlichkeit präsynaptischer Acetylcholin-Rezeptoren durch Galantamin erhöht werden, was zu einer vermehrten Freisetzung von Neurotransmittern führt [4, 14]. Der Effekt dieser zusätzlichen Wirkmechanismen ist allerdings umstritten [9].
Es ist anzumerken, dass eine medikamentöse Therapie von Alzheimer nur eingeschränkt möglich ist und dass keine kausale Behandlung existiert [9, 13]. Die vorhandenen Medikamente haben eine begrenzte Aktivität und eine mäßige Effektstärke, bessere Therapien fehlen jedoch. Medikamentös kann im besten Fall die Progression der Krankheit verlangsamt werden. Für Galantamin konnte eine Stabilisierung der kognitiven Leistungen für mindestens sechs Monate gezeigt werden [9]. Das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) hat im Jahr 2012 den Nutzen von Galantamin bewertet. Die Untersuchung hat ergeben, dass Galantamin zumindest in hohen Dosen bei leichter und mittelschwerer Demenz positive Einflüsse auf das Denkvermögen und die Merkfähigkeit hat [15].
Galantamin kommt nicht nur im Gemeinen Schneeglöckchen (Galanthus nivalis) sondern auch in anderen Arten aus der Familie der Amaryllisgewächse (Amaryllidaceae) vor [13]. Galantamin wurde früher aus Zwiebeln des Märzenbechers (Leucojum verum) oder des Woronow-Schneeglöckchens (Galanthus woronowii) gewonnen. Inzwischen wird das Alkaloid synthetisch hergestellt [5, 13].
Für Spezialextrakte einer anderen Arzneipflanze, dem Ginkgo (Ginkgo biloba), konnte ebenfalls eine Hemmung der Acetylcholinesterase sowie eine Hemmung des Platelet-activating-factors (PAF) nachgewiesen werden [1]. Außerdem verbessert der Spezialextrakt die Durchblutung des Gehirns. Trotz guter Verträglichkeit konnte der Nutzen von Ginkgo-Präparaten von Alzheimerdemenz nicht in allen Studien nachgewiesen werden [19]. Hier ist zu bedenken, dass je nach Extrakt, abhängig von der Extraktionsmethode, unterschiedliche Mengen an wirkbestimmenden Inhaltsstoffen vorliegen.
Osterglocke
Eine weitere Frühlingsblume ist die Osterglocke Narcissus pseudonarcissus, ebenfalls aus der Familie der Amaryllisgewächse [6] (s. Abb. 3). Die Pflanze enthält ebenso Amaryllidaceen-Alkaloide, hauptsächlich Lycorin und Galantamin [6]. Vergiftungen treten hauptsächlich durch den irrtümlichen Verzehr von Zwiebeln auf, die mit Küchenzwiebeln verwechselt wurden. Intoxikationssymptome sind Speichelfluss, Übelkeit, Erbrechen, Durchfall und Lähmungserscheinungen [6]. Lycorin ist ein starkes Zellgift. Es bindet an die 60S-Untereinheit von Ribosomen und hemmt dadurch die ribosomale Proteinbiosynthese [6].
Abb. 3: Narzissen im Elsass Die Osterglocke (Narcissus pseudonarcissus) ist die bekannteste Narzisse. Die charakteristischen Blüten sieht man vor allem im Frühjahr. Osterglocken werden von Weidetieren nicht gefressen, da alle Pflanzenteile das giftige Alkaloid Lycorin enthalten. Es existieren zahlreiche Unterarten, welche man sowohl wild als auch in Zuchtformen findet.
Neuartige antivirale Wirkstoffe sind vor allem seit der Pandemie mit dem Coronavirus SARS-CoV-2 in das Interesse der Forschung gerückt. Das während der ersten SARS-Pandemie 2002/2003 grassierende Virus SARS-CoV-1 ist eng mit dem aktuellen Virus verwandt. Zahlreiche sekundäre Pflanzenstoffe wurden auf ihre antivirale Aktivität gegen SARS-CoV-1 untersucht [20]. Dabei zeigte Lycorin eine besonders ausgeprägte antivirale Wirkung [21].
Ebenso interessant ist, dass Lycorin-enthaltende Pflanzen nicht von Insekten befallen werden [7]. Die als „Narzissenkrankheit“ oder „Gärtner-Dermatitis“ bezeichneten Hautreizungen werden allerdings nicht durch Amaryllidaceen-Alkaloide, sondern durch Oxalat-Kristalle ausgelöst [6].
Odysseus und das Schneeglöckchen
In Homers Odyssee wird die lange Reise des Herrschers von Ithaka, Odysseus, beschrieben [8]. Zahlreiche Abenteuer musste der Held bestehen, bevor er in seine Heimat zurückkehren konnte [8]. In einem Abenteuer werden die Gefährten des Odysseus durch einen Trank der Zauberin Kirke in Schweine verwandelt [2]. Höchstwahrscheinlich enthielt dieser Trank Alraune (Mandrago officinarum) oder Schwarzes Bilsenkraut (Hyoscyamus niger), welche Tropan-Alkaloide wie Scopolamin und L-Hyoscyamin enthalten [2]. Diese Substanzen sind für ihre halluzinogene Wirkung bekannt [6]. Nach oraler Gabe tritt ein traumreicher Schlaf ein. Es wurde berichtet, dass Menschen unter diesen Bedingungen träumten, dass sie Tiere wären, beispielsweise Schweine. Wenn diese Alkaloide auf die Haut (Achseln, Genitalbereich) aufgetragen werden, ergibt sich das Gefühl des Fliegens. Bekanntlich enthielten die Hexentränke des Mittelalters Extrakte mit Tropan-Alkaloiden.
Durch den Verzehr der Pflanze „Moly“ konnte sich Odysseus vor der Wirkung des Tranks der Kirke schützen [2]. Um welche Pflanze handelt es sich bei „Moly“? Aus der Odyssee wissen wir, dass es sich um eine Pflanze mit milchig weißer Blüte und schwarzer Wurzel handelt [8].
In der Odyssee heißt es:
Also sprach Hermeias, (Anm.: Hermes) und gab mir die heilsame Pflanze,
Die er dem Boden entriss, und zeigte mir ihre Natur an:
Ihre Wurzel war schwarz, und milchweiß blühte die Blume;
Moly wird sie genannt von den Göttern. Sterbliche Menschen
Ist sie schwer zu graben; doch alles vermögen die Götter.
Abb. 4: Schneeglöckchen mit weißen Blüten und schwarzen Zwiebeln Bei der in der Odyssee „Moly“ genannten Pflanze handelt es sich höchstwahrscheinlich um das Schneeglöckchen. Nicht nur weil die Beschreibung passt, sondern auch das enthaltene Galantamin die Wirkung von Tropan-Alkaloiden wie L-Hyoscyamin und Scopolamin antagonisiert.
Eine Zeit lang wurden verschiedene Laucharten, Herbstzeitlose und Steppenraute für Moly gehalten. Doch enthalten diese Pflanzen kein Antidot gegen eine Intoxikation mit Tropan-Alkaloiden. Die Beschreibung passt besser auf das Schneeglöckchen (Abb. 4), das im Mittelmeerraum verbreitet vorkommt [2]. Auch aus pharmakologischer Sicht ist die Verwendung von Schneeglöckchen als Antidot bei Vergiftungen mit Tropan-Alkaloiden plausibel. Tropan-Alkaloide sind Antagonisten an muscarinischen Acetylcholin-Rezeptoren [6]. L-Hyoscyamin und Scopolamin wirken parasympatholytisch, indem sie die Wirkung von Acetylcholin abschwächen. Galantamin aus dem Schneeglöckchen hemmt die Acetylcholinesterase, also den Abbau von Acetylcholin im synaptischen Spalt [6]. Durch die Verlängerung der Wirkdauer von Acetylcholin wirkt Galantamin parasympathomimetisch, also der entgegengesetzte Effekt von Tropan-Alkaloiden.
Forschung
Zahlreiche Amaryllidaceen-Alkaloide sind pharmakologisch aktiv. Lycorin besitzt eine stark antivirale Wirkung [1, 4]. Auch gegen den Malariaerreger Plasmodium falciparum zeigen Lycorin und Haemanthamin Wirksamkeit [10]. Ebenso ist die analgetische Potenz von Galantamin bekannt [2]. Aufgrund der geringen therapeutischen Breite und der Toxizität von Amaryllidaceen-Alkaloiden ist diese Forschung eher theoretischer Natur [3]. Aufgrund des parasympathomimetischen Wirkmechanismus wirkt Galantamin hypoton und senkt die Herzfrequenz, daher wird die Substanz off label als Kardioprotektivum verschrieben [3]. Die kardioprotektive Wirkung von Acetylcholinesterase-Hemmern wurde daher auch intensiver untersucht [11]. Aktuell wird die Eigenschaft von Galantamin, Wachträume auszulösen, näher untersucht [12]. |
Literatur
[1] van Wyk BE, Wink C, Wink M. Handbuch der Arzneipflanzen. 3. Auflage 2015. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[2] Niehaus M, Wink M. Wie man Männer in Schweine verwandelt. 2020. Hirzel-Verlag, Stuttgart
[3] Teuscher E, Lindequist U, Melzig M. Biogene Arzneimittel. 8. Auflage 2020. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[4] Teuscher E, Lindequist U. Biogene Gifte. 3. Auflage 2010. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[5] Wagner H, Vollmar A, Bechthold A. Pharmazeutische Biologie 2. 7. Auflage 2007. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[6] Wink M, van Wyk BE, Wink C. Handbuch der giftigen und psychoaktiven Pflanzen. 2008. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[7] Abbassy MA, El-Gougary OA, El-Hamady S, Sholo MA. Insecticidal, acaricidal and synergistic effects of soosan, Pancratium maritimum extracts and constituents. J Egypt Soc Parasitol 1998;28:197-205
[8] Homer: Ilias und Odyssee, übersetzt von Johann Heinrich Voss, Zürich 1980
[9] Geisslinger G, Menzel S, Gudermann T, Hinz B, Ruth P. Mutschler Arzneimittelwirkungen. Begründet von Ernst Mutschler, 11. Auflage 2020. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[10] Likhitwitayawiud K, Angerhofer CK, Cordell GA, Pezutto JM. Cytotoxic and Antimalarial bisbenzylisoquinolme alkaloids from Stephania erecta. J Nat Prod. 1993;56:30-38
[11] Nordström P, Religa D, Wimo A, Winbald B, Eriksdotter M. The use of cholinesterase inhibitors and the risk of myocardial infarction and death: a nationwide cohort study in subjects with Alzheimer’s disease. Eur Heart J. 2013;34:2585-91
[12] LaBerge S, LaMarca K, Baird B. Pre-sleep treatment with galantamine stimulates lucid dreaming: A double-blind, placebo-controlled, crossover study. PLoS One. 2018;13(8):e0201246
[13] Sticher O, Heilmann J, Zündorf I. Hänsel/Sticher Pharmakognosie Phytotherapie. 10. Auflage 2015. Wissenschaftliche Verlagsgesellschaft mbH, Stuttgart
[14] Heinrich M, Lee Teoh H. Galanthamine from snowdrop – the development of a modern drug against Alzheimer’s disease from local Caucasian knowledge. J Ethnopharmacol. 2004;92:147-62
[15] Pressemitteilung des IQWIG. Galantamin und Rivastigmin-Pflaster: Positiver Einfluss auf Kognition möglich. 2012. www.iqwig.de/presse/pressemitteilungen/pressemitteilungen-detailseite_10814.html, abgerufen am 28.02.2021
[16] Schwabe U, Ludwig WD. Arzneiverordnungs-Report 2020. 2020 Springer, Berlin
[17] Escher C, Jensen F. Prävention von kognitivem Abbau und Demenz durch Behandlung von Risikofaktoren. Nervenarzt. 2019;90:921-925
[18] Rote Liste® 2020. 2020. Rote Liste® Service GmbH, Frankfurt am Main
[19] Birks J, Grimley Evans J. Ginkgo biloba for cognitive impairment and dementia. Cochrane Database Syst Rev. 2009;1:CD3120
[20] Wink M. Potential of DNA Intercalating alkaloids and other plant secondary metabolites against SARS-CoV-2 causing COVID-19. Diversity. 2020;12:175
[21] Li SY, Chen C, Zhang HQ, Guo HY, Wang H et al. Identification of natural compounds with activities against SARS-associated coronavirus. Antivir Res. 2005;67:18-23



























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.