
- DAZ.online
- DAZ / AZ
- DAZ 10/2021
- Tempo sticht Genauigkeit
Pandemie Spezial
Tempo sticht Genauigkeit
Häufig wiederholte Antigentests können helfen, die Pandemie unter Kontrolle zu bringen
Damit sich die Hoffnungen erfüllen, die in Antigentests auf SARS-CoV-2 gesetzt werden, braucht es zunächst möglichst zuverlässige und benutzerfreundliche Testkits. Die ersten Sonderzulassungen von SARS-CoV-2-Testkits für die Anwendung durch Laien hat das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) am 24. Februar 2021 erteilt für Testkits für den nasalen Abstrich. Es handelt sich um beim BfArM gelistete, den Mindestkriterien entsprechende und vom Paul-Ehrlich-Institut bezüglich der Sensitivität evaluierte Tests, die schon eine CE-Kennzeichnung für professionelle Anwender besitzen, aber durch Ausstattung mit speziellen Tupfern für den Nasalabstrich und eine illustrierte Gebrauchsanweisung für die Anwendung durch Laien angepasst wurden [1]. Nach Herstellerangaben weisen sie gute Werte für Sensitivität (> 96%) und Spezifität (> 99%) auf (s. Tab.).
Hersteller | Antragsteller | Testname | Sensitivität | Spezifität |
|---|---|---|---|---|
Healgen Scientific LLC | Siemens Healthcare Diagnostics Products GmbH | Clinitest Rapid COVID-19 Self-Test | 97,3% | 100% |
Xiamen Boson Biotech Co., Ltd | Technomed Service GmbH | Rapid SARS-CoV-2 Antigen Test Card | 96,5% | 99% |
Hangzhou Laihe Biotech Ltd., Co. | Lissner Qi GmbH | Lyher® Covid-19 Antigen Schnelltest (Nasal) | 96,2% | 99,7% |
SD Biosensor Inc. | MT Promedt Consulting GmbH | SARS-CoV-2 Rapid Antigen Test | 96,5% | 99,7% |
Ameda Labordiagnostik GmbH | Ameda Labordiagnostik GmbH | AMP Rapid Test SARS-CoV-2 Ag | 97,3% | 100% |
Beijing Hotgen Biotech Co., Ltd | Beijing Hotgen Biotech Co., Ltd | Coronavirus (2019-nCoV)-Antigentest | 95,4% | 99,1% |
Aesku.Diagnostics GmbH & Co. KG | Aesku.Diagnostics GmbH & Co. KG | Aesku.Rapid SARS-CoV-2 | 96,0% | 98,0% |
Gretchenfrage Sensitivität
Immer wieder wird eine ausreichende Empfindlichkeit der Antigentests bezweifelt, da sie mangels Amplifikation nur bei hoher Viruslast anschlagen. Das Forschungsnetzwerk B-Fast weist auch darauf hin, dass Untersuchungen verschiedener SARS-CoV-2-Antigenschnelltests durch unabhängige universitäre Diagnostiklabore mancherorts eine deutlich unter der Testdeklaration liegende Leistungsfähigkeit gezeigt hatten, im Bereich von 45% bis 85% [2]. Zweifelsohne besteht im Vergleich zu PCR-Tests eine größere Abhängigkeit der Aussagekraft von Antigenschnelltests von der Viruslast im Nasen-Rachen-Raum, und damit von einer korrekten Abstrich-Entnahme und ihrem Zeitpunkt vor oder nach Auftreten von Symptomen. Aber wie maßgeblich ist die limitierte Testempfindlichkeit überhaupt, wenn es um ein Screening auf Infektionen geht, wie es in der derzeitigen Pandemiesituation vorgesehen ist? Dass zu diesem Zweck die Regelmäßigkeit und die Schnelligkeit des Testens entscheidender sind als die Testsensitivität, haben begutachtete Modellierungsstudien von Autoren der Harvard- und Yale-Universität gezeigt.
Die PCR-Test erkennt das Virus …
Für M. J. Mina und Mitarbeiter von der Harvard School of Public Health, die weltweit einige der größten Pilotprojekte mit Lateral-Flow-Tests auswerten, ist der PCR-Test nicht der Goldstandard eines SARS-CoV-2-Tests, wenn es statt um Einzeldiagnostik um Effekte auf die öffentliche Gesundheit geht. „Testen, um die Verbreitung von SARS-CoV-2 zu bremsen, fragt nicht, ob jemand RNA von einer vergangenen Infektion in der Nase hat, sondern ob er oder sie heute infektiös ist“, schreiben sie in einem Kommentar in The Lancet [4]. Die Kritik an der angeblich zu geringen Empfindlichkeit der Antigentests kehren die Experten um, indem sie argumentieren, dass diese Assays im Sinne eines Screenings genau im richtigen Bereich anschlagen. Antigentests, so führen sie aus, sprechen auf Oberflächenproteine von SARS-CoV-2 an, was bedeute, dass mit hoher Wahrscheinlichkeit biologisch aktive Viren in großer Menge vorliegen. Die untere Nachweisgrenze (limit of detection, LOD) betrage typischerweise ca. 105 Viruskopien/ml. Realtime-PCR-Tests weisen dank Nukleinsäure-Amplifikationstechnik (NAT) die RNA von SARS-CoV-2 mit einer um mindestens zwei Größenordnungen geringeren unteren Nachweisgrenze von ungefähr 103 Kopien/ml nach. Aber: Was für die Detektion kleinster Mengen zum Vorteil gereicht, könne bei einem Screening auf Infektiosität in die Irre führen. Nämlich dann, wenn bei Ct-Werten über 30 kleinste RNA-Mengen nachgewiesen werden, die längst zu klein für eine Transmission sind, etwa bei einer zurückliegenden Infektion, oder wenn irrelevante Nukleinsäure-Bruchstücke detektiert werden. In diesen Fällen würde der PCR-Test die Zahl infektiöser Menschen überschätzen.
… der Antigentest die Infektiosität
Die Sensitivität des Nachweises stellen die Harvard-Autoren in den Kontext der Infektionskinetik: Ansteckend bleiben die meisten Infizierten vier bis acht Tage nach Symptombeginn, mit einem Maximum an Tag 5. Danach nimmt die Infektiosität schnell ab. Bei asymptomatisch Infizierten geht man davon aus, dass die Viruslast initial genauso hoch ist, aber rascher abnimmt. Entscheidend für die Verbreitung des Virus ist in jedem Fall die Phase der Infektiosität: PCR-Tests weisen RNA-Bestandteile aus den Atemwegen noch mehr als 14 Tage lang nach, bislang gelang es aber in keiner Studie, aus Proben älter als neun Tage nach Erstsymptomen vermehrungsfähige Viren anzuzüchten [3]. „Das kurze Zeitfenster der Infektiosität – in dem Antigentests anschlagen –, kontrastiert mit der Spanne von median 22 bis 33 Tagen, die Infizierte PCR-positiv sind – länger bei schweren Infektionen und kürzer bei asymptomatischen Personen“, schreiben die Kommentatoren. „Dies legt nahe, dass 50 bis 75% der Zeit, in der eine Person PCR-positiv ist, sie wahrscheinlich nicht mehr infektiös ist“ [4].
Screening braucht Tempo
Larremore und Forscherkollegen bildeten Testszenarien unter besonderer Berücksichtigung der beschriebenen Kinetik von SARS-CoV-2. Auch nach deren Modellierung hängt die Effektivität des Screenings nur marginal von der Testempfindlichkeit ab, aber wesentlich von der Häufigkeit des Testens und zudem von der Dauer bis zum Ergebnis, das eine rasche Isolation positiv Getesteter erlaubt. Sie stimmen mit dem Kommentar von Mina und Kollegen darin überein, dass es während der exponentiellen Virusvermehrung nur ein kleines Zeitfenster gibt, in dem ein PCR-Test schon positiv ausfällt, aber ein weniger sensitiver noch nicht. Antigentests mit ihrer Detektionsgrenze von ca. 105 Viruskopien/ml, die auf eine hohe Viruslast anschlagen, seien ausreichend in ihrer Genauigkeit, aber eben schneller als PCR-Tests, zudem billiger [5].
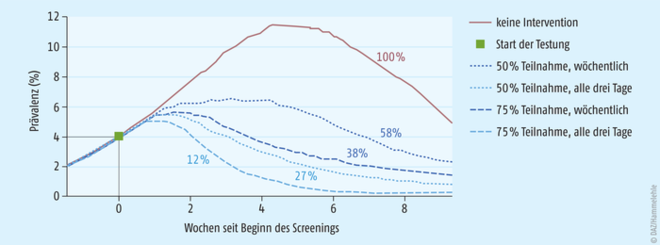
David Paltiel und Mitarbeiter berechneten die Effekte verschiedener Tests und Testfrequenzen (alle 2, 3 oder 7 Tage) in einer fiktiven Kohorte mit 0,2% Infizierten (Abb. 1 und 2). Heraus kam, dass schon mit einem Test von geringer Sensitivität (70%) aber guter Spezifität (mindestens 98%), der alle zwei Tage angewendet wird, die Zahl der Infektionen kontrollierbar bleibt. Verbunden mit strikten Verhaltensregeln würde dies z. B. Schulöffnungen erlauben, so die Autoren. Ihr Kernpunkt ist, dass das Anheben der Testfrequenz die kumulative Inzidenz positiver Fälle wesentlich stärker begrenzte als das Anheben der Testsensitivität. Letztere spielte unter den maßgebenden Faktoren die geringste Rolle; weit wichtiger sei eine hohe Spezifität zur Vermeidung falsch-positiver Resultate [6].
Abb. 1: Wiederholte Screeningtests helfen, das Fortschreiten der Pandemie zu unterdrücken: Ausgehend von einer 2%-Prävalenz und einem Testbeginn bei 4%, wird die Entwicklung des prozentualen Anteils infizierter Personen für verschiedene Testregime dargestellt: bei Testung von 50% bzw. 75% aller Personen und bei drei- bzw. siebentägiger Testfrequenz (nach [5]).
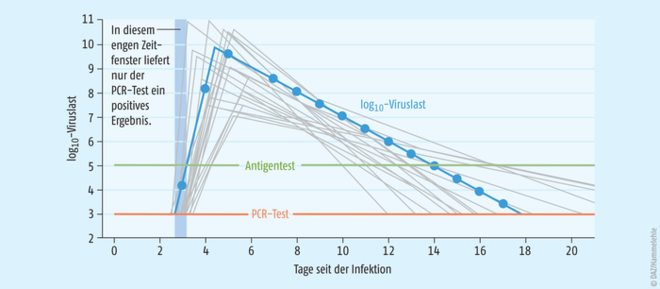
Abb. 2: Schematische Darstellung der Viruslast und der unteren Nachweisgrenze (limit of detection, LOD) für einen Antigentest (LOD 105 Viruskopien/ml Probe) und einen PCR-Test (LOD 103 Kopien/ml). Der PCR-Test schlägt wegen höherer Sensitivität etwas früher an. Das Zeitfenster, in dem nur der PCR-Test positiv ausfällt (blaue Fläche) ist im exponentiellen Viruswachstum sehr klein, das Risiko eines falsch negativen Ergebnisses beim Antigentest entsprechend gering. Im weiteren Verlauf der Infektion spielt die unterschiedliche Sensitivität keine Rolle, beide Tests bleiben während der infektiösen Phase (etwa Tage 4 bis 8) positiv, der PCR-Test noch (unnötig) lange darüber hinaus (nach [5]).
Für und wider serielles Testen
Die Konsequenzen falsch positiver Befunde fallen umso mehr ins Gewicht, je häufiger getestet wird und je geringer die Prävalenz in der Population, gibt auch Prof. Dr. Sandra Ciesek vom Universitätsklinikum Frankfurt zu bedenken. Menschen stur zweimal die Woche zu testen, unabhängig von Symptomen, sei die am weitesten gehende Strategie. Bei einer Test-Spezifität von z. B. 99% erscheinen von 1000 Personen zehn falsch positiv (s. Kasten „Glossar“). „Wenn man am selben Tag eine Abklärung hinbekommt, ist der Schaden begrenzt, aber wenn dies bei regelmäßigen Testreihen häufiger vorkommt, könnte es bei Laien auch zu einem Vertrauensverlust in die Tests kommen“, warnt die Direktorin des Instituts für Medizinische Virologie. Falsch positive Befunde träten nicht nur infolge einer nicht perfekten Spezifität auf, sondern recht häufig als Kreuzreaktion auf eine bakterielle Besiedelung, etwa mit Staphylococcus aureus, die keinen Krankheitswert habe. Die Kombination von häufigem Testen und schnellen Ergebnissen stellt nach Einschätzung von Ciesek dennoch ein sinnvolles Tool dar, um Infektionsketten zu erkennen und zu unterbrechen. Die breite Verfügbarkeit von Antigenschnelltest würde auch erlauben, Menschen großzügig bei subtilen Symptomen wie Kopf- oder Halsschmerzen zu testen, statt erst bei „typischen“ Beschwerden wie Fieber oder Husten [7].
Glossar
- PCR steht für Polymerase Chain Reaction, Polymerasekettenreaktion, eine Nukeinsäure-Amplifikationstechnik (NAT).
- Als Threshold Cycle, Ct-Wert oder kurz Ct wird bei der Realtime-PCR der Amplifikationszyklus bezeichnet, bei dem die Reaktion in die exponentielle Phase eintritt und das gesuchte Nukleinsäurefragment durch eine Fluoreszenzreaktion sichtbar wird. Bei konstanten Reaktionsbedingungen ist der Ct-Wert proportional zur Menge der untersuchten DNA oder RNA und kann zur Quantifizierung benutzt werden. Daher wird die Realtime-PCR auch als quantitative PCR oder qPCR bezeichnet. Je höher der Ct-Wert, desto geringer war die eingesetzte Menge DNA/RNA. Die ermittelten Ct-Werte sind zwischen PCR-Assays verschiedener Hersteller nur eingeschränkt vergleichbar. Eine Ct-Schwelle, ab der eine Person infektiös bzw. nicht mehr infektiös ist, kann nicht pauschal angegeben werden, ebenso wenig wie die Virusmenge, die zu einer Infektion bei exponierten Personen führt. Angaben zur Kontagiosität reichen von Ct-Werten zwischen 20 und 30. Ein Ct-Wert > 30 gilt als „nicht mehr infektiös“, da ab dieser Grenze SARS-CoV-2 in Studien nicht mehr in Kultur anzüchtbar war [4].
Ein Ct-Wert von 18 bis 21 spiegelt eine mit größter Wahrscheinlichkeit kontagiöse Viruslast von 100.000 (105) bis 1 Million (106) RNA-Kopien pro ml Probe. Diese Konzentration dürfte von evaluierten Lateral-Flow-Antigentests sicher nachgewiesen werden, eine korrekte Probeentnahme und Auswertung vorausgesetzt. Ihre untere Nachweisgrenze (limit of detection, LOD) wird bei ca. bei 100.000 (105) Kopien/ml gezogen. PCR-Assays reagieren schon bei einer um zwei Größenordnungen niedrigeren Viruslast positiv, ab etwa 103 Kopien/ml [5].
- Die Sensitivität beschreibt den Anteil der positiv getesteten Personen innerhalb einer Gruppe von tatsächlich Infizierten. 96% Sensitivität bedeutet, dass 96 von 100 Corona-Infizierten mithilfe des jeweiligen Testverfahrens ein positives und vier Personen ein falsch-negatives Ergebnis erhalten.
- Bei der Spezifität geht es um den Anteil falsch-positiver Ergebnisse. Eine Spezifität von 97% beschreibt die Zahl der negativen Ergebnisse unter den gesunden Personen. Bei einer Spezifität von 97% erhalten 97 von 100 getesteten Personen ein negatives Ergebnis. Bei drei Personen wird dagegen statistisch gesehen ein falsch-positives Ergebnis auftreten.
Was die Herausforderung durch falsch-positive Resultate angeht, ist die Antigentest-Expertin Priv.-Doz. Dr. Claudia Denkinger von der Universität Heidelberg gelassen, sie verweist auf die unterschiedliche Spezifität der Assays: „Wir haben mittlerweile über 40.000 Personen mit dem SD Biosensor-Test untersucht und hatten nur 20 falsch positive Ergebnisse, das heißt die Spezifität ist nicht 99% sondern 99,9%. Auch beim Abbott-Test sind es mindestens 99,7%. Das trifft nicht für alle zu, aber die guten Tests sind wirklich gut.“
Was können Antigenselbsttests?
Antigentests erkennen mangels Amplifikationstechnik nur eine (sehr) hohe Viruslast in den oberen Atemwegen. Dies am ehesten, wenn sie kurz vor Auftreten von Symptomen bzw. in der frühen symptomatischen Phase einer Infektion durchgeführt werden.
- Die Aussagekraft ist geringer, wenn die Tests sporadisch, anlasslos und bei niedriger Infektionsprävalenz eingesetzt werden (Vortestwahrscheinlichkeit sinkt).
- Ein positives Ergebnis im Antigentest ist nicht als Diagnose zu verstehen, sondern als Verdacht auf das Vorliegen einer Infektion mit SARS-CoV-2. Es soll zur eigenverantwortlichen häuslichen Absonderung führen und muss durch einen PCR-Test bestätigt werden.
- Ein negatives Ergebnis stellt immer nur eine Momentaufnahme dar und hat eine „Gültigkeit“ von ca. 24 Stunden. Es darf nicht zu falscher Sicherheit und der Vernachlässigung von Schutzmaßnahmen führen.
- Die Selbsttestung mit Antigentestkits für nasalen Abstrich ist praktikabel, stößt in unselektierten Populationen auf Akzeptanz und ist ausreichend genau [9, 10].
- Die Eigenanwendung der Selbsttests bringt hohe Anforderungen an das selbstverantwortliche Handeln der Anwender mit sich. Ihre breite Anwendung durch Laien sollte daher begleitet werden durch Informationskampagnen über die limitierte Sensitivität, die bleibende Notwendigkeit von Hygiene- und Abstandsregeln in der Pandemie und vor allem die Notwendigkeit von Quarantäne und PCR-Testung bei einem positiven Testergebnis.
- In gesellschaftlichem Maßstab könnte häufig wiederholtes (serielles) Testen mit schnellem Ergebnis, in Verbindung mit sofortigen Konsequenzen wie Quarantäne, die Verbreitung des neuen Coronavirus deutlich reduzieren, wobei die gegenüber PCR-Tests eingeschränkte Testsensitivität dann von untergeordneter Bedeutung ist.
- Ein Nadelöhr bei einer zunehmenden Zahl positiv bestätigter Befunde würde die Nachverfolgung durch die Gesundheitsämter darstellen (nach [1, 2]).
Auf die Frage, wann Antigenselbsttests für Laien empfehlenswert sind, nannte Priv.-Doz. Dr. Claudia M. Denkinger, Leiterin der Sektion Klinische Tropenmedizin am Universitätsklinikum Heidelberg, drei typische Situationen:
- Beim aktuellen Infektionsgeschehen (> 35/100.000) sollten sich Schüler und Lehrer testen, bevor sie in die Schule gehen, mindestens zweimal die Woche, unabhängig von Symptomen.
- Weiterhin z. B. Arbeitnehmer, die am Morgen Halskratzen verspüren, bevor sie zur Arbeit gehen.
- Testkandidaten sind auch Personen, die in einer möglichen Cluster-Situation waren, bevor sie wieder andere Personen treffen.
Gurgel- und Spucktests weniger zuverlässig
Eine noch einfachere Anwendung versprechen Antigentests, deren Probenmaterial nicht durch einen Abstrich, sondern aus Spucke, Rachenspülwasser oder Gurgelwasser gewonnen wird. Sie könnten dort eingesetzt werden, wo Abstriche aus der Nase schwierig bis unmöglich sind: in Kindergärten, Schulen oder Pflegeeinrichtungen. Die Fachwelt sieht allerdings bei Speichel- und Gurgeltests eine Datenlücke. „Die Sorge ist, dass ein Antigentest aus Speichel, aus Rachenspülwasser oder Gurgelwasser im Gegensatz zu PCR-Tests aus solchen Proben nicht so gut funktioniert. Speichel enthält Proteasen, die das Antigen, das der Test erkennen soll, zerstören können“, sagt Prof. Dr. Sandra Ciesek. Nach den Erfahrungen von Priv.-Doz. Dr. Claudia Denkinger ist bei Gurgel- und Speichelproben von einer 30% geringeren Empfindlichkeit im direkten Vergleich am Patienten zur Nasen-Probe auszugehen [8]. |
Literatur
[1] Tests zur Eigenanwendung durch Laien. Stand 6. März 2021, www.bfarm.de/DE/Medizinprodukte/Antigentests/_node.html
[2] Positionspapier des Netzwerk B-FAST im Nationalen Forschungsnetzwerk der Universitätsmedizin zu COVID-19 zur Anwendung und Zulassungspraxis von Antigen-Schnelltests zum Nachweis des neuen Coronavirus, SARS-CoV-2. Stand 5. Februar 2021
[3] Cevik M, Tate M, Lloyd O, Maraolo AE, Schafers J, Ho A. SARS-CoV-2, SARS-COV-1 and MERS-CoV viral load dynamics, duration of viral shedding and infectiousness: A living systematic review and meta-analysis. medRxiv 2020.07.25.20162107
[4] Mina MJ et al. Clarifying the evidence on SARS-CoV-2 antigen rapid tests in public health responses to COVID-19. Lancet online 17. Februar 2021, in Press, https://doi.org/10.1016/S0140-6736(21)00425-6
[5] Larremore DB et al. Test sensitivity is secondary to frequency and turnaround time for COVID-19 screening. Science Advances 1. Januar 2021;7(1): eabd5393 DOI: 10.1126/sciadv.abd5393
[6] Paltiel AD et al. Assessment of SARS-CoV-2 Screening Strategies to Permit the Safe Reopening of College Campuses in the United States. JAMA Netw Open 2020;3(7):e2016818
[7] Mutante, Schnelltests, Medikamente. NDR-Corona-Podcast Folge 77 vom 23. Februar 2021, www.ndr.de/nachrichten/info/77-Mutante-Schnelltests-Medikamente,audio838632.html
[8] Rapid antigen tests for the diagnosis of a SARS-Cov-2-Infection. Informationen des Universitätsklinikums Heidelberg, www.klinikum.uni-heidelberg.de/diagnostics-global-health
[9] Lindner AK et al. SARS-CoV-2 patient self-testing with an antigen-detecting rapid test: a head-to-head comparison with professional testing. medRxiv 2021.01.06.20249009; doi: https://doi.org/10.1101/2021.01.06.20249009
[10] Stohr JJJM et al. Self-testing for the detection of SARS-CoV-2 infection with rapid antigen tests. medRxiv preprint https://doi.org/10.1101/2021.02.21.21252153
Weitere Beiträge des Pandemie Spezials in DAZ 2021, Nr. 10
- Vektorimpfungen leicht erklärt: Wie man Apothekenkunden zur Corona-Impfung motiviert – Teil 1
- Richtiges Timing bei Standardimpfungen: Zwei Wochen vor oder nach den Corona-Vakzinen zu impfen ist kein Problem
- Hochdosiertes Vitamin C und Zink wirkungslos? Studie mit COVID-19-Patienten mangels Effekt vorzeitig gestoppt
- COVID-19-Todesfälle korrelieren mit Blutzuckerspiegel: Die Deutsche Diabetes Gesellschaft warnt
- Rätselhaftes Neuro-COVID: Ursachen für persistierende neurologische Symptome sind ungeklärt
- Und was macht die Therapie? Die Entwicklung von Arzneimitteln gegen COVID-19 führt ein Schattendasein
- Corona-Ticker: Neues zu SARS-CoV-2 in Kürze
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.