
- DAZ.online
- DAZ / AZ
- DAZ 6/2020
- Kleben gegen den Schmerz
Beratung
Kleben gegen den Schmerz
Wissenswertes rund um Schmerzpflaster
Wirkstoffhaltige Pflaster finden sich in zwei Arzneibuchmonographien. Dabei beschreibt die Monographie „Halbfeste Zubereitungen zur kutanen Anwendung“ solche Pflaster, bei denen die enthaltenen Wirkstoffe zur lokalen oder regionalen Therapie bestimmt sind. Dazu gehören die oben beschriebenen Pflaster, die nichtsteroidale Antirheumatika enthalten. Davon zu unterscheiden sind „transdermale Pflaster“, die eingesetzt werden, um eine systemische Wirkung zu erzielen. Bekannt sind hierbei z. B. Nicotinpflaster, Hormonpflaster oder Opioid-haltige Pflaster. Von ihrem Aufbau sind diese Pflaster aber prinzipiell vergleichbar. Die Einteilung erfolgt hierbei nach der Struktur in Membran- und Matrixpflaster. Heutzutage sind allerdings nur noch wenige Membranpflaster auf dem Markt. Bei den Matrixpflastern gibt es zahlreiche Weiterentwicklungen, sodass diese häufig eine komplexe Matrix aus verschiedenen Bestandteilen aufweisen.
Membranpflaster
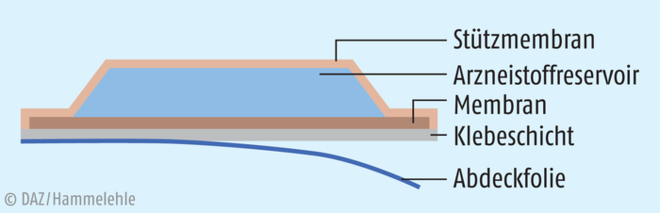
Membranpflaster werden auch als Reservoirpflaster bezeichnet, da sie ein Wirkstoffreservoir enthalten. In diesem liegt der Wirkstoff gelöst oder suspendiert in einem flüssigen oder festen Medium vor. Die Freigabe des Wirkstoffs aus diesem Reservoir wird durch eine Polymermembran kontrolliert. Zum Aufbringen auf der Haut enthält das Pflaster eine Klebeschicht aus einem geeigneten Haftkleber, welche mit einer Abdeckfolie bedeckt ist, die vor Verwendung abgezogen werden muss. Das Austreten des Wirkstoffs nach oben hin wird durch eine wasserdampf- und wirkstoffundurchlässige Folie (Stützmembran) vermieden. Diese hat gleichzeitig eine okklusive Wirkung, wodurch die Permeation des Wirkstoffs durch die Haut erhöht wird (s. Abb. 1).
Abb. 1:Bei Membranpflastern wird die Freisetzung durch eine Kontrollmembran zwischen Reservoir und Haut gesteuert. [nach: Fahr A. Voigt – Pharmazeutische Technologie. Deutscher Apotheker Verlag, 12. Auflage 2015]
Ein Vorteil von Membranpflastern ist, dass unter Sink-Bedingungen, das heißt der resorbierte Stoff wird permanent abtransportiert, eine Freigabekinetik 0. Ordnung (lineare Freisetzung) erreicht werden kann, solange die gelöste Arzneistoffkonzentration im Reservoir konstant bleibt. Membranpflaster haben allerdings auch eine Reihe von Nachteilen. So kann es bei Zerstörung oder Beschädigung der Membran zur schlagartigen Freisetzung des gesamten Wirkstoffes kommen (= Dose-Dumping). Membranpflaster dürfen deshalb niemals zerschnitten werden. Darüber hinaus hat die Kontrollmembran zur Haut hin eine zusätzliche Barrierewirkung, weshalb Membranpflaster meist deutlich größer sind als entsprechende Matrixpflaster. Direkt nach dem Wechsel des Pflasters kann es zu einem Anstieg des Wirkstoffspiegels kommen, da sich der Wirkstoff während der Lagerung aufgrund des Diffusionsausgleichs in der Klebeschicht anreichert. Die Wirkstofffreisetzung erfolgt dadurch nicht mehr konstant, was vor allem bei Pflastern problematisch sein kann, die zum Erreichen einer systemischen Wirkung eingesetzt werden.
Matrixpflaster
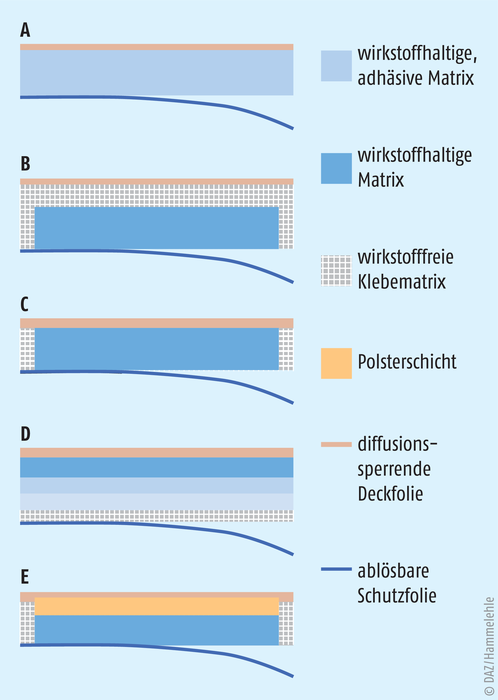
Die Mehrzahl der heute im Handel befindlichen transdermalen Pflaster sind Matrixpflaster. Sie bestehen aus einer hydrophilen oder lipophilen Klebeschicht, der sogenannten Matrix, in welcher der Wirkstoff homogen dispergiert vorliegt. Diese Schicht übernimmt gleichzeitig die Funktion von Wirkstoffreservoir, Kontrollelement und Haftkleber. Dazu kommen eine flexible, wasserundurchlässige Deckfolie und eine abziehbare Schutzfolie. Matrixpflaster können ein- oder mehrschichtig sein und eine zusätzliche Polsterschicht enthalten (s. Abb. 2).
Abb. 2:Bei Matrixpflastern ist der Wirkstoff homogen in eine Klebeschicht (Matrix) dispergiert. A: monolithisches Matrixsystem, B: Matrixsystem mit „Überpflasterung“, C: Matrixsystem mit zusätzlichem Klebering, D: mehrschichtiges Matrixsystem, E: Matrixsystem mit Pflasterschicht. [nach: Fahr A. Voigt – Pharmazeutische Technologie. Deutscher Apotheker Verlag, 12. Auflage 2015]
Die Freisetzung wird durch die Diffusion des Wirkstoffes in der Matrix bestimmt. Jedoch lässt sich auch bei Matrixpflaster eine Freisetzungskinetik 0. Ordnung erreichen, sofern nur ein kleiner Teil des in der Matrix vorhandenen Wirkstoffes verwendet wird. Das heißt, dass der Wirkstoff aber in einem deutlichen Überschuss vorhanden sein muss. Ein großer Vorteil von Matrixpflastern gegenüber Membranpflastern ist die hohe Anwendungssicherheit. Der Wirkstoff ist homogen verteilt, sodass ein Dose-Dumping nicht möglich ist. Auch sind moderne Matrixpflaster meist sehr dünn und dadurch angenehm zu tragen. Theoretisch können Matrixpflaster zerschnitten werden, jedoch fehlen meist Studien zur Sicherheit von zerschnittenen Pflastern, weshalb auch bei Matrixpflastern im Allgemeinen vom Zerteilen abgeraten wird.
Vor- und Nachteile gegenüber oralen Arzneiformen
Die transdermale Applikation bringt sowohl Vor- als auch Nachteile gegenüber oralen Arzneiformen mit sich. Ein sehr großer Vorteil ist die lange Wirkdauer von Pflastern (bis hin zu mehreren Tagen). Der Wirkstoff wird konstant über einen längeren Zeitraum abgegeben, sodass den Patienten eine mehrmals tägliche Tablettengabe erspart bleibt. Auch können dadurch in der Nacht sinkende Wirkspiegel vermieden werden. Durch eine transdermale Gabe lassen sich außerdem First-Pass-Effekte und Schluckbeschwerden umgehen. Bei wirkstoffhaltigen Pflastern, die zur lokalen Anwendung eingesetzt werden, kommt es zu geringen systemischen Wirkungen, wodurch Nebenwirkungen umgangen werden können.
Allerdings kommen für eine transdermale Applikation nicht alle Wirkstoffe infrage. Es können nur solche eingesetzt werden, die in ausreichender Menge die Hautbarriere durchdringen können und eine gute Hautverträglichkeit aufweisen. Darüber hinaus sind Pflaster, die auf eine systemische Wirkung abzielen, nicht zur Akutbehandlung geeignet, da ausreichende Plasmaspiegel erst nach einiger Zeit erreicht werden. Auch ist eine schnelle Dosisanpassung eher schwierig. Hier muss dann ergänzend zur transdermalen Gabe mit anderen Arzneiformen gearbeitet werden. Um eine lineare Freisetzung zu erreichen, kann das Pflaster nur solange genutzt werden, wie ein erheblicher Überschuss an Wirkstoff im Pflaster vorliegt. Das bedeutet aber auch, dass bei der Entsorgung das Pflaster noch größere Arzneistoffmengen enthält, was vor allem bei Opioiden problematisch sein kann. Geraten diese Pflaster in die Hände unbefugter Personen, können die noch vorhandenen Restmengen durchaus zu problematischen Wirkungen wie z. B. zur Atemdepression führen.
Korrekte Anwendung
Die korrekte transdermale Anwendung von Wirkstoffen erfordert eine gute Beratung, ganz unabhängig davon, ob der Wirkstoff zur systemischen oder für eine lokale Wirkung eingesetzt wird. Bereits bei der Lagerung ist genau darauf zu achten, welche Ober- bzw. Untergrenze bei der Temperatur vom Hersteller vorgegeben ist und ob eine Lagerung im Originalbeutel nötig ist bzw. wie lange das Medikament nach Öffnen der Originalverpackung noch anwendbar ist. Wird dies nicht beachtet, kann es zum Beispiel zum Auskristallisieren der Wirkstoffe kommen, sodass diese nicht mehr aus dem Pflaster freigesetzt werden können. Pflaster, die Wirkstoffe enthalten, dürfen niemals in der Reichweite von Kindern gelagert werden, egal ob es sich um neue Pflaster handelt oder bereits gebrauchte, da auch diese noch beträchtliche Mengen an Wirkstoff enthalten können.
Die Stelle, auf die das Pflaster aufgeklebt werden soll, muss selbstverständlich sauber, trocken, haar- und fettfrei sein. Beim Anbringen des Pflasters sollte die Klebefläche nicht berührt werden, außerdem dürfen keine Falten oder Luftblasen beim Aufkleben entstehen. Danach sollte das Pflaster für ca. 30 Sekunden fest mit der ganzen Handfläche aufgedrückt werden, falls nötig, kann das Pflaster anschließend zusätzlich fixiert werden. Zumindest bei Pflastern, die zur systemischen Anwendung eingesetzt werden, sollte die Klebestelle regelmäßig gewechselt werden, um Hautreizungen zu vermeiden. Der Pflasterwechsel sollte nach den von den Herstellern vorgegebenen Intervallen durchgeführt werden. Bei wirkstoffhaltigen Pflastern zur lokalen Anwendung ist dies natürlich nicht möglich.
Entsprechend der „4-S-Regel“ sollte die Einwirkung von Sonne, Sauna, Solarium oder Sommerhitze gemieden werden, da durch einen Temperaturanstieg die Freisetzungskinetik des Pflasters beeinflusst werden kann. Dies gilt natürlich auch für weitere Wärmequellen wie z. B. Heizstrahler oder Wärmflaschen. Sind die Pflaster wasserfest, brauchen sie zum Duschen oder Baden nicht entfernt werden, allerdings muss dann darauf geachtet werden, dass die Wassertemperatur 37 °C nicht übersteigt. Ebenfalls beeinflussen Okklusivverbände die Wirkstofffreisetzung und sind deshalb nicht anzuwenden.
Nach Gebrauch des Pflasters ist auf die korrekte Entsorgung zu achten. Dazu wird das Pflaster mit der Klebefläche nach innen zusammengeklappt und anschließend in den Hausmüll gegeben.
Schmerzpflaster
Schmerzpflaster stehen sowohl im Rx- (z. B. Fentanyl, Buprenorphin) als auch im OTC-Bereich (Diclofenac, Ibuprofen) zur Verfügung. Während eine Vielzahl an verschreibungspflichtigen Schmerzpflastern auf dem Markt ist, befinden sich gerade einmal drei Diclofenac- und nur ein Ibuprofen-Pflaster im Handel (s. Tab. 1).
Diclofenac-ratiopharm® Schmerzpflaster | Flector® Schmerzpflaster | Voltaren Schmerzpflaster | Nurofen®-24h-Schmerzpflaster | |
|---|---|---|---|---|
Wirkstoff | Diclofenac-Natrium | Epolamin-Diclofenac | Diclofenac-Natrium | Ibuprofen |
Wirkstoffgehalt | 140 mg Diclofenac-Natrium ≙ 130,33 mg Diclofenac | 180 mg Epolamin-Diclofenac ≙ 140 mg Diclofenac-Natrium ≙ 130,33 mg Diclofenac | 140 mg Diclofenac-Natrium ≙ 130,33 mg Diclofenac | 200 mg Ibuprofen |
Indikation | Kurzzeitbehandlung; lokale symptomatische Behandlung von Schmerzen bei akuten Zerrungen, Verstauchungen oder Prellungen im Bereich der Extremitäten infolge stumpfer Traumen | lokale, symptomatische Behandlung von Schmerzen bei Epicondylitis sowie Fußgelenkdistorsionen | Kurzzeitbehandlung; zur lokalen, symptomatischen Behandlung von Schmerzen bei akuten Prellungen, Zerrungen oder Verstauchungen infolge eines stumpfen Traumas | kurzzeitige, symptomatische Behandlung
|
maximale Anwendungsdauer | sieben Tage | drei Tage (bei Fußgelenkdistorsionen) 14 Tage (bei Epicondylitis) | sieben Tage | fünf Tage |
maximale Tagesdosis | zwei Stück | ein Stück (bei Fußgelenkdistorsionen) zwei Stück (bei Epicondylitis) | zwei Stück | ein Stück |
Altersbeschränkung | ab 16 Jahren | ab 16 Jahren | ab 16 Jahren | ab 16 Jahren |
Haltbarkeit | vier Monate nach Öffnen des Beutels | drei Monate nach Öffnen des Beutels | bis zum Verfalldatum, da Pflaster einzeln in Beuteln verpackt | sechs Monate nach Öffnen des Beutels |
Lagerung | nicht über 25 °C | nicht über 25 °C | nicht über 30 °C | nicht über 25 °C (Packung mit zwei Stück) nicht über 30 °C (Packung mit vier Stück) |
teilbar | nein | nein | nein | nein |
wasserfest | keine Angaben | nein | nein | nein |
Größe des Pflasters | 10 × 14 cm | 10 × 14 cm | 10 × 14 cm | 10 × 14 cm |
Packungsgröße | fünf Stück, zehn Stück | fünf Stück | fünf Stück | zwei Stück, vier Stück |
Art des Pflasters | Matrixpflaster | Matrixpflaster | Matrixpflaster | Matrixpflaster |
Besonderheit | mit elastischem Netzstrumpf | enthält Kollophonium → Cave: allergische Reaktionen |
Diclofenac-haltige Pflaster enthalten 180 mg Epolamin-Diclofenac (entspricht 140 mg Diclofenac-Natrium) oder 140 mg Diclofenac-Natrium. In verschiedenen Studien konnte sowohl eine gute Wirksamkeit von Epolamin-Diclofenac-haltigen [9, 10, 11] als auch Diclofenac-Natrium-haltigen Pflastern [12] gezeigt werden bei gleichzeitig guter Verträglichkeit. Das Epolamin-Diclofenac (Diclofenac-Hydroxyethylpyrrolidin) ist ein amphiphiles Molekül und weist gegenüber dem Natrium-Salz eine doppelt so hohe Wasser- und Fettlöslichkeit auf. Dadurch kann der Wirkstoff – wie in einer Studie nachgewiesen wurde [10] – mindestens drei Zentimeter tief ins Gewebe eindringen. Diclofenac-Pflaster können kurzfristig zur Behandlung von akuten Schmerzen bei Zerrungen, Verstauchungen und Prellungen, z. B. durch Sportverletzungen eingesetzt werden, sowie zur Behandlung der Epicondylitis („Tennisellenbogen“). Diclofenac wird dabei nur langsam und unvollständig aus der Zubereitung resorbiert. Die Wirkstofffreisetzung erfolgt konstant über zwölf Stunden. Die Spitzenplasma-Spiegel betragen ca. 1 bis 3 ng/ml [5, 7] bzw. ca. 17 ng/ml [6], das entspricht ca. 2 bis 10% dessen, was mit der gleichen, oral eingenommenen Dosis erreicht werden würde. Die beobachtete Wirksamkeit ist somit nicht durch eine Aufnahme des Wirkstoffes in die Blutbahn, sondern durch das Erreichen einer therapeutisch relevanten Konzentration am Wirkort zu erklären. Systemische Nebenwirkungen können dadurch weitgehend vermieden werden. Die maximale Tagesdosis liegt bei zwei Diclofenac-Pflastern, unabhängig vom Hersteller. Trotz der geringen systemischen Spiegel sollten nach Herstellervorgaben nicht gleichzeitig mehrere Stellen behandelt werden. Auch sollten während der Anwendung der Pflaster keine Diclofenac-haltigen Cremes oder Salben verwendet sowie eine gleichzeitige Einnahme von NSAR in oraler Form vermieden werden.
Auf einen Blick
- Pflaster, die einen Wirkstoff enthalten, gibt es zur systemischen und zur lokalen Anwendung.
- Nach der Struktur unterscheidet man Membran- und Matrixpflaster.
- Moderne Pflaster sind meist Matrixpflaster.
- Vorteile der Pflaster sind die lange Wirksamkeit, die Umgehung des First-Pass-Effektes und der Einsatz bei Schluckbeschwerden.
- Nachteile sind unter anderem ein mögliches „Dose-Dumping“ bei Membranpflastern und die Limitierung bei der Wirkstoffauswahl (Hautgängigkeit, Hautverträglichkeit).
- Für die Selbstmedikation stehen Diclofenac- und ein Ibuprofen-Pflaster zur lokalen Anwendung z. B. bei Sportverletzungen zur Verfügung.
Ibuprofen ist in Pflasterform derzeit nur als Nurofen®-24h-Schmerzpflaster erhältlich. Es enthält 200 mg Ibuprofen und kann zur kurzzeitigen, symptomatischen Behandlung von lokalen Schmerzen bei akuten Zerrungen oder Verstauchungen eingesetzt werden. Ebenso wie bei den Diclofenac-Pflastern konnte auch für das Ibuprofen-Pflaster eine gute Wirksamkeit und Anwendungssicherheit nachgewiesen werden [13, 14]. Der Wirkstoff wird dabei – wie der Name schon sagt – über 24 Stunden konstant abgegeben, dabei werden im Mittel über 24 Stunden nur 32,2 mg der 200 mg freigesetzt. Da der Wirkstoff direkt in den Schmerzbereich abgegeben wird, ist diese Wirkstoffmenge therapeutisch ausreichend. Der maximale Plasmaspiegel liegt mit ca. 0,5 µg/ml deutlich unter dem Wert, welcher mit einer oralen Gabe von 200 mg bis 400 mg Ibuprofen erreicht werden würde (20 µg/ml bis 50 µg/ml) [15]. Dennoch wird als maximale Tagesdosis ein Pflaster angegeben, sodass auch hier nicht mehr als eine Stelle gleichzeitig behandelt werden kann. Ebenso rät der Hersteller von einer zusätzlichen Einnahme oraler oder topischer NSAR ab. |
Literatur
[1] Fahr A. Voigt – Pharmazeutische Technologie. Deutscher Apotheker Verlag, 12. Auflage 2015
[2] Mäder K, Weidenauer U. Innovative Arzneiformen. Wissenschaftliche Verlagsgesellschaft Stuttgart 2009
[3] Kirchner W. Arzneiformen richtig anwenden. Deutscher Apotheker Verlag, 4. Auflage 2016
[4] Keiner D. Transdermale therapeutische Systeme. Med Monatsschr Pharm 2018;41(09):369-375
[5] Fachinformation Diclofenac-ratiopharm® Schmerzpflaster, Stand: August 2019
[6] Fachinformation Flector® Schmerzpflaster, Stand: Januar 2014
[7] Fachinformation Voltaren Schmerzpflaster, Stand: März 2019
[8] Fachinformation Nurofen®-24h-Schmerzpflaster, Stand: Mai 2019
[9] Galer BS et al. Topical Diclofenac Patch Relieves Minor Sports Injury Pain: Results of a Multicenter Controlled Clinical Trial. J Pain Symptom Manage 2000;19:287-294
[10] Affaitati G et al. Effects of Topical Diclofenac (DHEP Plaster) on Skin, Subcutis ans Muscle Pain Thresholds in Subjects Without Spontaneous Pain. Drugs Exp Clin Res 2001;27(2):69-76
[11] Rainsord KD et al. Review oft he pharmaceutical properties and clinical effects of the topical NSAID formulation, diclofenac epolamine. Curr Med Res Opin 2008;24(10):2967-2992
[12] Mutual Recognition Procedure Public Assessment Report Diclofenac Ratiopharm Schmerzpflaster. DE/H/1479-81-001/MR, Stand. 3. Januar 2018, https://mri.cts-mrp.eu/human/downloads/DE_H_1480_001_PAR.pdf
[13] Predel HG et al. Efficacy and safety assessment of acute sports-releated traumatic soft tissue injuries using a new ibuprofen medicated plaster: results from a randomized controlled clinical trial. The Physician and Sportsmedicine 2017;45(4):418-425
[14] Predel HG et al. Efficacy and tolerability of a new ibuprofen 200 mg plaster in patients with acute sports-related traumatic blunt soft tissue injury/contusion. Postgrad Med 2018;130(1):24-31
[15] Lewis F et al. A Pharmacokinetic Study of an Ibuprofen Topical Patch in Healthy Male and Female Adult Volunteers. Clin Pharmacol Drug Dev 2018;7(7):684-691























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.