
- DAZ.online
- DAZ / AZ
- DAZ 27/2020
- Der feine Unterschied
Beratung
Der feine Unterschied
Johanniskrautextraktpräparate in der Therapie von Depressionen
In der traditionellen Anwendung von Johanniskraut spielten psychiatrische Indikationen keine große Rolle, obwohl erste Hinweise auf eine Wirksamkeit viele Jahrhunderte zurückgehen [2]. Die Aufmerksamkeit erhöhte sich schlagartig, als Anfang der 80er-Jahre des zurückliegenden Jahrhunderts die frühere Firma Lichtwer Pharma in Berlin das hoch dosierte Extraktpräparat Jarsin® (300 mg pro Dragee, Tagesdosis 900 mg) auf den Markt brachte. Der Produkteinführung folgten Placebo-kontrollierte Studien an depressiven Patienten, was in der damaligen Zeit für Phytopharmaka eher unüblich war, besonders da die Zulassung auf die 1984 publizierte Monographie der Kommission E zurückging [2], die eher auf der traditionellen Anwendung, nicht aber auf wissenschaftlichen Daten beruhte.
Jarsin® wurde in der Allgemeinmedizin zur Anwendung bei leichteren depressiven Störungen mit großem Erfolg verordnet – vor allem wegen der problemlosen Anwendung und der guten Verträglichkeit. Eine wichtige Rolle spielte auch die große Akzeptanz durch die Patienten, die sich eher bereit erklärten „etwas Pflanzliches“ als ein synthetisches Antidepressivum einzunehmen. Einige andere Analogpräparate wie z. B. Neuroplant® oder Laif® folgten, und auch weitere, den modernen Kriterien besser entsprechende klinische Studien wurden vorgelegt. Die Akzeptanz war so groß, dass Ende der 1980er-Jahre Johanniskrautextraktpräparate circa 25% aller ärztlichen Verordnungen für Antidepressiva ausmachten. Mit der zunehmenden Erkenntnis, dass der Einsatz von Johanniskraut nicht immer hilft und zudem mit Problemen (z. B. unerwünschten Arzneimittelwirkungen, Interaktionen) verbunden sein kann, hat der ärztliche Einsatz von Johanniskrautextraktpräparaten inzwischen deutlich abgenommen. Grund dafür sind auch die Aussetzung der Erstattungsfähigkeit von nicht verschreibungsfähigen Phytopharmaka durch die gesetzlichen Kassen und die zunehmende Verfügbarkeit der relativ gut verträglichen selektiven Serotonin-Wiederaufnahmehemmer (SSRI). Lediglich drei Präparate erhielten in den folgenden Jahren aufgrund ausführlicher pharmakologischer, toxikologischer und klinischer Daten eine volle Arzneimittelzulassung für leichte bis mittelschwere depressive Episoden nach ICD-10, also für die Erkrankung Depression (siehe Tabelle 1). Sie wurden dadurch automatisch rezeptpflichtig und sind nach ärztlicher Verordnung erstattungsfähig.
Trockenextrakt (3 – 6 : 1); Methanol 80% (V/V) | |
Jarsin® Rx 300 mg überzogene Tablette | Rp. |
Jarsin® 300 mg überzogene Tablette | OTC |
Kira® 300 mg überzogene Tablette | OTC |
Jarsin® 450 mg Filmtablette | OTC |
Jarsin® 450 mg überzogene Tablette | OTC |
Jarsin® 750 mg Filmtablette | OTC |
Trockenextrakt (3 – 6 : 1); Ethanol 80% | |
Laif® 900 Filmtablette | Rp. |
Laif® Balance Filmtablette | OTC |
Trockenextrakt (3 – 7 : 1); Methanol 80% | |
Neuroplant®Filmtablette | Rp. |
Neuroplant® Aktiv Filmtablette | OTC |
Neuroplant® 300 mg Novo Filmtablette | OTC |
Trockenextrakt (3,5 – 6 : 1); Ethanol 60% | |
Felis® 425 mg Hartkapsel | OTC |
Felis® 650 mg Filmtablette | OTC |
Herbaneurin 250 mg Hartkapsel | OTC |
Jo-Sabona® forte 425 mg Hartkapsel | OTC |
Johanniskraut dura® 425 mg Hartkapsel | OTC |
Johanniskraut Madaus 425 mg Hartkapsel | OTC |
Johanniskraut-ratiopharm® 425 mg | OTC |
Lemur 425 mg | OTC |
Pharmakologie des Extraktes
Die hohe Akzeptanz von Johanniskrautextraktpräparaten wurde unter anderem dadurch gefördert, dass parallel zu den klinischen auch die pharmakologischen Untersuchungen große Analogien zwischen der Wirkweise von synthetischen Antidepressiva und Johanniskrautextrakt und seinen Inhaltsstoffen zeigten. Die in den Monographien der Kommission E und dem später folgenden Europäischen Arzneibuch noch benutzte traditionelle Formulierung „der Extrakt ist der Wirkstoff“ und die Erwähnung von Hypericin, Flavonoiden und Hyperforin als eher gleichwertige, aber nicht gut untersuchte wirkungsrelevante Inhaltsstoffe [1] ist moderneren Konzepten nach nicht mehr haltbar. In der Regel wirken Extrakte über ein oder mehrere Wirkstoffe an spezifischen Targets. Dies ist auch bei Johanniskrautextrakt der Fall, wo wir heute relativ klare Vorstellungen haben, welche Wirkstoffe in welchem Maß zur Wirksamkeit beitragen und welche molekularen Targets für die antidepressive Wirkung relevant sind.
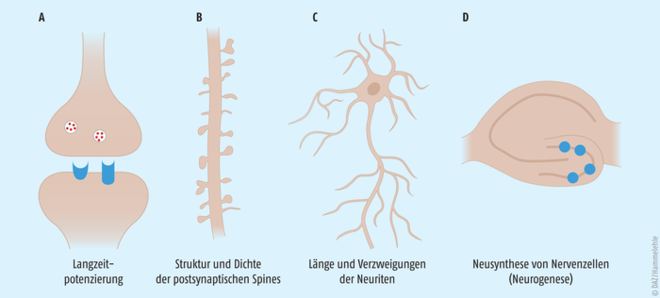
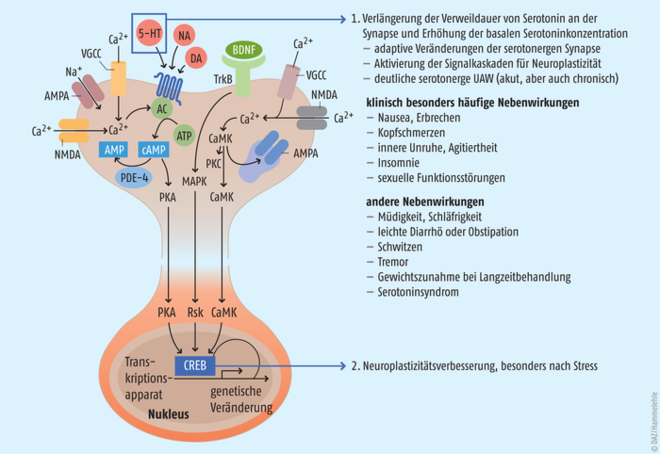
Fast alle synthetischen Antidepressiva hemmen direkt die hochaffinen Natriumionen-getriebenen Transportermoleküle der drei aminergen Neurotransmitter Serotonin, Noradrenalin und Dopamin in präsynaptischen Nervenendigungen. Dies kann in vitro an isolierten Nervenendigungen (Synaptosomen) untersucht werden, bei denen man sicherstellen kann, dass nur diese hochaffinen spezifischen Transporter erfasst werden. Bei der Verwendung von Hirnschnitten hingegen, wo unspezifische Diffusionseffekte erfasst werden, ist ein solcher Nachweis nicht möglich. Im Gehirn führt die Hemmung der Transporter zu einer erhöhten synaptischen Konzentration der Neurotransmitter. Die Konsequenz ist die Intensivierung des synaptischen Signals über eine stärkere Aktivierung postsynaptischer Rezeptoren. Auch Hemmstoffe der Monoaminoxidase A, beispielsweise das bei uns als Antidepressivum zur Verfügung stehende Tranylcypromin, erhöhen die synaptische Transmitterkonzentration. Neben einer Änderung der Funktion postsynaptischer Nervenzellen kommt es auch zu einer Aktivierung intrazellulärer Signalkaskaden, verbunden mit einer Zunahme des Transkriptionsfaktors CREB als wichtigstem Wirkungsmechanismus aller Antidepressiva (siehe Abbildung 2). In der Folge kommt es zur vermehrten Synthese neurotropher Faktoren wie z. B. dem Brain derived neurotrophic factor BDNF und letztlich zu einer Aktivierung der synaptischen Plastizität. Die Nervenzellen passen sich strukturell an Perioden der Unter- bzw. Überaktivität an (siehe Abbildung 1), z. B. durch Erhöhung der Synapsendichte und Wiederherstellung der dendritischen Verzweigungen, die für die Kommunikation zwischen einzelnen Neuronen in einem Hirnareal, aber auch zwischen unterschiedlichen Hirnarealen essenziell sind. Diese Effekte auf die synaptische Plastizität gelten heute als gemeinsame Endstrecke aller verfügbaren Antidepressiva (einschließlich Ketamin) und gehen parallel mit Befunden, dass die synaptische Plastizität bei depressiven Störungen gestört ist [3].
Abb. 1: Neuronale Plastizität bezeichnet die Veränderbarkeit neuronaler Verbindungen im Nervensystem. Unter dem Begriff werden verschiedene Mechanismen der synaptischen Funktionsanpassung zusammengefasst, z. B. A) die Langzeitpotenzierung (ein Mechanismus der Signalimprägnierung), histologisch fassbare Veränderungen wie B) die Dichte und Struktur postsynaptischer Spines, C) die Länge und Verzweigungen von Neuriten und D) die Neusynthese von Nervenzellen (Neurogenese), die allerdings hauptsächlich zwei kleinen Arealen des Hippocampus vorbehalten ist. Im weiteren Sinn gehört dazu auch die synaptische Plastizität auf der Ebene der Signaltransduktion (Rezeptoren, Transportermoleküle, Enzyme), die aber nur teilweise durch Änderungen der Syntheserate, häufig aber auch posttranslational, z. B. durch Internalisierung, vermittelt wird. Analog zu allen anderen Antidepressiva verändern Johanniskrautextrakt und / oder Hyperforin alle Aspekte der Neuroplastizität [6, 11, 12, 13, 14, 40, 41, 42].
Abb. 2: Die Rolle molekularer Mechanismen der Neuroplastizität bei der Wirkung von Antidepressiva am Beispiel von Serotonin-Wiederaufnahmehemmern: Bei SSRI werden durch die Erhöhung der synaptischen Serotoninkonzentration, die auch gleichzeitig die Ursache der vielen serotoninergen UAW der SSRI ist, verschiedene intrazelluläre Signalkaskaden angestoßen [3, 14, 15]. Sie resultieren in einer Aktivierung des Transkriptionsfaktors CREB, gefolgt von Effekten auf die Mechanismen der Neuroplastizität (siehe Abb. 1). Johanniskraut und der Inhaltsstoff Hyperforin können über eine Erhöhung der synaptischen Transmitterkonzentration und direkt über eine Aktivierung von TRPC6-Kanälen ebenfalls CREB aktivieren und so die Neuroplastizität verbessern. (Abbildung nach [3])
Die Targetselektivität der Antidepressiva wird durch ihre selektive Hemmung eines oder mehrerer Transporter determiniert. So sind SSRI beispielsweise hochselektiv für den präsynaptischen Serotonintransporter. Die Targetselektivität geht jedoch in den ähnlichen Effekten auf die Mechanismen der Neuroplastizität als gemeinsame Endstrecke verloren, was die vergleichbare therapeutische Wirksamkeit aller Antidepressiva erklärt [4].
Diese Darstellung des generellen Wirkungsmechanismus von Antidepressiva ist wichtig, um Gemeinsamkeiten und Unterschiede der spezifischen antidepressiven Pharmakologie von Johanniskraut zu verstehen. Schon in den ersten Untersuchungen konnte anhand verhaltenspharmakologischer Tiermodelle, die indikativ für eine antidepressive Wirksamkeit sind, z. B. dem Forced Swim Test, gezeigt werden, dass Johanniskrautextrakt analog zu anderen Antidepressiva wirksam ist [5, 6, 7]. Die früher beschriebene und immer noch in den Monographien und vielen Publikationen favorisierte Hemmung der Monoaminoxidase A konnte in neueren Untersuchungen nur für sehr hohe Konzentrationen bestätigt werden. Sie kann die bei niedrigen, therapierelevanten Dosen zu sehenden antidepressiven Effekte jedoch nicht erklären [5, 6, 7]. Dagegen hemmt Johanniskrautextrakt in therapeutisch relevanten Konzentrationen die synaptosomale Aufnahme von Noradrenalin, Serotonin, und Dopamin in vitro [8, 9] und führt in vivo zu ähnlichen Veränderungen dieser Neurotransmitter im Gehirn wie synthetische Antidepressiva [10].
In verschiedenen Modellen [12] wurde gesehen, dass Johanniskrautextraxt ebenfalls eine Aktivierung des Transkriptionsfaktors CREB als Ausdruck eines Effektes auf Mechanismen der Neuroplastizität bewirkt (siehe Abbildung 2). Auch In-vivo-Studien an Versuchstieren bzw. gesunden Probanden, denen Johanniskrautextrakt oral verabreicht wurde, bestätigen die Aktivierung von CREB und neurotrophen Faktoren und eine Verbesserung der Neuroplastizität [12, 13, 14]. Somit bedient Johanniskrautextrakt letztlich die gleichen Wirkungsmechanismen, die heute als gemeinsame Endstrecke des Wirkungsmechanismus aller Antidepressiva angesehen werden [3, 15, 16]. Und so wird auch verständlich, dass die Johanniskrautextrakte, die die Basis der pharmakologischen Untersuchungen waren, sich in klinischen Studien an depressiven Patienten gleichwertig zu synthetischen Antidepressiva zeigten [17].
Hyperforin wirkt nachweislich antidepressiv
In nachfolgenden Untersuchungen konnte die oben aufgeführte typische antidepressive Pharmakologie eindeutig dem Inhaltsstoff Hyperforin zugeordnet werden. Alle anderen Inhaltsstoffe hatten keine Effekte auf die synaptosomale Neurotransmitteraufnahme [8, 19], auf die Aktivierung von CREB und auf die Neurogenese als Ausdruck eines Effektes auf die Neuroplastizität als wichtigster Endpunkt in der Pharmakologie von Antidepressiva (siehe Abbildung 1) [11, 22]. Im direkten Vergleich gegen Placebo und einen Hyperforin-haltigen Extrakt zeigte ein Hyperforin-armer Extrakt keine klinische Wirksamkeit an depressiven Patienten und war auch in Tiermodellen nicht wirksam [18, 29].
Interessanterweise hemmt Hyperforin nicht analog zu anderen Antidepressiva die synaptosomale Aufnahme der Neurotransmitter durch kompetitive Bindung an die Transportermoleküle, sondern durch eine Erhöhung der intrazellulären Natriumkonzentration. Damit verbunden kommt es zu einer Reduktion des Natriumgradienten, der die treibende Kraft der durch Natrium-Kotransport vermittelten Transmitteraufnahme darstellt, von extra- zu intraneuronal [8, 20]. Dies erklärt, dass Hyperforin auch die durch Natriumionen-Kotransport vermittelte Aufnahme anderer Neurotransmitter in Nervenendigungen (GABA, L-Glutamat) reduziert [19]. Als spezifisches Target für Hyperforin konnte eine Aktivierung des Ionenkanals TRPC6 (transient receptor potential channel) identifiziert werden [21].
Wie bereits ausgeführt, gelten Effekte auf die Neuroplastizität heute als der wesentliche Wirkungsmechanismus aller Antidepressiva. Für Hyperforin konnten direkte Effekte auf verschiedene Mechanismen der Neuroplastizität gezeigt werden, die in Zellmodellen und hippokampalen Hirnschnitten sehr genau untersucht werden können und über eine Aktivierung von TRPC6-Kanälen vermittelt werden [11, 21, 22]. Diese Effekte sind wiederum nur für Hyperforin, nicht aber für die anderen Inhaltsstoffe von Johanniskraut bestätigt [11]. Die Aktivierung des wichtigen Transkriptionsfaktors CREB, des Rezeptors für den neurotrophen Faktor BDNF (TrkB) und von BDNF selbst durch Hyperforin konnte auch in Untersuchungen an Mäusen und Ratten nach subchronischer Gabe von Hyperforin gezeigt werden [23, 24].
Welche Rolle spielt Hypericin?
Bei dieser Fülle an Daten für Hyperforin stellt sich natürlich die Frage nach der Relevanz der anderen Inhaltsstoffe für die therapeutische Wirksamkeit, zumal immer noch von einigen Autoren das alte Konzept der Wirksamkeit des Gesamtextraktes, aber mit besonderer Betonung des Hypericins, verfolgt wird. Hypericin penetriert die Bluthirnschranke schlecht bis gar nicht [28]. Diese Befunde erklären, dass nur wenige belastbare tierexperimentelle Daten vorliegen, die (in therapeutisch relevanten Dosen) für eine antidepressive Wirkung in verhaltenspharmakologischen Modellen sprechen. Unter anderem war Hypericin als isolierter Inhaltsstoff im Immobilisationstest an der Ratte nicht wirksam [29, 30], sondern nur in Kombination mit Procyanidinen [30], wobei jedoch nicht berücksichtigt wurde, dass Procyanidine isoliert im gleichen Modell wirksam sein können [32, 33]. Für alle biochemisch-pharmakologischen Untersuchungen zum generellen Wirkungsmechanismus von Antidepressiva, in denen Hyperforin wirksam ist, gibt es keine Daten zu Hypericin. Effekte von Hypericin auf die Neuroplastizität als wesentlichem gemeinsamen Endpunkt antidepressiver Wirksamkeit von Johanniskrautextrakt und anderer Antidepressiva sind nicht bekannt [11]. Gezeigt werden konnte allerdings eine Beeinflussung der Funktion der Hypothalamus-Hypophysen-Nebennierenrinden-Achse (HPA-Achse), die außerhalb der Bluhirnschranke liegt. Ob eine Verbesserung der HPA-Achsen-Funktion an der antidepressiven Wirksamkeit beteiligt ist, ist umstritten. Es wird diskutiert, ob die bei depressiven Patienten oft vorliegende Dysfunktion der HPA-Achse kein spezifisches Symptom der Depression ist, sondern als chronisches Stressphänomen z. B. auch bei schizophrenen und Angst-Patienten vorliegen kann. Viele therapeutische Ansätze mit Wirkstoffen, die auf eine Normalisierung einer gestörten HPA-Achsenfunktion bei depressiven Patienten abzielten, sind in klinischen Studien leider gescheitert. Damit ist Hypericin der Inhaltsstoff, für den eine Beteiligung am antidepressiven Profil von Johanniskrautextrakt am schlechtesten belegt ist.
Flavonoide sind an der Wirkung des Gesamtextraktes beteiligt
Verschiedene Flavonoide besitzen antidepressive Eigenschaften, wenn auch die klinischen Evidenzen relativ gering sind und die Wirkung auch nur für wenige Flavonoide gezeigt werden konnte [31]. Ein Flavonoid-haltiger Extrakt vom Feigenkaktus und die beiden Hauptinhaltsstoffe Kämpferol und Quercitirin zeigten in einem experimentellen Tiermodell eine antidepressive Wirkung [35]. Ein ähnlicher Extrakt von der gleichen Pflanze war ebenfalls im Immobilisationstest wirksam und hatte moderate Effekte auf die synaptosomale Serotoninaufnahme in vitro und ex vivo. Er senkte die Stress-indizierte Erhöhung von Plasmacorticosteron an der Maus [43] und zeigte typische Stimmungseffekte an gesunden Probanden [44].
Für einige der in Johanniskrautextrakt zu findenden Flavonoide und Biflavone konnten im Tierexperiment ebenfalls antidepressive Eigenschaften gezeigt werden (Hyperosid, Isoquercitrin, Biapigenin) [29]. Das gleiche gilt für Procyanidine [32, 33]. Darüber hinaus könnte für die antidepressiven Effekte eine Reduktion von oxidativem Stress eine wichtige Rolle spielen [36], da Johanniskrautextrakt und die darin vorkommenden Flavonoide sehr potente Antioxidanzien sind und erhöhter oxidativer Stress bei affektiven Erkrankungen und auch bei Depression eine Rolle spielen [37].
Unterschiedliche Johanniskrautpräparate und deren Zulassungsstatus
In Deutschland gibt es eine große Zahl an nicht apothekenpflichtigen Johanniskrautpräparaten, die nicht zugelassen, sondern nur als traditionelle Arzneimittel registriert sind und zum Teil Extrakt, zum Teil aber auch nur das Drogenpulver als Tablette enthalten. Zur Registrierung müssen keine Studien zur Wirksamkeit oder Unbedenklichkeit vorgelegt werden, sondern nur der Beleg einer längeren traditionellen Anwendung (mindestens 30 Jahre). Allen traditionellen pflanzlichen Arzneimitteln ist gemein, dass durch eine gesetzliche Vorgabe der Johanniskrautextraktgehalt sehr niedrig gehalten werden muss, sodass mit einer relevanten Wirksamkeit bzw. relevanten Nebenwirkungen nicht gerechnet werden kann [38].
Neben den Supermarktartikeln gibt es auch eine große Anzahl von apothekenpflichtigen Johanniskrautpräparaten sowie drei rezeptpflichtige Präparate (siehe Tabelle 1), die sich im Hinblick auf die wissenschaftliche Datenlage erheblich unterscheiden und nicht als gleichwertig betrachtet werden können [1]. Die meisten apothekenpflichtigen Präparate beziehen sich auf eine Zulassung auf Basis der Monographie E, die global und ohne spezifischen Wirksamkeitsbeleg allen Extrakten mit relativ großer Varianz bezüglich Extraktionsmittel und Droge-Extrakt-Verhältnis eine Wirksamkeit zuspricht. Diese rezeptfreien Präparate haben keine Zulassung für die unipolare Depression als Erkrankung (ICD F33, F33.1), sondern nur für leichte vorübergehende depressive Störungen, was unter der Schwelle der Erkrankung einer klinisch relevanten unipolaren Depression liegt. Für die Erkrankung Depression sind die apothekenpflichtigen Präparate nicht zugelassen. Spezifische pharmakologische und / oder klinische Daten gibt es für diese Präparate bzw. für den verwendeten ethanolischen (60%) Extrakt nicht (siehe Tabelle 1) und ob sie tatsächlich wirksam sind, ist nicht belegt.
Lediglich drei Präparate legen ausreichende spezifische pharmakologische und klinische Daten zur Sicherheit (auch toxikologische Daten) und Wirksamkeit vor, sodass eine Arzneimittelzulassung zur Behandlung der unipolaren Depression (leichte bis mittelschwere Episode) erteilt wurde (Jarsin® RX 300, Laif®, Neuroplant®). So wie alle Antidepressiva sind auch diese drei Präparate rezeptpflichtig und – als Besonderheit für den deutschen Markt – erstattungsfähig. Für die Selbstmedikation stehen die Präparate auch in einer apothekenpflichtigen und in der Indikation (leichte depressive Störungen) abgespeckten Form zur Verfügung (siehe Tabelle 1).
Unterschiedliche klinische Datenlage
Beginnend mit den ersten klinischen Untersuchungen in den 1980er-Jahren sind eine Reihe von klinischen Prüfungen mit Johanniskrautextraktpräparaten an Patienten mit depressiven Störungen durchgeführt worden. Eine Metaanalyse, die vor wenigen Jahren publiziert wurde, listet die qualitativ akzeptablen Studien auf [16]. Die Metaanalyse zeigt eine klare Überlegenheit zu Placebo und eine vergleichbare Wirksamkeit zu verschiedenen anderen Antidepressiva wie z. B. Fluoxetin oder Sertralin. Der größte Teil der klinischen Daten bezieht sich auf die Fertigarzneimittel Jarsin®, Leif®, und Neuroplant®, der Rest auf bei uns nicht zugelassene Präparate. Für alle anderen zur Zeit in Deutschland gelisteten Präparate (siehe Tabelle 1) gibt es keine klinischen Prüfungen. Ihre Fachinformationen beziehen sich auf die klinischen Daten der anderen Präparate.
Im Fall von Jarsin® beziehen sich alle klinischen Daten auf eine dreimal tägliche 300-mg-Dosierung wie im rezeptpflichtigen Präparat Jarsin® RX 300 mg, für die anderen Wirkstärken gibt es keine Daten. Bei Laif® und Neuroplant® beziehen sich die klinischen Daten auf das rezeptpflichtige Laif® 900 bzw. das rezeptpflichtige Neuroplant®. Die rezeptfreien Präparate Laif® 900 Balance und Neuroplant® aktiv sind identisch zu den rezeptpflichtigen Präparaten, haben allerdings nur, wie erwähnt, eine Zulassung für die Selbstmedikation. Auch für das 300-mg-Präparat von Neuroplant® gibt es zwei positive Studien. Ein Hyperforin-armer, aber Flavonoid- und Hypericin-reicher Extrakt (Ze117) ist in der Schweiz auf dem Markt. Ob er ausreichend wirksam ist, erscheint nicht belegt, da es kaum belastbare pharmakologische Daten für diesen Extrakt gibt und zwei klinische Studien wegen methodischer Probleme sehr kritisch gesehen werden müssen [5, 6, 17].
Auf einen Blick
- Die Pharmakologie von Johanniskrautextrakt ist sehr gut untersucht.
- Nur für den Hauptwirkstoff Hyperforin konnte eine Wirkung (synaptosomale Aufnahmehemmung und Verbesserung der Neuroplastizität als gemeinsame Endstrecke im Wirkmechanismus aller Antidepressiva) zweifelsfrei belegt werden.
- Akzeptable Evidenzen für eine antidepressive Wirksamkeit und eine Beteiligung an der Wirkung des Gesamtextraktes gibt es auch für einige der Flavonoide, während eine wesentliche Relevanz von Hypericin eher fraglich erscheint.
- Von den vielen apothekenpflichtigen Johanniskrautextraktpräparaten auf dem deutschen Markt liegen nur für die Präparate Jarsin®, Leif® und Neuroplant® und die diesen Präparaten zugrunde liegenden Extrakte ausreichende pharmakologische und klinische Daten vor, um von einer gesicherten therapeutischen Wirkung ausgehen zu können.
- Für alle drei für die Behandlung der unipolaren Depression zugelassenen rezeptpflichtigen Präparate gibt es ein identisches OTC-Präparat, das nur für subsyndromale depressive Störungen zugelassen ist.
Arzneimittelwechselwirkungen
Nach anfänglicher Euphorie musste man bei der Anwendung von Johanniskrautextraktpräparaten mit den Jahren realisieren, dass ihre Einnahme, wie bei jedem wirksamen Arzneimittel, auch mit Problemen verbunden sein kann. Während die früher durch Hypericin ausgelöste mögliche Photosensibilisierung heute als ein eher seltenes Problem nur bei sehr starker Sonnenexposition gesehen wird, sind eine Reihe von möglichen Arzneimittelinteraktionen zu beachten, die ausführlich in den Patienten- bzw. Fachinformationen aufgeführt sind. Hier sind besonders die Induktion verschiedener CYP-Enzyme und des P-Glykoproteins (P-GP) zu erwähnen, wodurch die Plasmaspiegel verschiedener, zum Teil auch stark wirksamer Arzneimittel verändert werden können, sodass schwerwiegende Interaktionen beschrieben sind (besonders für verschiedene Immunsuppressiva). Hyperforin spielt bei diesen Induktionseffekten eine größere Rolle als die beiden anderen Wirkstoffklassen. So konnte z. B. für den Hyperforin-armen Extrakt Ze 117 keine relevante Beeinflussung der CYP-Enzyme im sogenannten Cocktail-Test an gesunden Probanden gefunden werden [45]. Wenn auch die Relevanz einiger der beschriebenen Interaktionen möglicherweise eher gering ist (z. B. das Risiko eines Serotoninsyndroms bei der Kombination mit SSRI oder die Wirkungsabschwächung oraler Antikontrazeptiva) [39], sind Arzt und Apotheker bzw. Patient gut beraten, die in den Informationen [39, 41] beschriebenen Gegenanzeigen und Warnhinweise strikt zu befolgen. |
Literatur
[1] Jenett-Siems K. Ausgezeichnete Heilpflanze, was in Hypericum perforatum steckt. Dtsch Apoth Ztg 2019;159:2792-2798
[2] Müller WE. St. Johnʼs Wort and its Active Principles in Depression and Anxiety. Müller WE Hrg., Birkhäuser Verlag 2005, Basel, pp. 1-43
[3] Müller WE. Normalisierung gestörter Neuroplastizitätsmechanismen als gemeinsame Endstrecke im Wirkungsmechanismus von Antidepressiva. Psychopharmakotherapie 2016;23:230-238
[4] Unipolare Depression. S3-Leitlinie, Nationale Versorgungsleitlinie, 2. Aufl., 2015
[5] Wurglices M, Westerhoff K, Holoubek G, Schuber-Zsilavecz M, Müller WE. Aktuelle Johanniskrautforschung. Dtsch Apoth Ztg 2002;142:1153-1175
[6] Müller WE. Current St. John’s Wort research from mode of action to clinical efficacy. Pharmacol Res 2003;47:101-109
[7] Gambarana C, Giachetti D. Efficacy in behavioural models of antidepressant activity. In Milestones in Drug Therapy „St John’s Wort and its active principles in depression and anxiety. Müller WE Hrg. Birkhäuser Verlag 2005, Basel, pp. 59-72
[8] Treiber K, Müller WE. Effects on transmitter uptake and their cellular and molecular basis. In Milestones in Drug Therapy „St John’s Wort and its active principles in depression and anxiety. Müller WE Hrg. Birkhäuser Verlag 2005, Basel pp. 59-72
[9] Chatterjee SS, Bhattacharya SK, Wonnemann, M, Singer A, Müller, WE. Hyperforin as a possible antidepressant component of Hypericum extracts. Life Sci 1998;63:499-510
[10] Kehr J, Ögren SO, Yoshitake T. Modulation of transmitter release and metabolism. In Milestones in Drug Therapy „St John’s Wort and its active principles in depression and anxiety. Müller WE Hrg., Birkhäuser Verlag 2005, Basel pp. 47-58
[11] Heiser J. Effekte von antidepressiv wirksamen Pflanzenextrakten auf das neuronale Wachstum und intrazelluläre Signalwege. Dissertation Goethe Universität Frankfurt, FB Biochemie, Chemie, Pharmazie 2012
[12] Trofimiuk E, Holownia A, Braszko JJ. Activation of CREB by St. Johm’s wort may diminish deletoriuos effects of aging on spatial memory. Arch Pharm Res 2010;33:469-477
[13] Trofimiuk E, Holownia A, Braszko JJ. St. John’s wort may relieve negative effects of stress on spatial working memory by changing synaptic plasticity. Nauny-Schmied Arch Pharmacol 2011;383:415-423
[14] Concerto C, Boo H, Hu C, Sandilya P, Krish A, Chusid E, Coira D, Aguglia E, Battaglia F. Hypericum perforatum extract modulates cortical plasticity in humans. Psychopharmacol 2018;235:145-153
[15] Harmer CJ, Duman RS, Cowen PJ. How do antidepressants work? New perspectives for refining future treatment approaches. Lancet Psychiatry 2017; May 4, 409-418
[16] Levy MJF, Boulle F, Steinbusch HW, van den Hove DLA, Kenis G, Lanfumey L. Neurotrophic factors and neuroplasticity pathways in the pathophysiology and treatment of depression. Psychopharmacology 2018;235:2195-2220
[17] Apaydin EA, Maher AR, Shanman R, Booth MS, Miles JNV, Sobero ME, Hempel S. A systematic review of St John’s wort for major depressive disorder. Systematic reviews 2016;5:148
[18] Laakmann G, Schüle C, Baghai T, Kieser M. St. John’s Wort in mild depression: The relevance of hyperforin fort he clinical efficacy. Pharmacopsychiatry 1998;31:suppl. 54-59
[19] Wonnemann M, Singer A, Sieber B, Müller WE. Evaluation of synaptosomal uptake inhibition of St John’s wort. Pharmacopsychiatry 2001;34:suppl. 1, 148-151
[20] Singer A, Wonnemann M, Muller W. Hyperforin, a major antidepressanr constituent of St. John’s wort inhibits serotonin uptake by elevating free intracellular Na+. J Pharmacol Exp Ther 1999;290:1363-1368
[21] Leuner K, Kazanski V, Muller M, Essin K, Henke B, Gollasch M, Harteneck C, Müller WE. Hyperforin a key constituent of St. John’s wort specifically activates TRC6 channels. FASEB J 2007; Dec;21(14):4101-4111
[22] Heiser JH, Schuwald AM, Sllani G, Ye L, Müller WE, Leuner K. TRPC6 channel-mediated neurite outgrowth in PC12 cells and hippocampal neurons involves activation of RAS/MEK/ERK, Pl3K, and CAMKlV pathways. J Neurochem 2013;127:303-313
[23] Gibon J, Deloulme JC, Chevallier T, Ladevezer E, Abrous DN, Bouron A. The antidepressant hyperforin increases the phosphorylation of CREB and the expression of TrkB in a tissue-specific manner. Int J Neuropsychopharmacol 2013;16:189-198
[24] Szewczyk B, Pochwat B, Muszynska B, Opoka W, Krakowska A, Rafalo-Ulnska A, Friedland K, Nowak G. Antidepressant-like activity of hyperforin and changes in BDNF and zinc levels in mice exposed to chronic unpredictable stress. Behav Brain Res 2019 in press
[25] Müller M, Essin K, Hill K, Berschmann H, Rubant S, Schemo CM, Gollasch M, Boencke WH, Harteneck C, Müller WE, Friedland K. Specific TRPC 6 channel activation, a novel approach to stimulate keratinocyte differentiation. J Biol Chem 2008;283:33942-33954
[26] Takada H, Yonekawa J, Matsumoto M, Furuya K, Sokabe M. Hyperforin/HP-cyclodestrin emhances mechanosensitive Ca2+ signalling in HaCaT keratinocytes and in atopic skin ex vivo which accelerates wound healing. Biomed Res Int 2017; 2017:8701801
[27] Wölfle U, Seelinger G, Schempp CM. Topical application of St. John’s Wort (Hypericum perforatum). Planta Med 2014;80:109-120
[28] Fox E, Murphy RF, McCully CL, Adamson PC. Plasma pharmacokinetics and cerebrospinal fluid penetration of hypericin in nonhuman primates. Cancer Chemother Pharmacol 2001;47:41-44
[29] Nöldner M. Comparative preclinical antidepressant activity of isolated constituents. In Milestones in Drug Therapy „St John’s Wort and ist active principles in depression and anxiety. Müller WE Hrg (2005) Birkhäuser Verlag, Basel, pp. 73-84
[30] Butterweck V, Petereit F, Winterhoff H, Nahrstedt A. Solubilized hypericin and pseudohypericine from Hypericum perforatum exert antidepressant activity in the forced swimming test. Planta Med 1998;64:291-294
[31] Pathak L, Agrawal Y, Dhir A. Natural polyphenols in the management of major depression. Expert Opin Investig Drug 2013;22:863-880
[32] Xu y, Li S, Chen R, Li G, Barish PA, You W, Chen L, Liu M, Ku B, Pan J, Ogle WO. Antidepressant-like effect of low molecular proanthocyanidin in mice: Involvement oft the monoaminergic system. Pharmacol Biochem Behav 2010;94:447-453
[33] Wang J, Ferruzzi MG, Ho L et al. Brain-targeted proanthocyanidin metabolites for Alzheimer’s disease treatment. J. Neurosci 2012;32:5144-515
[34] Butterweck, V, Winterhoff H, Herkenham M. St John’s Wort, hypericin, and imipramine: a comparative analysis of mRNA levels in brain areas involved in HPA axis control following short-term and long-term administration in normal and stressed rats. Mol Psychiat 2001;6:547-564
[35] Park S-H, Sim Y-B, Han P-L, Lee J-K, Suh H-W. Antidepressant-like effects of kaempferol and quercitirin, isolated from Opuntia ficus-indica var. Saboten. Exp Neurobiol 2010;19:30-38
[36] Grundmann O, Lv Y, Kelber O, Butterweck V. Mechanism of St. John’s wort extract (STW-Vl) during chronic restraint stress is mediated by the interrelationship of the immune, oxidativedefense, and neuroendocrine system. Neuropharmacol 2010;58:767-773
[37] Liu T, Zhong S, Liao X, Chen J, He T, Lai S, Jia Y. A meta-analysis of oxidative stress markers in Depression. PLOS one 2015;10(10):e0138904
[38] Abdel-Tawab M, Hüsch J, Schubert-Zsilavecz M, Dingermann T. Freiverkäufliche Johanniskrautpräparate unter der Lupe: Dtsch Apoth Ztg 2011; Nr. 17, 61-69
[39] Berry-Bibee EN, Kim MJ, Tepper NK, Riley HE Curtis KM. Co-administration of St. John’s wort and hormonal contraceptives: a systemic review. Contraception 2016;94:668-677
[40] Leuner K, Li W, Amaral MD, Rudolph S, Clfa G, Schuwald AM, Harteneck C, Inoue T, Pozzo-miller L. Hyperforin modulates dentritic spine morphology in hippocampal pyramidal neurons by activating Ca2+-permeable TRCP6 Channels 2013;23:40-52
[41] Bonaterra GA, Schwendler A, Hüther J, Schwarzbach H, Kolb C, Abdel-Aziz H, Kinscherf R. Preclinical data supporting/refuting the use of Hypericum perforatum in the treatment of depression. Front Pharmacol 2018 Jan 18;8:955
[42] Crupi R, Mazzon E, Mario A, La Spade G, Bramanti P, Cuzzocrea S, Spina E. Hypericum perforatum treatment effect on behaaviour and neurogenesis in a chronic stress model in mice. BMC Complement Altern Med 2011 Jan 27;11:7
[43] Fehske C. Antidepressive Eigenschaften flavonoidhaltiger Pflanzenextrake. Dissertation Fachbereich Biochemie, Chemie und Pharmazie, Goethe-Universität Frankfurt, 2011
[44] Kressel G, Willers J, Kohrs H, Zimmermann A, Klement S, Dienel A, Hahn A. Effects of Opuntiaficus-indica flower extract WS 1261 on mental and psychic function in subsyndromal fatigue – a pilot study. Int J Phytomed 2016;8:558-566
[45] Zahner C, Kruttschnitt E, Uricher J, Lissy M, Hirsch M, Nicolussi S, Krähenbühl S. No clinically relevant interactions of St. John’s Wort extract Ze 117 low in hyperforin with cytochrome P450 enzymes and P-glycoprotein. Clin Pharmacol Ther 2019;106:422-440
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.