
- DAZ.online
- DAZ / AZ
- DAZ 11/2020
- Mit löslichem ACE2 gegen...
COVID-19
Mit löslichem ACE2 gegen COVID-19
Neues Wirkprinzip soll Viren abfangen und Schutzmechanismen stärken
Prof. Dr. Josef Penninger konnte mit seinen Kollegen zeigen, dass ein lösliches rekombinantes humanes ACE2 zumindest im Tierversuch schwere durch SARS-Viren hervorgerufene Lungenschäden verhindern kann. Professor Penninger ist Leiter des Life Sciences Institute der University of British Columbia in Vancouver, Kanada, und Gründer der Firma Apeiron Biologics mit Sitz in Wien. Apeiron startet in Kürze in China eine Pilotstudie mit dem löslichen rekombinanten ACE2 bei schwer an COVID-19 erkrankten Patienten.
DAZ: Herr Professor Penninger, erklären Sie uns doch einmal kurz die Bedeutung von ACE2 für die Pathogenese einer Coronavirus-Infektion.
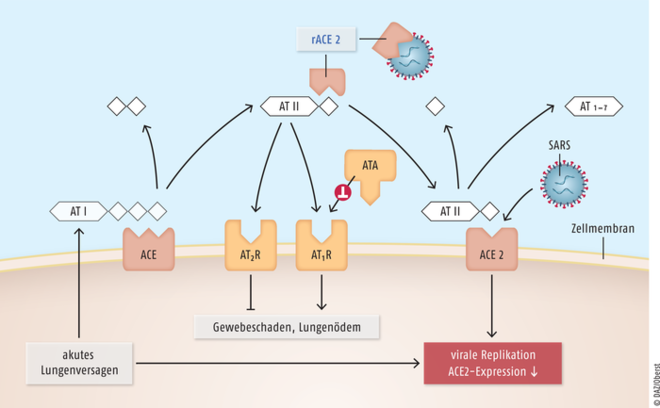
Penninger: ACE2 ist ein Enzym, das in vielen Zellen exprimiert wird, so beispielsweise in Herzmuskelzellen, Gefäßzellen des Herzens, in den Nieren, im Darm und in der Lunge. Unsere Forschungen rund um das für den SARS-Ausbruch 2002/2003 verantwortliche Coronavirus SARS-CoV haben gezeigt, dass diese Viren durch Bindung an ACE2 in die Zellen der Lunge gelangen und dort den Prozess des akuten Lungenversagens in Gang setzen (s. Abb).
Abb.: Wie SARS-Viren über das ACE-System die Lunge schädigen sollen. Angiotensin I wird durch das Angiotensin Converting Enzyme (ACE) in Angiotensin II gespalten. Angiotensin II seinerseits kann sowohl an die Angiotensin-II-Rezeptoren AT2R als auch an AT1R binden. Die Bindung an AT1-Rezeptoren fördert Gewebeschäden und ein Lungenödem, die Bindung an AT2-Rezeptoren soll dem entgegenwirken. Das Angiotensin Converting Enzyme 2 (ACE2) spaltet Angiotensin II in Angiotensin1-7, das nicht mehr an AT1R bindet. SARS-Viren nutzen den ACE2-Rezeptor zum Eintritt in die Zelle und starten dann die Virusreplikation. Parallel dazu nimmt die ACE2-Expression in den Zellen ab und damit auch die Möglichkeit, Angiotensin II durch Umwandlung in Angiotensin1-7 zu entschärfen. AT1R-Antagonisten wie Sartane (ATA) können nach dieser Hypothese die schädliche Angiotensin-II-Wirkung antagonisieren. Rekombinantes lösliches ACE (rACE) mit erhaltener Enzymfunktion soll nicht nur die Viren abfangen, es soll auch die Bildung des protektiven Angiotensin1-7 fördern [nach Nicholls J, Peiris M, Nature Medicine 2005;11(8):821; Penninger JM et al. Nature Medicine 2005;11(8):875].
DAZ: ACE2 weist Homologien mit ACE auf, wird aber nicht durch die klassischen ACE-Hemmer blockiert. Was ist seine physiologische Funktion?
Penninger: ACE2 hat eine wichtige Schutzfunktion innerhalb des Renin-Angiotensin-Systems. ACE wandelt bekanntermaßen Angiotensin I in Angiotensin II um, das seinerseits über Bindung an die Angiotensin-II-Rezeptoren AT2R und AT1R zu Lungenschäden bis hin zum Lungenödem führen kann. ACE2 hat hier eine Schutzfunktion, es spaltet Angiotensin II in Angiotensin1-7. Das bindet nicht mehr an die Angiotensin-II-Rezeptoren. So wird die Angiotensin-II-Konzentration reduziert und damit auch die schädlichen Angiotensin-II-Wirkungen.
DAZ: Nun sollen sowohl SARS-CoV als auch SARS-CoV-2 ACE2 nutzen, um in ihre Wirtszelle zu gelangen und sich dort zu vermehren.
Penninger: Das ist richtig. Diese beiden Coronaviren können beide an ACE2 binden, gelangen in die Zellen und starten ihre Replikation. Das geht fatalerweise mit einer Abnahme der ACE-2-Expression einher. ACE2 verschwindet quasi von der Zelloberfläche und kann dann das schädliche Angiotensin II nicht mehr spalten. Die Folge in der Lunge: schwere akute Lungenschäden bis hin zum Tod. Darüber hinaus wird ACE2 in bedeutendem Umfang in den Nieren, im Herz und im Darm exprimiert. Das könnte ein multiples Organversagen bei einigen COVID-19-Patienten erklären.
DAZ: Dieser Pathomechanismus bietet interessante Ansätze, um ihn zu unterbrechen.
Penninger: Ja, zum einen mit Angiotensin-II-Rezeptorantagonisten, oder, das ist der Weg, den wir beschritten haben, mit einem rekombinanten löslichen ACE2, dessen Enzymfunktion erhalten ist. Dabei kann das lösliche ACE2 auf zweifache Weise wirken:
- zum einen kann es wie ein Schwamm die Viren aufsaugen, also binden und
- zum anderen kann es durch die Spaltung von Angiotensin-II in das unschädliche Angiotensin1-7 vor Lungenschäden schützen.
Unser rekombinantes humanes ACE2 hat sich schon in Phase-I-Studien als sicher erwiesen, sodass wir nun eine Phase-II-Studie anstreben. Es hat interessanterweise keinen Einfluss auf den Blutdruck, denn theoretisch könnte ja durch Unterbinden der Angiotensin-II-Wirkung der Blutdruck sinken.
DAZ: Nun hat Ihr Unternehmen Apeiron Biologics mitgeteilt, dass mit Ihrem auch als APN01 bezeichneten rhACE2 eine Pilotstudie in China mit 24 schwer erkrankten COVID-19-Patienten startet. Wie ist der Stand?
Penninger: Die Vorbereitungen sind getroffen, der erste Patient wird in Kürze behandelt. Bei dem ganzen Vorgehen ist uns wichtig, dass wir aufbauend auf die Pilotstudie eine saubere, randomisierte Doppelblindstudie durchführen, die dann als sichere Basis für eine Zulassung dienen kann.
DAZ: Das bedeutet, dass wir auch hier noch warten müssen, ob sich dieser Ansatz bewährt. Wann rechnen Sie frühestens mit einer Zulassung?
Penninger: Das ist schwierig vorauszusagen. Insgesamt müssen jetzt verschiedene Ansätze schnell getestet werden. Um das neue Coronavirus erfolgreich bekämpfen zu können, werden wir Impfstoffe ebenso dringend benötigen wie unterschiedliche Virustatika. APN01 kann nur ein Teil des therapeutischen Spektrums sein.
DAZ: Eine für Pharmazeuten spannende Frage ist die, wie sich vor dem Hintergrund des ACE2-vermittelten Eintritts der Coronaviren in die Zellen Arzneistoffe verhalten, die in das Renin-Angiotensin-System eingreifen. Sind beispielsweise Angiotensin-II-Rezeptor-Antagonisten geeignet, dem durch verringerte ACE2-Expression entstandenen Übergewicht von Angiotensin II entgegenzuwirken und die Zelle zu schützen? Wie verhält sich eine ACE-Hemmer-Therapie? Hier kursiert auch die Hypothese, dass ACE-Hemmer zu einer Hochregulierung von ACE2 führen und so das Einschleusen der Viren in die Zellen und damit einen fatalen Verlauf begünstigen.
Penninger: ACE2 schützt vor Lungenversagen. Als Enzym inaktiviert ACE2 Angiotensin II und generiert Angiotensin1-7. In der Tat konnte die Inhibition von AT1R durch Sartane in unseren Experimenten vor Lungenversagen schützen, während die Blockade von AT2R die Erkrankung verschlechterte. Da ACE2 aber die Produktion von Angiotensin1-7 fördert, funktioniert ACE2 auch besser, besonders, da in unseren klinischen Studien ACE2 keine Effekte auf den Blutdruck hatte, aber Sartane sehr wohl. ACE-Blocker würden generell die Angiotensin-II-Produktion blockieren, aber damit auch die Produktion des „guten“ Angiotensin1-7.
DAZ: Herr Professor Penninger, wir danken Ihnen für das Gespräch. |
Camostat: Noch ein neuer Ansatz gegen SARS-CoV-2
Derzeit werden mit Hochdruck wirksame Therapien gegen das neuartige Coronavirus SARS-CoV-2 gesucht. Nun hat sich ein bereits in Japan zugelassenes Arzneimittel im In-vitro-Versuch als vielversprechend erwiesen. Camostat Mesilate wird in Japan zur Behandlung der chronischen Pankreatitis eingesetzt. Wie sich nun herausgestellt hat, hemmt der Wirkstoff auch die Serinprotease TMPRSS2 und damit einen entscheidenden Schritt in der Vermehrung des SARS-CoV-2. Um in die Wirtszelle eindringen zu können, muss das Virus mit dem Transmembranprotein ACE2 (Angiotensin-konvertierendes Enzym-2) interagieren. Das ist allerdings nur möglich, wenn zuvor das Anheftungsprotein Spike (S) auf der Virusoberfläche aktiviert wurde. Hierfür ist TMPRSS2 essenziell. Wird die zelluläre Protease gehemmt, können die Viren nicht mehr an die Wirtszellen binden. Dass Camostat Mesilate so eine Infektion mit SARS-CoV-2 verhindern kann, hat ein Team von Forschern des Deutschen Primatenzentrums, der Charité Berlin, der Stiftung Tierärztliche Hochschule Hannover, der BG-Unfallklinik Murnau, der LMU München, des Robert Koch-Instituts sowie des Deutschen Zentrums für Infektionsforschung nun nachgewiesen. Dazu haben sie SARS-CoV-2-Isolate von einem Patienten im Zellkulturexperiment untersucht. Eine Behandlung mit Camostat Mesilate verhinderte das Eindringen der Viren in Calu-3-Zellen, einer humanen Lungenkrebszelllinie. Da der Wirkstoff in Japan bereits auf dem Markt ist, wäre eine Off-Label-Anwendung theoretisch denkbar. Ob der Serinproteasehemmer nicht nur Zellen sondern auch Menschen vor einer Infektion mit SARS-CoV-2 schützt, muss nun im Rahmen von klinischen Studien geklärt werden.
Quelle: Hoffmann M et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a 2 clinically-proven protease inhibitor. Cell 2020; doi: 10.1016/j.cell.2020.02.052
cst






















4 Kommentare
Verwechslung von ACE mit ACE2
von vicente cerrato horst am 24.03.2020 um 9:06 Uhr
» Auf diesen Kommentar antworten | 0 Antworten
Was denn jetzt?
von Batropin am 14.03.2020 um 16:25 Uhr
» Auf diesen Kommentar antworten | 2 Antworten
AW: Was denn jetzt
von Fabian Spieker am 15.03.2020 um 8:12 Uhr
AW: Was denn jetzt
von jo am 16.03.2020 um 20:46 Uhr
Das Kommentieren ist aktuell nicht möglich.