
- DAZ.online
- DAZ / AZ
- DAZ 42/2019
- Von Prostatahyperplasie ...
Arzneimittel und Therapie
Von Prostatahyperplasie zu Parkinson
Terazosin und Co. könnten das Fortschreiten der neurodegenerativen Erkrankung verhindern
Schätzungen zufolge sind weltweit sechs Millionen Menschen an Parkinson erkrankt. Aufgrund der demografischen Entwicklung wird insbesondere in den industrialisierten Ländern mit einer Verdopplung der Erkrankungen bis zum Jahr 2030 gerechnet [1]. Pathophysiologisch liegt dem Morbus Parkinson der Untergang dopaminerger Neurone in der Substantia nigra pars compacta zugrunde, deren axonale Projektionen zum Corpus striatum ziehen. Die mit dem Dopamin-Mangel einhergehenden Symptome sind motorischer Natur (Rigor, Tremor, Akinese, posturale Instabilität), umfassen aber auch demenzielle und neuropsychiatrische Beeinträchtigungen. Bisherige Therapieansätze zielen darauf ab, die neuronale Transmission zu verbessern und so die Symptome zu mildern. Präventive Therapien zur Verminderung der Neurodegeneration existieren hingegen noch nicht, was sich auch in der Komplexität und der ungeklärten Pathogenese der Erkrankung begründet.
Energiestoffwechsel als Target
Es gibt jedoch Hinweise auf eine Beeinträchtigung des Energiestoffwechsels in den betroffenen Arealen der Basalganglien. Die zerebrale Glykolyse und die mitochondriale Funktion sind bei Patienten mit Parkinson verringert. Hier setzen Wissenschaftler nun mit einem bewährten Wirkstoff an, der zur Behandlung von benigner Prostatahyperplasie (BPH) zugelassen ist [2].
Aktivierung von PGK1
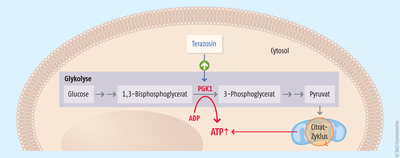
In Zellkulturmodellen wurde nachgewiesen, dass das Chinazolin-Derivat Terazosin – unabhängig von seiner antagonistischen Wirkung am α1–Adrenozeptor – das Enzym Phosphoglycerat-Kinase 1 (PGK1) aktiviert. PGK1 ist das erste ATP-erzeugende Enzym der Glykolyse (s. Abbildung).
In Mäusen stellten die Forscher nach Verabreichung von Terazosin erhöhte Pyruvat-Konzentrationen in der Substantia nigra, dem Striatum und der Großhirnrinde fest. Pyruvat treibt die oxidative Phosphorylierung an, was im Mausmodell in einer erhöhten Citrat-Synthase-Aktivität und höherer ATP-Produktion resultierte. Terazosin vermochte darüber hinaus, den Effekten von MPTP (1-Methyl-4-phenyl-1,2,3,6-tetrahydropyridin), einem bekannten Induktor der ParkinsonPathologie, entgegenzuwirken: Sowohl der Abfall der Pyruvat- und ATP-Spiegel als auch der Verlust von Mitochondrien sowie neurodegenerative Veränderungen nach MPTP-Applikation wurden durch Terazosin vermindert. Darüber hinaus wurden induzierte Defizite in der motorischen Funktion durch die Terazosin-Behandlung antagonisiert. Vergleichbare Ergebnisse wurden bei Ratten nach Gabe von 6-Hydroxydopamin, bei Fruchtfliegen nach Applikation von Rotenon sowie in genetischen Tiermodellen der Parkinson-Krankheit erzielt. Auch hier wurden neurodegenerative Prozesse durch Terazosin vermindert. Ähnliche Effekte wurden für die α1–Adrenozeptor-Antagonisten Doxazosin und Alfuzosin gefunden. Das ebenfalls bei BPH eingesetzte Tamsulosin, bei dem die für die Bindung an PGK1 notwendige Chinazolin-Struktur fehlt, zeigte in den Testmodellen hingegen keine Wirksamkeit.
Istradefyllin: Aus dem „off“
Bereits vor mehr als zehn Jahren hatte Kyowa Kirin vergeblich versucht, seinen selektiven A2A-Adenosin-Rezeptor-Antagonisten zur Behandlung des Morbus Parkinson in den USA auf den Markt zu bringen. Nachdem weitere Daten vorgelegt wurden, hat es im zweiten Anlauf geklappt: Ende August 2019 wurde Istradefyllin (Nourianz™) von der Food and Drug Administration (FDA) zugelassen. Eingesetzt werden die Tabletten zusätzlich zu einer Levodopa/Carbidopa-Therapie bei Patienten, die unter „Off“-Phasen leiden – also Zeiten, in denen die Parkinson-Symptome durch die bestehende Medikation nicht ausreichend kontrolliert werden. Durch die Antagonisierung der A2A-Adenosin-Rezeptoren wird der Dopamin-D2-Rezeptor-Signalweg aktiviert und die dopaminerge Neurotransmission erhöht.
Die Zulassung basiert auf vier randomisierten kontrollierten Studien, in denen Istradefyllin über einen Zeitraum von zwölf Wochen bei insgesamt 1143 Probanden im Vergleich zu Placebo untersucht wurde. Durch die zusätzliche Istradefyllin-Gabe zu einer bestehenden Levodopa/Carbidopa-Therapie verringerten sich die „Off“-Zeiten der Patienten. Als mögliche Nebenwirkungen können unter anderem Dyskinesien und Halluzinationen auftreten. Die FDA mahnt daher, auf etwaige Symptome zu achten und die Dosis gegebenenfalls anzupassen oder die Therapie zu beenden. In Japan ist das Präparat unter dem Namen Nouriast® bereits seit 2013 auf dem Markt. In Europa ist Istradefyllin bislang noch nicht zugelassen.
[Quelle: Pressemitteilung der FDA vom 27. August 2019]
Positive Effekte möglicherweise auch beim Menschen
Die präklinischen Daten wecken Hoffnung. Aber sind die Ergebnisse auf den Menschen übertragbar? Diesen Punkt adressierten die Autoren, indem sie mehrere Datenbanken wie die Truven-Datenbank hinsichtlich Korrelationen von Parkinson-Erkrankungen und der Einnahme von Terazosin, Doxazosin oder Alfuzosin untersuchten. Verglichen wurde mit Tamsulosin. In der Tat wurden unter den Chinazolin-Derivaten weniger Neudiagnosen festgestellt: Während unter Terazosin, Doxazosin oder Alfuzosin 118 Parkinson-Fälle bei initial 78.444 berücksichtigten Patienten auftraten, waren es unter Tamsulosin 190 Fälle bei vergleichbarer Gruppengröße (Hazard Ratio 0,62; 95%-Konfidenzintervall 0,49 bis 0,78; p < 0,0001). Anhand der Daten der Parkinson’s Progression Markers Initiative (PPMI) wurden bei Patienten mit bereits bestehendem Morbus Parkinson zudem Verbesserungen von motorischen und nicht motorischen Symptomen unter den PGK1-Aktivatoren beobachtet.
Von Kristallstrukturanalysen über Zellkultur- und Tiermodelle bis hin zu retrospektiven Analysen von Patientendatenbanken liegen nunmehr also vielversprechende Ergebnisse vor. Ob ein „Drug Repurposing“ der Alphablocker tatsächlich erfolgreich sein könnte, werden jedoch umfangreiche prospektive kontrollierte Studienprogramme zeigen müssen. |
Literatur
[1] Deutsche Gesellschaft für Neurologie (DGN). S3-Leitlinie „Idiopathisches Parkinson-Syndrom“. Aktualisierung 2016; AWMF-Register-Nummer: 030-010
[2] Cai R et al. Enhancing glycolysis attenuates Parkinson‘s disease progression in models and clinical databases. J Clin Invest 2019;129(10):4539-4549




















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.