
- DAZ.online
- DAZ / AZ
- DAZ 35/2019
- Metamizol
Beratung
Metamizol
Praxiswissen zu Wirkungen, Nebenwirkungen und Interaktionen
Im Jahre 1922 wurde Metamizol-Natrium/Metamizol (Novalgin®) als Arzneimittel zugelassen und ergänzte damit als besser wasserlösliche Verbindung die Wirkstoffgruppe der Pyrazolone, von denen bereits Phenazon und Aminophenazon als Analgetika und Antipyretika auf dem Markt existierten. Während Phenazon sowie das später noch zugelassene Propyphenazon heute kaum noch Anwendung finden (Otalgan® Ohrentropfen und vereinzelt in Schmerztabletten wie Migräne-Kranit®, Eu-Med®, Demex Zahnschmerztabletten®), hat Metamizol auch heute noch aufgrund seiner überzeugenden analgetischen, antipyretischen und spasmolytischen Wirkung eine hohe therapeutische Bedeutung. Die antiphlogistische Wirkung ist vernachlässigbar gering. Hinsichtlich seiner seit Jahrzehnten bekannten und gefürchteten Nebenwirkung, der Agranulozytose, wird die Anwendung von Metamizol kontrovers beurteilt. Dies ergibt beispielsweise auf europäischer Ebene ein sehr heterogenes Bild. Während in einzelnen Ländern Metamizol rezeptfrei verfügbar ist, haben andere Länder die Zulassung widerrufen. Seit 1987 steht Metamizol in Deutschland als Monopräparat unter Verschreibungspflicht. Kombinationspräparate wurden vom Markt entfernt und sind heute nur noch als Tierarzneimittel verkehrsfähig. Mit dem damit verbundenen engen Indikationsspektrum sollte einer überschießenden Anwendung dieses Arzneistoffes entgegnet werden.
Die Indikationen und der Off-label-Gebrauch
Das Indikationsspektrum umfasst ausschließlich die Behandlung von:
- akuten starken Schmerzen nach Verletzungen oder Operationen,
- Koliken,
- Tumorschmerzen,
- sonstigen akuten oder chronisch starken Schmerzen, wenn andere therapeutische Maßnahmen nicht indiziert sind und
- hohes Fieber, das auf andere Maßnahmen nicht anspricht.
Trotz dieser Einschränkungen hat die therapeutische Anwendung von Metamizol im letzten Jahrzehnt in Deutschland massiv zugenommen. So haben sich die verordneten definierten Tagesdosen (DDD) von 101 Mio. im Jahr 2008 auf 204 Mio. im Jahr 2016 verdoppelt und zum Jahr 2017 nochmals um 5,3% auf 215 Mio. DDD erhöht [1]. Außerdem steht Metamizol mit 24,3 Mio. Verordnungen auf Platz 2 der verordnungsstärksten Wirkstoffe nach Ibuprofen (26,4 Mio.), wobei seine Nettokosten von 303 Mio. Euro die von Ibuprofen um ca. 28 Mio. Euro übertreffen. Obwohl beide Wirkstoffe im letzten Jahrzehnt deutliche Steigerungen der Verordnung aufwiesen, stagnieren die des Ibuprofens aktuell gegenüber Metamizol. Diese Fakten sprechen für die herausragende Wirksamkeit des Arzneistoffes, offensichtlich aber auch für Anwendungen außerhalb des Indikationsfensters („off label“).
Die Eigenschaften
Metamizol kann oral, in Form von Tabletten oder Tropfen, oder rektal appliziert werden [2 – 5]. Durch seine gute Wasserlöslichkeit ist prinzipiell auch eine parenterale Anwendung einer 50%igen Lösung des Arzneistoffes i. m. oder i. v. möglich, wenn die erstgenannten Anwendungswege therapie- oder patientenbedingt ausscheiden. Dabei ist aber explizit auf eine langsame Injektion unter Atem-, Puls- und Blutdruckkontrolle zu achten.
Die Metabolisierung
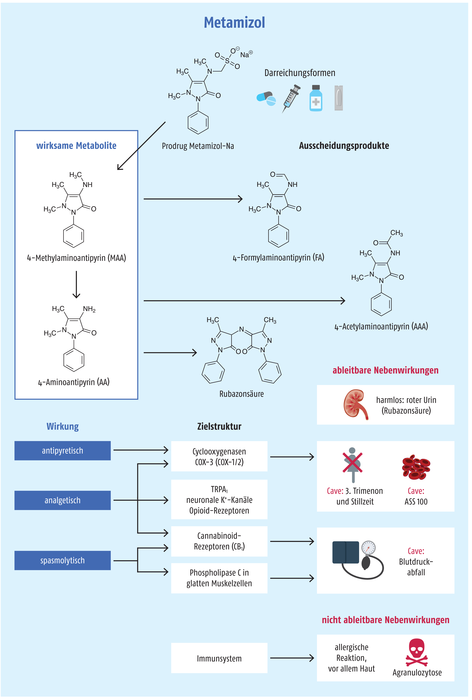
Das durch die Sulfonat-Struktur gut lösliche Prodrug Metamizol-Natrium wird im Körper zu seinem analgetisch wirksamen Hauptmetabolit 4-Methylaminoantipyrin (MAA) gespalten. Bei peroraler Einnahme geschieht dies bereits nicht-enzymatisch durch Hydrolyse in der Magensäure, sodass das Prodrug im Plasma nicht mehr nachweisbar ist. Eine von mehreren CYP-Enzymen induzierte Demethylierung in der Leber führt zu 4-Aminoantipyrin (AA) als zweiten wirksamen Metaboliten. Die Oxidation von MAA zu 4-Formylaminoantipyrin (FAA) und die Acetylierung via N-Acetyltransferase-2 von AA zu 4-Acetylaminoantipyrin (AAA) führen zu Inaktivierung und anschließender Eliminierung [6].
| Tablette (p. o.) | Tropfen (p. o.) | Zäpfchen | Injektionslösung (i. v./i. m.) | |
| Einzeldosis | 500 mg | 500 mg/ml = 1 Tropfen 25 mg | 1000 mg | 500 mg/ml |
Anwendung bei Kindern | nein | ja | 300 mg Kinderzäpfchen | 3 – 11 Monate (5 – 8 kg) nur i.m. |
| Packungsgrößen | N1 = 10 Tabletten | N1 = 20 ml | N1 = 10 Stück Kinder 5 Stück | N1 = 5 Ampullen |
| N2 = 30 Tabletten | N2 = 50 ml | N2 = 10 Ampullen | ||
| N3 = 50 Tabletten | N3 = 100 ml | à 2 ml /10 ml | ||
| DosierungErwachsene | 1 – 2 Tabletten 500 mg – 1000 mg | 20 – 40 Tropfen 500 mg – 1000 mg | 1 Zäpfchen 1000 mg | Einzeldosis 1 – 2 ml 500 mg – 1000 mg |
| Tageshöchstdosis für Erwachsene | 8 Tabletten = 4000 mg | 160 Tropfen = 4000 mg* | 4 Zäpfchen = 4000 mg | 10 ml = 5000 mg |
| Bioverfügbarkeit von MAA | 93% | 81% | Erwachsene: 54% Kinder: 61% | 87% (i. m.) |
| tmax | 1,42 ± 0,54 h | 1,15 ± 0,45 h | 2,40 ± 1,18 h | 1,67 ± 0,69 h (i. m.) |
| Eliminierung | 90% renal | |||
| Plasmakonzentration | therapeutisch: 10 µg/ml, toxisch 20 µg/ml (Gesamtzahl aller Metabolite) | |||
Der Wirkungsmechanismus
Der Wirkungsmechanismus von Metamizol ist noch nicht abschließend geklärt. Die Adressierung der Cyclooxygenase (COX) sowohl in einer im ZNS lokalisierten Form (COX-3) als auch in der Peripherie (COX-1 und COX-2) durch die aktiven Metabolite MAA und AA und damit eine verminderte Prostaglandinsynthese werden als gesichert angesehen. Auch die beschriebenen Kontraindikationen, unerwünschten Wirkungen (UAW) und Interaktionen spiegeln die Involvierung der COX wider. Inwieweit die Beeinflussung der einzelnen COX-Isoformen durch die aktiven Metabolite kompetitiv oder allosterisch erfolgt, ist noch Gegenstand von Untersuchungen.
Metamizol kann jedoch auch Prostaglandin-unabhängig seine analgetische, aber auch antipyretische Wirkung entfalten [6]. In diesem Zusammenhang reduziert MAA im Hypothalamus sowohl das klassische PGE2-induzierte, als auch das davon unabhängige Fieber [7]. Als weitere Zielstrukturen der analgetischen Wirkung werden die Agonisierung cannabinoider Rezeptoren (CB1) über Amide aus Arachidonsäure und MAA bzw. AA, eine Blockade von Transient-Receptor-Potential-Ankyrin-1(TRPA1)-Ionenkanälen an Schmerzrezeptoren und die Involvierung neuronaler, ATP-abhängiger Kalium-Kanäle diskutiert [8 – 10]. Für den spasmolytischen Effekt werden ebenfalls Wirkungen des Metamizols auf cannabinoide Rezeptoren, aber auch eine reduzierte intrazelluläre Ca2+-Freisetzung durch Hemmung der Phospholipase C in den glatten Muskelzellen diskutiert [6, 11].
Die Nebenwirkungen
Bei den unerwünschten Arzneimittelwirkungen steht eine mögliche Agranulozytose, also eine starke Verminderung von Granulozyten auf unter 500 Zellen/µl Blut als eine seltene, aber potenziell letale UAW im Fokus. Die Inzidenz des Auftretens einer Agranulozytose unter Metamizol-Exposition wird sehr kontrovers diskutiert, sie ist aufgrund ihrer Seltenheit aber schwer zu bestimmen. Trotz diverser Kritikpunkte wird oftmals auf eine Fall-Kontroll-Studie an 22 Mio. Patienten verwiesen (International Agranulocytosis and Aplastic Anemia Study/IAAAS), die eine Häufigkeit von 1,1 Fällen pro Million Patienten (einwöchentliche Behandlung mit Metamizol) feststellte. Dabei beeinflusst die Applikationsart (i. v. oder oral) des Metamizols laut Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) nicht das Agranulozytoserisiko [12]. Diese UAW lässt sich nicht auf bestimmte Strukturmerkmale des Metamizols zurückführen, da auch andere, strukturell komplett unterschiedliche Arzneistoffe wie Clozapin, Clomipramin, Ticlopidin, Carbimazol, Thiamazol, Sulfasalazin, Cotrimoxazol oder Carbamazepin Agranulozytosen induzieren können. Die Pathogenese der Agranulozytose basiert offensichtlich auf einer immunologischen Reaktion, die jederzeit auftreten kann, auch wenn Metamizol zuvor gut vertragen wurde. Das Erkennen der Frühwarnsymptome einer Agranulozytose (siehe Kasten „So war das!“) ist für die Patienten extrem wichtig. Bei Auftreten einer Agranulozytose muss die Behandlung sofort (!) abgebrochen und der Patient mittels Differenzialblutbild überwacht werden.
so war das
Indikation
- akute, starke Schmerzen nach Verletzungen oder Operationen
- Koliken
- Tumorschmerzen
- sonstige akute oder chronisch starke Schmerzen, wenn andere therapeutische Maßnahmen nicht indiziert sind
- hohes Fieber, das auf andere Maßnahmen nicht anspricht
Wirkung
- schmerzstillend
- fiebersenkend
- spasmolytisch
- nicht antiphlogistisch
Dosierungshinweis
- 1 – 4 × täglich 1 – 2 Tbl./20 – 40 Tropfen/1 Zäpfchen/1 – 2 ml Ampulle
- bei Kindern nach Gewicht und Alter dosieren
Anwendungshinweise
- Einnahme unabhängig von den Mahlzeiten
- Einnahme so kurz wie möglich (weniger als eine Woche), da im Gegensatz zu NSAR keine antiphlogistische Wirkung
- Verwendung nur in den angegebenen Indikationen; der „Off-label-Use“ bei einfachem Schmerz hat ein ungünstiges Risiko-Nutzen-Profil
- harmloser roter Urin kann auftreten (bei hohen Dosierungen)
- nicht in der Schwangerschaft (3. Trimenon) und der Stillzeit
- bei Langzeitanwendung regelmäßiges Differenzialblutbild durchführen lassen
Nebenwirkungen/Verweise an den Arzt
- Agranulozytose, Frühsymptome erkennen:
- Fieber
- Halsschmerzen
- Schleimhautläsionen
- unerwartete Verschlechterung des Allgemeinzustandes
- allergische Reaktionen, besonderes der Haut
- Blutdruckabfall
abzuklärende Arzneimittel
- ASS 100
- Chlorpromazin
- Immunsuppressiva (Ciclosporin, Tacrolimus)
- Bupropion
- Methotrexat
- sonstige durch CYP3A4 und CYP2B6 metabolisierte Wirkstoffe
Neben dieser schwerwiegenden immunologischen UAW kann Metamizol gelegentlich zu einem Arzneimittelexanthem oder anderen Überempfindlichkeitsreaktionen der Augen, Nase und Haut führen. Insbesondere ein Brennen, Jucken und Hitzegefühl unter der Zunge, an den Handflächen und Fußsohlen sind Anzeichen dafür. Da sich diese immunologischen Reaktionen potenziell verschlimmern und sogar tödliche Verläufe wie z. B. Stevens-Johnson-Syndrom möglich sind, aber auch Anzeichen einer möglichen Agranulozytose sein können, ist es besonders wichtig, im Patientengespräch auf diese Anzeichen hinzuweisen. Während diese UAW auf immunologische Ursachen zurückzuführen sind, basiert ein möglicher Blutdruckabfall, der vor allem bei der i.v.-Gabe auftritt, höchstwahrscheinlich dosisabhängig auf der eigentlichen Wirkung der Metamizol-Metaboliten [13]. Bei Einnahme hoher Dosierungen von Metamizol kann mit der Rotfärbung des Urins eine weitere, aber harmlose UAW auftreten. Diese resultiert aus der Dimerisierung zweier 4-Aminoantipyrin-Moleküle unter Bildung eines Imins, welches als Rubazonsäure bezeichnet wird.
Die Kontraindikationen
Kontraindiziert ist die Anwendung von Metamizol bei Patienten, die gegen strukturell ähnliche Pyrazolone Überempfindlichkeiten aufweisen oder bei denen eine Agranulozytose auftrat. Dies gilt ebenfalls für Menschen mit Unverträglichkeiten gegen Analgetika generell, z. B. bei Vorliegen eines Analgetika-Asthma-Syndroms oder einer Analgetika-Intoleranz. Durch die Gefahr der Agranulozytose sollen auch Patienten mit allgemeinen Störungen des hämatopoetischen Systems, insbesondere der Knochenmarksfunktion, einem Glucose-6-Phosphat-Dehydrogenasemangel oder einer akut intermittierenden hepatischen Porphyrie kein Metamizol einnehmen. Durch die angenommene Wirkung auf die COX, und damit einhergehende Gefahr des Verschlusses des Ductus arteriosus Botalli sollen Schwangere das plazentagängige Metamizol im letzten Trimenon und darauffolgend während der Stillzeit meiden. Dies wurde auch durch das Risikobewertungsverfahren des CHMP auf europäischer Ebene im Dezember 2018 erneut festgehalten und so vom Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) im März 2019 in dieser Richtlinie umgesetzt [14, 15]. Embryotox rät allerdings während der gesamten Schwangerschaft und Stillzeit von Metamizol ab und verweist auf Paracetamol als sicherere Alternative [16].
Die Pharmakokinetik
Aufgrund der vielseitigen Metabolisierungsmöglichkeiten des Wirkstoffes in der Leber und der renalen Eliminierung der Metabolite muss pharmakokinetisch der Status dieser Organe berücksichtigt werden. Die Halbwertszeiten der pharmakologisch aktiven Metabolite betragen 2,7 ± 0,5 Stunden bei MAA und 3,7 ± 1,3 Stunden bei AA [2]. Dabei ist die Acetylierung von AA zu AAA abhängig von der N-Acetyltransferase (NAT2), von der in der Bevölkerung unterschiedliche Polymorphismen existieren. Bei älteren Menschen mit eingeschränkten Organfunktionen zeigte sich grundsätzlich eine Verdoppelung bis Verdreifachung der AUC des Hauptmetaboliten MAA. Bei Leberfunktionsstörungen steigt die Halbwertszeit der Metabolite MAA und FAA auf das Dreifache, während bei eingeschränkter Nierenfunktion die Haupteliminierungsprodukte FAA und AAA vermindert ausgeschieden werden. In beiden Fällen der Insuffizienz sollte eine Dosisanpassung des Metamizols erfolgen. Metamizol induziert CYP2B6 und CYP3A4 und wird selbst unter der Beteiligung mehrerer CYP-Enzyme von MAA zu AA demethyliert. Die Bioverfügbarkeit von MAA ist abhängig von der jeweiligen Darreichungsform. Interessanterweise zeigt die perorale Applikation als Tablette mit 91% sogar eine leicht bessere Bioverfügbarkeit als die i. m.-Gabe (87%), gefolgt von der peroralen Aufnahme von Tropfen (81%) und der rektalen Anwendung (54%) [2 – 5].
Die Interaktionen
Aufgrund des Wirkmechanismus und der Pharmakokinetik des Metamizols sind verschiedene Wechselwirkungen mit anderen Pharmaka zu beachten:
Die Anwendung von niedrigdosierter Acetylsalicylsäure als Thrombozytenaggregationshemmer zur Prophylaxe kardiovaskulärer Erkrankungen kann durch die Gabe von Metamizol auf pharmakodynamischer Ebene der COX-1 in seiner Wirksamkeit deutlich eingeschränkt sein [17, 18]. Empfohlen ist daher ein zumindest 30-minütiger Abstand der Metamizol-Einnahme von der ASS-Gabe [19].
Durch die Proliferationshemmung hämatogener Zellen unter Methotrexat soll die gleichzeitige Gabe von Metamizol zur Verhinderung von Hämatotoxizität ausgeschlossen werden [20].
Die gemeinsame Anwendung von Chlorpromazin und Metamizol kann eine Hypothermie induzieren [2].
Es wird berichtet, dass die Pharmakokinetik von Bupropion durch Metamizol beeinflusst wird, wobei eine Induktion des CYP2B6 zu verringerten Wirkstoffspiegeln des Antidepressivums führen kann [21]. Auch CYP3A4 wird durch Metamizol induziert [22]. Von den vielfältigen Wirkstoffen (u. a. Antihypertensiva oder Diuretika), die pharmakokinetisch beeinflusst werden, erscheint die Verringerung der Konzentrationen von Ciclosporin oder Tacrolimus bei der Unterdrückung von Immunreaktionen bei Transplantationspatienten besonders schwerwiegend [23].
Zusammenfassung
Metamizol ist und bleibt aufgrund seiner überzeugenden Wirkpotenz und der jahrzehntelangen Erfahrung im Umgang mit diesem Arzneistoff in den angegebenen engen Indikationen eine wichtige und auch sichere Komponente des Arzneimarktes. Für einen sicheren Umgang mit Metamizol und eine Minimierung von Nebenwirkungen bedarf es einer intensiven Beratung der Patienten in der Apotheke. Eine herausragende Bedeutung besitzt dabei die Aufklärung über die möglichen Frühwarnsymptome einer Agranulozytose aber auch der Check auf Interaktionen mit anderen relevanten Arzneimitteln. Mit dem Hinweis auf eine möglichst kurzzeitige Anwendung in der angegebenen Indikation und dem Verständnis, Metamizol nicht als ein universelles Schmerzmittel zu verstehen, sollten die Apotheker zur Aufrechterhaltung eines günstigen Nutzen-Risiko-Verhältnisses der Metamizol-Anwendung beitragen können. |
Literatur
[1] Schwabe U, Paffrath D, Ludwig W-D, Klauber J Eds. Arzneiverordnungs-Report 2018; Springer-Verlag: Berlin Heidelberg, 2018; ISBN 978-3-662-57385-3
[2] Fachinformation Novalgin® Filmtabletten, Stand: Januar 2019, verfügbar unter www.fachinfo.de
[3] Fachinformation Novalgin® Tropfen, Stand: März 2019, verfügbar unter www.fachinfo.de
[4] Fachinformation Novalgin® Injektionslösung, Stand: Januar 2019, verfügbar unter www.fachinfo.de
[5] Fachinformation Novalgin® Zäpfchen, Stand: Januar 2019, verfügbar unter www.fachinfo.de
[6] Jasiecka A, Maślanka T, Jaroszewski JJ. Pharmacological characteristics of metamizole. Pol J Vet Sci 2014;17:207-214
[7] Malvar D do C, Aguiar FA, Vaz A de LL, Assis DCR, de Melo MCC, Jabor VAP, Kalapothakis E, Ferreira SH, Clososki GC, de Souza GEP. Dipyrone metabolite 4-MAA induces hypothermia and inhibits PGE2-dependent and -independent fever while 4-AA only blocks PGE2-dependent fever. Br J Pharmacol 2014;171:3666-3679
[8] dos Santos GG, Dias EV, Teixeira JM, Athie MCP, Bonet IJM, Tambeli CH, Parada CA. The analgesic effect of dipyrone in peripheral tissue involves two different mechanisms: neuronal K(ATP) channel opening and CB(1) receptor activation. Eur J Pharmacol 2014;741:124-131
[9] Rogosch T, Sinning C, Podlewski A, Watzer B, Schlosburg J, Lichtman AH, Cascio MG, Bisogno T, Di Marzo V, Nüsing R et al. Novel bioactive metabolites of dipyrone (metamizol). Bioorg Med Chem 2012;20:101-107
[10] Nassini R, Fusi C, Materazzi S, Coppi E, Tuccinardi T, Marone IM, De Logu F, Preti D, Tonello R, Chiarugi A et al. The TRPA1 channel mediates the analgesic action of dipyrone and pyrazolone derivatives. Br J Pharmacol 2015;172:3397-3411
[11] Gulmez SE, Gurdal H, Tulunay FC. Airway Smooth Muscle Relaxations Induced by Dipyrone. Pharmacology 2006;78:202-208
[12] Ärzteblatt, D.Ä.G., Redaktion Deutsche Arzneimittelkommission der Deutschen Ärzteschaft: Aus der UAW-Datenbank: Agranulozytose nach Metamizol – sehr selten, aber häufiger als gedacht. Dtsch Ärztebl 2011;A1258-1759
[13] Lebensbedrohliche hypotensive Reaktionen nach Metamizol (UAW – Aus Fehlern lernen). Dtsch Ärztebl 2009;A846
[14] Metamizole containing medicinal products. verfügbar unter: www.ema.europa.eu/en/medicines/human/referrals/metamizole-containing-medicinal-products, Stand: Mai 2019
[15] BfArM – Risikobewertungsverfahren – Metamizol: Uneinheitliche Angaben zu Dosierung und Kontraindikationen. verfügbar unter: www.bfarm.de/SharedDocs/Risikoinformationen/Pharmakovigilanz/DE/RV_STP/m-r/metamizol.html, Stand Mai 2019
[16] Embryotox – Arzneimittelsicherheit in Schwangerschaft und Stillzeit: Metamizol. verfügbar unter: www.embryotox.de/arzneimittel/details/metamizol/, Stand Mai 2019
[17] Dannenberg L, Erschoff V, Bönner F, Gliem M, Jander S, Levkau B, Kelm M, Hohlfeld T, Zeus T, Polzin A. Dipyrone comedication in aspirin treated stroke patients impairs outcome. Vascul Pharmacol 2016;87:66-69
[18] Schnabel A. Interaktion von Metamizol und ASS: Reicht die Evidenz für klinische Konsequenzen? Arzneiverordnung in der Praxis 2019;46:45-51
[19] Polzin A, Richter S, Schrör K, Rassaf T, Merx MW, Kelm M, Hohlfeld T, Zeus T. Prevention of dipyrone (metamizole) induced inhibition of aspirin antiplatelet effects. Thromb Haemost 2015;114:87-95
[20] Blaser LS, Tramonti A, Egger P, Haschke M, Krähenbühl S, Rätz Bravo AE. Hematological safety of metamizole: retrospective analysis of WHO and Swiss spontaneous safety reports. Eur J Clin Pharmacol 2015;71:209-217
[21] Qin WJ, Zhang W, Liu ZQ, Chen XP, Tan ZR, Hu DL, Wang D, Fan L, Zhou HH. Rapid clinical induction of bupropion hydroxylation by metamizole in healthy Chinese men. Br. J Clin Pharmacol 2012;74:999-1004
[22] Saussele T, Burk O, Blievernicht JK, Klein K, Nussler A, Nussler N, Hengstler JG, Eichelbaum M, Schwab M, Zanger UM. Selective induction of human hepatic cytochromes P450 2B6 and 3A4 by metamizole. Clin Pharmacol Ther 2007;82:265-274
[23] Sigaroudi A, Jetter A, Mueller TF, Kullak-Ublick G, Weiler S. Severe reduction in tacrolimus concentrations with concomitant metamizole (dipyrone) therapy in transplant patients. Eur J Clin Pharmacol 2019
*Bedauerlicherweise ist in DAZ 2019, Nr. 35, S. 38 die Tageshöchstdosis bei den Tropfen falsch angegeben worden mit 120 Tropfen = 3000 mg. In der Online-Ausgabe der DAZ haben wir den Fehler korrigiert, sodass es wie in Tabelle 1 stehend richtig ist, dass die Tageshöchstdosis bei den Tropfen bei 160 Tropfen = 4000 mg liegt.
Wir bitten um Entschuldigung!
Die DAZ-Redaktion
























2 Kommentare
Metamizol und ASS
von Dr. Jens Malte Bickert am 06.09.2019 um 11:50 Uhr
» Auf diesen Kommentar antworten | 1 Antwort
AW: Metamizol und ASS
von Prof. Dr. Gerd Bendas und Fabian Baltes am 06.09.2019 um 11:58 Uhr
Das Kommentieren ist aktuell nicht möglich.