
- DAZ.online
- DAZ / AZ
- DAZ 30/2019
- Gefürchtete Clostridien
Infektiologie
Gefürchtete Clostridien
Die Giftproduzenten unter den Bakterien
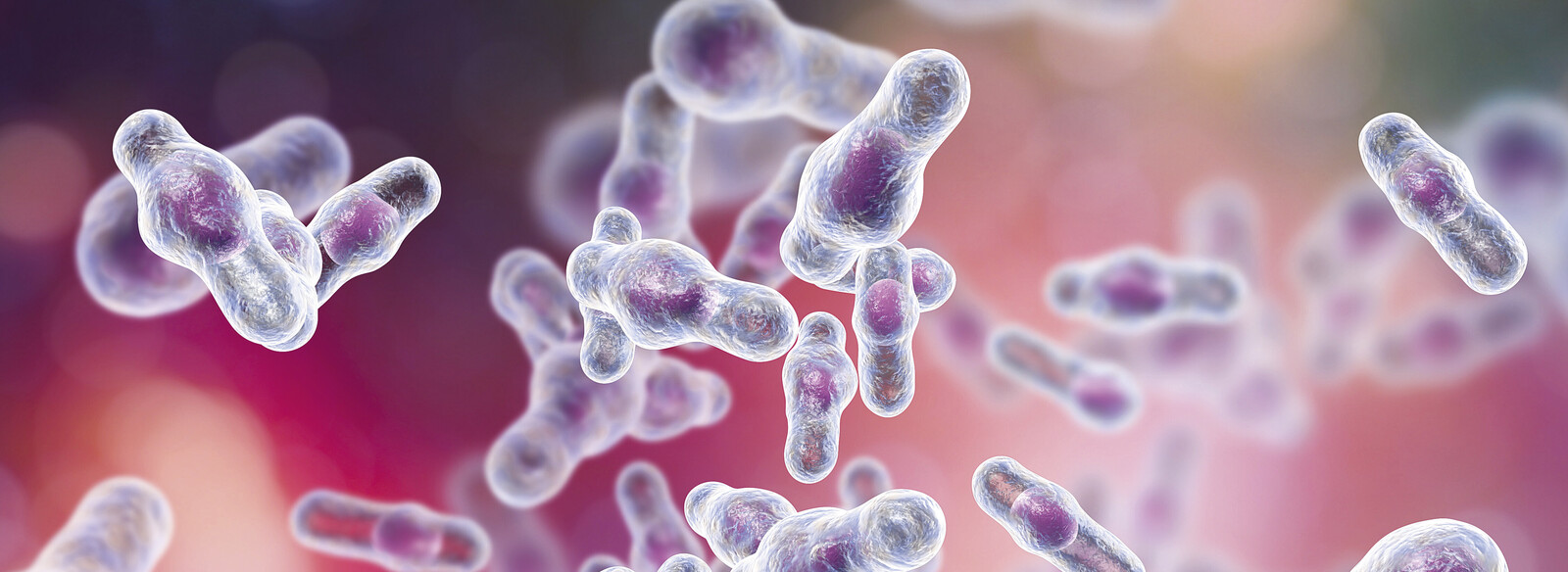
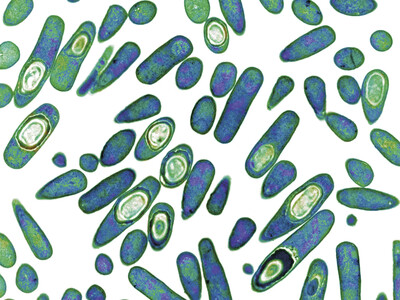
Clostridien sind stäbchenförmige grampositive Bakterien. Der Name geht auf das griechische Wort „closter“ (dt. Spindel) zurück (Abb. 1). Sie sind natürliche Bewohner von Böden, Staub und Gewässern [1]. Durch den Abbau von Cellulose, Zuckern und Aminosäuren besitzen Clostridien eine wichtige Funktion im ökologischen Kreislauf. Clostridium pasterianum ist ein bedeutender Stickstoff-Fixierer im Boden [2]. Clostridien produzieren Sporen, welche besonders resistent gegen Umwelteinflüsse wie Hitze oder UV-Licht sind [1]. Eine Besonderheit der Clostridien ist ihr Stoffwechsel. Durch das Fehlen von Katalase, Peroxidase und eines CYP-Systems können sie keine reaktiven Sauerstoffspezies abbauen und benötigen daher anaerobe (sauerstofffreie) Umweltbedingungen, um wachsen zu können [3]. Solche anaeroben Bedingungen sind im Boden, in Gewässern, im Darm und in geschlossenen Wunden vorhanden [1].
Die Pathogenität von Clostridien beruht auf der Fähigkeit, hochpotente Exotoxine bilden zu können. Die bekanntesten humanpathogenen Clostridien sind: Clostridium tetani (Wundstarrkrampf, Tetanus), C. perfringens (Gasbrand, Darmbrand) und C. botulinum (Botulismus) [1]. Clostridium difficile wurde 2016 taxonomisch als Clostridioides difficile neu eingeordnet [4]. Hierbei handelt es sich um den Erreger von den zunehmend gefürchteten Clostridium-difficile-Infektionen, die nach Behandlung mit Breitspektrum-Antibiotika auftreten können. Bei allen vier genannten Krankheitsbildern handelt es sich eher um Vergiftungen als um Infektionskrankheiten.
Clostridium tetani
Dem Auftreten des Wundstarrkrampfs Tetanus geht eine Infektion mit C. tetani voraus. Das Bakterium ist weltweit verbreitet und im Erdreich sowie in Darm und Fäzes von Pferden zu finden. Vorbedingung für eine Infektion ist eine Verletzung. Durch Verunreinigungen oder über Fremdkörper kann C. tetani in die Haut eindringen [5]. Unter anaeroben Bedingungen kann sich das Bakterium vermehren und Exotoxine produzieren [6]. Die Inkubationszeit ist abhängig von der Toxinproduktion und der Nähe zum Zentralnervensystem (ZNS) und beträgt zwischen 5 und 21 Tagen [5]. Die wichtigsten Toxine sind Tetanolysin und Tetanospasmin [6]. Bei Tetanolysin handelt es sich um ein hämolytisches Protein [7], bei Tetanospasmin um eine Zink-Metalloprotease. Tetanospasmin wandert mit einer Geschwindigkeit von 5 mm/Stunde entlang der Axone in das ZNS [5]. Dort werden inhibitorische Impulse mittels Glycin oder γ-Aminobuttersäure weitergeleitet. Diese Neurotransmitter werden in Vesikeln gespeichert, auf deren Oberfläche sich das Membranprotein Synaptobrevin befindet, das von Tetanospasmin gespalten wird [26]. Dadurch können nach einer Infektion mit C. tetani keine hemmenden Impulse mehr übertragen werden [6].
Symptome zeigen sich zuerst im Gesicht [6]. Dazu zählen tonisch-klonische Krämpfe, Kiefersperre (Trismus), Risus sardonicus (Teufelsgrinsen) und Opisthotonus (krampfhaft überstreckter Rücken/Nacken) [8]. Der Tod tritt durch Atemlähmung bei vollem Bewusstsein ein [9]. Bei ausgebrochener Erkrankung liegt die Letalität bei über 50% [9].
Als Behandlungsmaßnahme wird die Wunde chirurgisch ausgeschnitten und Tetanus-Immunglobulin injiziert [5]. Apotheken sind laut Apothekenbetriebsordnung dazu verpflichtet, Tetanus Hyper-Immun-Globulin 250 IE vorrätig zu halten. Dabei handelt es sich um ein Produkt aus menschlichem Blutplasma mit einem Anteil von mindestens 95% Immunglobulinen und mindestens 250 IE Antikörper gegen Tetanus-Toxin. Diese passive Immunisierung hält aber nicht lange vor. Durchschnittlich haben diese Antikörper eine Halbwertszeit von drei bis vier Wochen [25]. Eine antibiotische Behandlung mit Metronidazol verringert zwar nicht das zirkulierende Toxin, tötet jedoch C. tetani ab. Bei einer Intensivtherapie werden zusätzlich die Atemwege freigehalten und die Muskeln medikamentös relaxiert [5].
Neben dieser generalisierten Verlaufsform gibt es noch eine lokalisierte Form in unmittelbarer Umgebung der Wunde [8] und die neonatale Form. Die neonatale Form kann in den ersten zwei Lebenswochen auftreten und entsteht durch eine Infektion des Nabels. Symptome sind Rigidität, Trinkschwäche und Krämpfe [5].
Durch Impfungen ist Tetanus vermeidbar [1]. Die aktive Immunisierung ist die wichtigste Präventionsmaßnahme gegen Tetanus [1]. Sie wird mit einem Toxoid-Impfstoff durchgeführt und sollte alle zehn Jahre aufgefrischt werden. Besonders wichtig ist der Impfschutz, wenn Vorerkrankungen wie Durchblutungsstörungen, Hautleiden oder Diabetes vorhanden sind [5]. Vor allem in Entwicklungsländern mit niedriger Impfquote ist Tetanus eine häufige Todesursache. Weltweit sterben jährlich ca. eine Million Menschen an Tetanus [1]. In Industriestaaten mit hoher Impfquote ist die Inzidenz von Tetanus niedrig. In Deutschland werden durchschnittlich weniger als 15 Fälle pro Jahr gemeldet [5].
Clostridium perfringens
Zu den Auslösern des Gasbrand-Krankheitsbildes zählen mehrere Clostridien: C. perfringens, C. septicum, C. haemolyticum und C. oedematiens [8]. Der bedeutendste Erreger ist C. perfringens. Das anaerobe Bakterium lebt im Boden und im Darm von Menschen und Tieren [10]. Zahlreiche abbauende Enzyme wie Proteasen, Kollagenasen und Lecithinase können durch das Bakterium produziert werden [2]. C. perfringens wird weiterhin in die Serovare A bis E unterteilt, welche besonders potente Toxine bilden. Humanpathogen bedeutsam sind Serovar A als Auslöser des Gasbrands und Serovar C als Auslöser des Darmbrands [8]. Bakterien des Serovars C produzieren das β-Toxin, ein porenbildendes Protein [11]. Nach einer Inkubationszeit von ca. fünf Stunden tritt eine schmerzhafte, ödematöse, nekrotisierende Entzündung im Dünndarm auf. In diesem Stadium liegt die Letalität bei 40 bis 60%. Therapiemöglichkeiten sind neben einer chirurgischen Wundversorgung eine intravenöse antibiotische Therapie mit Penicillin G.
Gasbrand ist eine schwere Infektion, die in tiefen, verschmutzten Wunden entstehen kann. Die Wundinfektion wird durch das α-Toxin von C. perfringens Typ A ausgelöst. Bei dem Toxin handelt es sich um das Enzym Lecithinase [1]. Dieses Enzym kann Phosphatidylcholine, also essenzielle Phospholipide humaner Zellmembranen, abbauen. Dies führt zu gesteigerter Membranpermeabilität, Störungen im Elektrolythaushalt und Ödemen [9]. Die Inkubationszeit beträgt ein bis zwei Tage. Symptome sind Rötung, Schwellung und eine bräunliche, nekrotische Gewebsveränderung [1]. Die Abgabe von Enzymen in umliegendes Gewebe führt zu Myonekrosen [8]. Durch die Bildung von CO2 entstehen Gaseinlagerungen, die ein charakteristisches Zisch- und Knirschgeräusch, das sogenannte „Krepitus Zeichen“, erzeugen [6]. Der Tod erfolgt durch toxininduzierten Schock. Die Behandlung von Gasbrand erfolgt mit intravenösem Penicillin G und chirurgischer Wundrevision. Eine alleinige antibiotische Therapie ist nicht ausreichend, da in nekrotischem Gewebe keine ausreichenden Antibiotikaspiegel erzielt werden können [1].
Jährlich werden in den USA ca. 1000 Gasbrandfälle gemeldet [28]. Darmbrand ist eine klassische Lebensmittelvergiftung, die in den USA häufiger vorkommt [12]. In Deutschland sind Infektionen durch C. perfringens nicht meldepflichtig, daher gibt es keine aktuellen Fallzahlen.
Clostridium botulinum
Clostridium botulinum ist ein weltweit verbreiteter, natürlicher Bewohner von Böden und Gewässern [13]. Der Name geht auf das lateinische Wort botulus (dt. Wurst) zurück. Hieraus wurde das Bakterium erstmals isoliert [14]. Über Phagen (Bakterienviren) gelangt die genetische Information zur Toxinproduktion in die Bakterien. Es können sieben verschiedene Neurotoxine (Botulinumtoxin A bis G) produziert werden [8, 13]. Humanpathogen sind vor allem Toxine vom Typ A und B bedeutsam [9]. Botulinumtoxin A ist das stärkste Gift biologischer Herkunft [1]. Das Gift wird nur unter anaeroben Bedingungen produziert [6]. Botulinumtoxin A ist eine Metalloprotease, welche von Zellen der Darmschleimhaut resorbiert wird [6, 9]. Durch retrograden Transport entlang der Axone gelangt das Toxin ins Rückenmark [24]. Der Wirkmechanismus beruht auf einer Hemmung der Acetylcholin-Freisetzung und somit der Reizübertragung an der motorischen Endplatte aktivierender Neuronen. Als Folge entstehen schlaffe Lähmungen der Muskulatur. Da das Gift die Blut-Hirn-Schranke nicht überwinden kann, kommt es zu keinen Bewusstseinsstörungen während einer Vergiftung [13]. Vergiftungen mit Botulinumtoxin können je nach Infektionsweg in verschiedene Kategorien eingeteilt werden, wie Tabelle 1 zeigt.
Botulismusform |
Ursache |
Häufigkeit |
|---|---|---|
Lebensmittelbotulismus |
Verzehr kontaminierter Lebensmittel
Auskeimen der Sporen unter anaeroben Bedingungen im Darm
|
häufigste Form |
Wundbotulismus |
Infektion mit C. botulinum über kontaminierte Nadeln |
selten, bei intravenösem Drogenmissbrauch |
Säuglingsbotulismus |
Auskeimen der Sporen im Darm aufgrund fehlender kompetitiver Bakterienflora |
selten |
Inhalationsbotulismus |
Inhalation von Sporen, Auskeimen in der Lunge |
keine natürliche Form, nur nach gezielter Freisetzung |
Sonderformen |
iatrogen: als Folge einer Botulinumtoxin-Behandlung
bei bestimmten Vorerkrankungen: Morbus Crohn, Immunsuppression oder nach Antibiotika-Therapie
|
Die häufigste Form von Botulismus in Deutschland ist Lebensmittelbotulismus [1, 13]. Dabei keimen die Sporen von C. botulinum in unzureichend konservierten Lebensmitteln unter anaeroben Bedingungen aus. Ein typisches Zeichen für eine Kontamination sind ausgebeulte Konserven infolge von Gasbildung [1]. Die Latenzzeit ist abhängig von der Toxinmenge und kann bis zu 14 Tage betragen [13]. Die Primärsymptomatik kann mit den „4D“ zusammengefasst werden:
- Diplopie (Doppelsehen),
- Dysphagie (Schluckstörung),
- Dysphonie (Stimmstörung) und
- Dysarthrie (motorische Sprechstörung).
Im Anschluss folgt eine Lähmung der Pharynxmuskulatur und ein Versagen des Hustenreflexes [13]. Der Tod erfolgt durch Atemlähmung bei vollem Bewusstsein [9].
Wundbotulismus ist in Deutschland selten und kommt hauptsächlich bei Verwendung kontaminierter Nadeln beim intravenösen Drogenmissbrauch vor [13]. Kontamination und Verlauf zeigen Ähnlichkeiten zu lokal begrenztem Tetanus [8]. Die Latenzzeit beträgt bis zu zehn Tage. Als zusätzliches Symptom kann hier Fieber auftreten [13].
Säuglingsbotulismus entsteht durch Auskeimen der Sporen im Darm, bei fehlender kompetitiver Darmflora [13]. Früher wurde Honig mit Säuglingsbotulismus assoziiert [8]. Als Symptome zeigen sich eine allgemeine Muskelschwäche, Dyspnoe, Obstipation, schlaffe Lähmungen, Schluckstörungen und Trinkschwäche. Zur Behandlung von Botulismus steht ein polyvalentes Antitoxin zur Verfügung. Dabei handelt es sich um FAb-Antikörper (fragment antibody binding) gegen die Toxine A, B und E, welche in Pferden produziert und anschließend enzymatisch verdaut wurden [13]. Dieses Antitoxin befindet sich auch in den Notfalldepots der Landesapothekerkammern.
Bei Lebensmittelbotulismus wird der Nahrungsbrei endoskopisch entfernt, der Magen wird aber nicht gespült [13]. Medikamentös können Cholinesterase-Hemmer wie Neostigmin verabreicht werden. Bei Wundbotulismus wird als antibiotische Therapie intravenös Penicillin G appliziert. Ist eine intensivmedizinische Behandlung indiziert, erfolgt zusätzlich eine Beatmung.
Seit 2002 traten pro Jahr zwischen 0 bis 24 Fälle von Botulismus in Deutschland auf. Es ist somit eine seltene Erkrankung [13]. Prophylaktisch sollte auf den Verzehr von bombierten (aufgewölbten) Konservendosen verzichtet werden [1]. Botulinumtoxine sind als Proteine hitzelabil und können durch Kochen inaktiviert werden [1, 8]. Konserviert man Lebensmittel selbst, so sollte man darauf achten, den pH-Wert niedriger als 4,5 zu halten, denn darunter findet keine Sporenbildung mehr statt [6].
Botulinumtoxin wird auch medizinisch und kosmetisch verwendet. Zum Anwendungsbereich zählen idiopathischer Blepharospasmus, Spasmus hemifacialis, Torticolis spasmodicus, Stirnfalten und Krähenfüße [1].
Botulismus bedroht aber auch das Leben von Wasservögeln. Vor allem in stehenden Gewässern, die durch Algenwachstum „gekippt“ sind, herrschen anaerobe Bedingungen. Dadurch wird das Wachstum von C. botulinum gefördert. Die Aufnahme der Keime/Sporen führt zu klassischem Botulismus, welcher auch für Wasservögel tödlich ist [27].
Auf einen Blick
- Tetanus, Gasbrand und Botulismus sind Erkrankungen mit hoher Mortalität.
- Durch Impfungen, Hygiene und Lebensmittelhygiene sind sie aber in modernen Industriestaaten selten geworden. Dennoch ist die Gefahr durch die anaeroben, bakteriellen Giftproduzenten nicht gebannt.
- Es darf nicht vergessen werden, dass in Entwicklungsländern zahlreiche Menschen vor allem an Tetanus sterben.
- Ebenso darf C. difficile nicht aus den Augen verloren werden. Die steigenden Fallzahlen zeigen, dass sich die Problematik noch verschärft.
Clostridioides difficile
Letzter Vertreter der vorgestellten Reihe ist Clostridioides difficile. Bis 2016 hieß diese Bakterienart Clostridium difficile. Dieser Name ist heute noch weit verbreitet. Die Umbenennung erfolgte nach einer taxonomischen Neueinordnung, aufgrund molekularbiologischer Erkenntnisse nach Sequenzierung von 16s-RNA [4].
In den letzten Jahren hat das Bakterium als Auslöser nosokomialer Infektionen für Aufruhr gesorgt [15]. In den USA stieg die Infektionszahl in 2010er-Jahren um 400% [15, 16]. Dabei werden ca. 14.000 Todesfälle pro Jahr dem Erreger zugeschrieben [16]. Das anaerobe Stäbchenbakterium gehört zur normalen Darmflora des Menschen [1]. Es handelt sich somit um einen opportunistischen Krankheitserreger. Ein besonderes Infektionsrisiko stellt eine vorausgegangene Behandlung mit Breitspektrum-Antibiotika wie Clindamycin, Fluorchinolonen oder Cephalosporinen dar [17]. Durch natürliche Resistenzen überlebt C. difficile eine konventionelle Antibiotikabehandlung und kann sich an Epithelzellen der Darmwand anlagern [16].
C. difficile kann dort Exotoxine produzieren. Die Exotoxine A und B sind Monoglycosyltransferasen, welche nach Aufnahme in die Zelle GTPasen der Rho-Familie inaktivieren [18]. Diese GTPasen sind essenziell für den Aufbau des Zytoskeletts aus Aktinfilamenten; werden sie inaktiviert, kollabiert die Zelle. Als Folge kommt es zu einem Elektrolyt- und Wassereinstrom in das Darmlumen, was Durchfälle zur Folge hat [17]. Eine C.-difficile-Infektion kann von einer milden Diarrhö über eine pseudomembranöse Colitis bis hin zu einem toxischen Megakolon reichen [16]. Neben Durchfall können auch Symptome wie Fieber, Abdominalkrämpfe und Gewichtsverlust auftreten [17].
Zur Therapie des Durchfalls sind in erster Linie eine Wasser- und Elektrolytsubstitution indiziert. Motilitätshemmer wie Loperamid sind wie auch bei sonstigen bakteriell induzierten Durchfällen kontraindiziert [1]. Nach Möglichkeit sollte eine vorherige Antibiotikabehandlung abgebrochen werden. Zur antibiotischen Therapie einer C.-difficile-Infektion stehen Metronidazol und Vancomycin zur Verfügung [16]. Für leichtere Formen hat sich das kostengünstigere Metronidazol als ausreichend wirksam erwiesen [18, 19]. Für einen schweren Verlauf zeigte Vancomycin eine erhöhte Wirksamkeit und wird deshalb gerade bei schweren Verlaufsformen bevorzugt eingesetzt [20, 21]. Sekundär können auch Teicoplanin oder Fidaxomicin eingesetzt werden [16]. Dennoch kommt es bei etwa 20% der Patienten zu einem Rezidiv [17]. Seit 2018 steht mit Bezlotoxumab (Zinplava®) ein Antikörper gegen Exotoxin B als Rezidivprophylaxe zur Verfügung. In klinischen Studien hat sich auch eine fäkale Mikrobiota-Transplantation erfolgreich gezeigt [22].
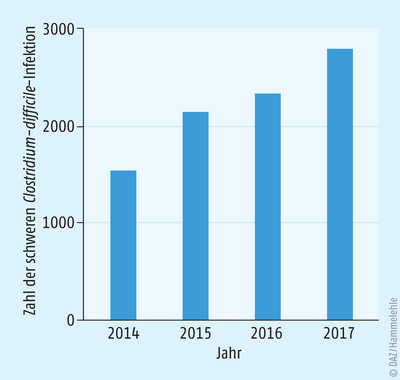
Aufgrund der steigenden Infektionszahlen wurde 2016 eine Meldepflicht für schwere Verläufe von C.-difficile-Infektionen in Deutschland eingeführt. Die Statistikdaten des Robert Koch-Instituts zeigen, trotz der größeren Aufmerksamkeit für C.-difficile-Infektionen, steigende Fallzahlen [23] (s. Abb. 2). |
Literatur
[1] Stock I. Bakterien, Viren, Wirkstoffe. 1. Auflage, Govi-Verlag, Eschborn 2009
[2] Madigan MT, Martinko JM, Stahl DA, Clark DP. Brock Mikrobiologie. 11. Auflage, Pearson Studium, Müchen 2006
[3] Hatheway C. Toxigenic Clostridia. Clin Microbiol Rev 1990;3:66-98
[4] Lawson PA, Citron DM, Tyrell KL, Finegold SM. Reclassification of Clostridium difficile as Clostridioides difficile (Hall and O’Toole 1935) Prevot 1938, Anaerobe 2016; 40:95-99
[5] Tetanus. RKI-Ratgeber, Version 02/2018. Robert Koch-Institut, www.rki.de
[6] Kayser FH, Bienz KA, Eckert J, Zinkernagel RM. Medizinische Mikrobiologie. 9. Auflage, Thieme Verlag, Stuttgart 1998
[7] Keyel PA, Heid ME, Salter RD. Macrophage responses to bacterial toxins: a balance between activation and suppression. Immunol Res 2011;50:118-123
[8] Hof H, Dörries R. Medizinische Mikrobiologie. in: Duale Reihe. 3. Auflage, Thieme Verlag, Stuttgart 2009.
[9] Baltz B. Medizinische Mikrobiologie systematisch. Uni-Med Verlag, Bremen 1999
[10] Wen Q, McClane BA. Detection of enterotoxigenic Clostridium perfringens type A isolates in American retail foods. Appl Environ Microbiol 2004;70:2685-2691
[11] Popoff MR. Clostridial pore-forming toxins: powerful virulence factors. Anaerobe 2004;30:220-238
[12] Grass JE, Gould LH, Mahon BE. Epidemiology of Foodborne Disease Outbreaks Caused by Clostridium perfringens, United States, 1998–2010. Foodborne Pathog Dis 2013;10:131-136
[13] Botulismus. Ratgeber des Robert Koch-Instituts, Epid Bull 2018;20:189-195
[14] van Ermengem E. Über einen neuen anaeroben Bacillus und seine Beziehung zum Botulismus. Med Microbiol Immunol 1897;26:1-56
[15] Antibiotic resistance treats in the United States 2013. Centers for Disease Control and Prevention (CDC) Atlanta, USA 2013
[16] Allerberger F, Hell M, Krause R, Högenauer C. Clostridium difficile-Infektion. Österreichische Ärztezeitung 2014;5:20-29
[17] Bahl H, Dürre B. Clostridia: Biotechnology and medical application. Wiley VCH Verlag, Weinheim 2011
[18] David G, Teasley MM, Olsen RL, Gebhard DN, Gerding LR, Peterson MJ, Schwartz JT, Lee RJ. Prospektive randomised trail of metronidazole versus vancomycin for Clostridium difficile associated diarrhea and colitis. Lancet 1983;322:1043-1046
[19] Wenisch C, Parschalk B, Hasenhündl M, Hirschl AM, Graninger W. Comparison of vancomycin, teicoplanin, metronidazole, and fusidic acid for treatment of Clostridium difficile-associated diarrhea. Clin Infect Dis 1996;22:813-818
[20] Zar FA, Bakkanagari SR, Moorthi KMLST, Davis MB. A cmparison of vancomycin and metronidazole for the treatment of Clostridium difficile-associated diarrhea, stratified by disease severity. Clin Infect Dis 2997;45:302-307
[21] Al-Nassir WN, Sethi AK, Nerandzic MM, Bobulsky GS, Jump RLP, Donskey CJ. Comparison of clinical and microbiological response to treatment of Clostridium difficile-associated disease with metronidazole and vancomycin. Clin Infect Dis 2008;47:56-62
[22] Liubakka A, Vaughn BP. Clostridium difficile infection and fecal microbiota transplant. AACN Adv Crit Care 2016;27:324-337
[23] Infektionsepidemiologisches Jahrbuch meldepflichtiger Krankheiten. Robert Koch-Institut 2017:69-73
[24] Matak I, Riederer P, Lachovic Z. Botulinum toxin’s axonal transport from periphery to the spinal cord. Neurochem Int 2012;61:236-239
[25] Gebrauchs- und Fachinformation Tetagam® P. CSL Behring, Stand Januar 2018
[26] Pellizzari R, Rossetto O, Schiavo G, Monteucco C. Tetanus and botulinum neurotoxins: mechanism of action and therapeutic uses. Philos Trans R Soc Lond B Biol Sci 1999:354:259-268
[27] Weitzel C. Botulismus bei Wasservögel. Schwanenschutz Komitee e.V., www.schwanenschutz-komitee.de/botulismus-bei-wasserv%C3%B6gel/
[28] Leikin JB, Paloucek FP. Clostridium perfringens poisoning. in: Poisoning and Toxicology Handbook. 4. Auflage, Informa 2008:892-893

























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.