
- DAZ.online
- DAZ / AZ
- DAZ 38/2018
- Was Listen leisten kö
Geriatrie
Was Listen leisten können
Mit Beers, Forta, Priscus und Co. die Therapie für Ältere optimieren
Jede Arzneimittelanwendung bleibt ein Individualexperiment. Neben unverzichtbarem Wissen um die Eigenschaften von Arzneimitteln müssen für jede individualisierte Arzneimitteltherapie auch patientenbezogene Merkmale und weitere Faktoren wie Krankheitseinflüsse berücksichtigt werden [3]. Doch wie kann man den Überblick behalten? Eine an Leitlinien orientierte Therapie ist eigentlich wünschenswert, doch ist sie auch bei älteren Patienten immer empfehlenswert? Ältere Patienten sind zwar bedingt durch Multimorbidität die Hauptanwendergruppe von Arzneimitteln und noch dazu eine durch den demografischen Wandel sowohl in Deutschland als auch weltweit stetig wachsende Personengruppe, jedoch werden sie aus Studien immer noch häufig ausgeschlossen und es existieren nur wenige Leitlinien speziell für Ältere.
2013 wurde die Hausärztliche Leitlinie „Multimedikation“ von der Leitliniengruppe Hessen veröffentlicht [4]. Sie bietet eine Hilfestellung dafür, was zu beachten ist, wenn Patienten multimorbide sind und mehrere Arzneimittel gleichzeitig einnehmen. Durch die Umsetzung der Empfehlungen sollen die bei Polymedikation auftretenden Probleme einer Über-, Unter- und Fehlversorgung erkannt, vermieden bzw. korrigiert werden. Dazu können z. B. eine Priorisierung der einzelnen Arzneistoffe und der Medication Appropriateness Index (MAI) [5] hilfreich sein. Der Medication Appropriateness Index umfasst zehn Fragen, die zu jedem Arzneimittel neu überdacht werden sollen:
1. Gibt es eine Indikation für das Arzneimittel?
2. Ist das Arzneimittel wirksam für die verordnete Indikation?
3. Stimmt die Dosierung?
4. Sind die Einnahmevorschriften korrekt?
(Applikationsmodus, Einnahmefrequenz, Einnahmezeit, Relation zu den Mahlzeiten)
5. Gibt es klinisch relevante Interaktionen mit anderen Arzneimitteln?
6. Gibt es klinisch relevante Interaktionen mit anderen Krankheiten/Zuständen?
7. Sind die Anwendungsvorschriften für den Patienten praktikabel?
8. Wurden unnötige Doppelverordnungen vermieden?
9. Ist die Dauer der medikamentösen Therapie (seit wann verordnet) adäquat?
10. Wurde die kostengünstigste Alternative vergleichbarer Präparate ausgewählt?
Der Bewertung der Medikation sollte stets eine vollständige Arzneimittelanamnese vorausgehen.
Zudem gilt es bei älteren Patienten auf potenziell inadäquate Medikation (PIM) zu achten. Als potenziell inadäquate Medikation für Ältere gelten Arzneimittel, bei deren Anwendung ein hohes Risiko für unerwünschte Arzneimittelwirkungen (UAW) besteht und für die es gleichzeitig eine sicherere Alternative gibt. Auch Arzneimittel mit einem (altersabhängigen) schlechten Nutzen-Risiko-Verhältnis, unsicheren therapeutischen Effekten bzw. einem Überwiegen der UAW gegenüber dem klinischen Benefit gelten als potenziell inadäquate Medikation. Außerdem können Arzneimittel bei bestimmten Erkrankungen sowie in bestimmten Dosierungen im Alter potenziell inadäquat sein [6–8].
Auch der Ausdruck potenziell inadäquate Verordnung/Verschreibung (PIP, engl.: potentially inappropriate prescribing) ist gebräuchlich, wobei dieser insbesondere auch die Qualität der Verordnung umfasst und Überverordnung von nicht oder nicht mehr notwendigen Arzneimitteln, Unterverordnung (fehlende Verordnung von Arzneimitteln, wenn keine Kontraindikation vorliegt) und Fehlverordnung (z. B. inadäquates Arzneimittel, inadäquate Dosierung oder Behandlungsdauer sowie die Verordnung von Arzneimitteln mit wesentlichen Interaktionen) mit einschließt.
Der Terminus „potenziell“ wird gebraucht, da es bedingt durch den bereits erwähnten häufigen Ausschluss von älteren Patienten aus Studien nur wenig Evidenz aus randomisierten, kontrollierten Studien für die Einstufung der Arzneimittel als inadäquate Medikation gibt. So wird eine potenziell inadäquate Medikation häufig aufgrund epidemiologischer Studien, pharmakologischer Überlegungen sowie klinischer Erfahrung eingestuft. Zudem können potenziell inadäquate Arzneimittel bei bestimmten Patienten und in bestimmten Situationen auch adäquat sein.
1991 erstellte der amerikanische Geriater Mark Beers die viel zitierte Beers-Liste, eine Negativliste, mithilfe derer Arzneimittel identifiziert werden können, welche im Alter nicht angewendet werden sollten [9]. In den folgenden Jahren wurden auch in weiteren Ländern wie Kanada, Frankreich und Norwegen Bemühungen unternommen, innerhalb der dort verfügbaren Arzneistoffe potenziell inadäquate zu identifizieren.
Die internationalen Medikationsempfehlungen für multimorbide, ältere Patienten sind, bedingt durch unterschiedliche Marktgegebenheiten und Verordnungspraktiken, lediglich begrenzt auf Deutschland übertragbar. Mit
- der deutschen Übersetzung der Beers-Kriterien,
- den START-STOPP-Kriterien,
- der FORTA-Einteilung,
- der Priscus-Liste und
- der EU(7)-PIM-Liste
stehen jedoch auch für den deutschen sowie allgemein für den europäischen Raum Kriterien-Kataloge zum Bewerten von potenziell inadäquater Medikation zur Verfügung. Die Kriterien-Kataloge haben verschiedene Entstehungsgeschichten und Schwerpunkte. Einige identifizieren problematische Arzneistoffe, andere beschreiben bestimmte Verordnungsszenarien bzw. Anwendungssituationen und wieder andere bewerten nach Kategorien von problematisch bis unverzichtbar. Im Folgenden sollen die Kriterien-Kataloge, die sich auch für den deutschen Arzneimittelmarkt eignen, genauer dargestellt werden.
Beers-Kriterien
Die sogenannte Beers-Liste wurde bereits in den 1990er-Jahren in den USA nach einer Literaturrecherche und einer modifizierten Delphi-Methode entwickelt [9, 10]. Sie war die erste Liste, mit welcher der Einsatz einer potenziell inadäquaten Medikation bei älteren Patienten minimiert bzw. regelmäßig auf einen kritischen Prüfstand gestellt werden sollte. Im Verlauf wurden die Kriterien mehrfach aktualisiert, zuletzt durch die American Geriatrics Society im Herbst 2015. Die Kriterien sind weltweit anerkannt und eine wichtige Grundlage in vielen Studien, welche die Prävalenz und die Auswirkungen potenziell inadäquater Medikation untersuchen. Die aktualisierte Liste der Beers-Kriterien wurde im Journal of the American Geriatrics Society publiziert [11] und ist auch auf www.geriatricscareonline.org zugänglich. Da die Beers-Kriterien für den amerikanischen Arzneimittelmarkt entwickelt wurden, sind sie nur bedingt für Deutschland anwendbar. Seit Herbst 2016 steht jedoch auch eine deutsche Übersetzung und Anpassung an den deutschen Arzneimittelmarkt zur Verfügung[12]. In die Übersetzung wurden nur Arzneistoffe aufgenommen, die in Deutschland als Fertigarzneimittel zugelassen sind. Auch Empfehlungen die Nierenfunktion betreffend wurden an die in Deutschland gültigen Empfehlungen und Grenzwerte angepasst bzw. ergänzt.
START-STOPP-Kriterien
Die STOPP-Kriterien (Screening Tool of Older Person’s Prescriptions) wurden 2008 von Gallagher und O’Mahony veröffentlicht [13]. STOPP beinhaltet in dieser ersten Version 65 klinisch signifikante Kriterien für potenziell inadäquate Verordnungen, wobei jedem Kriterium eine genaue Begründung folgt, z. B. tricyclic antidepressants (TCA) with dementia (risk of worsening cognitive impairment).
Die STOPP-Kriterien sind nach physiologischen Systemen geordnet und gehen neben Arzneimittelinteraktionen auch auf Interaktionen von Arzneimitteln und Komorbiditäten ein. Sie sind also diagnoseabhängig. Auch Doppelverordnungen werden negativ bewertet. Eine Assoziation zwischen STOPP-Kriterien-Medikation und UAW konnte nachgewiesen werden [14]. Die Kriterien wurden in Irland entwickelt und validiert und eignen sich für den europäischen Arzneimittelmarkt [15 – 17]. STOPP kann in Zusammenhang mit den START-Kriterien (Screening Tool to Alert doctors to Right Treatment) genutzt werden. START besteht in der ersten Version aus 22 evidenzbasierten Verordnungsindikatoren für Krankheiten, die im Alter häufig sind. Mit START wird die im Alter trotz Polymedikation häufig auch problematische Untertherapie adressiert (PPO, engl.: potential prescribing omission): Trotz vorliegender Indikation wird eine Erkrankung nicht therapiert, obwohl der Patient von einer Behandlung möglicherweise profitieren würde. Ein START-Kriterium lautet z. B. „Calcium and vitamin D supplement in patients with known osteoporosis (previous fragility fracture, acquired dorsal kyphosis)“. Im Oktober 2014 wurde die Version 2 der STOPP-Kriterien veröffentlicht [18].
Forta-Liste
Die Forta-Einteilung ist ein von Wehling et al. 2008 vorgeschlagenes Bewertungssystem, das die Arzneimittel in vier Gruppen von A bis D einteilt [19 – 21]. Forta steht in diesem Zusammenhang für „Fit fOR The Aged“ und ist die erste Positiv-Negativ-Arzneimittelliste. Geben Sie den Webcode E5LH9 bei DAZ.online unter www.deutsche-apotheker-zeitung.de in die Suchfunktion ein und Sie gelangen direkt zur Forta-Liste. Die Arzneimittel werden folgendermaßen kategorisiert:
- Kategorie A (absolutely): Arzneimittel, die im Alter in großen Studien geprüft sind und für welche eindeutig positive Nutzen-Risiko-Bewertungen vorliegen.
- Kategorie B (beneficial): Arzneimittel, die zwar eine nachgewiesene Wirksamkeit bei älteren Patienten haben, aber mit Einschränkungen hinsichtlich des Wirkungsausmaßes oder ihrer Sicherheit belegt sind.
- Kategorie C (careful): Arzneimittel mit einer ungünstigen Nutzen-Risiko-Relation für ältere Patienten. Sie erfordern eine genaue Beobachtung von Wirkungen und Nebenwirkungen und sind nur ausnahmsweise erfolgreich. Bei mehr als drei Arzneimitteln gleichzeitig sollten sie als erste weggelassen und möglichst Alternativen gesucht werden.
- Kategorie D (don’t): Diese Arzneimittel sollten fast immer vermieden werden. Stattdessen sollte man auf altersverträgliche Alternativen ausweichen. Der Einsatz ist nicht sinnvoll.
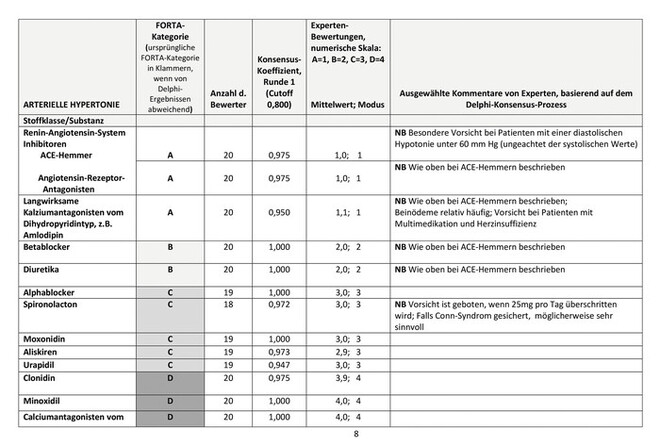
Die Grundidee von Forta ist die kritische Suche nach vorhandener Evidenz als Begründung für eine medikamentöse Behandlung (Abb. 1). Die Gruppeneinteilung der Arzneistoffe hinsichtlich ihrer Alterstauglichkeit erfolgt anhand der verfügbaren Evidenz und von Expertenmeinungen bei fehlender Evidenz. Ein wichtiger weiterer Bestandteil ist die Verbindung von Erkrankungen und geeigneter Pharmakotherapie. Damit erweitert Forta das Konzept der alleinigen Verwendung von Negativlisten und ermöglicht auch die Aufdeckung von Über- und Untertherapie. Forta bewertet zurzeit die zugelassene Medikation für die Krankheitsbilder arterielle Hypertonie, Herzinsuffizienz, koronare Herzkrankheit, Schlaganfall, Vorhofflimmern, obstruktive Lungenerkrankungen, Osteoporose, Diabetes mellitus, Demenz, Morbus Parkinson, Depression, Schlafstörungen, Suchterkrankungen, chronische Schmerzen und Tumorerkrankungen.
2016 wurde die über 200 Bewertungen von Arzneimitteln zur Behandlung chronischer Erkrankungen umfassende Forta-Liste 2015 veröffentlicht [22]. Sie ist im Internet frei zugänglich und wurde neben den vier Initiatoren der Forta-Liste durch 21 Experten aus Deutschland und Österreich in einem zweistufigen Delphi-Prozess geprüft und ergänzt. Seit Mai 2017 steht die Forta-Liste auch als Smartphone-App zur Verfügung. Zu beachten ist, dass es sich bei Forta um implizite Kriterien handelt, sodass die Anwendung genaue Informationen über Erkrankungen und weitere medizinische Umstände des Patienten erfordert. Es muss bei der Anwendung von Forta deswegen beispielsweise folgendes beachtet werden [21]:
- Ein Arzneimittel kann indikationsabhängig verschiedene Labels bekommen, z. B. werden Betablocker bei koronarer Herzkrankheit (KHK) mit A kategorisiert, bei Hypertonie „nur“ mit B.
- Kontraindikationen stehen über der Klassifikation, z. B. dürfen auch A-Arzneimittel bei Allergien nicht gegeben werden.
- Die individuelle Therapieentscheidung wird nicht ersetzt, Forta lässt wie jede Vereinfachung Ausnahmen (auch bei den Extremen A und D) zu und ist als schnelle Orientierungshilfe zum Gedankenanstoß gedacht.
Priscus-Liste
Die Priscus-Liste (lat.: priscus – altehrwürdig) wurde 2010 von Holt et al. veröffentlicht und ist eine speziell für den deutschen Raum gültige Liste [7]. Sie stuft 83 Arzneistoffe – teilweise dosisabhängig – als PIM ein, benennt Therapiealternativen und beinhaltet Empfehlungen bzw. Monitoring-Hinweise für den Fall des medizinisch alternativlosen Einsatzes von PIM (Abb. 2). Die 83 Arzneistoffe entstammen 18 verschiedenen Arzneistoffklassen aus einem breiten Spektrum an Indikationsgebieten. Die Priscus-
Liste beruht auf Expertenkonsens. Die Priscus-Liste ist im Internet frei zugänglich und umfasst 33 Seiten. Geben Sie den Webcode N4XV2 bei DAZ.online unter www.deutsche-apotheker-zeitung.de in die Suchfunktion ein und Sie gelangen direkt zur Priscus-Liste. In sechs Spalten sind jeweils der potenziell inadäquate Arzneistoff, die Bewertungsergebnisse aus der Delphi-Befragung, die Begründung für die Einstufung als PIM und mögliche Therapiealternativen sowie Maßnahmen, falls das Arzneimittel trotzdem verwendet werden soll, und zu vermeidende Komorbiditäten aufgeführt. Dabei sind die Arzneistoffe nach Indikationsgebieten und Arzneistoffklassen sortiert. Darüber hinaus gibt es überschaubarere gekürzte Fassungen „für den Schreibtisch“. Auch in vielen EDV-Systemen in der Apotheke ist die Priscus-Liste hinterlegt. Unter Verwendung der Priscus-Liste wurden mehrere Untersuchungen zur Prävalenz der Verordnung von PIM bei über 65-Jährigen in Deutschland durchgeführt. Gemäß Analysen der Verordnungsdaten gesetzlicher Krankenversicherungen erhielten etwa ein Viertel der Versicherten mindestens einmal im Jahr eine PIM-Verordnung, Frauen häufiger als Männer [23, 24]. Zu beachten ist, dass einige der Arzneistoffe der Priscus-Liste auch als nicht rezeptflichtige Präparate (OTC) verfügbar sind und die Prävalenz folglich noch höher liegen dürfte.
EU(7)-PIM-Liste
Die EU(7)-PIM-Liste wurde 2015 mit dem Ziel einer europäischen Harmonisierung verschiedener nationaler Empfehlungen entwickelt. Es sollte eine PIM-Liste entstehen, die auf die Arzneimittelmärkte mehrerer europäischer Länder angepasst ist und somit eine einheitliche Erhebung über die verschiedenen Länder hinweg ermöglicht. Zudem sollte die Liste auch eine Hilfestellung für die klinische Praxis bieten. Die EU(7)-PIM-Liste wurde in einem der Erstellung der Priscus-Liste stark ähnelnden Prozess konzipiert. Die fertige Liste beinhaltet 282 Arzneistoffe aus 34 Wirkstoffklassen. Es ist jeweils begründet, warum der jeweilige Arzneistoff als PIM eingestuft wurde, und es werden Empfehlungen für Dosisanpassungen sowie Therapiealternativen genannt [25].
Arbeiten mit den unterschiedlichen Listen
Negativlisten wie die Priscus-Liste sind durch die explizite diagnoseunabhängige Auflistung von Arzneistoffen leicht anzuwenden. Ihr besonderer Vorzug ist ihre gute Praktikabilität und sie eignet sich beispielsweise auch für eine schnelle Überprüfung der Medikation in der Apotheke. Gleichzeitig bedürfen sie durch diese explizite Auflistung einer ständigen Aktualisierung und bergen das Risiko der Annahme, nicht aufgelistete Arzneistoffe wären in jedem Fall geeignet. Durch Forta wird eine krankheitsbezogene Bewertung möglich und es können Über- und Untertherapie aufgedeckt werden, sowie „D-Substanzen“ auf möglicherweise besser geeignete Substanzen der Kategorie A oder B umgestellt werden. Jedoch ist die Anwendung komplexer und es werden weitere Informationen wie beispielsweise die Diagnosen und weitere medizinische Umstände des Patienten benötigt. In der Apotheke könnte Forta bei einer ausführlichen Medikationsanalyse eingesetzt werden. Im Artikel „Schritt für Schritt - Der Weg zu einer adäquaten Pharmakotherapie“ auf S. 48 in dieser DAZ zeigen wir an einem Patientenfall beispielhaft die Arbeit mit diesen Listen.
Literatur
[1] Stausberg J, Hasford J. Drug-related admissions and hospital-acquired adverse drug events in Germany: a longitudinal analysis from 2003 to 2007 of ICD-10-coded routine data. BMC Health Serv Res 2011;11:134
[2] Pirmohamed M, James S, Meakin S et al. Adverse drug reactions as cause of admission to hospital: prospective analysis of 18 820 patients. BMJ 2004; 329:15–19
[3] Von Renteln-Kruse W, Frilling B, Neumann L. Arzneimittel im Alter. De Gruyter, Berlin/Boston 2014
[4] Bergert FW, Braun M, Ehrenthal K, Feßler J, Gross J, Hüttner U et al. Hausärztliche Leitlinie Multimedikation – Empfehlungen zum Umgang mit Multimedikation bei Erwachsenen und geriatrischen Patienten. 2013
[5] Hanlon JT, Schmader KE, Samsa GP, Weinberger M, Uttech KM, Lewis IK et al. A method for assessing drug therapy appropriateness. J Clin Epidemiol 1992;45(10):1045–1051
[6] Thiem DU. Potenziell inadäquate Medikation. Internist 2012;53(9):1125–1130
[7] Holt S, Schmiedl S, Thürmann PA. Potentially inappropriate medications in the elderly: the PRISCUS list. Dtsch Ärztebl Int 2010;107(31–32):543–551
[8] Gallagher P, Ryan C, Byrne S, Kennedy J, O’Mahony D. STOPP (Screening Tool of Older Person’s Prescriptions) and START (Screening Tool to Alert doctors to Right Treatment). Consensus validation. Int J Clin Pharmacol Ther 2008;46(2):72–83
[9] Beers MH, Ouslander JG, Rollingher I, Reuben DB, Brooks J, Beck JC. Explicit criteria for determining inappropriate medication use in nursing home residents. UCLA Division of Geriatric Medicine. Arch Intern Med 1991;151(9):1825–1832
[10] Beers MH. Explicit criteria for determining potentially inappropriate medication use by the elderly. An update. Arch Intern Med 1997;157(14):1531–1536
[11] American Geriatrics Society 2015 Beers Criteria Update Expert Panel. American Geriatrics Society 2015 Updated Beers Criteria for Potentially Inappropriate Medication Use in Older Adults. J Am Geriatr Soc 2015;63(11):2227–2246
[12] Prax K, Abbas Z, Friedland K et al. Aktuelles Update der Beers-Kriterien. Deutsche Übersetzung und Anpassung an den deutschen Arzneimittelmarkt. MMP 2016;10:39
[13] Gallagher P, Ryan C, Byrne S, Kennedy J, O’Mahony D. STOPP (Screening Tool of Older Person’s Prescriptions) and START (Screening Tool to Alert doctors to Right Treatment). Consensus validation. Int J Clin Pharmacol Ther 2008;46(2):72–83
[14] Hamilton H, Gallagher P, Ryan C, Byrne S, O‘Mahony D. Potentially inappropriate medications defined by STOPP criteria and the risk of adverse drug events in older hospitalized patients. Arch Intern Med 2011;171:1013–1019
[15] Gallagher P, O’Mahony D. STOPP (Screening Tool of Older Persons’ potentially inappropriate Prescriptions): application to acutely ill elderly patients and comparison with Beers’ criteria. Age Ageing 2008;37(6):673–679
[16] Kruse J. Priscus, STOPP and Beers’ criteria – A German-Irish comparison using several screening tools in the residential home setting. Beitrag auf dem ESCP International Workshop on Geriatrics. Utrecht, Niederlande 2011
[17] Siebert S, Elkeles B, Hempel G, Kruse J, Smollich M. Die PRISCUS-Liste im klinischen Test. Z Gerontol Geriatr 2012;46(1):35–47
[18] O’Mahony D, O’Sullivan D, Byrne S et al. STOPP/START criteria for potentially inappropriate prescribing in older people: version 2. Age Ageing 2015;44(2):213–218
[19] Wehling M. Drug therapy in the elderly: too much or too little, what to do? A new assessment system: fit for the aged FORTA. Dtsch Med Wochenschr 2008;133(44):2289–2291
[20] Kuhn-Thiel AM, Weiß C, Wehling M. The FORTA authors/expert panel members. Consensus Validation of the FORTA (Fit fOR The Aged) List: A Clinical Tool for Increasing the Appropriateness of Pharmacotherapy in the Elderly. Drugs Aging 2014;31(2):131–140
[21] Wehling M, Burkhardt H. Arzneitherapie für Ältere. 4. Aufl., Springer-Verlag Berlin Heidelberg, 2016
[22] Pazan F, Weiss C, Wehling M et al. The FORTA (Fit fOR The Aged) List 2015: Update of a Vali- dated Clinical Tool for Improved Pharmacotherapy in the Elderly. Drugs Aging 2016;33(6):447–449
[23] Amann U, Schmedt N, Garbe E. Prescribing of potentially inappropriate medications for the elderly: an analysis based on the PRISCUS list. Dtsch Ärztebl Int 2012;109:69–75
[24] Thürmann PA, Holt-Noreiks S, Nink K, Zawinell A. Arzneimittelversorgung älterer Patienten. In: Günster C, Klose J, Schmacke N., Hrsg. Versorgungs-Report 2012. Stuttgart 2011
[25] Renom-Guiteras A, Meyer G, Thürmann PA. The EU(7)-PIM list: a list of potentially inappropriate medications for older people consented by experts from seven European countries. Eur J Clin Pharmacol 2015;71(7):861–875
[26] Rudolph JL, Salow MJ, Angelini MC et al. The anticholinergic risk scale and anticholinergic adverse effects in older persons. Arch Intern Med 2008;168(5):508-513
[27] Boustani MA, Campbell NL, Munger S et al. Impact of anticholinergics on the aging brain: a review and practical application. Aging Health 2008;4(3):311-320
[28] Fachinformation Iscover® 75 mg und 300 mg, Stand 12/2016
Lesen Sie hier weiter:
- Dr. Beate Mussawy Wer oder was ist „alt“? Wie sich die physiologischen Organfunktionen bei älteren Patienten verändern
- Dr. Beate Mussawy Schritt für Schritt: Der Weg zu einer adäquaten Pharmakotherapie
























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.