
- DAZ.online
- DAZ / AZ
- DAZ 25/2018
- Priorisierung ist die ...
Gesundheitsökonomie
Priorisierung ist die Regel
Die Gesundheitssysteme wählen aus, welche Hepatitis-C-Patienten geheilt werden
Unzweifelhaft hat die Einführung der oralen, direkt antiviral wirkenden Substanzen (direct-acting antiviral drugs, DAA) die Behandlung der chronischen Hepatitis C revolutioniert. DAA erzielen genotypübergreifend binnen etwa zwölf Wochen SVR-Raten (SVR, sustained virological response) von weit über 90%. Die bisherigen Interferon-haltigen Kombinationstherapien, die über 16 bis 72 Wochen angewendet werden, haben eine Vielzahl von erheblichen Nebenwirkungen, beispielsweise Depressionen. Mediziner diskutieren längst nicht mehr den grundsätzlichen medizinischen Nutzen der direkt antiviral wirkenden Substanzen, sondern spezielle Fragen wie Therapiedauer, Anwendung bei älteren Patienten oder bei einem sehr schlechten Leberzustand.
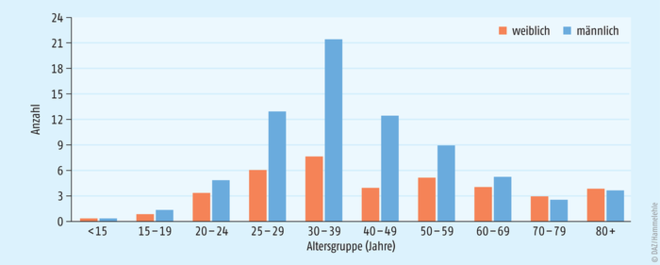
Denn die Krux der neuen Medikamente ist nach wie vor ihr Preis. Je nach Behandlungsdauer – in der Regel zwischen acht und 24 Wochen – bewegten sich die Kosten für die pharmakologische Behandlung eines Hepatitis-C-Patienten zwischen 35.000 und 105.000 Euro (siehe Tab. 1). Das hat sich auch nach Rabattverhandlungen mit den Krankenkassen nicht entscheidend geändert. Zum Zeitpunkt der Einführung dieser Medikamentengruppe waren Therapiekosten von bis zu fünf Milliarden Euro im Jahr im Gespräch. Tatsächlich hätten sich laut dem Berliner IGES-Institut für die Jahre seit 2014 im Schnitt lediglich Kosten von gut 750 Millionen Euro im Jahr ergeben [2]. Dabei seien rund 25.000 Patienten mit Arzneimitteln wie Sofosbuvir (Sovaldi®), Ledipasvir/Sofosbuvir (Harvoni®), Daclatasvir (Daklinza®), Dasabuvir (Exviera®), Elbasvir/Grazoprevir (Zepatier®), Ombitasvir/Paritaprevir/Ritonavir (Viekirax®), Simeprevir (Olysio®) und Sofosbuvir/Velpatasvir (Epclusa®) behandelt worden [1]. Die Zahl der Infizierten Patienten wird in Deutschland auf rund 300.000 geschätzt [2] (Abb. 1).
Wirkstoffe |
Präparate |
Hersteller |
Zulassung |
HWZ
Stunden
|
DDD |
Therapie-dauer, Wochen |
Kosten pro Therapiedauer in Euro |
|---|---|---|---|---|---|---|---|
Nukleosidanaloga | |||||||
Ribavirin |
Copegus®
|
Roche |
1992 |
300 |
1000 mg |
24 – 48 |
5021 – 10.042 |
Ribavirin |
Ribavirin |
Teva |
2012 |
300 |
1000 mg |
24 – 48 |
1655 – 3330 |
Alfa-Interferone | |||||||
Peginterferon alfa 2b |
PegIntron®
|
MSD |
2000 |
40 |
15 μg |
24 – 48 |
5925 – 11.850 |
Peginterferon alfa 2a |
Pegasys®
|
Roche |
2002 |
70 – 160 |
26 μg |
24 – 48 |
6799 – 13.598 |
Protease-Inhibitoren | |||||||
Boceprevir |
Victrelis®
|
MSD |
2011 |
3,4 |
2400 mg |
24 – 48 |
18.877 – 37.753 |
Telaprevir |
Incivo®
|
Janssen |
2011 |
9 – 11 |
2250 mg |
24 – 48 |
außer Vertrieb |
Simeprevir |
Olysio®
|
Janssen |
2014 |
10 – 41 |
150 mg |
12 |
28.079 |
Paritaprevir |
in Viekirax®
|
AbbVie |
2015 |
5,5 |
150 mg |
12 – 24 |
siehe unten |
Grazoprevir |
in Zepatier®
|
MSD |
2016 |
31 |
100 mg |
12 |
siehe unten |
Polymerase-Inhibitoren | |||||||
Sofosbuvir |
Sovaldi®
|
Gilead |
2014 |
18 – 26 |
400 mg |
12 – 24 |
50.624 – 100.851 |
Dasabuvir |
Exviera®
|
AbbVie |
2015 |
18 – 26 |
500 mg |
6 |
2331 |
Replikations-Inhibitoren | |||||||
Daclatasvir |
Daklinza®
|
BMS |
2014 |
13 – 15 |
60 mg |
12 – 24 |
26.892 – 53.784 |
Ledipasvir |
Harvoni®
|
Gilead |
2014 |
47 |
90 mg |
8 – 24 |
35.332 – 105.997 |
+ Sofosbuvir |
Harvoni®+ Ribavirin |
Gilead |
12 – 24 |
61.478 – 122.956 |
|||
Ombitasvir |
Viekirax®
|
AbbVie |
2015 |
21 – 25 |
12,5 mg |
12 – 24 |
48.445 – 96.890 |
+ Paritaprevir |
+ 75 mg |
||||||
+ Ritonavir |
+ 50 mg
pro Tablette, 2 ×/Tag
|
||||||
|
Viekirax® +
Exviera® +
Ribavirin
|
12 – 24 |
54.571 – 109.141 |
|||||
Elbasvir |
Zepatier®
|
MSD |
2016 |
24 – 31 |
50 mg |
12 |
35.390 |
+ Grazoprevir |
+ 100 mg |
||||||
Sofosbuvir |
Epclusa®
|
Gilead |
2016 |
400 mg |
12 |
56.554 |
|
+ Velpatasvir |
+ 100 mg |
||||||
„DAA für alle“ ist ein Problem, dessen „Lösung“ derzeit weltweit ähnlich angegangen wird: Reiche wie ärmere Länder haben für die Therapien mit den direkt antiviral wirkenden Substanzen seit 2014 Beschränkungen hinsichtlich der Erstattungsfähigkeit eingeführt. Um die Kosten der Therapie zu deckeln, werden medizinische Kriterien wie das Fibrose-Stadium zu Filtern für die Erstattung umfunktioniert, der Zugang der Patienten zur medizinisch besten Hepatitis-C-Therapie wird somit eingeschränkt. Dabei gerät aus dem Blick, dass eine kurz- bis mittelfristige „Kostenexplosion“ auf lange Sicht billiger kommen könnte, wie verschiedene Berechnungen gezeigt haben. Es muss auch berücksichtigt werden, dass rund 80% der HCV-bedingten Gesundheitsaufwendungen (ohne HCV-Therapie) für Spätfolgen wie Zirrhose, Leberkrebs und Lebertransplantationen aufgewendet werden [3]. In Europa gehen etwa 35% der Leberzirrhosen und 32% der hepatozellulären Karzinome auf eine Infektion mit dem Hepatitis-C-Virus zurück [4].
Wer soll wann mit DAA behandelt werden?
Aus medizinischer Sicht geben nationale wie internationale Leitlinien klare Antworten auf diese Frage. Die im Jahr 2016 überarbeitete Guideline der European Association for the Study of the Liver (EASL) gibt mit Grad A1 (A = hohe Evidenz, 1 = starke Empfehlung) die Ziele vor:
- Allen therapienaiven und therapieerfahrenen Patienten mit kompensierter oder dekompensierter chronischer Lebererkrankung durch das Hepatitis-C-Virus, die eine Behandlung wünschen und bei denen keine Kontraindikationen bestehen, sollte eine antivirale Therapie angeboten werden.
- Ein unverzüglicher Therapiebeginn wird empfohlen bei Patienten mit signifikanter Fibrose oder Zirrhose (Metavir-Score F2 = mittelgradige Fibrose, F3 = hochgradige Fibrose oder F4 = Zirrhose) inklusive dekompensierter Zirrhose, bei Patienten mit extrahepatischen Manifestationen (z. B. HCV-assoziierte Vaskulitis, Nephropathie, Non-Hodgkin-B-Zell-Lymphom), bei Wiederauftreten von HCV nach Lebertransplantation sowie bei potenziellen HCV-Überträgern (unter anderem Drogengebrauch, Hochrisiko-Sexualpraktiken, Frauen mit Kinderwunsch, Hämodialyse-Patienten).
- Nicht empfohlen wird die Therapie explizit bei Patienten mit begrenzter Lebenserwartung wegen nicht-Leber-assoziierter Komorbiditäten (Grad B2).
- Nationale Eliminationspläne sollten ökonomische Strategien entwickeln, um den unbeschränkten Zugang zur Therapie voranzutreiben, heißt es vorausschauend (Grad B1) [5].
Soweit die medizinische Sicht. Die Sicht der Kostenträger ist angesichts der hohen Preise der oralen direkt antiviral wirkenden Substanzen zwangsläufig eine andere. Eine der ersten Studien, die im Jahr 2014 die Erstattungskriterien für Sofosbuvir in den USA untersuchte, fand in neun von zehn Bundesstaaten Beschränkungen auf Basis von Alkohol- und Drogenkonsum; in zwei von drei Staaten durften nur spezialisierte Ärzte das Mittel verschreiben und drei von vier Staaten setzten ein fortgeschrittenes Fibrose-Stadium (> F3) voraus. Ein Update der Studie aus 2016 zeigte zwar eine Tendenz zu weniger Erstattungsbeschränkungen. Aber auch die verbliebenen Limitationen stehen im Konflikt mit den medizinischen Empfehlungen und im Gegensatz zur Hepatitis-C-Strategie der Weltgesundheitsorganisation WHO: Die sieht bis 2030 eine Reduktion der HCV-Inzidenz um 80% vor, eine Diagnoserate von 90% der Betroffenen, und eine Therapiequote von 80% bei infizierten Menschen [6].
Wer sind die Betroffenen?
Dem Global Hepatitis Report der WHO zufolge waren im Jahr 2015 etwa 1% der Weltbevölkerung chronisch mit dem Hepatitis-C-Virus infiziert. Die höchste Prävalenz fand sich mit 2,3% in der östlichen Mittelmeerregion (WHO-Region EMRO), vor allem bedingt durch in der Vergangenheit erfolgte nosokomiale Transmissionen, gefolgt von der WHO-Region Europa mit 1,5%, in der ein Großteil der Infektionen injizierendem Drogenkonsum zugeschrieben wird. Die Spanne der Antikörperprävalenz (anti-HCV) bewegt sich zwischen 0,1% in Irland, 5% in Italien und 13% in Usbekistan. In den anderen WHO-Regionen liegt die Prävalenz chronischer HCV-Infektionen zwischen 0,5% und 1,0%.
In Deutschland stellen der gemeinsame Gebrauch von Injektionsutensilien bei Drogenabusus sowie homosexuelle Kontakte unter Männern die wesentlichen Transmissionsrisiken dar. Die parenteralen Übertragungsrisiken durch Blut und Blutprodukte wurden durch die Einführung serologischer und molekularer Tests im Jahr 1991 praktisch eliminiert. Das Robert Koch-Institut geht bei Hepatitis-C-Virus-Infektionen (Vorliegen von anti-HCV) von diesen Prävalenzraten aus [9]:
Allgemeinbevölkerung Deutschlands: 0,3 bis 0,5%
injizierende Drogengebrauchende: zwischen 37 und 75%
Gefängnisinsassen: zwischen 8,6 und 17,6%
Migranten: zwischen 1,2 und 6,3%
Transplantatempfänger (vor 1991): „erhöhte Prävalenz“
dialysepflichtige Patienten: 4%
Heterogene Erstattungskriterien in Europa
Diese Gesundheitsziele stehen auch im europäischen Raum infrage. Zwar ist die HCV-Inzidenz in Europa im Sinken begriffen. Doch werden 20 bis 30% der geschätzten 3,2 Millionen HCV-infizierten Menschen in der nächsten Dekade versterben oder schwere Komplikationen wie Leberzirrhose und -karzinome entwickeln – wenn kein breiter Zugang zu DAA-Therapien gewährleistet ist. Das haben Forscher erst im letzten Jahr hochgerechnet [7].
Die Verfügbarkeit und die Erstattungsregularien für Interferon-freie DAA-Therapien untersuchte jüngst das International Network on Hepatitis in Substance Users (INHSU) in 35 Ländern des europäischen Wirtschaftsraumes einschließlich der Schweiz [8]. Grundsätzlich stehen in allen Ländern DAA-Therapien zur Verfügung und sind mit unterschiedlichen Einschränkungen erstattungsfähig. Die am meisten verbreitete Therapie bestand aus Ombitasvir, Paritaprevir und Ritonavir (Viekirax®, AbbVie), plus Dasabuvir (Exviera®, Abbvie) und mit oder ohne Ritonavir (Norvir®, Abbvie). Dieses Therapieregime war in allen Länder mit Ausnahme von Finnland und Malta erstattungsfähig. Die geringste Akzeptanz diesbezüglich genoss die Kombination Sofosbuvir (Sovaldi®, Gilead) plus Daclatasvir (Daklinza®, BMS) mit oder ohne Ribavirin (erstattungsfähig in 22 von 35 Ländern).
Verschreibertypus: Universell sind in Europa Restriktionen hinsichtlich des verschreibenden Arztes: 33 Länder (94%) verlangen einen Spezialisten, z. B. Gastroenterologen, Hepatologen, Internisten oder Infektionsmediziner, für die Verschreibung von direkt antiviral wirkenden Substanzen. Nur in England (nach Konsultation eines multidisziplinären Komitees) und in Deutschland dürfen auch Allgemeinärzte die Therapeutika verordnen.
Fibrose-Stadium: Fast jedes zweite Land (16 von 35) setzt ein Fibrose-Stadium von F2 oder höher für die antivirale Therapie voraus (F2: zehn Länder; F3: fünf Länder; F4: nur Malta). Teils ist die Erstattung abhängig vom HCV-Genotyp und vom Alter des Patienten, teils werden je nach Fibrose-Stadium unterschiedliche Wirkstoffe erstattet. Deutschland zählt zu den Ländern ohne Restriktionen.
Drogen- oder Alkoholmissbrauch: Sechs Länder (17%) verlangen eine mindestens sechsmonatige Abstinenzphase vor einer antiviralen HCV-Therapie. Kroatien fordert zusätzlich Urinkontrollen, Ungarn eine psychiatrische Bestätigung der „Compliancefähigkeit“ zur Therapie und zur Drogenabstinenz. Hingegen dürfen in Lichtenstein und der Schweiz intravenös Drogenabhängige sogar prioritär und ohne Ansehen des Fibrose-Stadiums mit direkt antiviral wirkenden Substanzen behandelt werden.
Regularien im Widerspruch zu Leitlinien
Zu den Limitationen der Studie zählt, dass ausschließlich schriftliche Regularien und Verordnungen erfasst wurden und nicht die tatsächliche Vorgehensweise der Ärzte. So könnte es vorkommen, diskutieren die Autoren, dass Ärzte gewisse Patienten bewusst oder unbewusst für die Therapie auswählen oder sie ihnen vorenthalten, wobei Drogenabhängigkeit, Versicherungsstatus und weiteres mehr eine Rolle spielen könnten. Auch ein unterschiedlicher Zugang zu Behandlern je nach sozialem, städtischem oder ländlichem Umfeld könne zu Diskrepanzen innerhalb eines Landes führen.
Ungeachtet dessen betonen die Autoren, dass auch moderate Einschränkungen der Erstattungsfähigkeit im Widerspruch zu den aktuellen medizinischen Empfehlungen stehen, wonach jedem HCV-Infizierten eine Behandlung angeboten werden soll, bei dem sie nicht kontraindiziert ist. Um das WHO-Ziel der Elimination der viralen Hepatitis als Kardinalproblem der öffentlichen Gesundheit zu erreichen, müssten Erstattungsbeschränkungen minimiert werden. Vor allem die medizinisch fragwürdige Beschränkung der DAA-Therapie auf Menschen mit fortgeschrittenem Fibrose-Stadium (wie sie die Hälfte der europäischen Länder praktiziert) werten die Autoren kritisch als Priorisierung im Kontext der durch hochpreisige direkt antiviral wirkende Substanzen belasteten Kostenbudgets der Länder. Dahinter stehe eine Interimsstrategie, die auf fallende Preise hoffe.
Mehr statt weniger Therapie
Die Hepatitis-Experten zeigen in ihrer hochrangig publizierten Studie konkrete Ansätze, wie den Betroffenen der Zugang zu wirksamen Therapien zu erleichtern ist:
- Vorurteile bekämpfen: Intravenös Drogengebrauchende stellen in Europa die Gruppe mit dem höchsten Anteil an viralen Leberinfektionen. Die dauerhafte Virus-Eradikation eliminiert das individuelle Transmissionsrisiko. Gerade die Behandlung drogenabhängiger Menschen als Multiplikatoren der Virusinfektion hätte nicht nur individuelle, sondern auch Public-Health-Effekte, so die Autoren. Die Praxis sieht noch anders aus: In einer aktuellen Befragung von 108 spezialisierten HCV-Behandlern waren nur 15% bereit, eine DAA-Therapie bei Drogen-injizierenden HCV-Patienten einzuleiten [12]. Reinfektionsrisiko und Kosten wurden als Hinderungsgründe angegeben. Die Autoren zitieren mehrere aktuelle Studien, die eine hervorragende Adhärenz und hohe Ansprechraten auf eine Therapie mit direkt antiviral wirkenden Substanzen sowohl bei aktuell Drogenabhängigen als auch bei jenen unter einer Substitutionstherapie nachgewiesen haben. Reinfektionen waren eher selten.
- Niederschwellige Verschreibung: Die Länder Europas sollten Regularien abschaffen, wonach Allgemeinärzte keine Anti-HCV-Therapien verordnen dürfen. Zugang zu Behandlung und Kontrollen seien dann erleichtert, der Outcome unter den sehr sicheren DAA-Therapien der gleiche: In einer amerikanischen Studie, in der 600 HCV-Infizierte mit Ledipasvir und Sofosbuvir behandelt wurden, machte es für den Therapieerfolg keinen Unterschied, ob ein Facharzt, ein Allgemeinarzt oder geschultes Pflegepersonal die Medikamente verabreichte: Die Adhärenz für Kontrolltermine war bei den Spezialisten niedriger.
- Training und Schulung von Allgemeinärzten, Pflegepersonal, Alkohol- und Drogenberatern zum Thema Hepatitis C durch spezialisierte Ärzte seien weitere breitenwirksame Maßnahmen.
- Niedrigere und transparente Preise: Rabatte auf die hohen Listenpreise der direkt antiviral wirkenden Substanzen sind in den Ländern Europas nicht ohne weiteres einsehbar, ihr Zustandekommen oft intransparent. Im Sinne der Patienten und der öffentlichen Gesundheit müssten zügige und offenere Preisverhandlungen geführt werden, um letztlich Erstattungsbeschränkungen und Priorisierung obsolet zu machen. |
Quelle
[1] NN. Hepatitis C: GKV-Verband bestätigt einen Rückgang der Kosten von Hepatitis-C-Therapien, übt aber weiterhin Kritik. Ärzte Zeitung online, 31. Juli 2017, www.aerztezeitung.de/politik_gesellschaft/krankenkassen/article/940478/hepatitis-c-gkv-bestaetigt-kostenrueckgang.html, abgerufen am 23. Mai 2018
[2] Poethko-Muller C et al. Ergebnisse der Studie zur Gesundheit Erwachsener in Deutschland (DEGS1). Bundesgesundheitsblatt, Gesundheitsforschung, Gesundheitsschutz. 2013;56(5-6):707-715
[3] Leberhilfe Projekt gUG in: Sucker-Sket K. Gesamtökonomische Studie: Der Traum von Deutschland ohne Hepatitis C. DAZ.online vom 4. März 2016, www.deutsche-apotheker-zeitung.de/news/artikel/2016/03/04/der-traum-von-deutschland-ohne-hepatitis-c
[4] Prophylaxe, Diagnostik und Therapie der Hepatitis-C-Virus(HCV)-Infektion. S3-Leitlinie der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS), Stand: 31. Dezember 2017, AWMF-Register-Nr.: 021/012
[5] European Association for the study of the Liver. EASL recommendations on treatment of hepatitis C 2016. J Hepatol 2017;66:153–194
[6] Global health sector strategy on viral hepatitis 2016 – 2021. Towards ending viral hepatitis. WHO, Juni 2016
[7] Razavi H et al. Hepatitis C virus prevalence and level of intervention required to achieve the WHO targets for elimination in the European Union by 2030: a modelling study. Lancet Gastroenterol Hepatol 2017;2:325–336
[8] Marshall AD et al. Restrictions for reimbursement of interferon-free direct-acting antiviral drugs for HCV infection in Europe. Lancet Gastroenterol Hepatol 2018;3:125–133
[9] Hepatitis C – Ratgeber für Ärzte, Robert Koch-Institut, www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_HepatitisC.html;jsessionid=9F87E4CB0B33AA18037754A6DC745100.2_cid390#doc2389942bodyText3, abgerufen am 24. Mai 2018
[10] Hepatitis C – GBE-Themenheft. Gesundheitsberichterstattung des Bundes gemeinsam getragen von RKI und Destatis, Robert Koch-Institut, Berlin 2016
[11] Schwabe U, Paffrath D, Ludwig W-D, Klauber J. Arzneiverordnungsreport 2017, Springer-Verlag GmbH
[12] Asher AK et al. Clinicians' views of hepatitis C virus treatment candidacy with direct-acting antiviral regimens for people who inject drugs. Subst Use Misuse 2016;51:1218–1223






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.