
- DAZ.online
- DAZ / AZ
- DAZ 12/2018
- Therapie der Hämophilie ...
Arzneimittel und Therapie
Therapie der Hämophilie A in Bewegung
In 2018 wurden bereits zwei neue Produkte zur Behandlung der Blutgerinnungsstörung zugelassen
Hämophilie A – auch als „Bluterkrankheit“ bekannt – ist eine seltene Störung der Blutgerinnung, die auf einem absoluten oder relativen Mangel an Gerinnungsfaktor VIII beruht. In Deutschland leben schätzungsweise 4000 Patienten mit der angeborenen Gerinnungsstörung. Meist ist die Krankheit erblich bedingt. Da die genetischen Defekte das X-Chromosom betreffen, tritt die Hämophilie A nur bei Jungen und Männern auf. Frauen können allerdings Träger der Mutation sein und die Blutgerinnungsstörung über Generationen weitervererben.
Unbehandelt schwere Folgen
Das klinische Erscheinungsbild korreliert mit der Faktor-VIII-Konzentration im Blut: Je weniger funktionaler Faktor VIII vom Körper produziert wird, umso schwerer verläuft die Hämophilie. Schwer zu stillende traumatische und spontane Blutungen – insbesondere in die Gelenke – sind die Folge des angeborenen Faktormangels. Unbehandelt haben die Blutungen gravierende Auswirkungen: Sie können lebensbedrohlich sein und zu langfristigen Gelenkschäden führen.
Fortschritte in der Therapie
In den letzten Jahrzehnten konnten in der Therapie der Hämophilie ständig neue Fortschritte erzielt werden, sodass betroffene Patienten mittlerweile – zumindest in entwickelten Ländern wie Deutschland – ein fast normales Leben führen können. Grundlage der Therapie ist es nach wie vor, den fehlenden Gerinnungsfaktor zu ersetzen. Dazu wurden ursprünglich vor allem Faktor-VIII-Konzentrate eingesetzt. Nicht zuletzt wegen des großen Skandals in den 1980er-Jahren, bei dem sich viele Patienten mit HIV infizierten, werden diese aus menschlichen Blutprodukten gewonnenen Präparate jedoch immer seltener verwendet. Dank der Biotechnologie stehen mit einer Vielzahl an rekombinanten Produkten mittlerweile sicherere Alternativen zur Verfügung (s. Tabelle): Diese bergen kein Risiko einer Ansteckung mit Pathogenen.
Handelsname (Beispiele) |
Wirkstoff |
Zulassung |
|---|---|---|
Hämophilie A | ||
Faktor-VIII-Konzentrate | ||
Beriate®, Fahndi®, Faktor VIII SDH® Intersero, Haemoctin®, Immunate®, Octanate®, Voncento®, Wilate®
|
Blutgerinnungsfaktor VIII vom Menschen |
1983 bis 2013 |
Rekombinante Faktor-VIII-Präparate | ||
ReFacto AF®
|
Moroctocog alfa |
April 1999 |
|
Helixate® NexGen
Kogenate®Advate®
Iblias®
Kovaltry®
|
Octocog alfa |
August 2000
August 2000
März 2004
Februar 2016
Februar 2016
|
NovoEight®
|
Turoctocog alfa |
November 2013 |
Nuwiq®Vihuma®
|
Simoctocog alfa |
Juli 2014
Februar 2017
|
Afstyla®
|
Lonoctocog alfa |
Januar 2017 |
Rekombinante Faktor-VIII-Präparate mit verlängerter Halbwertszeit | ||
Elocta®
|
Efmoroctocog alfa (rekombinanter humaner Gerinnungsfaktor VIII, Fc-Fusionsprotein) |
November 2015 |
Adynovi®
|
Rurioctocog alfa pegol (Octocog
alfa verknüpft mit Polyethylenglykol)
|
Januar 2018 |
Hämophilie A mit Inhibitoren | ||
NovoSeven®
|
Eptacog alfa (Rekombinanter Faktor VII) |
Februar 1996 |
FEIBA NF® (factor eight inhibitor bypassing activity)
|
aktivierter Prothrombinkomplex (mit Faktor VIII-Inhibitor-Bypassing-Aktivität angereicherte Humanplasmafraktion) |
Dezember 2005 |
Hemlibra®
|
Emicizumab (monoklonaler bispezifischer Antikörper) |
Februar 2018 |
Längere Wirkdauer
Die neueste Entwicklung sind rekombinante Gerinnungsfaktoren mit verlängerter Halbwertszeit. Eine längere Wirkdauer kann auf verschiedenen Wegen erreicht werden, beispielsweise durch kovalente Fusionierung mit einem Fc-Fragment von Immunglobulin G1, wie es bei dem seit 2016 erhältlichen Elocta® (Efmoroctocog alfa) der Fall ist. Ein weiterer Ansatz ist die kontrollierte PEGylierung des rekombinanten Faktor VIII Octocog alfa mit Polyethylenglykol (PEG). So auch bei dem neu zugelassenen Präparat Adynovi® (Rurioctocog alfa pegol), das im Vergleich zum konventionellen rekombinanten Faktor VIII eine 1,4- bis 1,5-fach längere Halbwertszeit aufweist. Da Patienten häufig eine prophylaktische Therapie anwenden und dann mehrmals wöchentlich intravenös injizieren müssen, besteht die Hoffnung, dass halbwertszeitverlängerte Produkte eine geringere Injektionsfrequenz ermöglichen. Lange werden die beiden bereits verfügbaren Produkte aber wohl nicht alleine bleiben. Weitere stehen in den Startlöchern: Damoctocog alfa pegol und Turoctocog alfa pegol wurden bereits in den USA und in Europa zur Zulassung eingereicht.
Wirkverlust durch Hemmkörper
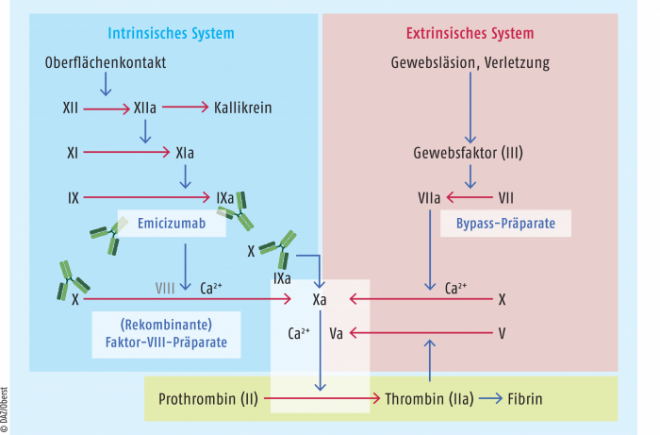
Ungefähr jeder dritte Patient mit einer schweren Hämophilie entwickelt Hemmkörper gegen exogen zugeführte Gerinnungsfaktoren. Diese neutralisierenden Antikörper, auch Inhibitoren genannt, vermindern die Wirksamkeit der Ersatztherapie dann oft so sehr, dass ein anderer Ansatz gewählt werden muss, um Blutungen zu vermeiden oder zu stoppen. Hier werden sogenannte Bypass-Präparate eingesetzt, die die Blutgerinnungskaskade über das extrinsische System aktivieren und das intrinsische System „umgehen“. Rekombinanter Faktor VII und aktivierter Prothrombinkomplex werden seit vielen Jahren eingesetzt.
Neuer Wirkansatz
Ein völlig neuer Wirkansatz zur Behandlung von Patienten mit Hämophilie A mit Inhibitoren steht nun mit Hemlibra® (Emicizumab) zur Verfügung: Der monoklonale bispezifische Antikörper aktiviert das intrinsische System, indem er gleichzeitig an Faktor IXa und Faktor X bindet (s. Abbildung). Als Antikörper kann der Wirkstoff subkutan injiziert werden – im Gegensatz zu den anderen Therapien, die intravenös appliziert werden müssen. Emicizumab ist zugelassen zur Routineprophylaxe von Blutungsereignissen bei Patienten mit Hämophilie A und Faktor-VIII-Hemmkörpern in allen Altersgruppen und wird einmal wöchentlich angewendet. Für Patienten könnte diese neue Therapie einen Vorteil bedeuten: Rekombinanter Faktor VII ist nicht zur Routineprophylaxe zugelassen, und aktivierter Prothrombinkomplex muss mehrmals wöchentlich injiziert werden. Wie bei den anderen Therapien sind allerdings auch unter Emicizumab thrombotische Ereignisse als unerwünschte Nebenwirkungen möglich. |
Quelle
National Heart, Lung and Blood Institute. What is hemophilia. https://www.nhlbi.nih.gov/health-topics/hemophilia, Abruf am 28. Februar 2018
Srivastava A et al. Guidelines for the management of hemophilia. Haemophilia 2013;19(1):e1-47
World Federation of Hemophilia. Report on the Annual Global Survey 2015. Oktober 2016. www1.wfh.org/publication/files/pdf-1669.pdf, Abruf am 28. Februar 2018
Balkaransingh P, Young G. Novel therapies and current clinical progress in hemophilia A. Ther Adv Hematol 2018;9(2):49-61
Launch Pressekonferenz Adynovi®. 22. Februar 2018
Fachinformation Adynovi® (Rurioctocog alfa pegol). Stand Dezember 2017
Fachinformation Hemlibra® (Emicizumab). Stand März 2018
Fachinformation NovoSeven® (Eptacog alfa). Stand Dezember 2016
Fachinformation FEIBA NF® (Aktivierter Prothrombinkomplex). Stand Dezember 2017





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.