
- DAZ.online
- DAZ / AZ
- DAZ 3/2017
- Kein Piperacillin
Hintergrund
Kein Piperacillin
Warum der Ausfall so schwer zu kompensieren ist
Im Dezember 2016 wurde gemeldet, dass sich in einer Produktionsstätte in China eine Explosion ereignet habe, in der die Rohstoffe für die Kombination aus Piperacillin und Tazobactam hergestellt werden. Seitdem findet nur noch eine rationierte Belieferung von Krankenhausapotheken mit diesem wesentlichen Antibiotikum gegen gramnegative Bakterien statt. Schaut man auf die Website der „American Society of Health System Pharmacists“ (ASHP) unter „Drug Shortages“, so findet man noch eine Reihe weiterer β-Lactamantibiotika, wie die Kombinationen aus Ampicillin und Sulbactam (was ebenfalls in Deutschland rationiert ist), Amoxicillin und Clavulansäure, Benzylpenicillin-Benzathin sowie einige Cephalosporine [2].
Biosynthese von Benzylpenicillin
Betrachtet man die Herstellung der Penicilline, lässt sich verstehen, warum nicht nur ein bestimmter Arzneistoff aus dieser Gruppe von der Verknappung betroffen ist. Penicilline sind komplexe Moleküle, die allein am β-Lactam-Grundgerüst drei Stereozentren besitzen (Abb. 1). Die aufwendige Totalsynthese liefert nur sehr geringe Ausbeuten von etwa 1,5 Prozent [3] und fällt somit für die Produktion aus wirtschaftlichen Gründen weg, da jährlich zehntausende Tonnen an Penicillinen benötigt werden. Deshalb erfolgt der Aufbau des Grundgerüstes vornehmlich fermentativ.
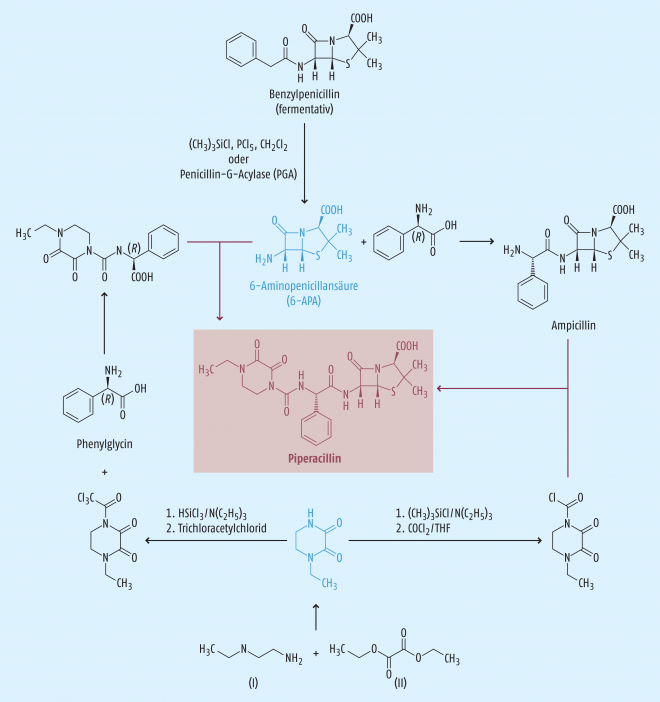
Schon in den 1950er-Jahren wurde Benzylpenicillin (Penicillin G) biotechnologisch mithilfe von Penicillium chrysogenum hergestellt; heute nutzt man dafür spezialisierte Hochleistungsstämme, die bis zu 40 Gramm Produkt pro Liter Kulturmedium in einem hochtechnisierten Prozess computergesteuert sezernieren [4]. Nur in Anbetracht der Tatsache, dass dies in Fermentern mit bis zu 200.000 Litern Volumen durchgeführt wird, können so enorme Mengen an Rohprodukt gewonnen werden. Benzylpenicillin wird anschließend in mehreren Schritten aus dem Kulturmedium extrahiert und isoliert.
Partialsynthese von Penicillinen
Sollen semisynthetische Penicilline wie z. B. Piperacillin hergestellt werden, beginnt an dieser Stelle die eigentliche Herausforderung. Um die 6-Aminopenicillansäure (6-APA) zu erhalten, die der Ausgangsstoff für fast alle Penicillin-Antibiotika ist [5], muss die Phenylessigsäure von der Aminogruppe in 6-Stellung abgespalten werden, ohne dass dabei der Hydrolyse-empfindliche β-Lactamring geöffnet wird. Diese Amidhydrolyse kann man entweder chemisch mit relativ giftigen Chemikalien wie Trimethylchlorsilan, Phosphorpentachlorid und Dichlormethan bei niedrigen Temperaturen [6] oder enzymatisch mit der Penicillin-G-Acylase (PGA) durchführen. Der letztere Weg wird heute zumeist beschritten, sodass jährlich über 10.000 Tonnen 6-APA hergestellt werden können. Diese Mengen sind vor allem durch die Verwendung von immobilisierter PGA aus rekombinanten Escherichia-coli- oder Fusarium-oxysporum-Stämmen in einer Wasser-Isobutylmethylketon-Mischung [7] möglich geworden. Die enzymatische Hydrolyse erfolgt mit 80- bis 90-prozentiger Ausbeute.
Piperacillin kann semisynthetisch sowohl direkt aus 6-APA als auch aus dem ebenfalls semisynthetischen Ampicillin hergestellt werden (Abb. 1). In beiden Fällen ist es zunächst notwendig, 4-Ethyl-2,3-dioxopiperazin aus N-Ethylethylendiamin und Oxalsäurediethylester aufzubauen und nach Aktivierung entweder direkt mit Ampicillin zu verknüpfen oder mit (R)-Phenylglycin und 6-APA zu Piperacillin umzusetzen [8]. Ampicillin wiederum ist durch die hydrolytische Spaltung von Benzylpenicillin und die anschließende Umsetzung mit (R)-Phenylglycin zugänglich.
Globale Verteilung der Hersteller
Da jährlich weltweit zehntausende Tonnen β-Lactamantibiotika verbraucht werden, liegt die Vermutung nahe, dass es nicht nur einen Hersteller hierfür gibt. Kürzlich stellten Dahl und Horn (BfArM) im Bulletin zur Arzneimittelsicherheit die Länder, die Deutschland mit Ampicillin/Sulbactam, Clindamycin und Piperacillin/Tazobactam beliefern, mit der jeweiligen Herstellerzahl zusammen (Tab. 1) [9]. Dabei steht China zwar an der Spitze, macht aber dennoch nur ein gutes Drittel der Produzenten aus. Leider wurden die jeweiligen Produktionsmengen nicht berichtet, allerdings scheint es, als ob die Herstellung von Piperacillin und Ampicillin auf mehreren Schultern lastet. Ob alle Hersteller die beiden Penicilline de novo produzieren oder ihre Synthese auf 6-APA aufbauen, bleibt unklar. Wenn Letzteres der Fall ist, könnte die Verknappung von Piperacillin/Tazobactam darauf zurückzuführen sein, dass eventuell keine ausreichenden Mengen von 6-APA in GMP-konformer Qualität zur Verfügung stehen.
Produktionsland |
Ampicillin/Sulbactam |
Clindamycin |
Piperacillin/Tazobactam |
Summe |
|---|---|---|---|---|
China |
2 |
9 |
7 |
18 |
Italien |
3 |
2 |
3 |
8 |
Spanien |
2 |
3 |
1 |
6 |
Indien |
1 |
– |
2 |
3 |
Irland |
1 |
– |
– |
1 |
Japan |
1 |
– |
2 |
3 |
Mexiko |
1 |
– |
– |
1 |
Niederlande |
1 |
– |
– |
1 |
Österreich |
1 |
– |
– |
1 |
Puerto Rico |
– |
2 |
– |
2 |
Südkorea |
– |
– |
3 |
3 |
Türkei |
3 |
– |
– |
3 |
USA |
1 |
1 |
– |
2 |
|
Summe
davon in EU
|
17
8
|
17
5
|
18
4
|
52
17
|
* Auswertung des Arzneimittel-Informationssystems der deutschen Zulassungsbehörden (AMIS, Stand: 27.4.2016). Die Liste ist unvollständig, da die Wirkstoffhersteller erst seit etwa zehn Jahren systematisch erfasst werden. | ||||
Sehr hohe Qualitätsanforderungen
Die Herstellung von Antibiotika ist durch strenge FDA- und ICH-Richtlinien geregelt [10 – 12]. Kürzlich ist zusätzlich eine Richtlinie zur Reinigungsvalidierung in Kraft getreten, die dafür sorgen soll, dass zukünftig alle β-Lactamantibiotika inklusive inaktiver Vorstufen nur in sogenannten „dedicated facilities“ hergestellt werden dürfen [13]. Damit einhergegangen ist die Regelung, in den internationalen Arzneibüchern (z. B. dem Europäischen Arzneibuch) die Grenzen für Verunreinigungen in Antibiotika enger zu fassen.
Diese sehr qualitätsorientierten Anforderungen werden dafür sorgen, dass es zukünftig für jedes Antibiotikum weltweit nur noch einzelne Produktionsanlagen gibt. Die augenblicklichen Lieferengpässe von Penicillinen sind als erstes Zeichen der Konzentrierung der Herstellung auf wenige bis eventuell nur einzelne Anlagen zu verstehen. Mit dieser Entwicklung wird es in Zukunft nahezu unmöglich werden, ausgefallene Anlagen – ob nun für 6-APA oder fertige Penicilline – zu ersetzen. Auf jeden Fall wird es immer eine lange Zeit dauern, bis man eine GMP-gerechte Produktion aufgebaut und etabliert hat. Das bei großen Chemikalienhändlern wie Sigma-Aldrich, Merck oder Alfa-Aesar gelagerte 6-APA beläuft sich auf wenige Kilogramm – viel zu wenig, um Europa ausreichend zu versorgen.
Probleme bei Alternativen
In den Krankenhausapotheken, die seit Monaten mit den Rationierungen oder Lieferausfällen befasst sind, stellt sich mit der Frage der geeigneten Alternativen auch die Frage der Arzneimitteltherapiesicherheit. Anstatt der derzeit knappen Kombinationen aus β-Lactamantibiotikum und β-Lactamase-Inhibitor wie Piperacillin/Tazobactam und Ampicillin/Sulbactam stellen z. B. bei Patienten mit mittelschweren bis schweren Pneumonien die Cephalosporine mögliche Alternativen dar, vor allem Cephalosporine der Gruppe 3a wie Ceftriaxon oder Cefotaxim. Es gibt aber seit mehr als 20 Jahren ernstzunehmende Hinweise, dass Ceftriaxon in hohem Maße das Auftreten von Clostridium difficile verursacht [14]. Ein Ausweichen auf Carbapeneme ist ebenso möglich; dies kann aber die ohnehin angespannte Resistenzsituation bei den Carbapenemase-bildenden Bakterienstämmen verschärfen. Carbapeneme sind – als Antibiotika mit sehr breitem Wirkspektrum – „verführerisch“ für die Therapie; zu selten wird aber nach einer Keimdetektion des Patienten auf Antibiotika mit engerem Wirkspektrum deeskaliert.
Das Thema „Antibiotic Stewardship“ (ABS) erlangt immer höhere Bedeutung in Krankenhäusern: So sollen ABS-Teams zügig alternative Therapieregime vorschlagen und deren Anwendung engmaschig begleiten. Dadurch gelingt es, gewohnte Antibiotika durch andere zu ersetzen, die in passenden Dosierungen gegen die vermuteten oder nachgewiesenen Keime wirksam sind.
Fazit
Angesichts der immer kleiner werdenden Zahl an Produktionsstätten für Antibiotika aufgrund regulatorischer Vorgaben einerseits und der immer schwierigeren Resistenzlage andererseits stellt sich die Frage, ob hier nicht die Regierungen eingreifen sollten. In den letzten Jahren wird zwar die Auffindung und Entwicklung neuer Antibiotika zunehmend staatlich gefördert, aber der Konzentration der Antibiotikaherstellung auf wenige Produktionsstätten – davon die meisten außerhalb von Europa – wird nichts entgegengesetzt. |
Literatur
[1] www.bfarm.de/DE/Arzneimittel/zul/amInformationen/Lieferengpaesse/_node.html
[2] www.ashp.org/menu/DrugShortages/CurrentShortages
[3] Sheehan JC, Henery-Logan KR. The Total Synthesis of Penicillin V. J Am Chem Soc 1959;81:3089-3094
[4] Elander RP. Industrial production of beta-lactam antibiotics. Appl Microbiol Biotechnol 2003;61:385-392
[5] Rolinson GN, Geddes AM. The 50th anniversary of the discovery of 6-aminopenicillanic acid (6-APA). Int J Antimicrob Agents 2007;29:3-8
[6] Brugging A, Roos EC, de Vroom E. Penicillin acylase in the industrial production of β-lactam antibiotics. Org Process Res Dev 1998;2:128-133
[7] Fang SG et al. Enhanced production of 6-aminopenicillanic acid in aqueous methyl isobutyl ketone system with immobilized penicillin G acylase. Prep Biochem Biotechnol 2010;40:38-45
[8] Kleemann A, Engel J. Pharmaceutical substances: syntheses, patents, applications, 3rd ed, Thieme, Stuttgart/New York 1999
[9] Dahl C, Horn M. Liefer- und Versorgungsengpässe bei Humanarzneimitteln – Eine Übersicht über die Aktivitäten des BfArM. Bull Arzneimittelsicherheit 2016;(4):22-29
[10] European Commission. EudraLex: The Rules Governing Medicinal Products in the European Union, Volume 4, EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use, Annex 15: Qualification and Validation, 2014
[11] U.S. Food and Drug Administration. Guidance for Industry, Non-Penicillin Beta-Lactam Drugs: A CGMP Framework for Preventing Cross-Contamination, 2013
[12] EudraLex (wie [10]), Part 1, Chapter 3: Premises and Equipment, 2014
[13] European Medicines Agency. Guideline on setting health based exposure limits for use in risk identification in the manufacture of different medicinal products in shared facilities (EMA/CHMP/CVMP/SWP/169430/2012), 2014
[14] Gerding DN et al. Clostridium difficile-associated diarrhea and colitis. Infect Control Hosp Epidemiol 1995;16:459-477


























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.