
- DAZ.online
- DAZ / AZ
- DAZ 3/2017
- Erster oraler Proteasom-...
Arzneimittel und Therapie
Erster oraler Proteasom-Inhibitor
Ixazomib erweitert das Behandlungsspektrum beim multiplen Myelom
Das multiple Myelom zählt zu den seltenen hämatologischen Neoplasien. Es ist jedoch die zweithäufigste Krebserkrankung der blutbildenden Organe. Nach den WHO-Kriterien gehört es zu den B-Zell-Lymphomen. Multiple Myelome entstehen im Knochenmark aus Plasmazellen, die als Teil des Immunsystems normalerweise Antikörper produzieren. Bei Myelom-Patienten entwickeln sich jedoch einige Vorläuferzellen zu malignen Zellen (Myelom-Zellen), die unkontrolliert funktionslose, monoklonale Antikörper bilden. Diese werden auch als Paraprotein oder monoklonales Protein („M-Protein“) bezeichnet und können im Serum und/oder Urin nachgewiesen werden. Bei der Verbreitung des multiplen Myeloms spielen Geschlecht, Alter und ethnische Zugehörigkeit eine Rolle. Männer erkranken häufiger als Frauen. Das mediane Alter bei Diagnose liegt derzeit zwischen 70 und 75 Jahren.
Unspezifische Symptome
Die Ursachen des multiplen Myeloms sind noch unbekannt. Als Risikofaktoren werden unter anderem belastende Expositionen im Lebens- und Arbeitsumfeld, zum Beispiel ionisierende Strahlung, diskutiert. In den Frühstadien der Erkrankung treten häufig keine oder unspezifische Symptome wie Rückenschmerzen auf. In fortgeschritten Stadien kommt es zu Knochenschmerzen oder -brüchen, starker Erschöpfung, Gewichtsverlust, erhöhter Anfälligkeit gegenüber Infektionen sowie gesteigertem oder auch vermindertem Wasserlassen. Durch die Verdrängung blutbildender Zellen im Knochenmark entstehen häufig Anämien. Derzeit ist das multiple Myelom eine unheilbare Erkrankung. Das Ziel der Behandlung besteht darin, sie in einen chronischen Zustand mit bestmöglicher Lebensqualität zu überführen. Ein multiples Myelom kann operativ, mit Bestrahlung, autologer Stammzelltransplantation und Arzneimitteln behandelt werden. Die Zahl der zur Verfügung stehenden medikamentösen Optionen hat sich in jüngster Zeit stark erhöht – allein seit Februar 2015 wurden von der EMA sechs neue Substanzen zugelassen (siehe Tab.).
Wirkstoff |
Handelsname |
Applikationsweg |
|---|---|---|
Proteasom-Inhibitoren | ||
Bortezomib |
Velcade®
|
i.v. |
Carfilzomib |
Kyprolis®
|
i.v. |
Ixazomib |
Ninlaro®
|
oral |
Immunmodulatoren | ||
Lenalidomid |
Revlimid®
|
oral |
Pomalidomid |
Imnovid®
|
oral |
Thalidomid |
Thalidomide® Celgene
|
oral |
monoklonale Antikörper | ||
Daratumumab |
Darzalex®
|
i.v. |
Elotuzumab |
Empliciti®
|
i.v. |
Histon-Deacetylase-Inhibitor | ||
Panobinostat |
Farydak®
|
oral |
Zytostatika | ||
Bendamustin |
Levact®, Generika
|
i.v. |
Cyclophosphamid |
Endoxan®
|
oral, i.v. |
Doxorubicin |
Caelyx®, Generika
|
i.v. |
Melphalan |
Alkeran®
|
oral, i.v. |
Vincristin |
Vincristinsulfat-Teva®
|
i.v. |
Corticosteroide | ||
Dexamethason |
Fortecortin®, Generika
|
oral, i.v. |
Prednison |
Decortin®, Generika
|
oral |
Das zugrunde liegende Prinzip
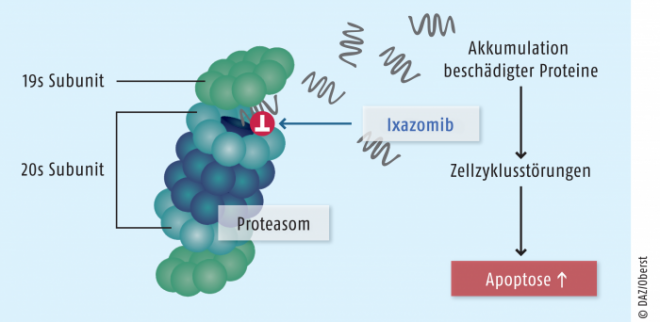
Ixazomib ist wie Bortezomib und Carfilzomib ein Proteasom-Inhibitor. Beim Proteasom handelt es sich um einen Enzymkomplex, der in Zellkern und -plasma für den Abbau nicht mehr benötigter Proteine verantwortlich ist. Wird der Komplex in seiner Funktion behindert, akkumulieren diese Proteine und lösen apoptotische Signale aus – die Zelle stirbt (siehe Abb.). Die Affinität von Proteasom-Inhibitoren zu schnell teilenden Zellen ist viel höher als zu gesunden Zellen, daher werden diese bevorzugt in den programmierten Zelltod überführt.
Bedingte Zulassung
Ixazomib wurde in einem breit angelegen Studienprogramm bisher bei mehr als 1800 Patienten angewendet. Die bedingte Zulassung beruht auf den Ergebnissen der multizentrischen, randomisierten, doppelblinden Studie Tourmaline-MM1, in die 722 Patienten mit rezidiviertem und/oder refraktärem multiplem Myelom eingeschlossen worden waren. Primärer Endpunkt war das progressionsfreie Überleben. Zu den wichtigsten sekundären Endpunkten zählten das Gesamtüberleben (overall survival, OS) sowie das OS bei Patienten mit einer bestimmten Mutation auf den Chromosomen 4, 7 und 14, die mit einer besonders schlechten Prognose der Krebserkrankung assoziiert sind (Hochrisiko-Mutationen). Die Studienteilnehmer erhielten innerhalb eines Behandlungszyklus von 28 Tagen an den Tagen 1, 8 und 15 eine Kapsel mit 4 mg Ixazomib (IRd-Gruppe, N = 360) oder Placebo (Placebo-Rd-Gruppe, N = 362). Als Kombinationstherapie nahmen alle Patienten der Studie an den Tagen 1 bis 21 Lenalidomid (25 mg bzw. 20 mg bei reduzierter Nierenfunktion) und an den Tagen 1, 8, 15 und 22 je 40 mg Dexamethason oral ein. Dieses Behandlungsschema wurde bis zur Krankheitsprogression oder nicht tolerablen Toxizität wiederholt. Das mediane progressionsfreie Überleben war in der IRd-Gruppe rund sechs Monate länger als in der Rd-Gruppe (20,6 vs. 14,7 Monate, p = 0,012). Dies entspricht einer Risikoreduktion für das Fortschreiten der Erkrankung bzw. Tod um 35%. Die Nebenwirkungsrate war in beiden Gruppen ähnlich. Zu den unerwünschten Wirkungen zählten unter anderem Diarrhö, Verstopfung, Übelkeit, Erbrechen, Hautausschlag, Fatigue, Rückenschmerzen, periphere Neuropathien und Ödeme. Als hämatologische Nebenwirkungen (alle Grade) traten Neutropenie, Thrombozytopenie und Anämie auf. Durch Dosismodifikationen und supportive Maßnahmen (z. B. die Gabe von Thrombozytenkonzentraten) ließen sich die meisten Nebenwirkungen kontrollieren. Die bedingte Zulassung von Ixazomib ist an die Auflage gebunden, dass der Hersteller Daten zur Sicherheit und Wirksamkeit aus dem laufenden Studienprogramm nachliefert, um die langfristigen Effekte der Therapie zu belegen.
Ixazomib (Ninlaro®) wird als Kapsel über drei Wochen an den Tagen 1, 8 und 15 eines vierwöchigen Behandlungszyklus eingenommen. Die Kapsel soll spätestens eine Stunde vor und frühestens zwei Stunden nach einer Mahlzeit eingenommen werden. Für Apotheken besteht die Möglichkeit des Direktbezugs beim Hersteller Takeda. Bestellungen, die montags bis donnerstags bis 17 Uhr und freitags bis 15 Uhr erfasst werden, werden im Regelfall bis 14 Uhr am folgenden Werktag ausgeliefert.
Vorteile und Ausblick
Da neben Ixazomib auch die Kombinationspartner Lenalidomid und Dexamethason oral verabreicht werden, steht für Erwachsene mit multiplem Myelom erstmals eine komplett orale Triplet-Therapie zur Verfügung. Nach Expertenansicht bietet dies den Patienten und ihren Betreuern mehr Freiraum gegenüber den Infusionstherapien. Die zahlreichen verfügbaren Therapieoptionen eröffnen die Möglichkeit, die Überlebensraten von Myelom-Patienten weiter zu erhöhen. Während die Fünf-Jahres-Überlebensrate zwischen 1990 und 1992 bei 29% lag, war sie zwischen 2006 und 2012 bereits auf 50% gestiegen. Derzeit befinden sich zwei weitere Proteasom-Inhibitoren, Oprozomib und Marizomib, in Phase III der klinischen Prüfung. |
Quelle
Kortüm M, et al. Multiples Myelom. Leitlinie der Deutschen Gesellschaft für Hämatologie und Medizinische Onkologie (DGHO). September 2013, www.onkopedia.com
Krebs in Deutschland 2011/2012. Publikation der Gesellschaft der epidemiologischen Krebsregister e.V. (GEKID) und des Zentrums für Krebsregisterdaten (ZfKD) im Robert Koch-Institut. 10. Ausg.
Moreau P, et al. Oral ixazomib, lenalidomide, and dexamethasone for Multiple Myeloma. N Engl J Med 2016;374:1621-1634






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.