
- DAZ.online
- DAZ / AZ
- DAZ 8/2016
- Die Oxidation im Griff
Rezeptur
Die Oxidation im Griff
So klappt es mit Dithranol in der Rezeptur
Von wertmindernden oxidativen Prozessen können zum Beispiel Wirk- und Hilfsstoffe mit Phenol-, Olefin-, Endiol-, Ether-, Hydroxymethylketon- oder Amin-Struktur betroffen sein [1 – 3]. Oxidationsprodukte, die infolge einer oxidativen Zersetzungsreaktion entstehen, zeigen meist keine oder nur eine verminderte pharmakologische Wirkung. Gleichzeitig treten häufig, bedingt durch die Oxidation und etwaige Folgereaktionen, Veränderungen in Farbe, Geruch oder Geschmack auf. Auch zu einer Veränderung der Löslichkeit kann es infolge oxidativer Abbaureaktionen kommen.
Mechanismus der Oxidation
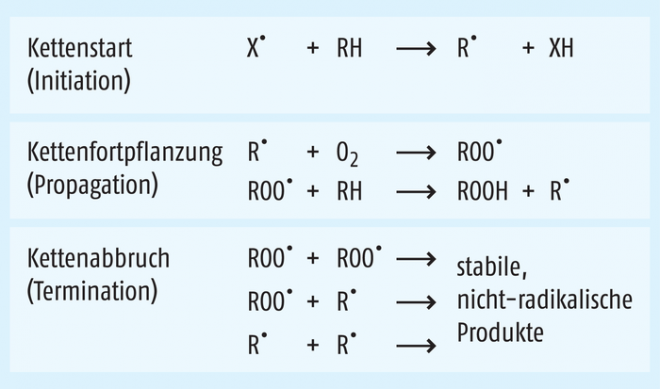
Die in pharmazeutischen Formulierungen beobachtete Oxidation von Wirkstoff- oder Hilfsstoffmolekülen läuft meist als Autoxidation ab. Von einer Autoxidation wird gesprochen, wenn molekularer Sauerstoff an der Reaktion beteiligt ist. Sie läuft dabei spontan und unter normalen Bedingungen sehr langsam ab [3]. Der Mechanismus der Autoxidation ist in der Regel eine mehrstufige und recht komplizierte Kettenreaktion unter dem Auftreten freier Radikale. Eine solche Kettenreaktion kann in drei Abschnitte unterteilt werden, den Kettenstart (Initiation), die Kettenfortpflanzung (Propagation) und den Kettenabbruch (Termination). In Abbildung 1 ist die im Folgenden ausführlich erklärte Kettenreaktion dargestellt.
In der Initiationsphase der Kettenreaktion kommt es durch die Einwirkung von Licht, Wärme oder die Präsenz von Spuren von Übergangsmetallen (z. B. Kupfer oder Eisen) zur Entstehung eines Startradikals. Dieses Startradikal abstrahiert dann von einem oxidationsempfindlichen Wirk- oder Hilfsstoffmolekül ein Wasserstoffatom unter Bildung eines Alkylradikals [4]. In dem sich anschließenden ersten Schritt der Kettenfortpflanzung verbindet sich das Wirk- bzw. Hilfsstoffradikal mit molekularem Sauerstoff zu einem Peroxidradikal. Dieses Peroxidradikal reagiert nun im zweiten Schritt der Kettenreaktion mit einem weiteren, noch nicht umgesetzten Wirk- oder Hilfsstoffmolekül, entfernt von diesem ein Wasserstoffatom und bildet somit ein Hydroperoxid. Gleichzeitig entsteht wieder ein neues Alkylradikal und der Prozess beginnt erneut. Die Kettenreaktion setzt sich so lange fort, bis im Rahmen des Kettenabbruchs alle freien Radikale durch Inhibitoren oder Nebenreaktionen zerstört sind. Peroxide und Hydroperoxide sind photosensitiv. Unter Lichteinfluss zerfallen sie in Hydroxylradikale (∙ OH) oder Alkoxylradikale (RO ∙), die selbst stark oxidierend wirken [4, 5].
Das bekannteste Beispiel für eine Autoxidation ist die oxidative Zersetzung von Ölen und Fetten, insbesondere solche mit einem hohen Anteil an ungesättigten Fettsäuren. Der intensive ranzige Geruch und Geschmack entsteht hierbei durch minimale Mengen Aldehyde, Ketone und Säuren geringer Kettenlänge, die aus dem Zerfall der Peroxide und Hydroperoxide entstehen. Entsprechend sind ranzig gewordene fetthaltige Arzneimittelformulierungen nicht auf mikrobiellen Verfall sondern auf oxidative Zersetzung zurückzuführen [2].
Nernst-Redoxpotenzial
Die Bereitschaft, mit der eine Oxidationsreaktion abläuft, kann quantitativ mithilfe der Nernst-Gleichung ausgedrückt werden. Da bei vielen Redoxreaktionen die Wasserstoffionenkonzentration beachtet werden muss, ergibt sich somit die folgende allgemeine Reaktionsgleichung:
[Red] ↔ [Ox] + m [H3O+] + n × e-
Entsprechend der obigen Reaktion hat die Nernst-Gleichung zur Berechnung des Redoxpotenzials einer Substanz die folgende Form:
Dabei steht E für das Redoxpotenzial, E0 für das konzentrationsunabhängige Normalpotenzial, R für die universelle Gaskonstante, T für die absolute Temperatur, n für die Anzahl der übertragenen Elektronen und F für die Faraday-Konstante. [Ox] und [Red] steht für die Aktivität oder näherungsweise auch Konzentration an oxidierter bzw. reduzierter Substanz und [H3O+] für die Wasserstoffionen-Konzentration. Hieraus wird deutlich, dass das Redoxpotenzial neben den Aktivitäten der Reaktanten und dem Normalpotenzial der Substanz auch direkt von der Temperatur und dem pH-Wert abhängt [3].
Einflussgrößen und Stabilisierungsmaßnahmen
pH-Wert und Oxidation
Auch bei Oxidationsreaktionen kommt dem pH-Wert eine wichtige Bedeutung zu. Ein hoher pH-Wert, das heißt eine niedrige Konzentration an H3O+-Ionen, führt gemäß Gleichung 1 zu einem niedrigen Redoxpotenzial. Je niedriger das Redoxpotenzial einer Substanz ist, desto schneller und vollständiger läuft die entsprechende Oxidationsreaktion ab [2]. Es ist also vorteilhaft, sofern möglich, einen niedrigen pH-Wert einzustellen, um die oxidative Zersetzung zu minimieren. Hierbei sind aber unbedingt auch die physiologische Verträglichkeit und die Gegebenheiten am Applikationsort zu beachten.
Der Faktor Sauerstoff
Da Autoxidationsreaktionen gemäß Abbildung 1 an die Präsenz von Sauerstoff gebunden sind, besteht ein wirksamer Schutz der Zubereitung im möglichst vollständigen Luftausschluss. Bei wässrigen Arzneiformen kann dies effektiv durch Destillation des verwendeten Wassers mit anschließender Inertbegasung unter Verwendung von Stickstoff (N2) oder Kohlendioxid (CO2) erfolgen. Die Inertgase verdrängen den Luftsauerstoff aus dem Wasser und minimieren somit den Gehalt des in Wasser gelösten Sauerstoff. CO2 hat hierbei die bessere Löslichkeit im Vergleich zu N2 und kann somit den Sauerstoff schneller verdrängen. Allerdings führt die Verwendung von CO2 in wässriger Lösung zur Bildung von Kohlensäure, die sauer reagiert und den pH-Wert senkt. Die Verwendung ist deshalb auch von der pH-Stabilität des zu formulierenden Wirkstoffes abhängig. In Salben und Cremes kann die Stabilität autoxidationsempfindlicher Wirk- und Hilfsstoffe durch eine Verminderung der Luftatmosphäre verbessert werden. Hierzu gehört das Abpacken in dicht verschlossene Gefäße, idealerweise mit einer möglichst kleinen Expositionsfläche der Formulierung zum Luftüberstand.
Licht und Schwermetallionen
Neben dem Schutz vor Luftsauerstoff kommt dem Schutz der Zubereitung vor Licht bei oxidationsempfindlichen Wirk- und Hilfsstoffen eine große Bedeutung zu. Da Licht kurzer Wellenlänge als Initiator bei radikalisch verlaufenden Oxidationsreaktionen dienen kann, sollten für die Lagerung lichtundurchlässige Behältnisse verwendet werden. Auch Schwermetallionen wie Kupfer oder Eisen, die leicht durch Arbeitsgeräte, Behältnisse aber auch Hilfsstoffe in die Rezeptur eingeschleppt werden, können bereits in Spuren oxidative Reaktionen katalysieren und somit die Zersetzung von Wirkstoffen beschleunigen. Die effektivste Inaktivierung erfolgt durch Zusatz von Komplexbildnern. Hier bieten sich für pharmazeutische Formulierungen vor allem Wein- oder Zitronensäure, 8-Hydroxychinolin oder auch das Natrium-Salz der Ethylendiamintetraessigsäure (Natriumedetat) an. Letzteres wird in Konzentrationen zwischen 0,005% bis 0,1% eingesetzt. Der ADI-Wert (Acceptable Daily Intake) des Dinatrium-Salzes von EDTA liegt gemäß WHO bei 2,5 mg/kg Körpergewicht [6].
Antioxidanzien
Neben den obigen Maßnahmen zur Verbesserung der Stabilität bietet der Zusatz von Antioxidanzien eine weitere effektive Möglichkeit, um Oxidationsvorgänge zu hemmen. Nach ihrem Wirkungsmechanismus werden Antioxidanzien prinzipiell in zwei Gruppen eingeteilt, in die Reduktionsmittel und in die Radikalfänger. Antioxidanzien der Kategorie Reduktionsmittel haben ein sehr niedrigeres Redoxpotenzial und werden eher oxidiert als der zu schützende Wirk- oder Hilfsstoff. Bekanntestes Beispiel dieser Kategorie ist die Ascorbinsäure. Antioxidanzien der Kategorie Radikalfänger bilden hingegen reaktionsträge stabile Radikale und führen so zum Abbruch der Reaktionskaskade. Bekanntestes Beispiel für diese Gruppe ist α-Tocopherol. Tabelle 1 zeigt eine Übersicht von Antioxidanzien und ihrer typischen Konzentrationsbereiche. Bei der Auswahl des geeigneten Antioxidans ist natürlich besonders auf die Art der Zubereitung zu achten, das heißt, ob es es sich um eine hydrophile oder eine lipophile Zubereitung handelt.
Antioxidanzien für hydrophile Systeme |
pharmazeutisch eingesetzte Konzentrationen |
|---|---|
Ascorbinsäure |
0,01 bis 0,1% |
Natriumsulfit |
0,01 bis 0,1% |
Natriumpyrosulfite |
0,01 bis 0,1% |
Cystein |
0,05 bis 0,15% |
Glutathion |
0,05 bis 0,15% |
Antioxidanzien für lipophile Systeme |
|
α-Tocopherol |
0,001 bis 0,05% |
Butylhydroxyanisol |
0,002 bis 0,02% |
Butylhydroxytoluol |
0,01 bis 0,05% |
Palmitoylascorbinsäure-Ester |
0,01 bis 0,05% |
Gallussäure-Ester (z. B. Propylgallat) |
0,05 bis 0,1% |
Dithranol in der Individualrezeptur
Ein Musterbeispiel für einen oxidationsempfindlichen Arzneistoff, der immer wieder in Individualrezepturen in der Apotheke vorkommt, ist Dithranol. Dithranol wird in Deutschland auch als Cignolin und im Angloamerikanischen als Anthralin bezeichnet. Es wird therapeutisch in Konzentrationen von 0,05 bis 3,0% bei der Behandlung als Antipsoriatikum eingesetzt. Hierbei werden in der Regel bei Erstversorgung zu Therapiebeginn Zubereitungen mit maximal 0,1% und im weiteren Behandlungsverlauf mit maximal 3,0% verwendet [7].
Chemische und physikalische Eigenschaften
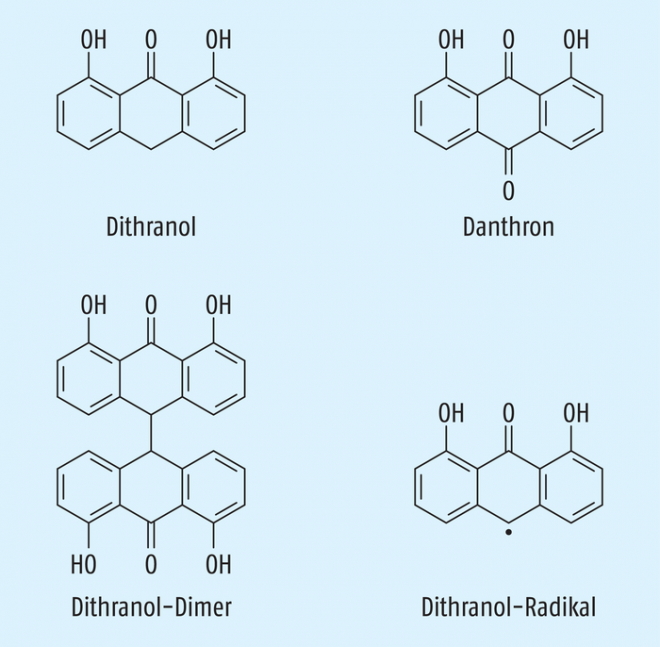
Chemisch handelt es sich bei Dithranol um 1,8-Dihydroxyanthracen-9(10H)-on mit der Summenformel C14H10O3 und der in Abbildung 2 dargestellten Strukturformel [9]. Die Substanz ist erhältlich als gelbes bis bräunliches, feinkristallines Pulver mit einem Schmelzpunkt von 178 bis 182 °C. Dithranol ist ausgesprochen lipophil, was durch die intramolekularen Wasserstoffbrückenbindungen bedingt ist. Es ist daher praktisch unlöslich in Wasser und nur schwer löslich in Ethanol (96%). Der Verteilungskoeffizient in n-Octanol/Wasser (log P-Wert) beträgt 4,23. Auch in Paraffinkohlenwasserstoffen wie Vaselin zeigt Dithranol praktisch keine Löslichkeit, löst sich aber in fetten Ölen und Octyldecanol [10].
Abb. 2: Chemische Struktur von Dithranol, Danthron, Dithranol-Dimer und dem 1,8-Dihydroxy-9-anthron-10-yl-Radikal.
Stabilität von Dithranol
Frisch synthetisiertes und gereinigtes Dithranol ist schwach gelb gefärbt. Orangene bis bräunliche Verfärbungen sind meist durch die oxidativ gebildeten Abbauprodukte Danthron oder Dithranolbraun bedingt, die selbst keine antipsoriatische Wirkung mehr haben [10]. Im Alkalischen kommt es über die Zwischenstufe des Dithranol-Anions durch Cycloaddition mit Singulett-Sauerstoff schnell zur Bildung des Danthron. Lichteinwirkung begünstigt diese Reaktion [11]. Bei der Autoxidation von Dithranol entsteht als Primärprodukt durch Abstraktion eines Wasserstoffatoms das 1,8-Dihydroxy-9-anthron-10-yl-Radikal. Durch Kombination zweier Radikale bildet sich anschließend das Dithranol-Dimer. Die Strukturen der durch Oxidation entstehenden Abbauprodukte sind in Abbildung 2 dargestellt.
Typische Inkompatibilitäten in der Rezeptur
Aufgrund der ausgeprägten Oxidationsempfindlichkeit des Dithranol ist die Kombination mit Oxidationsmitteln zu vermeiden. Selbst die Kombination mit Iod, das mit einem Normalpotenzial von E0 = + 0,536 V nur ein schwaches Oxidationsmittel darstellt, gilt als Inkompatibilität. Gemäß den obigen Ausführungen ist Dithranol lediglich bei pH-Werten ≤ 7 ausreichend stabil, lipophil und wirksam. Vorsicht ist deshalb bei basisch reagierenden Stoffen geboten. Auch die Kombination von Dithranol mit Zinkoxid in wässrigen Systemen gilt als Inkompatibilität. Aber hierzu später noch mehr.
Aufgrund der phenolischen Struktur kann es bei Dithranol zur Wechselwirkung mit den Ethylenoxid-Einheiten von Macrogol-haltigen Strukturen kommen. Hier sind vor allem die Interaktionen mit Emulgatoren, die einen Polyethylenglykol-Anteil besitzen, hervorzuheben. Die Wechselwirkungen können die Wirkung der Emulgatoren stark beeinträchtigen und zu einem Brechen der Emulsionszubereitungen führen. Aber noch eine weitere Problematik ist bei der Kombination mit Polyethylenglykolen nicht zu vernachlässigen. Da es sich bei Polyethylenglykol chemisch um einen Polyether handelt, können durch Lagerung bei höherer Temperatur, durch Lichteinfluss und metallische Verunreinigung Peroxide entstehen, die dann ihrerseits wieder den oxidativen Abbau von Dithranol beschleunigen können [13].
Standardisierte Rezepturen
Nach den obigen Ausführungen ist es nun fast selbstverständlich, dass Individualrezepturen mit Dithranol vor der Herstellung im Rahmen des Plausibilitätschecks genau hinsichtlich möglicher Inkompatibilitäten mit anderen Formulierungsbestandteilen und Instabilitäten des Wirkstoffes betrachtet werden müssen. Wenn möglich sind standardisierte Rezepturen vorzuziehen. Doch bei genauer Betrachtung führen selbst die Standardrezepturen erst einmal zu etwas Verwirrung. So finden sich im NRF Rezepturen mit der Kombination von Dithranol und Zinkoxid oder die Verwendung von Macrogolen als Grundlage wieder. Wie ist das denn überhaupt möglich?
Kombination mit Zinkoxid
In der NRF-Monographie 11.56 ist die weiche Dithranol-Zinkpaste zur Anwendung bei Psoriasis vulgaris aufgeführt. Formulierungsbestandteile der Rezeptur sind natürlich der Wirkstoff Dithranol in Konzentrationen von 0,05 bis 2%, Salicylsäure-Verreibung und weiche Zinkpaste DAB. Die weiche Zinkpaste DAB ist ihrerseits aus Zinkoxid, dickflüssigem Paraffin, gebleichtem Wachs und weißem Vaselin zusammengesetzt [14]. Der Schlüssel zu einer stabilen Zubereitung liegt in der Wahl der oben aufgeführten Rezeptur-Hilfsstoffe. Erstens werden Dithranol und Zinkoxid in einer Wasser-freien Zubereitung verarbeitet und zweitens wird der Rezeptur Salicylsäure als Stabilisator zugesetzt. Deshalb sollte man sich nicht wundern, wenn die Konzentration der eingearbeiteten Salicylsäure weit unterhalb der therapeutischen Konzentration liegt. Experimentelle Daten konnten zeigen, dass Dithranol in Salicylsäure-stabilisierten, Wasser-freien Vaselin-Zubereitungen bei Lagerung im Kühlschrank und auch bei Raumtemperatur ausreichend stabil ist, selbst bei einer Kombination mit Zinkoxid [15].
Aber woher kommt die Inkompatibilität von Dithranol und Zinkoxid in Wasser-haltigen Zubereitungen? Hierzu gibt es in der Literatur verschiedene Hypothesen. So wurde diskutiert, dass Dithranol zusammen mit Zinkoxid inaktive Komplexe bildet, deren Entstehung durch den Zusatz von Salicylsäure teilweise aufgrund der pH-Verschiebung zum Sauren und teilweise durch die Entstehung von Zinksalicylat zurückgedrängt wird [16]. Andere Untersuchungen kamen zur Auffassung, dass die Bildung des Zink-Dithranol-Komplexes nur eine untergeordnete Rolle spielt. Weitaus relevanter scheint die Alkalisierung von Wasser-haltigen Medien durch die Bildung von Zinkhydroxid zu sein, die die Oxidation von Dithranol stark begünstigt. Der Zusatz von Salicylsäure verhindert die pH-Verschiebung und damit den raschen oxidativen Abbau des Dithranols [17, 18].
Verarbeitung in der Macrogol-Salbe DAC
Neben dem oben diskutierten Effekt auf den pH-Wert in Wasser-haltigen Grundlagen spielt der antioxidative Effekt der Salicylsäure eine bedeutende Rolle. Salicylsäure kann als phenolische Carbonsäure mit OH-Radikalen zu Hydroxy-Derivaten reagieren, wodurch die ausgeprägte antioxidative Wirkung zustande kommt [19]. Hierdurch wird Dithranol nicht nur vor Autoxidation geschützt, sondern auch vor oxidativ wirkenden Verunreinigungen, die zum Beispiel in Dermatika-Grundlagen vorkommen können. Gerade in den Polyethylenglykolen, wie sie in der Macrogol-Salbe DAC verwendet werden, können durch Einwirkung von Luft, Licht und metallischen Verunreinigungen Peroxide entstehen. Diese Peroxide beschleunigen ihrerseits wiederum die oxidative Zersetzung von Dithranol. Um diesem Problem vorzubeugen wird deshalb die Dithranol-Macrogol-Salbe NRF standardmäßig mit 3% Salicylsäure stabilisiert. Die Salicylsäure fungiert in diesem Zusammenhang nicht als Wirkstoff. Da laut NRF-Monographie die Salicylsäure in der Macrogol-Salbe vollständig gelöst vorliegt, ist für den stabilisierenden Effekt eine 3%-ige Salicylsäure-Konzentration einzusetzen [20]. Generell ist zu beachten, dass die Dithranol-Macrogol-Salben mit 0,25% und 0,5% Wirkstoffanteil instabiler sind als die höherdosierten Varianten mit hauptsächlich suspendiertem Wirkstoff. Eine Braunfärbung der Salben ist deshalb immer ein deutliches Zeichen für einen Gehaltsverlust.
Allgemeine Hinweise bei der Verarbeitung von Dithranol
Zusammenfassend lässt sich sagen, dass Dithranol sicher keine einfach zu verarbeitende Substanz in der Individualrezeptur ist. Die Herstellung stabiler Rezepturen ist aber durch Einhalten einiger wichtiger Arbeitshinweise möglich. Im Folgenden sind deshalb nochmals die wichtigsten Punkte aufgeführt:
- keine Kombination mit Steinkohlenteer oder Steinkohlenteer-haltigen Lösungen
- keine Kombination mit Zinkoxid in wässrigen Formulierungen
- Wärmeanwendung bei Einarbeitung des Dithranols vermeiden
- pro-oxidative Rezepturbestandteile vermeiden
- antioxidative Stabilisierung durch Zusatz von Salicylsäure
- Abfüllung in lichtundurchlässigen dicht verschließbaren Aluminium-Tuben |
Literatur
[1] Barnes AR. Product stability and stability testing. In „Aulton’s Pharmaceutics. The Design and Manufacture of Medicines.“ 3rd edition 2007, Editor: Aulton ME. Churchill Livingstone, London
[2] Fahr A, Voigt R. Pharmazeutische Technologie für Studium und Beruf. 12. Auflage 2015, Deutscher Apotheker Verlag, Stuttgart, S. 539–559
[3] Martin AN. Physikalische Pharmazie: pharmazeutisch angewandte physikalisch-chemische Grundlagen. Hrsg. Hans Leuenberger. 4. Auflage 2002. Wissenschaftliche Verlagsgesellschaft Stuttgart, S. 295–353
[4] Simic MG. Free radical mechanisms in autoxidation processes. Journal of Chemical Education 1981;58(2);125-131
[5] Florence AT and Attwood D. Physical Principles of Pharmacy. 4th edition 2006. Pharmaceutical Press, London: 91–138
[6] Rowe RC, Shesky PJ, Quinn ME. Handbook of Pharmaceutical Excipients. 6th edition 2009. Pharmaceutical Press, London
[7] Ziegler A. Plausibilitäts-Check Rezeptur. 2. Auflage. Deutscher Apotheker Verlag, Stuttgart, 2013
[8] Schmidt PC, Lang S. Pharmazeutische Hilfsstoffe. Govi-Verlag Pharmazeutischer Verlag, Eschborn, 2013:1-15
[9] European Pharmacopeia 8.0. Dithranol 2014;1007:3108-3110
[10] Bracher F et al. Dithranol (4.08/1007). Kommentar zum Ph.Eur 4.08, 19. Wissenschaftliche Verlagsgesellschaft Stuttgart
[11] Müller K, Wiegrebe W, Younes M. Dithranol, Active Oxygen Species and Lipid Peroxidation in vivo. Arch Pharm 1987;320:59-66
[12] Davies AW, Hawari JAA, Whitefield M. Generation and E.S.R. Spectrum of the 1,8-Dihydroxy-9-Anthron-10-yl Radical. Tetrahedron Letters 1983;24(41):4465-4468
[13] Bracher F et al. Macrogole (4.05/1444). Kommentar zum Ph.Eur. 4.05, 20. Wissenschaftliche Verlagsgesellschaft Stuttgart
[14] Weiche Dithranol-Zinkpaste 0,05% bis 2% (NRF 11.56.) Neues Rezeptur Formularium (NRF). Stand NRF 2010 (CD-Fassung Stand 02/2013)
[15] Braun C, Wiegrebe W. Notiz zur Haltbarkeit von Dithranol-Salben. Pharm Ztg 1988;133(10):691-692
[16] Lukacs S, Braun-Falco O. Über das Verhalten von Dithranol (Cignolin®) in Pasten und Lösungen und seine Beeinflussbarkeit durch Salicylsäure. Hautarzt 1973;24:304-309
[17] Raab W, Gmeiner B. The inhibition of glucose-6-phosphate dehydrogenase activity by dithranol (Anthralin), zinc ions and/or salicylic acid. Archiv für dermatologische Forschung 1974;254(2):87-94
[18] Raab W, Gmeiner B. Influence of Ultraviolet Light, Various Temperatures, and Zinc Ions on Anthralin (Dithranol). Dermatologica 1975;150;267-276
[19] Ebermann R, Elmadfa I. Lehrbuch der Lebensmittelchemie und Ernährung. 2. Auflage 2011, Springer Verlag, Wien, S. 620
[20] Macrogolsalbe 0,25% bis 3% (NRF 11.53.). Neues Rezeptur Formularium (NRF). Stand NRF 2010 (CD-Fassung Stand 02/2013)


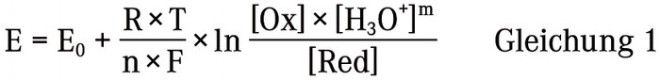





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.