
- DAZ.online
- DAZ / AZ
- DAZ 1/2016
- Gebärmutterhalskrebs ...
Arzneimittel und Therapie
Gebärmutterhalskrebs durch therapeutische Impfung heilbar?
Neuer HPV-Impfstoff gegen Präkanzerosen
Durch Einführung wirksamer Früherkennungsmaßnahmen (zytologische Untersuchung des Schleimhautabstrichs vom Gebärmutterhals) und das rechtzeitige Erkennen und operative Entfernen von Vor- und Frühstadien hat die Diagnose fortgeschrittener Stadien von Gebärmutterhalskrebs (invasives Zervix-Karzinom) sowie die Zahl der Todesfälle in den letzten 30 Jahren deutlich abgenommen. Nach den aktuellsten Schätzungen des Robert Koch-Instituts erkranken in Deutschland pro Jahr dennoch knapp 4700 Frauen neu an Gebärmutterhalskrebs (Zahlen aus dem Jahr 2011). Ursache ist fast immer eine persistierende Infektion mit humanen Papillomaviren (HPV). Bei humanen Papillomaviren handelt es sich um eine Familie unbehüllter, doppelsträngiger DNA-Viren, die nach ihrem onkogenen Potenzial in Niedrigrisiko-Typen, die Genitalwarzen (Condylomata acuminata) verursachen können, und Hochrisiko-Typen, die Krebs auslösen können, eingeteilt werden. HPV 16 ist der dominierende onkogene HPV-Typ, der in 50% aller Zervixkarzinome nachgewiesen werden kann, gefolgt von HPV 18, der in ca. 20% aller Zervixkarzinome nachweisbar ist.
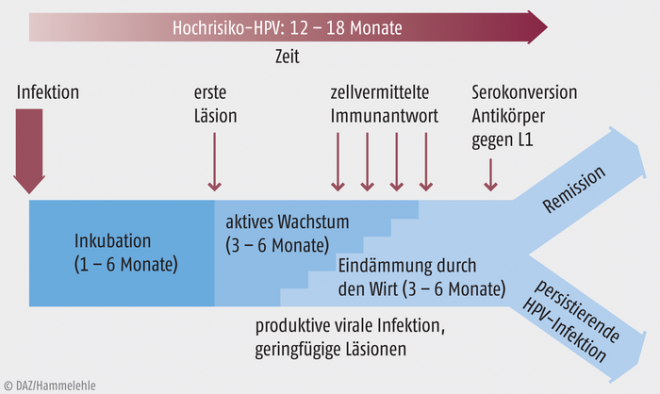
Man schätzt, dass 70 bis 80% der sexuell aktiven Männer und Frauen im Laufe ihres Lebens mit einem Vertreter der HPV-Familie in Berührung kommen. Dabei ist die Prävalenz von HPV-Infektionen, die mittels DNA-Nachweis in Abstrichuntersuchungen festgestellt werden, unter jungen Frauen am höchsten. Die meisten dieser Infektionen (70 bis 90%) verlaufen symptomlos und werden, ohne dass es zu einer Erkrankung kommt, im Laufe von ein bis zwei Jahren überwunden (Abb. 1). Lediglich bei etwa 10 bis 15% der infizierten Frauen entwickelt sich eine persistierende HPV-Infektion, bei der die HPV-DNA nicht mehr episomal im Zytoplasma der infizierten Zelle vorliegt, sondern in das Wirtsgenom eingebaut wird. Persistierende Infektionen können sich – in Abhängigkeit vom HPV-Typ – zu höhergradigen Dysplasien und Neoplasien entwickeln.
Natürlicher Verlauf genitaler Human-Papillomavirus-Infektionen [nach Stanley M, 2006]. L1: virales Hauptkapsidprotein, das im menschlichen Körper die Bildung von Antikörpern induziert
Je nach Schweregrad der zervikalen intraepithelialen Neoplasien (CIN) werden drei Grade unterschieden: CIN I (geringgradig), CIN II (mäßiggradig) und CIN III (hochgradig sowie Karzinoma in situ). Bei CIN I und II Läsionen kann abgewartet und kontrolliert werden, da sich diese Läsionen in über 90% der Fälle spontan zurückbilden. Im Stadium CIN III wird üblicherweise operiert (Konisation), da hier die Wahrscheinlichkeit, dass sich ein invasives Karzinom entwickelt, deutlich erhöht ist und die Prognose nicht vorhersagbar ist. Das mittlere Alter der Frauen, die von einer CIN-III-Zellveränderung betroffen sind, liegt nach Daten des Robert Koch-Instituts bei gerade einmal 34 Jahre. Damit sind die betroffenen Frauen häufig in einem Alter, in dem die Familienplanung noch nicht abgeschlossen ist. Die chirurgische Entfernung des betroffenen Gewebes im Bereich der Transformationszone des Gebärmutterhalses kann in manchen Fällen bei nachfolgenden Schwangerschaften das Risiko für eine Frühgeburt erhöhen.
Um der Entwicklung dieser Krebsvorstufen vorzubeugen, empfiehlt die Ständige Impfkommission (STIKO) seit März 2007 eine HPV-Impfung für Mädchen im Alter zwischen zwölf und 17 Jahren. Seit 2014 ist das empfohlene Impfalter auf neun Jahre herabgesetzt. Die aus drei Einzeldosen bestehende Grundimmunisierung sollte vor dem ersten Geschlechtsverkehr und damit vor einer Infektion mit HPV abgeschlossen sein. Die zugelassenen Impfstoffe Gardasil® (tetravalent) und Cervarix® (bivalent) enthalten als antigene Strukturen die Hauptkapsidproteine L1 der häufigsten onkogenen HPV-Typen. Damit können sie vor einer Infektion mit den häufigsten Hochrisiko-HPV-Typen schützen, sind aber bei bereits bestehender Infektion wirkungslos. Ob auch bereits mit HPV infizierte Frauen von einer Stimulation der körpereigenen Immunantwort profitieren können, wurde nun in einer Proof-of-principle-Studie untersucht.
Proof-of-principle: Präkanzerosen durch Impfung heilen
Grundsätzlich scheint dies möglich, wie jetzt das als vorläufig zu wertende Ergebnis einer Phase-II-Studie zeigt. An dieser doppelblinden, randomisierten, Placebo-kontrollierten Studie nahmen 169 Frauen, die durch HPV 16 oder 18 verursachte Krebsvorstufen entwickelt hatten, teil. Das durchschnittliche Alter der Frauen war 30 Jahre, die Mehrheit hatte CIN-III-Läsionen. Von diesen erhielten 127 drei Dosen des neuartigen Impfstoffs VGX-3100, 42 Teilnehmerinnen wurden nur zum Schein geimpft. Der neue Impfstoff enthält zwei DNA-Plasmide, die gegen die von infizierten Zellen gebildeten Onkoproteine E6 und E7 der HPV-Typen 16 und 18 gerichtet sind. Die Impfung erfolgt mit einem Spezialgerät zur intramuskulären Elektroporation. Es erzeugt nach der Injektion vorübergehend ein elektrisches Feld, das die Aufnahme der Plasmide in die Immunzellen erleichtern soll. Das Immunsystem startet dann eine Abwehrreaktion, die zur Bildung von zytotoxischen T-Zellen führt. Neun Monate nach der ersten Dosis war bei knapp der Hälfte der Geimpften die Neoplasie abgeheilt im Vergleich zu einer Spontanremissionsrate von 30% in der Placebogruppe. Dieser Unterschied war statistisch signifikant. Der Impfstoff war gut verträglich, die häufigsten unerwünschten Wirkungen waren Reaktionen an der Injektionsstelle. Im Vergleich dazu ermöglicht allerdings eine chirurgische Entfernung Heilungsraten von über 90% und auch ohne Impfung heilten die Läsionen bei gut einem Drittel der Frauen ab. Das bedeutet, dass auch geimpfte Frauen sorgfältig und engmaschig überwacht werden müssen und dass wohl nicht allen geimpften Frauen eine chirurgische Entfernung erspart werden kann. Nun gilt es abzuwarten, ob die induzierte Immunantwort die Infektion dauerhaft beseitigt und wie der Impfstoff in der vom Hersteller Inovio Pharmaceuticals geplanten Phase-III-Studie abschneidet.
Erste Hinweise für die Effizienz der HPV-Impfung
Die langfristigen Effekte der HPV-Impfung werden erst in einigen Jahrzehnten abschätzbar sein. Um erste Hinweise auf die kurzfristigen Effekte der Impfempfehlung zu erhalten, untersuchten Wissenschaftler vom Robert Koch-Institut 2014 die HPV-Prävalenz bei jungen Frauen im Alter von 20 bis 24 Jahren.
In einer Querschnittsstudie werteten sie Daten von 787 Teilnehmerinnen zu Impfstatus, HPV-Prävalenz, Genotyp-Verteilung und Risikofaktoren für eine HPV-Infektion aus.
65% der Frauen waren nicht gegen HPV geimpft. Von diesen waren 22,5% mit HP-Viren der Hochrisikogruppen 16 und 18 infiziert, im Gegensatz zu 13,9% der geimpften Frauen. Bei der Auswertung nach Altersgruppen ergab sich, dass die Prävalenz von HPV-Typ 16 und 18 bei den jüngeren geimpften Teilnehmerinnen (20 und 21 Jahre) am niedrigsten war. In dieser Altersgruppe hatten 40% die Impfung vor dem ersten sexuellen Kontakt erhalten. Als Risikofaktoren für eine HPV-Infektion wurden die Anzahl der sexuellen Partner und ein niedriger Bildungsstand identifiziert.
Die Ergebnisse bestätigen, dass Mädchen vor dem ersten Sexualkontakt gegen HPV geimpft werden sollten, und legen nahe, dass die seit 2007 geltende Impfempfehlung erste positive Effekte zeigt.
Deleré Y et al. Human Papillomavirus prevalence and probable first effects of vaccination in 20 to 25 year-old women in Germany: a population-based cross-sectional study via home-based self-sampling. BMC Infect Dis 2014;14:87
Ausblick: Weitere denkbare Anwendungsgebiete
Humane Papillomaviren werden auch mit Karzinomen der Vulva, Vagina, des Penis, des Anus und des Mundrachenraums in Verbindung gebracht. Deren Vorstufen sind chirurgisch schwieriger zu behandeln als die des Gebärmutterhalses. Nach den Ergebnissen dieser Proof-of-principle-Studie scheint es vielversprechend, Immuntherapien gegen die für diese Tumoren ursächlichen HPV-Typen zu entwickeln.
Zur Früherkennung von Gebärmutterhalskrebs kommen zunehmend auch HPV-Tests zum Einsatz. Während ein negatives Testergebnis beruhigend ist, ist das weitere Vorgehen bei einem positiven Testergebnis weitgehend unklar. Ist der Test nach einer gewissen Wartezeit immer noch positiv, kann von einer persistierenden Infektion ausgegangen werden. In diesen Fällen könnte eine therapeutische Impfung eine gute Behandlungsoption darstellen. |
Quelle
Robert Koch-Institut. Zentrum für Krebsregisterdaten: http://www.krebsdaten.de
Schiffman M, Wentzensen N. Towards therapeutic vaccination against cervical precancer? Lancet 2015;386:2036-2038
Stanley M. Immune responses to human papillomavirus. Vaccine 2006;30:S16-S22
Trimble CL et al. Safety, efficacy, and immunogenicity of VGX-3100, a therapeutic synthetic DNA vaccine targeting human papillomavirus 16 and 18 E6 and E7 proteins for cervical intraepithelial neoplasia 2/3: a randomised, double-blind, placebo-controlled phase 2b trial. Lancet 2015;386:2078-88





















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.