
- DAZ.online
- DAZ / AZ
- DAZ 34/2015
- Resistente ...
Antibiotika-Resistenz
Resistente Reisemitbringsel
Gefährliche Infektionen durch Antibiotika-resistente Bakterien

Cook it, peel it or forget it!
Wer kennt nicht diesen Spruch? Man sollte beim Essen bestimmte Vorkehrungen treffen, schließlich will man sich in der Fremde keine Reisediarrhö einfangen. Wahlweise unter „Montezumas Rache“ oder auch „Pharaos Rache“ bekannt, deuten die Umschreibungen bereits die Regionen an, in denen man im Verlauf einer Reise bevorzugt mit einer Diarrhö rechnen muss. Zwar ist die Inzidenz mittlerweile etwas zurückgegangen: Während sie vor ca. 20 Jahren noch bei bis zu 65% lag, ist sie inzwischen auf 10 bis 40% gesunken. Will man jedoch auf alle Fälle vermeiden, selbst die Rache des Montezumas zu spüren, sollte man einen weiten Bogen um Länder in Asien, in Afrika, im Mittleren Osten, in Zentral- und Südamerika sowie um Mexiko machen.
Verursacher der Durchfallerkrankung sind überwiegend Bakterien und hier vor allem enterotoxische und enteroaggregative Escherichia-coli-Stämme, daneben aber auch Viren und Parasiten (siehe Tab. 1). Kommt man in den zweifelhaften Genuss von Montezumas Rache, passiert das üblicherweise in der ersten Ferienwoche. In der zweiten oder gar dritten Woche ist die Gefahr bereits erheblich geringer. Meist dauert ein unbehandelter Durchfall vier bis fünf Tage und nur 3 bis 17% der Betroffenen leiden tatsächlich unter lang andauernden Problemen, die sie noch bis nach Hause begleiten.
Der gut gemeinte Rat, nur gekochte oder zumindest geschälte Ware zu essen, hilft nur bedingt. Natürlich ist es nicht ganz ungefährlich, Essen bei Straßenständen zu kaufen. Aber es gibt auch immer wieder Berichte, dass in Fünf-Sterne-Hotels gehäuft Durchfallerkrankungen aufgetreten sind – bevorzugt nach Gesellschaftsabenden, bei denen Buffets angerichtet waren. Denn dort werden Speisen über längere Zeit warm gehalten, und auf den angewärmten Nahrungsmitteln können sich eventuell vorhandene Bakterien wunderbar vermehren. Demgegenüber ist frisch und heiß gekochtes Essen aus der Küche einer einheimischen Familie, direkt serviert, sogar vergleichsweise ungefährlich.
Mehr Sicherheit vor bakteriellen Infektionen in Hochrisiko-Ländern bieten Kreuzfahrten mit nur kurzen Landgängen. Dafür besteht auf dem Schiff die realistische Gefahr einer Norovirus-Infektion, die dann auch nur sehr schlecht in den Griff zu bekommen ist.
Das veränderte Mikrobiom
Es ist schon verwunderlich, dass Menschen, die in den jeweiligen Ländern zu Hause sind, dort ganz munter und ohne Durchfall leben können, während unsereins – kaum im Land angekommen – fast nicht mehr von der Toilette wegkommt. Etwas Licht in das Geschehen bringt die Betrachtung des Mikrobioms in unserem Darm.
Jeder Mensch lebt in einer Wohngemeinschaft mit ungefähr 100 Billionen Bakterien in seinem Darm – das sind mehr Zellen, als der eigene Körper aufweist! Welche Art Bakterien sich in unserem Darm verlustiert, hängt von vielen Faktoren ab, unter anderem natürlich vom Kulturkreis und der üblichen Ernährung. Unser „industrialisierter“ Körper unterscheidet sich somit in seinem Mikrobiom – der Gemeinschaft unserer bakteriellen Mitbewohner – dramatisch von den Körpern in Afrika, Indien oder Mexiko, in deren Därmen sich etliche andere Bakterien tummeln. Setzen wir uns im Urlaub diesen fremden Mikroorganismen aus – und das eben nicht nur über ungeschälte Früchte und unsauberes Trinkwasser, sondern auch über Toiletten, Wasserhähne, Türgriffe, Geldscheine, länger warm gehaltene Mahlzeiten etc. – kann es zu einer Invasion mit fremden Bakterien und nachfolgend zu Irritationen und Diarrhö kommen. Sobald wir nach den Ferien in die gewohnten Umgebung mit der üblichen Ernährung zurückkommen, stabilisiert sich das Ganze meist schnell, und unser normales Mikrobiom übernimmt wieder die Vorherrschaft in unserem Darm.
Organismus |
beschriebene Pathogene [%] |
|||
|---|---|---|---|---|
Lateinamerika und Karibik |
Afrika |
Südasien |
Südostasien |
|
|
enterotoxische E. coli
|
≥ 35 |
25 – 35 |
15 – 25 |
5 – 15 |
|
enteroaggregative E. coli
|
25 – 35 |
< 5 |
15 – 25 |
keine Daten verfügbar |
Campylobacter |
< 5 |
< 5 |
15 – 25 |
25 – 35 |
Salmonella |
< 5 |
5 – 15 |
< 5 |
5 – 15 |
Shigella |
5 – 15 |
5 – 15 |
5 – 15 |
< 5 |
Norovirus |
15 – 25 |
15 – 25 |
5 – 15 |
< 5 |
Rotavirus |
15 – 25 |
5 – 15 |
5 – 15 |
< 5 |
Giardia |
< 5 |
< 5 |
5 – 15 |
5 – 15 |
Das weltweite Problem: Antibiotika-Resistenz
In den meisten Fällen normalisiert sich also die Situation für den Einzelnen. Allerdings trifft das nicht unbedingt auch für die Gesellschaft zu. Denn nicht jedes intestinale Problem, mit dem man auf einer Reise konfrontiert wird, wird noch vor Ort gelöst. Und da unter den am Urlaubsort eingesammelten, örtlich vorkommenden Bakterien auch vermehrt solche sind, die Antibiotika-Resistenzen tragen, treten auch diese als blinde Passagiere immer öfter die Reise zurück in die Heimat an. Und dort können sie unter Umständen zu einer großen Gefahr werden.
Erst im Januar ging die Nachricht durch die Presse, dass vermutlich über einen Patienten aus dem Mittelmeerraum ein multiresistenter Acinetobacter-baumannii-Stamm in das Universitätsklinikum in Kiel gelangt war. 31 Patienten mussten daraufhin strikt isoliert werden, und bei drei Todesfällen wurde ein kausaler Zusammenhang mit der Infektion vermutet. Der mutmaßliche Überträger des multiresistenten Bakteriums war zuvor in der Türkei in einem Krankenhaus behandelt worden und hatte sich wahrscheinlich dort den Mikroorganismus eingefangen. Bekanntermaßen findet sich gerade Acinetobacter baumannii in einer multiresistenten Variante in zahlreichen Krankenhäusern des Mittleren Ostens. Als Tourist sollte man sich an seinem Ferienort also nur dann stationär behandeln lassen, wenn dies unbedingt notwendig ist.
Wie häufig es vorkommt, dass Reisende ungewollt Antibiotika-resistente Bakterien aus dem Urlaub mitbringen, beschreiben zwei relativ aktuelle Veröffentlichungen.
Die finnische Studie
In einer finnischen Studie wurden Proben von 430 Reisenden ausgewertet, die zwischen März 2009 und Februar 2010 in sieben verschiedenen Regionen unterwegs waren. Getestet wurde auf Extended-Spectrum Betalactamase-produzierende Enterobacteriaceae (ESBL-PE) und auf Carbapenemase-produzierende Enterobacteriaceae (CPE) als zwei wesentliche Gruppen von Problemkeimen. Von den 430 Reisenden hatte sich niemand mit einem CPE-Keim infiziert, aber 90 Personen (21%) brachten ESBL-PE-Keime mit nach Hause. Bei sieben dieser Patienten wurden sogar zwei unterschiedliche Stämme identifiziert. Bei immerhin fünf der Teilnehmer (1%) wurde bereits vor Reiseantritt eine entsprechende Kontamination im Stuhl nachgewiesen. Die meisten Reisenden hatten sich in Südasien infiziert, gefolgt von Südostasien, Ostasien und Nordafrika inklusive dem Mittleren Osten (siehe Abb. 1). Insgesamt 288 der Studienteilnehmer (67%) berichteten über eine überstandene Reisediarrhö; aus dieser Gruppe hatten später 75 ESBL-PE-Keime im Stuhl. Bei 15 Reisenden, die ebenfalls positiv auf die Bakterien getestet wurden, war hingegen kein Durchfall aufgetreten. 52 der insgesamt 288 Personen, die unter Reisediarrhö litten, nahmen gezielt Antibiotika gegen diese Beschwerden ein. Bei 24 Antibiotika-Anwendern wurden später ESBL-PE-Keime im Stuhl nachgewiesen. Bei einer Nachuntersuchung, die ein Jahr später durchgeführt wurde, konnten in keiner Stuhlprobe der ursprünglich infizierten Reisenden mehr ESBL-PE-Keime nachgewiesen werden.
Als Ergebnis der umfangreichen Untersuchung halten die Autoren fest, dass zunächst natürlich das Reiseziel ein wichtiger Risikofaktor für eine Ansiedelung resistenter Keime ist. Außerdem erhöhen eine Reisediarrhö und vor allem eine dagegen eingesetzte Antibiotika-Therapie das Risiko. Ältere Reisende wurden nur dann im Vergleich zu Jüngeren bevorzugt von den Bakterien besiedelt, wenn sie keinen Durchfall erlitten hatten. Ob das allerdings statistisch signifikant und aussagekräftig ist, muss kritisch hinterfragt werden. Interessanterweise konnten die Autoren keinen schützenden Einfluss von eingenommenen Probiotika feststellen, und es bedeutete auch kein erhöhtes Risiko, wenn die Reisenden zusammen mit Einheimischen gegessen hatten.
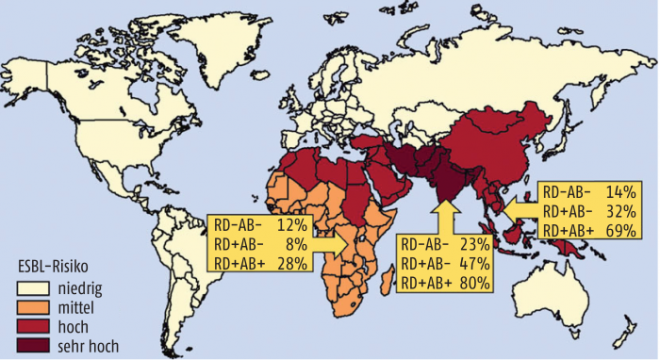
Abb. 1: Weltkarte des Risikos einer Infektion mit ESBL-PE (Extended-Spectrum Betalactamase-produzierender Enterobacteriaceae), wie es sich in der finnischen Studie abgezeichnet hat. In der gesamten Studienpopulation brachten 21% der Reisenden ESBL-PE-Keime mit nach Hause; 11% in der Untergruppe RD-AB- (Reisedurchfall/antimikrobielle Wirkstoffe), 21% mit RD+AB-, und 37% mit RD+AB+. Die jeweiligen Subgruppenanalysen für die Regionen mit dem höchsten Risiko (Afrika, Südasien und Südostasien) werden gesondert angegeben. (Modifiziert nach Kantele et al.)
Die deutsche Studie
Eine ähnliche Untersuchung wurde 2013 in Leipzig an 205 Probanden durchgeführt. Hier waren sogar 14 Teilnehmer (7%) vor Reiseantritt positiv auf ESBL-produzierende Escherichia coli getestet worden. Nach der Rückkehr hatten sich 58 Reisende (30%) neu mit diesen E.-coli-Varianten infiziert. Fünf davon wurden zusätzlich positiv auf ESBL-produzierende Klebsiella pneumoniae getestet, und vier trugen ESBL-negative Salmonella-Stämme. Eine Testung der Stuhlproben ergab keine Bakterien, die Carbapenemase produzieren. Das höchste Risiko, sich ESBL-PE-Keime einzufangen, trugen Reisende mit den Zielen Indien und Südostasien. Außerdem litten 30 der 58 positiv Getesteten während ihres Urlaubs unter einer Gastroenteritis, während bei den 147 Nicht-Infizierten 43 Fälle aufgetreten waren. Insgesamt 24 Probanden hatten während der Reise Antibiotika eingenommen, allerdings nur vier davon, um ihre Gastroenteritis mit Ciprofloxacin zu behandeln. Alle anderen hatten zur Malaria-Prophylaxe oder zur Behandlung von Atemwegserkrankungen Doxycyclin oder andere Wirkstoffe eingenommen. Erschreckend war jedoch, dass drei der mit Ciprofloxacin behandelten Probanden E.-coli-Stämme aufgenommen hatten, die resistent gegenüber Fluorchinolonen waren. Nur bei 35 der insgesamt 58 positiv getesteten Reisenden war eine Nachuntersuchung nach sechs Monaten möglich. Hier wiesen noch drei Teilnehmer eine Besiedlung mit ESBL-produzierenden E.-coli-Zellen auf. In dieser Studie wurde kein signifikanter Zusammenhang zwischen einer Verabreichung von Antibiotika und der Besiedelung durch resistente Keime hergestellt. Allerdings konnte gezeigt werden, dass für Vegetarier und Teilnehmer von geführten Touren, die mehr Essen auf Märkten konsumiert hatten, das Risiko für eine Infektion höher war. Und offensichtlich hatten Vorsichtsmaßnahmen wie sorgfältige Händehygiene und der ausschließliche Konsum abgepackter Getränkeeinheiten keinen Einfluss auf den Befall mit resistenten Bakterien.
Fazit
Bei der Verbindung zwischen Reise und Bakterien denkt man eigentlich immer an die Reisediarrhö. Es ist nicht nur unangenehm, während des Urlaubs unter Durchfall zu leiden, sondern fördert zudem eine Besiedelung mit Antibiotika-resistenten Bakterien. Inwieweit eine Antibiotika-Gabe eine derartige Besiedelung noch zusätzlich unterstützt, lässt sich aus den beiden kürzlich veröffentlichten Studien nicht eindeutig ableiten. In beiden Studien waren zwar sehr viele Teilnehmer eingeschlossen. Runtergebrochen auf einzelne Subgruppen bleiben dennoch nur wenige Einzelfälle übrig, deren Signifikanz sich kaum statistisch belegen lässt.
Jedoch ist es erschreckend, wie viele Reisende sich in den Ferien resistente Keime einfangen. Zwar sind diese Bakterien bei den meisten Betroffenen nach sechs bzw. zwölf Monaten meist wieder komplett verschwunden. Dennoch wurden sie zunächst in eine neue Umgebung eingebracht. Erschreckend ist zudem, dass bei der deutschen Studie deutlich mehr Personen Antibiotika-resistente Keime trugen. Während bei den Finnen initial nur 1% der Teilnehmer und nach der Reise 21% positiv auf ESBL-PE-Keime getestet waren, lagen die Anteile in Leipzig mit 7% und 30% deutlich höher. Inwieweit das damit zusammenhängt, dass die Studie in Leipzig drei Jahre später durchgeführt wurde als die finnische Studie, oder ob eventuell lokale Gegebenheiten für diese Unterschiede verantwortlich sind, lässt Platz für Spekulationen.
Bislang herrschte die weit verbreitete Meinung, dass Antibiotika-resistente Bakterien ohne einen entsprechenden Selektionsdruck keine Überlebensvorteile haben und deshalb von Antibiotika-sensitiven Wildtyp-Bakterien überwachsen werden. Inzwischen mehren sich aber die Hinweise, dass einige Bakterienstämme, die Resistenzen erworben haben, auch in Gesellschaft mit Wildtyp-Bakterien gut überleben können. Entsprechende Versuche wurden mit den Problemkeimen Pseudomonas aeruginosa, Acinetobacter baumannii und Vibrio cholerae am Tiermodell durchgeführt, und die Bakterien vermehrten sich prächtig, selbst in Anwesenheit von Wildtyp-Bakterien und ohne Selektionsdruck. Ähnliche Beobachtungen wurden bereits mit Chinolon-resistenten Escherichia-coli- und Salmonella-typhi-Stämmen gemacht. Tatsächlich funktioniert es also nicht so einfach, Antibiotika-resistente Bakterien wieder loszuwerden. Sehr viel besser wäre es, die Resistenzen nicht weiter zu verbreiten. Die WHO empfiehlt hier folgende Vorgehensweise:
- Jeder sollte die Hände sorgfältig waschen und vor allem den Kontakt zu Kranken meiden, um die Übertragung bakterieller und viraler Infektionen zu verhindern. Bei Sexualkontakt sollten Kondome verwendet werden, um die sexuell übertragbaren Krankheiten zu vermeiden.
- Jeder sollte sich impfen lassen und die Impfungen rechtzeitig auffrischen.
- Antimikrobielle Wirkstoffe sollten nur dann angewendet werden, wenn sie unbedingt nötig sind und dann auch nur nach Verschreibung durch einen Arzt.
- Der empfohlene Behandlungszyklus mit antimikrobiellen Wirkstoffen sollte auf jeden Fall eingehalten werden, selbst wenn die Therapie lebenslang erfolgen muss und man sich eigentlich gesund fühlt.
- Antimikrobielle Wirkstoffe sollten nicht zwischen Patienten geteilt und auch keine alten, verschriebenen Medikamente aufgebraucht werden.
Für Heilberufler gibt die WHO folgende Empfehlung:
- Infektionsprävention und -kontrolle in Krankenhäusern sollte verbessert werden.
- Antimikrobielle Wirkstoffe sollen nur dann verschrieben und abgegeben werden, wenn sie unbedingt nötig sind.
- Für die zu behandelnde Krankheit sollen die richtigen antimikrobiellen Wirkstoffe verschrieben und abgegeben werden.
Sicher ist, dass Antibiotika-resistente Keime ein weltweit relevantes Thema sind. Immerhin hatte die Bundeskanzlerin einen entsprechenden Tagesordnungspunkt für das G7-Gipfeltreffen in Elmau auf die Agenda gesetzt. Seitdem ist es aber leider wieder sehr ruhig geworden um den zu hohen Antibiotika-Verbrauch und um die Gefahr Antibiotika-resistenter Bakterien. Es wird Zeit, dass hier weltweit entsprechende Maßnahmen ergriffen werden. |
Literatur
Steffen R, Hill DR, DuPont HL. Traveler‘s diarrhea: a clinical review. JAMA 2015;313:71–80
Kantele A et al. Antimicrobials increase travelers‘ risk of colonization by extended-spectrum betalactamase-producing Enterobacteriaceae. Clin. Infect. Dis. 2015;60:837–846
Lübbert C et al. Colonization with extended-spectrum beta-lactamase-producing and carbapenemase-producing Enterobacteriaceae in international travelers returning to Germany. Int. J. Med. Microbiol. 2015;305:148–156
Roux D et al. Fitness cost of antibiotic susceptibility during bacterial infection. Sci. Transl. Med. 2015;7:297ra114
de Lastours V et al. Quinolone-resistant Escherichia coli from the faecal microbiota of healthy volunteers after ciprofloxacin exposure are highly adapted to a commensal lifestyle. J Antimicrob Chemother. 2014;69:761–768
Baker S et al. Fitness benefits in fluoroquinolone-resistant Salmonella Typhi in the absence of antimicrobial pressure. Elife 2013, doi: 10.7554/eLife.01229
Autoren
Prof. Dr. Theo Dingermann ist Seniorprofessor am Institut für Pharmazeutische Biologie an der Goethe-Universität Frankfurt.
Dr. Ilse Zündorf ist dort als akademische Oberrätin tätig.
Institut für Pharmazeutische Biologie
Biozentrum
Max-von-Laue-Straße 9
60438 Frankfurt/Main






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.