
- DAZ.online
- DAZ / AZ
- DAZ 14/2015
- Unterschiede in Gehalt ...
UniDAZ
Unterschiede in Gehalt und Zusammensetzung der Flavonoide in Moringa-Arten
Siegerbeitrag im Wettbewerb um den UniDAZ-Wissenschaftspreis 2015
Editorial
Liebe Leserinnen, liebe Leser!
Der Siegerbeitrag im Wettbewerb um den diesjährigen UniDAZ-Wissenschaftspreis ging aus einer Diplomarbeit mit dem Titel „Comparative Study of Flavonoids in Moringa stenopetala and Moringa oleifera“ hervor, die im Rahmen eines vom Deutschen Akademischen Austauschdienst (DAAD) geförderten Projekts angefertigt wurde.
Ruth Ilchmann verfasste diese Diplomarbeit an der Addis Abeba University in Äthiopien und am Institut für Pharmazeutische Technologie und Biopharmazie der Martin-Luther-Universität Halle-Wittenberg unter der Leitung von Prof. Dr. Reinhard Neubert. Dabei beschäftigte sie sich mit den Flavonoiden in zwei Moringa-Arten, die in Ostafrika und Indien angebaut werden. Die Flavonoide sind das wesentliche Qualitätsmerkmal der als gesundes Nahrungsmittel geschätzten Blätter.
Der UniDAZ-Wissenschaftspreis wurde auf der Interpharm in Hamburg verliehen (siehe DAZ 2015, Nr. 11, S. 55).
Viel Spaß beim Lesen!
Ihre UniDAZ-Redaktion
Von der Gattung Moringa, der einzigen in der Familie Moringaceae (Ordnung Kreuzblütlerartige, Brassicales), sind bislang zehn bis 14 Arten bekannt [1, 2]. Es sind Sträucher oder bis zehn Meter hohe Bäume mit heller Rinde, fragilen Ästen, gefiederten Blätter und Kapselfrüchten (Schoten) [2]. Während M. stenopetala aus Äthiopien und dem nördlichen Kenia stammt, ist M. oleifera in der Himalayaregion beheimatet. Mittlerweile werden Moringa-Pflanzen aber beinahe in allen tropischen Gebieten angebaut. Am Horn von Afrika ist die natürliche Artenvielfalt besonders groß: In Äthiopien beispielsweise gibt es fünf verschiedene Arten [3].
Vielfältige Verwendung
Bekannt wurde M. oleifera unter den Namen „Meerrettichbaum“ und „Baum des Lebens“. Die Blätter werden als Nahrungsmittel verwendet und enthalten wichtige Mineralstoffe und Vitamine. Mit gepulverten Samen kann verschmutztes Wasser zu Trinkwasser aufbereitet werden [4, 5]. Die in den Samen enthaltenen Proteine koagulieren durch ihre Oberflächenladung mit Schwebeteilchen und Bakterien, die dann abfiltriert werden können [6]. Zudem wirken die Samen bakterizid [7]. Moringa-Spezies sind an raue Bedingungen gewöhnt. Sie benötigen nur wenig Wasser und werden daher auch zur Aufforstung der sudanesischen Sahelzone genutzt [8]. In einigen afrikanischen Ländern werden in der Trockenzeit die Blätter und unreifen Schoten aufgrund ihres hohen Nährwertes als Tierfutter verwendet [9, 10, 11].
ist in Äthiopien unter dem amharischen Namen „Shifara“ bekannt und wird vor allem im Süden des Landes, in der Region Konso und um Arba Minch herum, angebaut [12]. Die Blätter, Schoten und Samen sind etwas größer als bei M. oleifera [13]. Im Mausmodell führt die Gabe von M. stenopetala-Extrakt zur signifikanten Senkung des Serumglucose- sowie des Serumcholesterolspiegels [14]. In-vitro-Untersuchungen zeigen außerdem antifungale Aktivität [15]. Inwieweit diese Wirkungen auf die Flavonoide zurückzuführen sind, ist derzeit noch unklar.
Flavonoide als Radikalfänger
Flavonoide gehören zu den Sekundärstoffen vieler höherer Pflanzen [16]. Der Name leitet sich vom Lateinischen (flavus = gelb) ab, da sie zuerst in gelben Blüten identifiziert wurden. Heute sind mehrere Tausend verschiedene Verbindungen dieser Stoffklasse bekannt. In Zellen liegen sie meist als Glykoside vor, die die Wasserlöslichkeit der lipophilen Strukturen gewährleisten.
Flavonoide erfüllen verschiedene Funktionen in pflanzlichen Zellen: Sie stellen die wichtigste Gruppe der Blütenfarbstoffe dar und locken somit Bestäuber an; einige Flavonoide dienen als Fraßschutz, andere schützen vor der UV-Strahlung.
Als Radikalfänger sorgen Flavonoide vor allem für einen ausgeglichenen Oxidationsstatus. In vitro wurden antivirale, antiallergene und antiproliferative sowie antikarzinogene Eigenschaften nachgewiesen [13]. Da viele Erkrankungen mit oxidativem Stress verbunden sind – unter anderem tritt dieser vermehrt bei neurodegenerativen Erkrankungen, Krebs, Arteriosklerose und Diabetes auf –, spielen Antioxidanzien in der Prävention eine immer größere Rolle [17, 18].
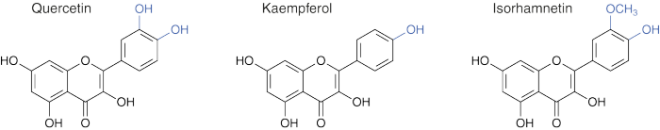
Die Flavonoide Quercetin und Kaempferol wurden in verschiedenen Moringa-Arten nachgewiesen [19, 20]. In der vorliegenden Arbeit erfolgte nicht nur die Bestimmung dieser beiden Flavonoide in Proben von M. stenopetala und M. oleifera, sondern auch von Iso-rhamnetin, dessen Vorkommen durch massenspektroskopische Messungen evident war. Das Untersuchungsmaterial von Moringa stenopetala stammte aus Äthiopien, das von Moringa oleifera – der wohl bekanntesten Moringa-Spezies – aus Indien und Ruanda.
Analytische Methoden
Die Quantifizierung erfolgte mittels HPLC-UV (Hochleistungsflüssigchromatografie, Detektion durch UV-Absorption), die Identität der detektierten Flavonoide wurde mit nachgeschalteter massenspektroskopischer Analyse (HPLC-MS) zusätzlich bestätigt.
Vorversuche, Messmethode und Validierung
Weil die Flavonoide an verschiedene Zucker geknüpft sind, entstehen zahlreiche unterschiedliche Strukturen. Um die Analytik zu vereinfachen, werden häufig die Aglyka der Flavonoide anstelle ihrer Glykoside untersucht [22]. Gespalten werden die glykosidischen Bindungen durch Hydrolyse.
Vor den Messungen wurden verschiedene Vorversuche durchgeführt, um die optimalen Bedingungen für Extraktion und Hydrolyse der Flavonoide herauszufinden und die Korrektheit der Messergebnisse sicherzustellen.
Ausgehend von Untersuchungen durch Hertog et al. wurden 50%iger Methanol zur Extraktion und Salzsäure zur Hydrolyse verwendet [23]. Die Autoren postulieren eine Abhängigkeit des Flavonoidgehaltes von der Reaktionszeit und der verwendeten Salzsäurekonzentration für verschiedene Probenmatrices. Um die besten Hydrolysebedingungen für das vorliegende Pflanzenmaterial zu finden, wurden drei verschiedene Säurekonzentrationen und drei Reaktionszeiten getestet. Optimale Reaktionsbedingungen für beide Arten zeigten sich bei einer zweistündigen Hydrolyse mit 1,6-molarer Salzsäure. Extraktion und Hydrolyse fanden im Messkolben bei 90 °C für zwei Stunden statt. Anschließend wurden die Proben gefiltert, mit Methanol auf 50 ml aufgefüllt und erneut durch einen Filter mit 0,45 µm Porenweite gegeben. Direkt im Anschluss wurden die Proben mittels HPLC-UV quantifiziert.
Zur Validierung der Messmethode mussten die LoD (Limit of Detection) und LoQ (Limit of Quantification) sowie Präzision und Richtigkeit bestimmt werden. Dabei zeigte sich, dass innerhalb eines Laufs, bei dem drei Proben eines Pflanzenmaterials vermessen wurden, reproduzierbare Ergebnisse mit erforderlicher Richtigkeit und Präzision vorlagen, die Werte an verschiedenen Tagen jedoch stark voneinander abwichen. Aus diesem Grund wurde vor jedem Lauf eine Kalibrierung durchgeführt.
Flavonoidgehalte
M. stenopetala: Die M. stenopetala-Proben wurden an vier verschiedenen Orten in Äthiophien gesammelt. Das Material aus Adama und Awassa – beide Gebiete gehören zu den mittleren Höhenlagen des Rift Valley – weist eine ähnliche Zusammensetzung der Flavonoide auf. Die Proben, die weiter südlich in Arba Minch und in Konso gesammelt wurden, weichen davon ab: Die Probe aus Konso enthält zusätzlich eine quantifizierbare Menge Iso-rhamnetin, während in der Probe aus Arba Minch nur Quercetin quantifiziert werden konnte.
Obwohl alle Proben von derselben Art stammen, unterscheiden sie sich in ihrem absoluten Gehalt deutlich (s. Tab. 1). Die Annahme, dass die Höhenlage der Anbaugebiete einen Einfluss auf den absoluten Gehalt hat, kann aufgrund der geringen Probenanzahl jedoch nicht belegt werden.
| Sammelort in Äthiopien | Quercetin[mg/100 g DM] | Kaempferol[mg/100 g DM] | Isorhamnetin[mg/100 g DM] |
|---|---|---|---|
| Adama | 943 ± 25 | 57 ± 0,3 | < LoQ |
| Arba Minch | 306 ± 10 | < LoQ | < LoQ |
| Konso | 2204 ± 98 | 48 ± 0,2 | 68 ± 2 |
| Awassa | 1189 ± 20 | 65 ± 1,7 | < LoQ |
Ein Vergleich mit der Literatur bestätigt, dass die Messergebnisse der Proben aus Indien und Ruanda im Bereich der veröffentlichten Werte liegen (s. Tab. 2). Grundsätzlich variiert der Quercetingehalt in M. oleifera-Proben stark [20]. In dieser Arbeit konnte in beiden Proben erstmalig Isorhamnetin quantifiziert werden.
| Herkunftsland | Quercetin[mg/100 g DM] | Kaempferol[mg/100 g DM] | Isorhamnetin[mg/100 g DM] |
|---|---|---|---|
| Nicaragua [20] | 2545 ± 90 | 647 ± 26 | – |
| Indien [20] | 957 ± 48 | 476 ± 6 | – |
| Niger [20] | 657 ± 76 | 154 ± 14 | – |
| Indien* | 889 ± 31 | 157 ± 2 | 253 ± 2 |
| Ruanda* | 2162 ± 42 | 554 ± 11 | 245 ± 5 |
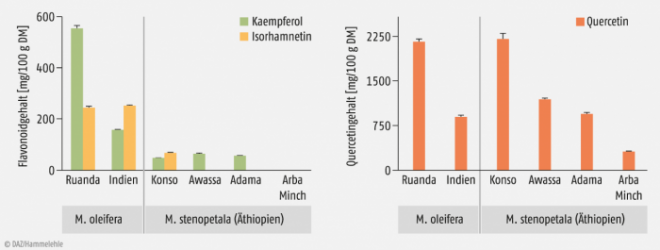
Vergleich: Beim Vergleich der gemessenen Flavonoidgehalte beider Arten wird deutlich, dass der absolute Gehalt an Quercetin sowohl in M. oleifera als auch in M. stenopetala stark schwankt (s. Abb. 2).
Alle untersuchten Proben von M. stenopetala weisen einen deutlich geringeren Kaempferolgehalt als die von M. oleifera auf. Die höchste Konzentration an Kaempferol wurde in der Probe aus Ruanda ermittelt.
Isorhamnetin konnte in allen Proben von M. oleifera in ähnlicher Konzentration quantifiziert werden. In M. stenopetala kam dieses Flavonoid nur in der Probe aus Konso vor – allerdings in einer deutlich geringeren Konzentration.
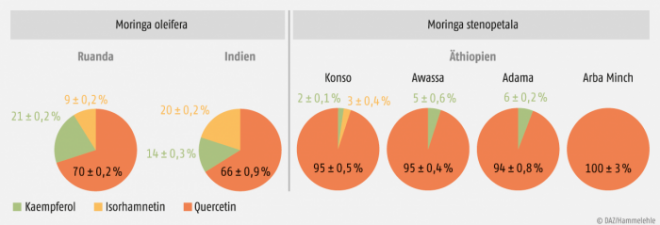
Beim Vergleich der Flavonoid-Zusammensetzung ist ein signifikanter Unterschied zwischen den Arten erkennbar (s. Abb. 3). Flavonoide in M. stenopetala bestehen in allen Fällen zu über 94% aus Quercetin, während es in M. oleifera 66 – 70% sind. Die letztere Art enthält außerdem 14 – 21% Kaempferol und 9 – 20% Isorhamnetin.
Abb. 3: Prozentuale Zusammensetzung der Flavonoide in den beiden Moringa-Arten (Gesamtflavonoidgehalt [mol] = 100%).
Gehalt abhängig vom Anbaugebiet?
Im Rahmen dieser Arbeit konnten Proben einer noch wenig untersuchten Moringa-Spezies, M. stenopetala, gesammelt und hinsichtlich des Flavonoidgehaltes analysiert werden. Die Ergebnisse wurden mit den Gehalten von M. oleifera verglichen. Zudem wurde eine geeignete Extraktions- und Hydrolysemethode entwickelt und validiert. Innerhalb derselben Spezies zeigen die Proben signifikant unterschiedliche Werte für Quercetin, Kaempferol und Isorhamnetin. Dies legt die Vermutung nahe, dass der absolute Gehalt von den Wachstums- und Anbaubedingungen beeinflusst wird. Betrachtet man die Zusammensetzung der Flavonoide innerhalb einer Probe, ist ein bestimmtes Verteilungsmuster je nach Art deutlich zu erkennen. Der Einfluss der Höhenlage des Anbaugebietes auf den absoluten Gehalt an Kaempferol bleibt noch zu untersuchen, denn die Probenanzahl war für diese Fragestellung nicht ausreichend.
Heilmittel aus der Natur
Derzeit wird Moringa als Nahrungsergänzung angeboten oder in Pflegeprodukten verarbeitet. Um die Möglichkeiten der medizinischen Nutzung weiter zu erforschen und gegebenenfalls voranzutreiben, wäre die Herstellung von standardisierten Extrakten wünschenswert. Damit könnten verschiedene Arzneiformen, wie beispielsweise Kapseln und Tabletten, entwickelt und getestet werden.
Zudem gilt es zu klären, ob die in den Tropen beobachteten immunstärkenden Effekte auf europäische Konsumenten übertragbar sind. Afrikanische Patienten profitieren aufgrund einer weniger ausgeglichenen Ernährung möglicherweise deutlich stärker als Personen im westlichen Kulturkreis.
Da in Europa das Interesse an „Heilmitteln aus der Natur“ wächst, könnten Moringa-Produkte in den nächsten Jahren auch hierzulande eine größere Rolle spielen. |
Literatur
[1] Morton JF. The horseradish tree, Moringa pterygosperma (Moringaceae) – a boon to arid lands?. Economic Botany 1991;45:318-33
[2] Verdcourt B. Moringaceae. Flora of Ethiopia 2002, Addis Abeba
[3] http://explorelifeonearth.org/moringahome.html (Zugriff: 03.05.2014)
[4] Jahn SAA. Proper use of African natural coagulants for rural water supplies. Research in the Sudan and a guide for new projects. Schriftenreihe der GTZ, Eschborn 1986
[5] Ndabigengesere A, Narasiah KS, Talbot BG. Active agents and mechanism of coagulation of turbid waters using Moringa oleifera. Water Research 1995;29:703-10
[6] Broin M, Santaella C, Cuine S, Kokou K, Peltier G, Joet T. Flocculent activity of a recombinant protein from Moringa oleifera Lam. Seeds. Applied microbiology and biotechnology 2002;60:114-9
[7] Walter A, Samuel W, Peter A, Joseph O. Antibacterial activity of Moringa oleifera and Moringa stenopetala methanol and n-hexane seed extracts on bacteria implicated in water borne diseases. African Journal of Microbiology Research 2011;5:153-7
[8] Pasternak D, Senbeto D, Nikiema A, Kumar S, Fatondji D, Woltering L, Ratnadass A, Ndjeunga J. Bioreclamation of degraded African lands with women empowerment, Chronica Hortic 2009;49:24-7
[9] Debela E, Tolera A. Nutritive value of botanical fractions of Moringa oleifera and Moringa stenopetala grown in the mid-Rift Valley of southern Ethiopia. Agroforestry Systems 2013;87:1147-55
[10] Melesse A. The feeding value of deseeded pods from Moringa stenopetala and Moringa oleifera as evaluated by chemical analyses and in vitro gas production. Journal of Animal and Feed Sciences 2012;21:537-50
[11] Gebregiorgis F, Negesse T, Nurfeta A. Feed intake and utilization in sheep fed graded levels of dried moringa (Moringa stenopetala) leaf as a supplement to Rhodes grass hay. Tropical animal health and production 2012;44:511-7
[12] Abuye C, Urga K, Knapp H, Selmar D, Omwega A, Imungi J, Winterhalter P. A compositional study of Moringa stenopetala leaves. East African medical journal 2004;80:247-52
[13] Hirt HM. Natural Medicine in the Tropics I: foundation text. Anamed, Winnenden 2008
[14] Ghebreselassie D, et al. The effects of Moringa stenopetala on blood parameters and histopathology of liver and kidney in mice. Ethiopian Journal of Health Development 2011;25.1:51-7
[15] Chuang PH, et al. Anti-fungal activity of crude extracts and essential oil of Moringa oleifera Lam. Bioresource Technology 2007;98.1:232-6
[16] Hänsel R, Sticher O. Pharmakognosie Phytopharmazie. Springer Verlag Heidelberg, Heidelberg 2010
[17] Keli SO, Hertog MG, Feskens EJ, Kromhout D. Dietary flavonoids, antioxidant vitamins, and incidence of stroke: the Zutphen study. Archives of Internal medicine 1996;156:637-42
[18] Knekt P, Järvinen R, Seppänen R, Heliövaara M, Teppo L, Pukkala E, Aromaa A. Dietary flavonoids and the risk of lung cancer and other malignant neoplasms. American Journal of Epidemiology 1997;146:223-30
[19] Bennett RN, Mellon FA, Foidl N, Pratt JH, Dupont MS, Perkins L, Kroon PA. Profiling glucosinolates and phenolics in vegetative and reproductive tissues of the multi-purpose trees Moringa oleifera L. (horseradish tree) and Moringa stenopetala L. Journal of Agricultural and Food Chemistry 2003;51:3546-53
[20] Siddhuraju P, Becker K. Antioxidant properties of various solvent extracts of total phenolic constituents from three different agroclimatic origins of drumstick tree (Moringa oleifera Lam.) leaves. Journal of Agricultural and Food Chemistry 2003;51:2144-55
[21] Gey MH. Instrumentelle Analytik und Bioanalytik – Biosubstanzen, Trennmethoden, Strukturanalytik, Applikationen. Springer Berlin Heidelberg, Heidelberg 2008
[22] Holiman PC, Hertog MG, Katan MB. Analysis and health effects of flavonoids. Food Chemistry 1996;57:43-6
[23] Hertog MGL, Hollman PCH, Venema DP. Optimization of a Quantitative HPLC Determination of Potentially Anticarcinogenic Flavonoids in Vegetables and Fruits. Journal of Agricultural and Food Chemistry 1992;40:1591-8























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.