
- DAZ.online
- DAZ / AZ
- DAZ 13/2015
- Damit es wieder läuft
Benignes Prostatasyndrom
Damit es wieder läuft
Watchful Waiting, Arzneistoffe, Phytotherapie und operative Verfahren in der neuen BPS-Leitlinie
Aufgrund der Anzahl der Betroffenen und der Kosten für Diagnostik und Therapie ist das benigne Prostatasyndrom als eine Volkskrankheit anzusehen. Die variable Trias aus Symptomatik, Prostatavolumen und Blasenauslassobstruktion bei Männern wird heute in der Fachliteratur als „Beni-gnes Prostatasyndrom“ (BPS) bezeichnet. Der Ausdruck „benigne Prostatahyperplasie“ (BPH) gilt heute als veraltet und bezeichnet nur noch die histologisch zugrunde liegende Gewebeveränderung. Die Prävalenz des BPS steigt mit zunehmendem Alter. Haben bei den 50 bis 59-Jährigen etwa 20% aller Männer mittlere bis schwere Symptome, so sind es in der Gruppe der über 70-Jährigen etwa 40%.
Leitlinienerstellung
Die kürzlich erschienene aktualisierte Leitlinie der Qualität S2e zur Therapie des BPS ist ein evidenzbasiertes Instrument, um die Therapie des BPS zu verbessern. Die vorliegende Version stellt eine Aktualisierung der vorherigen Leitlinie aus dem Jahr 2009 dar. Die Leitlinie soll dazu beitragen, eine angemessene, wissenschaftlich begründete und aktuelle Therapie anzubieten. Mittel- und langfristig sollen so die Morbidität gesenkt und die Lebensqualität erhöht werden. Die Leitlinienerstellung wurde durch die Deutsche Gesellschaft für Urologie finanziell unterstützt – unabhängig von Wirtschaft, Politik und Industrie. Die Leitlinie ist bis zur nächsten Aktualisierung im September 2017 gültig.
Die Leitliniengruppe konzentrierte sich bei der Evidenzaufarbeitung hinsichtlich Nutzen und Schaden auf folgende Interventionen:
- kontrolliertes Zuwarten (Watchful Waiting)
- medikamentöse Therapie
- Phytotherapie
- instrumentelle/operative Therapieoptionen.
Watchful Waiting als konservative Therapieoption
Im Gegensatz zu medikamentösen und operativen Verfahren handelt es sich beim Watchful Waiting (kontrolliertem Zuwarten) um eine konservative Therapieoption. Im Rahmen der Leitlinienaktualisierung konnten keine neuen klinischen Daten gefunden werden. Es bleibt daher bei den bereits bekannten Statements: Die Strategie des Watchful Waitings sollte bei Patienten in Erwägung gezogen werden, die einen geringen Leidensdruck haben, die zunächst Änderungen im Lebensstil zur Linderung der Symptomatik umsetzen können und darüber hinaus ein geringes Risiko für eine Progression des BPS und seine Komplikationen aufweisen. Darüber hinaus kann das kontrollierte Zuwarten eine Strategie für solche Patienten sein, die operative Verfahren oder Medikamente grundsätzlich ablehnen. Watchful Waiting kann durch eine Reihe von Verhaltensmaßnahmen unterstützt werden (s. Kasten).
Verhaltensmaßnahmen beim Watchful Waiting
- Regulierung der Flüssigkeitszufuhr (ca. 1500 ml/24 Stunden)
- gleichmäßige Verteilung über den Tag, Vermeidung übermäßiger Flüssigkeitszufuhr am Abend
- Reduktion bzw. Vermeidung des diuretischen und irritativen Effekts von übermäßiger Kaffee- und Alkoholzufuhr sowie scharfen Gewürzen
- Überprüfung bzw. Vermeidung von diuretischen Medikamenten am Abend, gegebenenfalls Medikamentenumstellung
- „Ausstreichen“ der Harnröhre nach der Miktion zur Verhinderung des Nachträufelns
- Blasentraining
α1-Blocker: Vorteil schneller Wirkungseintritt
Die Auswertung der aktuellen klinischen Daten bestätigte, dass die α1-Blocker Alfuzosin, Terazosin, Doxazosin, Tamsulosin und Silodosin bei Patienten mit BPS die Symptomatik gegenüber Placebo verbessern (Nachbeobachtungszeit von bis zu vier Jahren). Gegenüber Placebo erhöhen α1-Blocker das Risiko für Synkopen und Schwindel sowie möglicherweise für erektile Dysfunktion. Die Wirksamkeit der verschiedenen α1-Blocker ist vergleichbar. Hinsichtlich relevanter Nebenwirkungen zeigen sich für Tamsulosin Vorteile gegenüber Doxazosin, Silodosin (bei beiden gehäuftes Auftreten von Ejakulationsstörungen) und Terazosin (gehäuftes Auftreten von Schwindel). Gegenüber einer Monotherapie mit 5α-Reduktasehemmern wurde unter α1-Blockern eine geringfügig stärkere Symptomenreduktion beobachtet. Allerdings geht dies mit einem signifikant höheren Risiko für Schwindel einher. Grundsätzlich gilt: Die Therapie mit α1-Blockern führt bei BPS-Patienten zur raschen Symptomreduktion und zur Hemmung der symptomatischen Progression. Die langfristigen Effekte der α1-Blocker sind abhängig vom Prostatavolumen bei Therapiebeginn. Mit zunehmendem Prostatavolumen reduziert sich die Langzeiteffizienz.
5α-Reduktasehemmer zur Langzeittherapie
Die Auswertung aktueller klinischer Studien lässt den Schluss zu, dass eine langfristige Gabe von 5α-Reduktasehemmern bei BPS-Patienten die Symptomatik verbessern und das Risiko für akuten Harnverhalt reduzieren kann. Zum Vergleich der beiden 5α-Reduktasehemmer Finasterid und Dutasterid liegen derzeit keine belastbaren Daten vor. Grundsätzlich gilt: 5α-Reduktasehemmer sind bei Patienten mit BPS und einem Prostatavolumen ab 30 bis 40 ml zur Symptomreduktion und Progressionshemmung bei einer geplanten Langzeittherapie geeignet. Eine relevante Symptomreduktion tritt erst nach mehreren Monaten ein.
α1-Blocker und 5α-Reduktasehemmer in Kombination
Die Auswertung aktueller Daten zur Kombinationstherapie ergab gegenüber den jeweiligen Einzelsubstanzen einen geringen positiven Effekt auf die Symptomatik. Positive Effekte auf Progressionsparameter gegenüber einer Monotherapie mit einem 5α-Reduktasehemmer sind gering. Es fehlen Hinweise auf einen deutlichen Einfluss auf krankheitsbezogene Lebensqualität und Blasenauslassobstruktion. Das Nebenwirkungsprofil der Kombinationstherapie besteht aus den bekannten Nebenwirkungen der Einzelsubstanzen. Einen zusätzlichen negativen Effekt scheint die Kombinationstherapie auf die erektile Funktion zu haben.
Dennoch wird in der Leitlinie die Kombinationstherapie aus α1-Blocker und 5α-Reduktasehemmer als Primärtherapie für Patienten mit moderaten bis ausgeprägten Miktionsbeschwerden verbunden mit einem erhöhten Progressionsrisiko empfohlen. Die Kombination nutzt die klinischen Vorteile der Einzelsubstanzen (rascher Wirkeintritt der α1-Blocker und positiver Effekt der 5α-Reduktasehemmer auf die Krankheitsprogression).
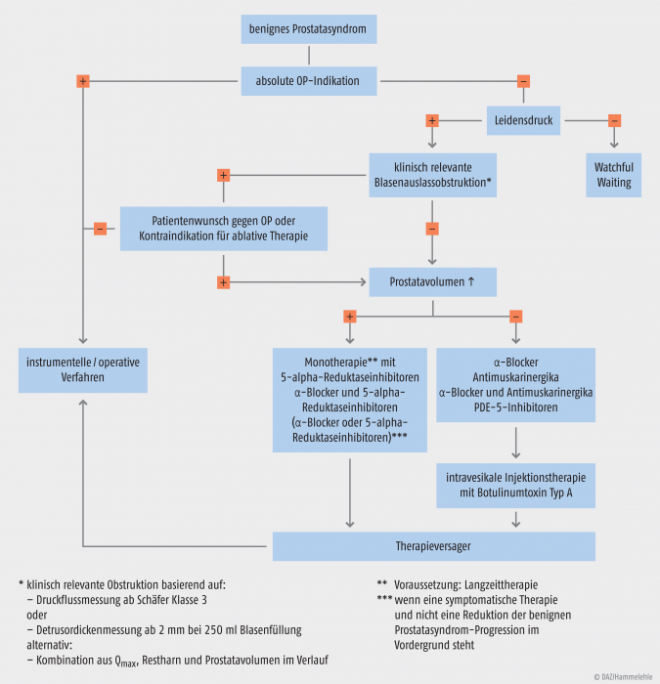
Therapiemöglichkeiten Abhängig von Symptomatik, Stadium und Zustand des Patienten werden alpha-1-Rezeptorenblocker und 5-alpha-Reduktasehemmer eingesetzt. alpha-1-Rezeptorenblocker führen über die Antagonisierung der alpha-1-Rezeptoren zu einer Erschlaffung der Muskulatur an Blasenhals, Harnröhre und Prostata. 5-alpha-Reduktasehemmer blockieren die Dihydrotestosteronsynthese in der Prostata und führen zu einer Verringerung des Prostatavolumens. Therapieziele sind dabei die Linderung von Beschwerden und das Verhindern von Komplikationen. [Quelle: Leitlinie zur Therapie des benignen Prostatasyndroms, 2014]
Muscarin-Rezeptorantagonisten: Kombination sinnvoll
Die ausgewerteten Daten zu den Muscarin-Rezeptorantagonisten Tolterodin, Solifenacin, Oxybutynin, Fesoterodin und Propiverin als Monotherapie ergeben keine sicheren Zusatznutzen-Belege bei Patienten mit BPS. Es zeigen sich allerdings Vorteile bei Anwendung der Kombination aus Muscarin-Rezeptorantagonisten und α1-Blockern. Muscarin-Rezeptorantagonisten werden grundsätzlich zur Therapie des imperativen Harndranges, der Dranginkontinenz und der gesteigerten Miktionsfrequenz bei Männern ohne Blasenauslassobstruktion eingesetzt. Die Kombinationstherapie aus α1-Blockern und Muscarin-Rezeptorantagonisten ist effektiv hinsichtlich der Verbesserung von Blasenspeichersymptomen und diesbezüglich der Monotherapie mit α1-Blockern überlegen.
PDE-5-Hemmer: Evidenz fraglich
Aus den aktuellen klinischen Daten lässt sich kein Zusatznutzen ableiten. Laut Leitlinie können Inhibitoren der Phosphodiesterase 5 (PDE 5) die Symptomatik bei Männern mit moderaten und schweren Symptomen des unteren Harntraktes mit oder ohne erektile Dysfunktion verbessern. Die Kombinationstherapie aus einem PDE-5-Hemmer und α1-Blocker lässt einen positiven Effekt auf die Symptomatik annehmen, allerdings ist die Studienlage uneinheitlich (beides Evidenzniveau 1-).
Phytotherapie: schwierige Datenlage
Zur Phytotherapie des BPS wurden klinische Daten zu verschiedenen pflanzlichen Extrakten untersucht. Aus den ausgewerteten Studien lassen sich zwar Hinweise auf positive Effekte hinsichtlich der Symptomreduktion bei mehreren Präparaten ableiten. Aufgrund methodischer Mängel der Studien ist jedoch für keine der untersuchten Extrakte sicher belegt, dass sie relevante Endpunkte langfristig und in einem relevanten Ausmaß positiv beeinflussen. Für die Monotherapie mit Präparaten der Sägezahnpalme (Serenoa repens) liegen mittlerweile methodisch hochwertige Studien vor, die einen Effekt auf die Symptomatik des BPS nicht nachweisen konnten und somit die positiven Ergebnisse älterer, methodisch schlechterer Studien grundsätzlich infrage stellen. Ein Kombinationspräparat aus Serenoa repens- und Brennnesselwurzel-Extrakt wurde mit Placebo verglichen und es zeigte sich eine statistisch signifikante Überlegenheit gegenüber Placebo bezüglich verschiedener Parameter. Allerdings war auch hier die Wertigkeit der Studie wegen der kleinen Fallzahl limitiert. Gleiches gilt für eine Studie, in der die Kombination aus Serenoa repens- und Brennnesselwurzel-Extrakt gegen Finasterid verglichen wurde. Auch hier konnte eine Besserung einiger Parameter beobachtet werden, aber diese Studie hatte keine Placebo-Gruppe.
Für β-Sitosterin ergaben sich Hinweise auf eine symptomreduzierende Wirkung und eine Verbesserung der Lebensqualität, die jedoch bisher nicht reproduziert wurden. Eine Symptomreduktion wurde auch für Roggenpollen-Extrakt (Secale cereale) afrikanischen Pflaumenbaum (Pygeum africanum), Kürbiskern-Extrakt (Cucurbita pepo) sowie Brennnesselwurzel-Extrakt (Urtica dioica) gezeigt. Mit Ausnahme einer Studie zum Kürbiskern-Extrakt haben die zugrunde liegenden Studien eine Nachbeobachtungszeit von weniger als einem Jahr und erlauben somit keine Einschätzung langfristiger Effekte. Hinweise auf spezifische Nebenwirkungen der untersuchten Extrakte sowie Hinweise auf Veränderungen der Obstruktion oder des Risikos für akute Harnverhalte ergaben sich in keiner Studie. Prinzipiell liegt die Besonderheit und gleichzeitig das Problem der Phytotherapeutika in ihrer komplexen Zusammensetzung. Abgesehen von der verwendeten Pflanze oder dem Pflanzenteil differieren die Extraktionsverfahren der einzelnen Herstellerfirmen, sodass die Fertigarzneimittel nur schwer vergleichbar sind. Wegen der Heterogenität der Phytotherapeutika und unterschiedlicher Studienergebnisse mit Produkten verschiedener Hersteller ist somit derzeit keine abschließende und generelle Beurteilung der Phytotherapie möglich. Eine allgemeine Empfehlung kann nicht gegeben werden. Zumindest gilt, dass Phytotherapeutika, die in Studien eine Überlegenheit gegenüber Placebo gezeigt haben, bei Patienten mit geringen bis moderaten Beschwerden und Leidensdruck in Betracht kommen, wenn chemisch definierte Präparate abgelehnt werden.
| verwendete Pflanzenteile | Stammpflanze | Präparatebeispiel |
|---|---|---|
| Früchte der Sägezahnpalme | Sabal serrulata, Serenoa repens | Prostagutt® mono/-uno Kapseln |
| Phytosterole | Harzol® Hartkapseln | |
| Brennnesselwurzel | Urtica dioica | Prosta-Truw® Weichkapseln |
| Kürbiskerne | Cucurbita pepo | Granu Fink® Prosta forte Weichkapseln |
| Gräserpollen | z.B. Secale cereale | Pollstimol® Hartkapseln |
| Rinde des Afrikanischen Pflaumenbaums | Pygeum africanum | kein Arzneimittel in D auf dem Markt |
Jede Menge operativer Verfahren!
Neben konservativen und therapeutischen Optionen werden in der Leitlinie auch diverse instrumentelle Verfahren erläutert: Für die transurethrale und die bipolare Resektion der Prostata, die transurethrale Inzision der Prostata, die offene Adenomenukleation und diverse Laserverfahren wurden in der aktuellen Leitlinie Evidenzniveaus von 1++ bis 1+ vergeben. Als Alternativen sind die transurethrale Hochenergie-Mikrowellen-Thermotherapie und die transurethrale Nadel-Ablation akzeptiert. Für andere Verfahren wie intraprostatische Stents, intraprostatische und intravesikale Injektion von Botulinumtoxin Typ A oder von dehydriertem Ethanol liegt derzeit nur ein geringes Evidenzniveau vor. |
Quelle
Leitlinie zur Therapie des benignen Prostatasyndroms der Qualität S2e, Arbeitskreis Benignes Prostatasyndrom (AK BPS) der Akademie der Deutschen Urologen, Deutsche Gesellschaft für Urologie e. V., Berufsverband der Deutschen Urologen e.V. 2014
Ärztliches Zentrum für Qualität in der Medizin (ÄZQ), Deutsche Gesellschaft für Urologie, Akademie der Deutschen Urologen 2013. Evidenzanalysen 2012 zur Therapie des benignen Prostatasyndroms (BPS) – Recherche von randomisierten kontrollierten Studien sowie systematischen Übersichtsarbeiten und Metaanalysen von 2007 bis August 2012






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.