
- DAZ.online
- DAZ / AZ
- DAZ 10/2015
- Geriatrische Pharmazie
Geriatrische Pharmazie
Paradigmenwechsel in der Geriatrie?
Das neue Denken über die Arzneimitteltherapie im Alter
Im Wesentlichen ist die Polymedikation (oder Polypharmazie) geriatrischer Patienten auf drei Ursachen zurückzuführen, die sich (in nach ihrer quantitativen Bedeutung abnehmender Reihenfolge sortiert) wie folgt darstellen:
Multimorbidität: Der Patient leidet an mehreren Erkrankungen, entsprechend treffen auf ihn mehrere Leitlinien zu, von denen jede den Einsatz mehrerer Arzneimittel fordert. Dabei kann es auch zu Kollisionen kommen, das heißt das von einer Leitlinie geforderte Arzneimittel ist wegen einer zweiten Erkrankung kontraindiziert oder führt zumindest zu Problemen.
Kommunikationsprobleme: Die Kommunikation zwischen den Disziplinen (z. B. Arzt und Apotheker, aber auch zwischen Fachärzten und Hausarzt) und zwischen den Sektoren (stationär und ambulant) ist insuffizient und störanfällig. Ein Beispiel für eine allzu oft unnötige Weiterverordnung sind Protonenpumpenhemmer (PPI). Werden sie in der Klinik beispielsweise zur Vermeidung von postoperativen Komplikationen bei antiphlogistischer Medikation angesetzt, stehen sie im Arztbrief als Entlassmedikation (in der Regel ohne Angabe eines empfohlenen Verordnungszeitraums) und werden vom Hausarzt (oder schlimmstenfalls von dessen eigenmächtiger Arzthelferin) jahrelang fortgeführt, oft bis zum nächsten Klinikaufenthalt – nicht zufällig sind Protonenpumpenhemmer die meistabgesetzten Arzneimittel in der Akutgeriatrie.
Verschreibungskaskaden: Die Nebenwirkung eines Arzneimittels wird als neues Symptom bzw. als neue Erkrankung fehlinterpretiert und mit einem weiteren Arzneimittel behandelt. Ein immer wieder zu beobachtendes Beispiel ist das Entstehen von Knöchelödemen unter Calcium-Antagonisten wie Amlodipin (sehr häufig bei Frauen über 70 Jahren), das statt mit einer Modifikation der Antihypertensiva-Kombination durch den Einsatz eines Schleifendiuretikums therapiert wird. Daran können sich weitere Kaskadenstufen anschließen, wie dies in der DAZ in einem POP-Fall aus dem Jahr 2013 beschrieben wird [1].
Aus dieser Problematik und der Erkenntnis, dass die Behandlung multimorbider geriatrischer Patienten nicht nur unnötig teuer, sondern auch therapeutisch suboptimal ist, resultiert ein Handlungsbedarf, den auch die Kostenträger und der Gesetzgeber erkannt haben. Da es sich um ein weltweites, alle Industrieländer betreffendes Problem handelt, lohnt sich ein Blick auf das, was in anderen Ländern bereits getan wird. Der auffälligste und provokanteste Ansatz stammt aus Israel und wurde erstmals im Jahr 2007 publiziert [2].
Anfang 2004 teilte der Geriater Doron Garfinkel 190 Patienten eines Alten- und Pflegeheims in zwei Gruppen ein. In der 119 Patienten umfassenden Studiengruppe (Durchschnittsalter 81,2 ± 8,3 Jahre) wurde die Medikation nach einem vorab ausgearbeiteten Schema reduziert, in der 71 Patienten umfassenden Kontrollgruppe (Durchschnittsalter 82,0 ± 8,7 Jahre) wurde sie unverändert beibehalten. Die Erkrankungen waren alterstypisch (Herzinsuffizienz, KHK, Diabetes mellitus, Demenz, COPD u.a.) und in den beiden Gruppen quantitativ nicht signifikant unterschiedlich verteilt.
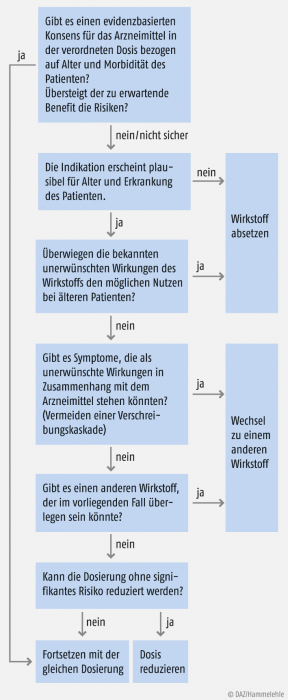
Abb. 1: Garfinkels Algorithmus zur Revision der Polymedikation eines geriatrischen Patienten (nach [2]). Um die Therapie für geriatrische Patienten zu optimieren, sollten Ärzte diese Fragen mit den Patienten bzw. mit den Betreuern klären.
Der in Abbildung 1 gezeigte Algorithmus führte vor allem zum Absetzen von Nitraten, H2-Blockern (in der zweiten Publikation von 2010 auch von PPI), Diuretika, Psychopharmaka, Kalium- und Eisenpräparaten sowie zu einer deutlichen Reduzierung von Antihypertensiva (siehe Tabelle 1). Nur in wenigen Fällen mussten die Medikationen wieder angesetzt werden, weil das Absetzen nach ebenfalls vordefinierten Kriterien als Fehlschlag einzustufen war.
| abzusetzendes Arzneimittel | Bedingung | Fehlschlag, wenn | Erfolgsquote [%] |
|---|---|---|---|
| Nitrate | kein Brustschmerz seit drei Monaten | erneuter Brustschmerz, EKG-Veränderungen | 100 |
| H2-Blocker (PPI) | kein Ulcus, keine gastrointestinale Blutung oder Dyspepsie seit einem Jahr | Wiederauftreten der gastrointestinalen Symptome | 94 |
| Kaliumpräparate | Serumkalium > 4 mmol/l | Serumkalium < 3,5 mmol/l | 100 |
| Eisenpräparate | Serumspiegel > 80 µg/dl | Serumspiegel < 50 µg/dl | 95 |
| Antihypertensiva | wenn mehrere, Absetzen von einem | RR-Anstieg > 140 mmHg systolisch bzw. > 90 mmHg diastolisch | 82 |
Weitere erfolgreich abgesetzte Medikationen (ohne Angabe von Kriterien): Pentoxifyllin (100% Erfolg), Diuretika, v.a. Furosemid (85%), Sedativa und Tranquilizer (88%), Antidepressiva (74%), Antipsychotika (69%) | |||
Das Ergebnis war beeindruckend: Die Mortalität innerhalb eines Jahres betrug 45% in der Kontrollgruppe, aber nur 21% in der Studiengruppe (p < 0,001). Innerhalb dieses einen Jahres mussten 30% aus der Kontrollgruppe, aber nur 12% aus der Gruppe mit reduzierter Medikation in ein Krankenhaus eingewiesen werden (p < 0,002). Selbst ohne die Berücksichtigung der Krankenhauskosten ergab sich für die Versuchsgruppe ein beträchtlicher Kostenvorteil.
2010 publizierte Garfinkel eine zweite Studie, in der er seinen Algorithmus von dem beschützenden Ambiente eines Alten- und Pflegeheims auf ein häusliches Lebensumfeld übertrug. Er verzichtete in dieser Studie auf eine Kontrollgruppe und untersuchte lediglich 70 Patienten. Die Untersuchung ist daher allein aus methodischen Gründen von geringerem Wert als seine erste. Bei 64 der 70 Patienten wurden 311 Arzneistoffe (entsprechend 58%) abgesetzt, in 81% der Fälle war die Reduzierung der Medikation erfolgreich und dauerhaft. Ernsthafte Zwischenfälle traten nicht auf, 88% der Patienten gaben eine verbesserte Lebensqualität zu Protokoll [3].
Dass Garfinkels erste Studie noch im vergleichsweise regionalen Journal der Israelian Medical Association erschien, seine methodisch weit kleinere zweite Publikation aber schon in Archives of Internal Medicine, dem renommierten Journal der American Medical Association, zeigt die Aufmerksamkeit, die seiner Methode entgegengebracht wird. Insgesamt stehen zwei wesentliche Prinzipien hinter Garfinkels Ansatz.
Erstens: Leitlinien sind nicht in jeder Population evidenzbasiert. Leitlinien beruhen großenteils auf klinischen Studien, die aus methodischen Gründen an einer nicht zu alten Studienpopulation durchgeführt wurden. Die bei geriatrischen Patienten meist anzutreffende Multimorbidität ist in solchen Untersuchungen in aller Regel ein Ausschlusskriterium. Wenn die aus diesen Studien resultierenden Leitlinien auf Populationen Anwendung finden, die in diesen Studien gar nicht repräsentiert sind, so ist das kaum als evidenzbasierte Medizin zu bezeichnen. Eines der einprägsamsten Beispiele war das um die Jahrtausendwende aufgetretene Spironolacton-Debakel. Die 1999 publizierte RALES-Studie hatte positive Effekte des Diuretikums bei Herzinsuffizienz an einer vergleichsweise jungen Studienpopulation beschrieben. Daraufhin kam es zu einem sprunghaften Anstieg der Anwendungen von Spironolacton – zum Teil in höheren Dosierungen, vor allem aber an älteren Patienten. Die Folge war eine Flut von Klinikeinweisungen und Todesfällen durch Spironolacton-induzierte Hyperkaliämien [4].
Zweitens: Palliative Therapie kann lange vor dem Sterben beginnen. Garfinkel definiert jeden Patienten mit nicht ausheilbaren Erkrankungen als palliativen Fall. Dies ist ein von unserer derzeitigen Betrachtungsweise abweichender, aber durchaus nachvollziehbarer Denkansatz, den er in den auf seiner Homepage einsehbaren Vorträgen ausführlich erläutert [5]. Er stellt die logische Konsequenz aus der Erkenntnis der hier eingeschränkten Anwendbarkeit von Leitlinien dar. Will man vor diesem Hintergrund nicht in einen Zustand der Polypragmasie zurückfallen, wie man ihn vor der Erstellung und Kommunikation verbindlicher Leitlinien kannte, so bleibt nur die Lösung des palliativ-typischen kritischen Hinterfragens jeder Maßnahme nach den Kriterien zu erwartende Restlebensdauer und erreichbare Lebensqualität. Jede Therapie wird, ähnlich wie beim Medication Appropriateness Index (MAI), darauf geprüft, ob sie in der jeweiligen Situation angemessen und erwünscht ist. Aus der Sicht der Kostenträger hat diese Einstellung eine Kehrseite, von der noch zu sprechen sein wird: In mindestens demselben Maße, in dem die Sachkosten für Arzneimittel sinken, steigen die Personalkosten für Menschen, die qualifiziert sind, solche Überlegungen erfolgreich anzustellen.
Umsetzung in Deutschland: Von PRISCUS zu FORTA
Die ersten Fragen von Garfinkels Algorithmus lauten: „Gibt es einen evidenzbasierten Konsens für das Arzneimittel bezogen auf Alter und Morbidität des Patienten? Übersteigt der zu erwartende Benefit die Risiken?“
Bereits dieser Einstieg macht klar, dass man mit den bisher gängigen Instrumenten, nämlich Leitlinien plus PRISCUS-Liste, nicht sehr weit kommt: Das Instrument zum kritischen Hinterfragen des Arzneimittels als Bestandteil der Leitlinie anhand der Situation des Patienten fehlt. Ein erster Ansatz zur Annäherung an Garfinkels Algorithmus wurde federführend von Professor Martin Wehling an der Uni Heidelberg (Medizinische Fakultät Mannheim) entwickelt: Die FORTA-Liste („Fit for the Aged“) ist ähnlich wie die PRISCUS-Liste das Ergebnis der Befragung einer Gruppe von 20 Experten nach der Delphi-Methode [6]. Unterteilt nach Indikationen klassifiziert sie Arzneistoffe in die vier Kategorien:
- Kategorie A: Das Arzneimittel ist schon geprüft an älteren Patienten in größeren Studien, die Nutzenbewertung ist eindeutig positiv.
- Kategorie B: Die Wirksamkeit ist bei älteren Patienten nachgewiesen, aber es gibt Einschränkungen bezüglich Sicherheit und Wirksamkeit.
- Kategorie C: Ungünstige Nutzen-Risiko-Relation bei älteren Patienten. Erfordern genaue Beobachtung von Wirkungen und Nebenwirkungen, sind nur ausnahmsweise erfolgreich. Bei mehr als drei Arzneimitteln gleichzeitig als erste weglassen, Alternativen suchen.
- Kategorie D: Diese Arzneimittel sollten fast immer vermieden und Alternativen gefunden werden. Diese Kategorie entspricht weitgehend der PRISCUS-Liste.
Anders als die PRISCUS-Liste ist die FORTA-Klassifikation mehr als nur eine Negativliste und damit als Entscheidungshilfe geeigneter. Man kann sie als einen ersten, gemäßigten Schritt zur Umsetzung der Garfinkel-Methode betrachten, insgesamt ist sie im Ansatz weniger provokant und damit konsensfähiger. Ob sie letztendlich das Modell ist, das sich (in dieser oder in modifizierter Form) durchsetzt, wird davon abhängen, wie sie sich künftig in EDV-Programmen für das Medikationsmanagement abbilden lässt. Dies ist bei FORTA sicher komplexer als eine bloße PRISCUS-Warnung in der Verordnungssoftware des Arztes oder im CAVE-Modul der Apotheke, aber es könnte in der Lenkung des Verordnungsprozesses auch deutlich wertvoller sein.
Praxis- und Apothekenprogramme der Zukunft
Praktische Ärzte dürfen seit einiger Zeit einen nicht unerheblichen Betrag für „Polypharmazie-Beratung“ bei Patienten mit mehr als fünf verschiedenen Arzneimitteln abrechnen. Wie sich im Dialog zeigt, gibt es innerhalb der Ärzteschaft noch kaum konkrete Vorstellungen, wie die Leistung auszusehen hat, die hier abgerechnet werden soll. Dass ein bloßer Interaktionscheck weder zielführend ist, noch von einer Arztpraxis aus deren Praxis-EDV heraus vollständig durchgeführt werden kann, bildet sich als Erkenntnis in der hausärztlichen Leitlinie „Multimedikation“ der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin ab. Darin wird ein Medikationsprozess, bestehend aus Bestandsaufnahme, Medikationsbewertung nach dem MAI, Abstimmung mit dem Patienten, Verordnungsvorschlag, Kommunikation, Arzneimittelabgabe (in der Apotheke, s. u.), Arzneimittelanwendung und Monitoring beschrieben. Legt man diesen Prozess im Dialog offen, so muss man seitens der Ärzte mit einer konsternierten Reaktion rechnen. Niemand hatte erwartet, dass das Geld für die Polypharmazie-Beratung derart sauer verdient sein würde.
In der DEGAM-Leitlinie wird dem Hausarzt nahegelegt, dem Patienten die Wahl einer Stammapotheke zu empfehlen, mit der der Arzt dann einen möglichst vollständigen Informationsaustausch pflegt. Damit wäre zumindest sichergestellt, dass die vorliegenden Daten zur Medikation des Patienten vollständig sind. Wie dann mit diesen Informationen weiter zu verfahren ist, klärt vielleicht in naher Zukunft ein gigantischer Feldversuch namens ARMIN. Alle großen (und viele kleinere) Softwarehäuser für Apotheken- und Praxissoftware blicken derzeit gebannt auf Sachsen und Thüringen. Dort wird sich unter anderem entscheiden, wie der Prozess letztlich aussehen soll, den sie in künftigen Programmgenerationen abbilden werden. Wer jemals in der Weiterbildung Geriatrische Pharmazie und/oder Medikationsmanagement einen komplexen Fall bearbeitet hat, weiß sehr genau, dass das in der Ausbildung eingesetzte Schema extreme Sorgfalt und viel Zeitaufwand erfordert und damit zwar lehrreich, aber kaum unverändert in den Berufsalltag übertragbar ist. Die erfolgreiche Umsetzung der Leitlinie Multimedikation (oder was auch immer bei ARMIN daraus entsteht) wird also wesentlich davon abhängen, ob und vor allem wie effizient und zeitsparend sich der Prozess des Medikationsmanagements in einer EDV abbilden lässt. Man kann heute den multimorbiden Patienten von morgen nur eine fruchtbare Zusammenarbeit der Anwenderseite (Pharmazeuten und Mediziner) mit den Softwareentwicklern wünschen. |
Literatur
[1] Baumgärtner G et al. Eine Patientin mit Juckreiz und Ödemen. DAZ 2013;11:48-57
[2] Garfinkel D et al. The war against Polypharmacy: A New Cost-Effective Geriatric-Palliative Approach for Improving Drug Therapy in Disabled Elderly People. IMAJ 2007;9:430-434
[3] Garfinkel D, Mangin D. Feasibility Study of a Systemic Approach for Discontinuation of Multiple Medications in Older Adults. Arch Intern Med 2010;170(18):1648-1654
[4] Stahl V. Risiko Spironolacton: Hyperkaliämie als problematische Nebenwirkung. DAZ 2013;29:50-53
[5] Less, rather than more, medication can better mean better quality of life and longer life. Garfinkel Method for Appropriate Medication. www.drugstop.co.il
[6] Kuhn-Thiel AM, Weiß C, Wehling M. Die Forta-Liste „Fit for The Aged“. Expert Consensus Validation, 2012
Perspektive 2030 – haben wir wirklich noch so viel Zeit?
Ein Gastkommentar von Dr. Markus Zieglmeier
Vor zehn Jahren schickte die Verbraucherzentrale Bremen Senioren als Testkäufer in die Apotheken, um sich nach Nahrungsergänzungsmitteln zu erkundigen. Auf Rückfrage gaben sie völlig normale, „ausgewogene“ Ernährungsgewohnheiten an. Der Test wäre in den Augen der Verbraucherzentrale dann bestanden worden, wenn der Kunde nach einem viertelstündigen Gespräch die Apotheke ohne Einkauf wieder verlassen hätte. Die Reaktionen der Apothekerschaft bescheinigten der Verbraucherzentrale einen kompletten Realitätsverlust. Dabei ist es grundsätzlich legitim, im Interesse einer perfekten Beratung dergleichen zu fordern – wenn man vorher das Honorierungssystem für Pharmazeuten völlig neu geregelt hat. Der Realitätsverlust besteht lediglich darin, von einem umsatzorientierten Unternehmen wie einer Apotheke hochqualifizierte Arbeit ohne Entlohnung einzufordern.
Genau diese Situation droht sich jetzt in verschärfter Form zu wiederholen. Gutes Medikationsmanagement führt nach Garfinkel und vielen anderen Autoren zu niedrigeren Arzneimittel- und Krankenhauskosten und liegt damit im Interesse von Gesetzgeber und Kostenträgern. Die Kehrseite der Medaille sind niedrigere Umsätze der Leistungserbringer, die dafür im Gegenzug mehr und immer höher qualifizierte Arbeit erbringen müssen – der Weg in den betriebswirtschaftlichen Suizid. Die derzeitige Finanzierungsart der öffentlichen Apotheke setzt Anreize in die falsche Richtung, und es ist bisher nicht erkennbar, wann dies korrigiert wird. 2030, im Jahr, das uns als Perspektive genannt wurde? Das wird zu spät sein, denn wesentliche Entwicklungen bahnen sich bereits heute an und werden 2030 längst abgeschlossen sein – zur Not auch ohne uns Apotheker, auch wenn der Informationsaustausch dann gravierende Defizite aufweisen wird.
Vor der Forderung, auch ohne ausreichende Honorierung in Vorleistung zu gehen, um zu beweisen, dass man es kann, ist andererseits ausdrücklich zu warnen. Gerade Krankenhausapotheker haben damit in der Vergangenheit verheerende Erfahrungen gemacht. Sie haben nämlich mit ihrer Vorleistung ihren zynischen Verwaltungsfürsten nur bewiesen, dass sie es können – und zwar mit dem Personal, das sie vorher schon hatten. Das für die jeweilige Leistung versprochene Personal blieb aus oder wurde an anderer Stelle der Apotheke wieder eingespart. Dergleichen Fehler im kleinen sollten die Berufspolitiker im großen Maßstab nicht wiederholen.
Man darf gespannt sein, welche Ergebnisse nach den Erkenntnissen aus ARMIN in Bezug auf die bundesweite Honorierung des Medikationsmanagements erzielt werden.






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.