
- DAZ.online
- DAZ / AZ
- DAZ 46/2014
- Vom Hersteller zum ...
Arzneimittelrecht
Vom Hersteller zum Patienten
Vertrieb von Arzneimitteln und Vertriebsabgrenzung
Das Arzneimittelgesetz sieht vor, dass nur eigens hierzu qualifizierte Personen und Stellen an der Arzneimitteldistribution teilnehmen dürfen. Eine Übersicht über die wichtigsten Regelungen, die sich im Wesentlichen im Siebten Abschnitt „Abgabe von Arzneimitteln“ (§§ 43–53 AMG) finden, bietet Tabelle 1.
Inverkehrbringen und pharmazeutische Unternehmer
Inverkehrbringen ist nach dem AMG das Vorrätighalten eines Arzneimittels zum Verkauf oder zu sonstiger Abgabe, das Feilhalten (zum Verkauf vorrätig halten), das Feilbieten (zum Kauf anregende Handlungen) und die Abgabe an andere (§ 4 Abs. 17 AMG). Der Verantwortliche für das Inverkehrbringen ist der pharmazeutische Unternehmer (§ 9 Abs. 1 AMG). Er, d.h. in der Regel eine Firma, muss auf der Arzneimittelpackung und in der Packungsbeilage mit Namen und Anschrift angegeben werden. Bei zulassungs- oder registrierungspflichtigen Arzneimitteln muss der pharmazeutische Unternehmer auch Inhaber der Zulassung sein. Es können aber auch andere Personen zum pharmazeutischen Unternehmer werden, ohne dass ihnen die Zulassung gehört (§ 4 Abs. 18 AMG). Dies gilt z.B. für Mitvertreiber. Räumt der Inhaber der Zulassung einem anderen das Recht ein, das Arzneimittel unter dessen Namen zu vertreiben, so wird der Mitvertreiber zum pharmazeutischen Unternehmer und muss dann auch auf der Arzneimittelpackung stehen.
Der pharmazeutische Unternehmer muss seinen Sitz in Deutschland oder einem anderen Mitgliedstaat der EU oder des EWR haben. Er kann einen örtlichen Vertreter benennen, aber das entbindet ihn nicht von seiner Verantwortung (§ 9 Abs. 2 AMG).
Der pharmazeutische Großhandel
Großhandel mit Arzneimitteln ist jede Tätigkeit, die berufs- oder gewerbsmäßig zum Zwecke des Handeltreibens ausgeübt wird und bei der es um die Beschaffung, Lagerung, Abgabe oder Ausfuhr von Arzneimitteln geht, mit Ausnahme der Abgabe von Arzneimitteln an die Öffentlichkeit (§ 4 Abs. 22 AMG). Großhändler brauchen für ihre Geschäftstätigkeit eine Erlaubnis, die von den zuständigen Landesbehörden auf Antrag innerhalb einer Frist von drei Monaten erteilt wird (§ 52a AMG).
Näheres zu den internen Betriebsabläufen bestimmt die Verordnung über den Großhandel und die Arzneimittelvermittlung (Arzneimittelhandelsverordnung). Sie schließt die Lücke in der Qualitätssicherungskette zwischen der Arzneimittel- und Wirkstoffherstellungsverordnung (Hersteller) und der Apothekenbetriebsordnung (Apotheken).
Noch weiter konkretisiert werden die Anforderungen in den EU-Leitlinien für die Gute Vertriebspraxis von Arzneimitteln. Im Zentrum der Guten Vertriebspraxis steht eine übersichtliche Lagerung, um Verwechslungen auszuschließen und zu verhindern, dass nicht verkehrsfähige Arzneimittel oder Arzneimittelfälschungen in den Handel gelangen. Genauso wichtig ist eine penible Dokumentation der Bezugs- und Liefervorgänge. Nur so können alle relevanten betrieblichen Vorgänge nachträglich überprüft und Rückrufaktionen wirkungsvoll durchgeführt werden.
Bereitstellung und Belieferung
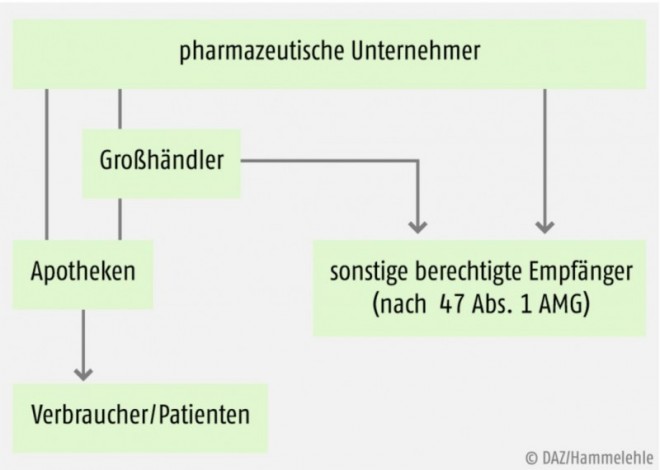
Nach dem Apothekengesetz haben die Apotheken den Auftrag, die Bevölkerung ordnungsgemäß mit Arzneimitteln zu versorgen. Diese gemeinwirtschaftliche Verpflichtung können sie jedoch nur einlösen, wenn sie ihrerseits von der Industrie und vom Großhandel regelmäßig, ausreichend und zeitnah beliefert werden (Abb. 1). Aus der Sicht der Pharmaunternehmen oder auch der Großhändler kann es durchaus Gründe geben, ihr Sortiment einzuschränken, etwa aus Rentabilitätserwägungen oder auch, um den Parallelexport zu verhindern. Dem hat der Gesetzgeber allerdings mit der 15. AMG-Novelle im Jahr 2009 einen Riegel vorgeschoben: Gemäß § 52a AMG müssen pharmazeutische Unternehmer und Großhändler zugelassene und tatsächlich vermarktete Arzneimittel angemessen und kontinuierlich bereitstellen, um damit den Bedarf der Patienten auf dem hiesigen Markt zu decken. Die Pharmaunternehmen müssen außerdem vollversorgende Arzneimittelgroßhandlungen bedarfsgerecht und kontinuierlich beliefern, denn sie haben für die Versorgung eine zentrale Stellung und Funktion. Dabei müssen die vorzuhaltenden Arzneimittel mindestens dem durchschnittlichen Bedarf von zwei Wochen entsprechen.
Vollversorgende Arzneimittelgroßhandlungen müssen ihrerseits eine bedarfsgerechte und kontinuierliche Belieferung der mit ihnen in Geschäftsbeziehung stehenden Apotheken gewährleisten. Dies gilt auch für Teilsortimenter im Umfang der von ihnen jeweils vorgehaltenen Arzneimittel.
In welchem Umfang eine Direktbelieferung der Apotheken durch die Pharmafirmen zulässig ist, regelt das AMG dagegen nicht.
Lieferengpässe
Lieferengpässe bei Arzneimitteln sind in den letzten Jahren zunehmend in die Diskussion geraten. Die Gründe hierfür sind vielfältig: Herstellungsprobleme, Produktions- oder Lieferverzögerungen für Wirkstoffe oder Ausgangsmaterialien und Rentabilitätsfragen spielen hierbei eine große Rolle.
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) unterhält auf seiner Website ein datenbankgestütztes Register über voraussichtlich länger als zwei Wochen andauernde Lieferengpässe bei Arzneimitteln (www.bfarm.de → Pharmakovigilanz → Risikoinformationen → Lieferengpässe). Es berücksichtigt derzeit nur Präparate, die überwiegend zur Behandlung lebensbedrohlicher oder schwerwiegender Erkrankungen bestimmt sind und für die es keine Alternativpräparate gibt. Die Zulassungsinhaber sollen einen vorhersehbaren Lieferengpass spätestens sechs Monate im Voraus und unvorhersehbare Engpässe unverzüglich elektronisch mitteilen.
Arzneimittelvermittlung
Arzneimittelvermittlung (broking) ist jede berufs- oder gewerbsmäßig ausgeübte Tätigkeit von Personen, die, ohne Großhändler zu sein, selbstständig und im fremden Namen mit zulassungspflichtigen Humanarzneimitteln (gem. § 2 Abs. 1 oder Abs. 2 Nr. 1) handeln, ohne tatsächliche Verfügungsgewalt über diese Arzneimittel zu erlangen. Mit dieser noch relativ neuen Definition (§ 4 Abs. 22a AMG) wurde eine Vorgabe der europäischen Richtlinie gegen Arzneimittelfälschungen umgesetzt und eine weitere Lücke in der Absicherung der legalen Distributionskette für Arzneimittel geschlossen. Die Tätigkeit ist zwar nicht erlaubnispflichtig, muss aber bei der zuständigen Landesbehörde angezeigt werden (§ 52c AMG). Außerdem müssen Arzneimittelvermittler in einer öffentlichen Datenbank des DIMDI oder einer Datenbank eines anderen EU-/EWR-Mitgliedstaates registriert werden, damit sich die Handelspartner von ihrer Legitimation überzeugen können. Wie Großhändler müssen sie auch ihren Sitz in einem Mitgliedstaat der EU oder des EWR haben und sind, soweit dort bestimmt, an die Vorgaben der Arzneimittelhandelsverordnung und der Guten Vertriebspraxis für Arzneimittel gebunden.
Apothekenmonopol
Das Arzneimittelgesetz sieht vor, dass zulassungspflichtige Arzneimittel (gem. § 2 Abs. 1 oder Abs. 2 Nr. 1) im Einzelhandel mit wenigen Ausnahmen nur über Apotheken abgegeben werden dürfen (Apothekenmonopol, § 43 AMG). Daran sind im Großen und Ganzen auch die pharmazeutischen Unternehmen und der Großhandel gebunden (s.u.). Das Monopol soll darüber hinaus die Apotheke als Institution absichern, denn zur Sicherstellung einer ordnungsgemäßen Arzneimittelversorgung müssen die Abgabestellen auch wirtschaftlich uninteressante Arzneimittel vorrätig halten. Die zentralen Rechtsvorschriften im Apothekenbereich sind das Gesetz über das Apothekenwesen (ApoG) und die Apothekenbetriebsordnung (ApBetrO), auf die hier allerdings wegen der Schwerpunktsetzung auf das Arzneimittelgesetz nicht näher eingegangen werden soll.
Was geht nicht über die Apotheke?
Die Möglichkeiten für pharmazeutische Unternehmer und Großhändler, apothekenpflichtige Arzneimittel an andere Empfänger abzugeben, sind sehr stark eingeschränkt. Sie betreffen jeweils unter bestimmten Bedingungen u.a. die Abgabe an:
- andere pharmazeutische Unternehmer und Großhändler,
- Krankenhäuser und Ärzte, jedoch nur bestimmte Arzneimittel, wie etwa aus menschlichem Blut gewonnene Blutzubereitungen oder Gewebezubereitungen, großvolumige Infusionslösungen, Diagnostika-Zubereitungen oder radioaktive Arzneimittel,
- Krankenhäuser, Gesundheitsämter oder Ärzte, soweit es sich um Impfstoffe für öffentliche Impfaktionen handelt, oder auch antibakterielle oder antivirale Arzneimittel zur spezifischen Prophylaxe nach dem Infektionsschutzgesetz,
- Tierärzte im Rahmen des Betriebes einer tierärztlichen Hausapotheke oder auch zur Ausübung der Zahnheilkunde berechtigte Personen, jeweils unter eingeschränkten Bedingungen,
- Wissenschafts- und Forschungseinrichtungen,
- Hochschulen für die Pharmazeutenausbildung.
Freiverkäufliche Arzneimittel
Die Abgrenzung der Vertriebsmöglichkeiten für Arzneimittel im Einzelhandel, d.h. Möglichkeit der Abgabe außerhalb der Apotheke (Freiverkäuflichkeit) findet sich im Arzneimittelgesetz in den §§ 44 bis 46. Die Vorschriften sind sehr komplex.
Nach § 44 AMG werden Arzneimittel für den Verkehr außerhalb der Apotheken freigegeben, die „ausschließlich zu anderen Zwecken als zur Beseitigung oder Linderung von Krankheiten, Leiden, Körperschäden oder krankhaften Beschwerden“ dienen. Dies sind in erster Linie die Vorbeugungsmittel sowie Stärkungs- und Kräftigungsmittel. Darüber hinaus sind folgende Produktgruppen von der Apothekenpflicht ausgenommen:
- natürliche und künstliche Heilwässer und deren Salze, auch als Tabletten oder Pastillen,
- Heilerde, Bademoore und andere Peloide, Zubereitungen zur Herstellung von Bädern, Seifen zum äußeren Gebrauch,
- mit ihren verkehrsüblichen deutschen Namen bezeichnete Pflanzen und Pflanzenteile, deren Mischungen als Fertigarzneimittel sowie deren Destillate und Presssäfte,
- Pflaster,
- überwiegend zum äußeren Gebrauch bestimmte Desinfektionsmittel sowie Mund- und Rachendesinfektionsmittel.
Der § 44 AMG stellt pauschal ganze Arzneimittelgruppen für den Verkehr außerhalb der Apotheke frei. § 46 AMG enthält wiederum eine Verordnungsermächtigung, mit der diese Pauschalfreistellung eingeschränkt wird, quasi als „Ausnahme von der Ausnahme“. Ein Beispiel für die Anwendung dieser Regelung sind Arzneipflanzen mit stark wirksamen Inhaltsstoffen, die ansonsten ebenfalls freiverkäuflich wären.
Anteile am Arzneimittelmarkt
Im Jahr 2013 lag der Anteil der rezeptpflichtigen Arzneimittel (Rx) am deutschen Arzneimittelmarkt nach Endverbraucherpreisen bei 84,5%; der Anteil der rezeptfreien, in der Apotheke abgegebenen Präparate betrug 14% (davon 2,9% ärztlich verordnet); lediglich 0,4% wurden außerhalb der Apotheke inklusive beim Discounter abgesetzt.
Bezüglich der Packungseinheiten lagen Rx und Nicht-Rx in der Apotheke mit jeweils 48% gleichauf, und der Vertrieb außerhalb der Apotheke machte 4% aus.
Quelle: Bundesverband der Arzneimittel-Hersteller (BAH) 2013
Außerdem können im Wege einer Rechtsverordnung noch weitere Arzneimittel von der Apothekenpflicht ausgenommen werden (§ 45 AMG). Hierfür kommen auch Arzneimittel infrage, mit denen teilweise oder ausschließlich Krankheiten geheilt oder gelindert werden sollen.
Die komplizierte Systematik der §§ 45 und 46 AMG ist in der „Verordnung über apothekenpflichtige und freiverkäufliche Arzneimittel“ zusammengefasst. In ihren insgesamt zehn Anlagen benennt sie Stoffe, die in freiverkäuflichen Arzneimitteln enthalten oder nicht enthalten sein dürfen. Letzteres gilt generell für Wirkstoffe mit antibiotischen, blutgerinnungsverzögernden, histaminwidrigen, hormonartigen oder das autonome Nervensystem beeinflussenden Eigenschaften. Auch bestimmte Arzneiformen, wie parenteral, rektal und vaginal anzuwendende Mittel sowie verschreibungspflichtige Stoffe sind prinzipiell vom Verkehr außerhalb der Apotheken ausgeschlossen. Außerdem enthält die Verordnung in der Anlage 3 einen Katalog von Krankheiten, die in den Indikationsangaben bei freiverkäuflichen Arzneimitteln nicht vorkommen dürfen.
Auf EU-Ebene macht der Gemeinschaftskodex keine Vorgaben bezüglich des Vertriebswegs (Tab. 1). Während einige EU-Mitgliedstaaten die Arzneimittelabgabe komplett auf die Apotheke beschränken, gibt es in anderen sogar Schmerzmittel im Drogeriemarkt.
Einzelhandel und Selbstbedienung mit Arzneimitteln
Der Einzelhandel mit freiverkäuflichen Arzneimitteln außerhalb der Apotheke, etwa in Drogeriemärkten, bedarf zwar keiner besonderen persönlichen Erlaubnis, ist jedoch mit Ausnahme weniger Produktgruppen nur zulässig, wenn eine Person mit einer entsprechenden Sachkenntnis zum Inverkehrbringen dieser Arzneimittel vorhanden ist (§ 50 AMG).
Nähere Einzelheiten über den Nachweis der Sachkunde sind in einer gesonderten Rechtsverordnung niedergelegt. Für die Arzneimittelabgabe im Reisegewerbe sind die Vertriebsmöglichkeiten noch weiter eingeschränkt (§ 51 AMG). Freiverkäufliche Arzneimittel dürfen auch in der Selbstbedienung abgegeben werden. Dies gilt sowohl für die Apotheke als auch für andere Abgabestellen, dort aber nur, wenn eine Person mit der erforderlichen Sachkenntnis zur Verfügung steht.
Verschreibungspflicht
Die Unterstellung unter die Verschreibungspflicht soll die Anwendungssicherheit von Arzneistoffen erhöhen,
- deren Wirkungen in der Wissenschaft noch nicht allgemein bekannt sind (neue Wirkstoffe und neue Kombinationen bekannter Wirkstoffe),
- die die Gesundheit auch bei bestimmungsgemäßem Gebrauch unmittelbar oder mittelbar gefährden können, wenn sie ohne ärztliche Überwachung angewendet werden, oder
- deren Anwendung wegen eines möglichen Missbrauchspotenzials ärztlich überwacht werden soll (§ 48 AMG).
Ziel der Verschreibungspflicht ist also zum einen die präventive ärztliche Kontrolle und zum anderen die ärztliche Überwachung der Reaktionen des Patienten auf die Therapie. Dabei spielt auch die Beratung bei der Abgabe in der Apotheke eine große Rolle. Sie hilft, die Compliance zu sichern, und sollte vor den Gefahren einer unkontrollierten Selbstmedikation mit diesen Arzneimitteln warnen. Welche Stoffe konkret von der Rezeptpflicht erfasst sind, bestimmt die Verordnung über die Verschreibungspflicht von Arzneimitteln (Arzneimittelverschreibungsverordnung, AMVV). Der Abgabestatus eines Arzneimittels wird im Zulassungsbescheid niedergelegt und bei der Zulassungsverlängerung nach fünf Jahren überprüft (§ 31 Abs. 3 Satz 3 AMG).
Was ist ein „switch“?
Unter „switching“ ist die Entlassung eines Wirkstoffs aus der Rezeptpflicht und damit die Freigabe für die Selbstmedikation zu verstehen. Der umgekehrte Vorgang wird als „re-switch“ bezeichnet. Entsprechende Anträge müssen wissenschaftlich begründet sein. Welche Kriterien bei einem Antrag auf Entlassung aus der Rezeptpflicht zu prüfen sind, hat die Europäische Kommission in einer eigenen Guideline (Switch-Guideline) zusammengefasst. Die Freigabe kann auf bestimmte Dosierungen, Potenzierungen, Darreichungsformen oder Anwendungsbereiche beschränkt werden, was häufig der Fall ist. Beispiele hierfür sind Präparate mit den Arzneistoffen Ibuprofen oder Loperamid.
Kernpunkte des Betäubungsmittelrechts
Für Betäubungsmittel gelten nicht nur die Anforderungen des AMG, sondern zusätzlich die Vorschriften des Betäubungsmittelgesetzes (BtMG). Es beruht auf dem internationalen Übereinkommen gegen den unerlaubten Verkehr mit Suchtstoffen und psychotropen Stoffen und regelt die Kontrolle des legalen Verkehrs mit Betäubungsmitteln wie auch die straftrechtlichen Folgen bei Verstößen. Hierzu gehört auch die Rauschgiftkriminalität.
Was unter einem Betäubungsmittel zu verstehen ist, definiert das Gesetz nicht explizit, sondern bezeichnet als Betäubungsmittel die in seinen Anlagen I bis III aufgeführten Stoffe und Zubereitungen:
- Anlage I enthält die nicht verkehrsfähigen Betäubungsmittel.
- Anlage II nennt die verkehrsfähigen, aber nicht verschreibungsfähigen BtM. Es handelt sich hierbei um Stoffe und Pflanzenmaterialien, die als Rohstoffe, Halbsynthetika und Zwischenprodukte zur Herstellung von Wirkstoffen eingesetzt werden. Da in der missbräuchlichen Weiterverarbeitung solcher Stoffe ein erhebliches Gefahrenpotenzial liegt, sind sie außerdem in einem eigenen Grundstoffüberwachungsgesetz (GÜG) geregelt.
- Die Anlage III des Betäubungsmittelgesetzes gibt in ihren Teilen A, B und C Aufschluss darüber, welche Stoffe in welchen Dosierungen verschreibungsfähig sind. Weitere Details bestimmt die Betäubungsmittel-Verschreibungsverordnung (BtmVV).
Wer Betäubungsmittel anbauen, herstellen, mit ihnen Handel treiben, sie einführen, ausführen, erwerben, abgeben bzw. in den Verkehr bringen will, braucht dazu, von einigen Ausnahmen abgesehen, eine spezielle Erlaubnis. Die hierfür zuständige Stelle beim BfArM heißt Bundesopiumstelle.
Sachverständigenausschüsse
Zur Vorbereitung der Verordnungen über die Verschreibungspflicht, Apothekenpflicht/Freiverkäuflichkeit und für die Unterstellung von Stoffen und Zubereitungen unter das Betäubungsmittelgesetz sind nach dem AMG bzw. dem BtMG in der Regel Experten anzuhören. Es gibt hierzu jeweils eigene Sachverständigenausschüsse, in die im Wesentlichen Mitglieder aus Kreisen der Wissenschaft, der Krankenhäuser, der Heilberufe und der Industrie vom Bundesministerium für Gesundheit berufen werden.
Die Geschäfte der Ausschüsse werden beim BfArM geführt. Sie erstellen nach eingehender Beratung eine Entscheidungsempfehlung (Votum) an den Gesetzgeber. Auf Basis dieses Votums wird dann der Entwurf einer Rechtsverordnung erstellt. Bevor die Rechtsverordnung schließlich durch die Bundesregierung erlassen wird, kann die Fachöffentlichkeit hierzu Stellung nehmen. Meistens ist auch die Zustimmung des Bundesrates erforderlich. Änderungsverordnungen zur Verschreibungspflicht treten turnusmäßig im Halbjahresrhythmus am 1. Januar bzw. am 1. Juli eines Jahres in Kraft.
Versandhandel
In Deutschland ist seit dem Jahr 2004 der Versandhandel sowohl mit OTC- als auch mit verschreibungspflichtigen Arzneimitteln grundsätzlich zulässig (§ 43 Abs. 1 Satz 1 AMG), allerdings nur für öffentliche Apotheken und nur nach Erteilung einer speziellen Erlaubnis (Versandhandelslizenz) durch die für sie zuständige Behörde (§ 11a Apothekengesetz).
Versandapothekenmarkt
Der Versandapothekenmarkt erreichte im 1. Halbjahr 2013 zu Apothekenverkaufspreisen einen Umsatz von 709 Mio. € (davon 59% mit OTC) und einen Absatz von 60 Mio. Packungen (davon 74% für OTC). Im Februar 2013 besaßen 3010 der rund 20.900 öffentlichen Apotheken eine Versandhandelserlaubnis. Nur 5,4% von ihnen betrieben einen aktiven Online-Apothekenversandhandel.
Quellen: Bundesverband Deutscher Versandapotheken (www.bvdva.de), IMS Health
Auch ausländische Versandapotheken in der EU dürfen Arzneimittel nach Deutschland versenden, wenn sie nach ihrem nationalen Recht dazu befugt sind und zu dem deutschen Recht vergleichbare Standards einhalten. Das BMG macht diese Länder im Bundesanzeiger bekannt. Derzeit ist der Versand aus Island, den Niederlanden (s.u.), Großbritannien, Tschechien (nur OTC-Arzneimittel) und Schweden (nur Rx-Arzneimittel) nach Deutschland ausdrücklich zugelassen. Niederländische Apotheken dürfen nach Deutschland versenden, wenn sie gleichzeitig eine Präsenzapotheke betreiben (www.bmg-bund.de).
Vor dem unkontrollierten Internet-Handel mit Arzneimitteln wird vor allem wegen der Gefahren, die mit Fälschungen verbunden sind, immer wieder gewarnt. Für die ordnungsgemäß lizenzierten Apotheken wird beim DIMDI ein eigenes Register geführt, über das man sich per Mausklick Sicherheit verschaffen kann, ob man es mit seriösen Anbietern zu tun hat (§ 43 Abs. 1 Satz 3 AMG). Sie tragen das Sicherheitslogo des Instituts. Im kommenden Jahr wird ein EU-weit einheitliches Logo für Online-Apotheken eingeführt (siehe Kasten).
Beim Arzneimittelkauf im Internet gibt künftig ein neues Logo Auskunft über die Seriosität von Online-Apotheken. Die Vorschriften hierzu hat die Europäische Kommission im Juni 2014 auf der Basis der Fälschungsrichtlinie erlassen. Ab spätestens Mitte 2015 gelangen die Verbraucher über einen Klick auf das neue Logo zu einer Liste aller in ihrem Land zugelassenen Online-Apotheken oder sonstigen zugelassenen Arzneimittelvertreiber.
Quelle: http://ec.europa.eu/deutschland/press/pr_releases/12489_de.htm
Literatur bei der Verfasserin






















0 Kommentare
Das Kommentieren ist aktuell nicht möglich.