
- DAZ.online
- DAZ / AZ
- DAZ 40/2014
- Hoffnungsträger ZMapp
Immunologie
Hoffnungsträger ZMapp
Drei Antikörper sollen das Ebola-Virus unschädlich machen
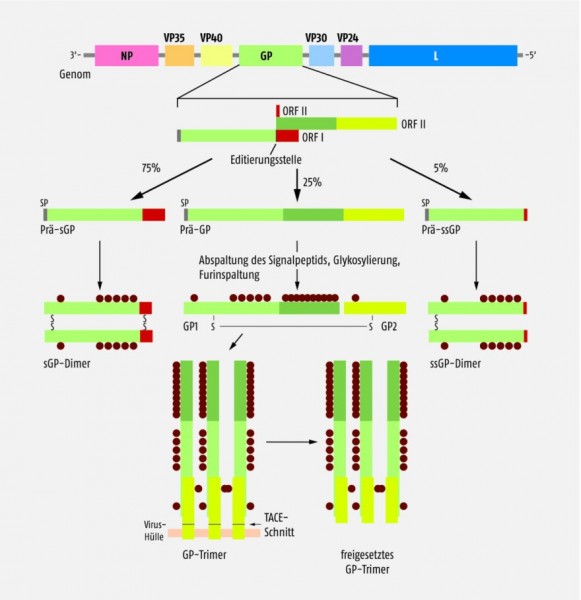
Die ersten Arbeiten, die zur Entwicklung des Wirkstoffs geführt haben, liefen bereits Ende des letzten Jahrhunderts. Sowohl die U.S. Army als auch die kanadische Public Health Agency finanzierten Versuche zur Entwicklung von monoklonalen Antikörpern gegen das Ebola-Virus (EBOV), die eventuell zur passiven Immunisierung eingesetzt werden könnten. Problematisch an der Aufgabe ist, dass das einzige Protein auf der Oberfläche des Virus, das als Zielstruktur infrage kommt, von infizierten Zellen in verschiedenen Varianten gebildet wird (Abb. 1). Potenziell wirksame Antikörper müssen an dieses Glykoprotein binden, finden aber im infizierten Körper auch andere Bindungspartner, die die Wirksamkeit beeinträchtigen könnten.
Ziel der beiden unabhängig voneinander arbeitenden Forschergruppen war also, Antikörper zu finden, die trotz dieser Problematik neutralisierende Eigenschaften aufweisen und im Sinne der passiven Immunisierung wirksam sind. Diese Antikörper würden sich in das bisher sehr dünn besetzte Feld der rekombinant hergestellten Antikörper zur passiven Immunisierung einfügen: Nur Synagis® (Palivizumab) ist seit 1999 für eine Gruppe frühgeborener Babys zur passiven Immunisierung gegen das respiratorische Syncytial-Virus zugelassen.
Ein klassischer Hintergrund ...
Der erste Schritt war bei beiden Arbeitsgruppen zunächst die Herstellung monoklonaler Antikörper über die klassische Hybridomatechnologie: BALB/c-Mäuse wurden mit harmlosen, rekombinanten Virus-Varianten immunisiert, die derart verändert waren, dass sie das EBOV-Oberflächenprotein trugen. Nach der Fusion der isolierten Maus-Milzzellen mit unsterblichen Myelomzellen konnten geeignete Hybridomzelllinien identifiziert werden, die Antikörper gegen das EBOV-Glykoprotein bilden.
Aus drei Antikörpern wird MB-003
Am U.S. Army Medical Research Institute of Infectious Diseases wurden insgesamt 14 monoklonale Antikörper genauer untersucht, die aufgrund ihrer Reaktivität in fünf verschiedene Gruppen eingeteilt wurden [1]. Zehn dieser Antikörper zeigten im Ebola-Mausmodell eine Virus-neutralisierende Aktivität. Nach weiteren Charakterisierungen waren letztlich drei Antikörper wirklich interessant für eine weitere Testung im Tiermodell:
- 13F6, der an die Aminosäuren 401–417 von Glykoprotein 1 (GP1) bindet,
- 6D8 mit der Bindungsstelle zwischen den Aminosäuren 389 und 405 in GP1 und
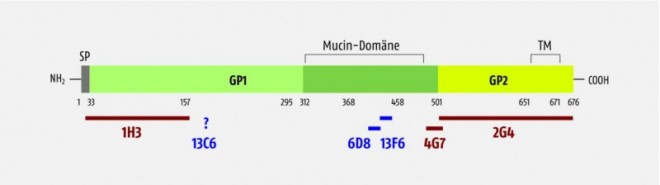
- 13C6, der eine dreidimensionale Struktur sowohl von GP1 als auch von sGP erkennt (Abb. 2).
dunkelrot: ZMab-Antikörper; dunkelblau: MB-003-Antikörper. Für 13C6 konnte das Epitop nicht genau angegeben werden; es ist allerdings bekannt, dass 13C6 sowohl sGP als auch GP1 erkennt (TM: Transmembrandomäne).
Die Antikörper 13C6 und 6D8 neutralisierten Viruspartikel in Anwesenheit von Komplementfaktoren auch in vitro, während 13F6 nur in vivo protektiv wirksam war [2, 3].
Für eine spätere Anwendung im Menschen wurden die Aminosäurensequenzen dieser drei Maus-Antikörper chimärisiert und deimmunisiert. Dazu wurden ihre konstanten Bereiche auf DNA-Ebene durch entsprechende menschliche DNA-Sequenzen ersetzt (Chimärisierung) und ihre variablen Bindedomänen so verändert, dass sie keine Epitope für CD4+-T-Zellen enthalten (Deimmunisierung). Diese derart optimierten Antikörper-Moleküle erhielten die Bezeichnungen c13C6, c6D8 und h-13F6 („c“ für chimärisiert, „h“ für humanisiert).
Die Kombination dieser drei Antikörper, die unter dem Namen MB-003 bei Mapp Biopharmaceutical Inc. entwickelt und zwecks Produktion und Vertrieb an die Firma Leaf Biopharmaceutical Inc. in San Diego auslizenziert wurde, zeigte in Rhesus-Affen eine recht gute Schutzwirkung: Zwei von drei Tieren, die 24 oder 48 Stunden und dann 4, 6 und 8 Tage nach der EBOV-Infektion jeweils 16,67 mg/kg KG Antikörper erhielten, überlebten den Versuch [3].
Drei andere Antikörper bilden ZMab
Die Herstellung der monoklonalen Antikörper in Kanada unterschied sich von der US-amerikanischen Strategie dahingehend, dass die BALB/c-Mäuse mit rekombinanten Viren immunisiert wurden, die sich bereits relativ erfolgreich als Antigene für eine aktive Immunisierung in Mäusen, Meerschweinchen und nicht-humanen Primaten bewährt hatten. Aus den resultierenden Hybridomzelllinien wurden acht monoklonale Antikörper genauer charakterisiert [4]. Nur drei dieser Antikörper – 1H3, 2G4 und 4G7 – zeigten im Zellmodell eine Virus-neutralisierende Aktivität. Obwohl diese drei Antikörper im Mausmodell schlechtere protektive Ergebnisse lieferten als die übrigen fünf Moleküle, konnten sie im Meerschweinchenmodell überzeugen: Als Einzelgabe am Tag 1 nach der EBOV-Infektion führten 2G4 und 4G7 immerhin zu einer 60-prozentigen Überlebensrate, während durch die Gabe der anderen Antikörper keines der Tiere die Infektion überlebte. Durch die Kombination der drei Antikörper konnte sogar ein noch besserer Schutz erzielt werden [5]. Auch Javaneraffen konnten durch die drei kombinierten Antikörper recht erfolgreich vor Ebola geschützt werden [6].
Die genauere Charakterisierung der Bindungsstellen der drei Antikörper ergab, dass 1H3 eine dreidimensionale Struktur in den ersten 157 Aminosäuren von GP1 und sGP erkennt. 2G4 bindet an eine dreidimensionale Struktur, die entweder von GP2 allein oder von GP2 und GP1 gebildet wird, und das Epitop für 4G7 liegt außerhalb der stark glykosylierten Mucin-Domäne im Bereich des C-Terminus von GP1 (Abb. 2) [4].
Die von der Firma Defyrus Inc. in Toronto unter dem Namen ZMab weiterentwickelte Kombination dieser drei Antikörper zeigte in Javaneraffen eine effiziente Schutzwirkung, wenn die Tiere dreimal im Abstand von je drei Tagen 25 mg/kg KG Antikörper erhielten. Begann die Therapie 24 h nach der EBOV-Infektion, überlebten alle vier Tiere; wurden die Antikörper erstmalig 48 h nach der Infektion verabreicht, starben hingegen zwei Tiere [6].
Das Beste aus MB-003 und ZMab ergibt ZMapp
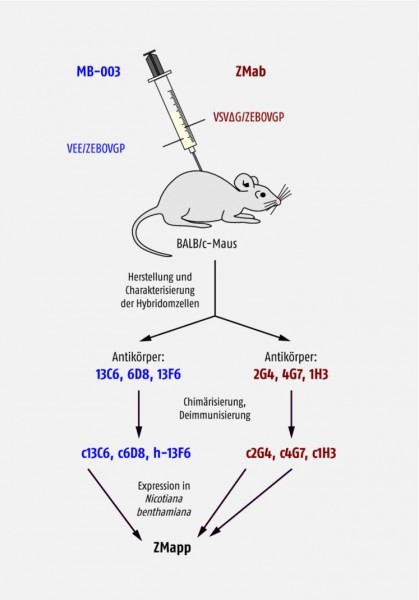
Im Juli 2014 übernahm Leaf Biopharmaceutical Inc. auch die Lizenz für ZMab von Defyrus Inc. in Toronto. Durch den Zusammenschluss beider Antikörpermischungen sollte nun ein optimierter Wirkstoff zur passiven Immunisierung entwickelt werden (Abb. 3).
Zunächst wurden die drei murinen Antikörper in ZMab ebenfalls chimärisiert, indem sie humane konstante Regionen erhielten; sie heißen folglich c1H3, c2G4 und c4G7.
In einem direkten Vergleichsexperiment wurden die Antikörper aus MB-003 einzeln und in Kombination an Meerschweinchen und Javaneraffen getestet. Als der am besten schützende Antikörper erwies sich c13C6. Dieser wurde – kombiniert mit jeweils zwei ZMab-Bestandteilen – darauf dem gleichen Testprogramm unterzogen [7]. Dabei zeigte die Kombination von c13C6 mit c2G4 und c4G7 die beste Protektion der Testtiere: Vier von sechs Meerschweinchen überlebten, wenn sie drei Tage nach der EBOV-Infektion eine Antikörperdosis von insgesamt 5 mg erhielten, und sechs von sechs Javaneraffen überstanden die Infektion nach dreimaliger Gabe von 50 mg/kg Körpergewicht Antikörperdosis, beginnend drei Tage nach der Infektion und mit einem Abstand von jeweils drei Tagen.
Ein neues Expressionssystem
Das Ungewöhnliche am Antikörper-Cocktail ZMapp ist das Expressionssystem. Mittlerweile sind etliche rekombinante Antikörper auf dem Markt, die in Säugerzelllinien wie z.B. CHO-Zellen (chinese hamster ovary) hergestellt werden. Diese Zellsysteme sind hinreichend bekannt und validiert. Der Nachteil ist allerdings, dass die Glykosylierungsmuster der Antikörper aus CHO-Zellen nicht einheitlich und nicht optimal für die gewünschte Interaktion mit den verschiedenen Fc-Rezeptoren sind. Aus diesem Grund wurde als Alternative die Expression der Antikörper in der dem Tabak verwandten Pflanze Nicotiana benthamiana getestet [2]. Für jeden der drei Antikörper ist ein eigenes Expressionssystem nötig, und da jedes Antikörpermolekül aus je zwei identischen schweren und leichten Proteinketten besteht, müssen diese möglichst in äquimolaren Mengen gebildet werden. Es zeigte sich, dass eine derartige Expression nur dann effizient abläuft, wenn die Gene für die beiden Proteine auf verschiedenen Vektoren liegen. Deshalb wurden die codierenden Sequenzen für die schwere und die leichte Antikörperkette in virale Vektoren eingefügt, die sich von den Genomen des Tabakmosaikvirus (TMV) und des Kartoffelvirus X (potato virus X, PVX) ableiten [8].
Beide virale Vektoren werden zunächst in Agrobacterium tumefaciens transformiert; sie können gleichzeitig in den Bakterienzellen persistieren und werden bei der Zellteilung auch an die nächste Generation weitergegeben. Dann werden die oberirdischen Teile von ca. 4 Wochen alten N. benthamiana-Pflanzen in einer Vakuumkammer in eine Suspension der transformierten Agrobakterien eingetaucht. Nach Anlegen eines Unterdrucks gelangen die transformierten Agrobakterien in die Pflanzenzellen, in denen die Antikörpergene exprimiert werden. Anschließend gehen die modifizierten Pflanzen für ca. 7 Tage in die normale Anzucht; danach werden die Blätter geerntet und die Proteine extrahiert.
Um eine möglichst einheitliche Glykosylierung der Antikörpermoleküle zu erhalten, die zudem noch optimierte Affinitäten zu den Fc-Rezeptoren auf Effektorzellen bzw. zu Proteinen des Komplementsystems aufweisen, wird eine Variante von Nicotiana benthamiana für die Antikörperexpression verwendet, bei der über einen RNA-Interferenz-Ansatz die pflanzeneigenen Enzyme Xylosyl- und Fucosyltransferase abgeschaltet wurden.
Die optimierten viralen Vektoren firmieren unter der Bezeichnung magnICON® und stammen ursprünglich von der Icon Genetics AG in München. Die Produktion der Antikörper findet bei Kentucky BioProcessing (Owensboro, KY) statt. Der Prozess selbst wird als Rapid Antibody Manufacturing Platform (RAMP) bezeichnet und kann nach den Angaben der Hersteller auch in größerem Maßstab unter GMP-Bedingungen durchgeführt werden. Unter optimalen Bedingungen können bis zu 4,5 mg Antikörper pro Gramm frisches Blattmaterial produziert werden.
Der Einsatz von ZMapp
Bisher ist ZMapp nur an Tiermodellen getestet worden. Keinerlei klinische Untersuchungen wurden bisher am Menschen durchgeführt. Insofern war es sehr mutig, diesen Wirkstoff jetzt für die Ebola-Patienten freizugeben.
Nun kann man natürlich auf dem Standpunkt stehen, dass ZMapp chimäre Antikörper wie beispielsweise Infliximab oder Rituximab sind, die bereits vielfach eingesetzt werden. Allerdings wurden die Antikörper für ZMapp eben nicht in CHO-Zellen oder anderen bereits hinreichend charakterisierten Säugerzellen hergestellt, sondern in Nicotiana benthamiana, einer Pflanze, die bisher nicht als Expressionssystem zertifiziert wurde. Zudem erfolgt die Expression transient, d.h. nur für einen kurzen Zeitraum, denn nach den sieben Tagen Anzucht würde die Expressionsrate stark zurückgehen. Es gibt also kein stabiles Wirt-Vektor-System, das umfänglich charakterisiert wurde, bevor es zur Synthese der therapeutischen Proteine eingesetzt wird.
Allerdings war und ist die Not in Westafrika groß, und diese Antikörper waren ein letzter „Strohhalm“ für einige Patienten. Im Gegensatz zu Synagis® wurde ZMapp nicht prophylaktisch eingesetzt, sondern bereits infizierten Patienten verabreicht, um das körpereigene Immunsystem bei der Bekämpfung des Pathogens zu unterstützen. Es bleibt abzuwarten, welche Konsequenz die Anwendung von ZMapp in dieser Epidemie für die Weiterentwicklung des Wirkstoffs hat.
Literatur
[1] Wilson JA, et al. Epitopes involved in antibody-mediated protection from Ebola virus. Science 2000;287:1664-1666
[2] Zeitlin L, et al. Enhanced potency of a fucose-free monoclonal antibody being developed as an Ebola virus immunoprotectant. Proc Natl Acad Sci USA 2011;108:20690-20694
[3] Olinger GG Jr, et al. Delayed treatment of Ebola virus infection with plant-derived monoclonal antibodies provides protection in rhesus macaques. Proc Natl Acad Sci USA 2012;109:18030-18035
[4] Qiu X, et al. Characterization of Zaire ebolavirus glycoprotein-specific monoclonal antibodies. Clin Immunol 2011;141:218-227
[5] Qiu X, et al. Ebola GP-specific monoclonal antibodies protect mice and guinea pigs from lethal Ebola virus infection. PLoS Negl Trop Dis 2012;6:e1575
[6] Qiu X, et al. Successful treatment of ebola virus-infected cynomolgus macaques with monoclonal antibodies. Sci Transl Med 2012;4:138ra81
[7] Qiu X, et al. Reversion of advanced Ebola virus disease in nonhuman primates with ZMapp. Nature; Epub 2014 Aug 29
[8] Giritch A, et al. Rapid high-yield expression of full-size IgG antibodies in plants coinfected with noncompeting viral vectors. Proc Natl Acad Sci USA 2006;103:14701-14706























0 Kommentare
Das Kommentieren ist aktuell nicht möglich.